一种用于检测次磺酸化蛋白质的荧光探针、制备方法及其应用与流程
本发明涉及生物检测领域,特别涉及对于细胞内巯基次磺酸化蛋白质原位显影,并通过荧光共振能量转移fret原理定量检测次磺酸化蛋白质的荧光探针的制备和应用。
背景技术:
氧化应激是指在各种内外因素刺激作用下,生物体内的活性氧,即过氧化氢、超氧阴离子、烷氧自由基、羟自由基等(reactiveoxygenspecies,ros)产生过多或发生代谢障碍,并且内源性抗氧化防御系统不能对其有效消除时,ros在体内增多并参与氧化生物大分子,诱发基因突变、蛋白质修饰变性和脂质过氧化,进而损伤溶酶体、线粒体等,最终导致细胞的氧化损伤。氧化应激已被证实与多个系统疾病的发生有着密切联系,尤其是阿兹海默病、帕金森氏病、亨丁顿舞蹈症等神经退行性疾病;这些疾病发生过程中氧化应激导致脑细胞凋亡、自噬等过程造成组织损伤和病变。其中,次磺酸化蛋白是ros氧化蛋白质的关键中间产物,即蛋白质巯基-sh被ros氧化后转化为次磺酸基团-soh,次磺酸基团-soh可被还原为硫醇/巯基状态,或继续氧化为亚磺酸和磺酸。因此,次磺酸化蛋白质是机体和细胞感受氧化应激的重要瞬时标志物,是表征氧化应激进程的重要信号。近年来蛋白质巯基次磺酸化修饰作为一个新兴的研究热点,越来越受到科学家的重视,发展能对生物体内巯基次磺酸化修饰进行实时追踪检测的方法,可极大推动相关的生物氧化应激机制及生理病理学研究。
早期的巯基次磺酸化修饰检测方法主要是利用比色法、间接法(先把样品中巯基选择性封闭,再用亚砷酸将次磺酸基团还原成巯基测定其含量)。但存在定量分析检测限高或反应步骤多的缺点。目前应用最广泛、体系发展最成熟的是生物素开关法,该法目前虽然接受度高,准确度好,但存在操作步骤繁琐、样本必须通过分离后进行质谱检测,很难应用于活细胞成像及实时监测等缺点。也无法获取蛋白质巯基次磺酸化修饰后动态变化等任何信息。小分子荧光探针成像由于灵敏度高,操作简单,可用于活体检测,近年来已成为检测完整生物样本的理想而不可缺少的辅助工具。
但是现有的荧光小分子探针存在以下问题:一是稳定性不够好,不能长期保存;二是使用时吸收发射波长差较小,不能够有效避免激发光的干扰,三是灵敏度相对不够高,四是选择性较小,适用范围不够广。
技术实现要素:
有鉴于此,本发明的目的在于提供一种用于检测次磺酸化蛋白质的荧光探针、制备方法及其应用,该荧光探针能够对细胞内巯基次磺酸化蛋白质原位显影,并通过荧光共振能量转移fret原理定量检测次磺酸化蛋白质。
本发明的用于检测次磺酸化蛋白质的荧光探针,具有如下结构通式(ⅰ):
其中,x为化学单键或者为
进一步,结构通式(ⅰ)中,所述r为
本发明还公开一种用于检测次磺酸化蛋白质的荧光探针的制备方法,所述用于检测次磺酸化蛋白质的荧光探针经可识别次磺酸的化合物与荧光化合物经缩合反应制得;
进一步,所述可识别次磺酸的化合物包括带有次磺酸-soh特征识别基团的羧酸或者其衍生物;
进一步,所述可识别次磺酸的化合物为带有次磺酸-soh特征识别基团的羧酸,在咪唑盐酸盐及微量水存在的条件下,以n,n'-羰基二咪唑作为缩合剂,经研磨,与溴乙胺或者对氨苯甲酸发生缩合反应,其化学反应式如下:
进一步,所述可识别次磺酸的化合物为带有次磺酸-soh特征识别基团的羧酸,在咪唑盐酸盐及微量水存在的条件下,以n,n'-羰基二咪唑作为缩合剂,经研磨,与8-氨基-1,3,6-萘磺酸二钠盐发生缩合反应,其化学反应式如下:
进一步,所述可识别次磺酸的化合物为带有次磺酸-soh特征识别基团的羧酸衍生物,加入三乙胺作为缩合剂和溶剂,经研磨,与8-氨基-1,3,6-萘磺酸二钠盐发生缩合反应,其化学反应式如下:
进一步,还包括缩合反应后经萃取分离纯化的步骤;
本发明还公开一种用于检测次磺酸化蛋白质的荧光探针在检测蛋白质巯基次磺酸化修饰中的应用。
本发明的有益效果:荧光小分子探针定量检测次磺酸化蛋白质是基于荧光共振能量转移fret原理。fret原理是:两个荧光发色基团在足够靠近时,当供体分子吸收一定频率的光子后被激发到更高的电子能态,在该电子回到基态前,通过偶极子相互作用,实现了能量向邻近的受体分子转移。fret发生条件:a.能量匹配:供体分子的发射光谱可以被受体分子吸收并产生荧光信号。供体分子的发射光谱应与受体分子的激发光谱必须有显著重叠(>30%);b.作用距离:供体分子与受体分子的作用距离为1-10nm。
本发明利用次磺酸-soh与含有亲核性的α-碳原子类化合物间,发生亲核取代反应,设计可与蛋白质中次磺酸化位点特异性反应的荧光探针,这些荧光探针本身在亲水性环境中荧光较弱,与-soh反应后可生成疏水性、具有较强荧光的加合产物,因而可用于蛋白质次磺酸化修饰程度的灵敏检测。其测定原理是蛋白质中的色氨酸残基作为fret的荧光供体其最大发射波长在330nm左右,荧光小分子探针的荧光基团作为fret的荧光受体其激发谱的范围在330nm左右。fret原理实现的条件是:反应前,荧光小分子探针的荧光基团与次磺酸化蛋白质的色氨酸残基相距可超过10nm;反应后,荧光小分子探针的荧光基团与次磺酸化蛋白质的色氨酸残基相距可小于2nm。
本发明的荧光探针稳定性好,能够长期保存使用;对于环境很敏感,探针在亲水环境中(如细胞胞浆)本身荧光不强,只有在与次磺酸化蛋白反应后荧光基团处于蛋白质结构内疏水环境,产生较强荧光,能在细胞内原位显影巯基次磺酸化蛋白质。同时,具有良好的水溶性和较大的吸收发射波长差,在细胞外水溶液检测体系,与蛋白质中色氨酸残基(其发射波长与探针激发波长重叠)能够配对产生荧光共振能量转移fret效应,有效避免激发光和蛋白质样品中发射光的干扰能在复杂生物样品中特异性地定量检测次磺酸化蛋白质,检测信噪比高,灵敏度好,具有优秀的选择性。从而实现对细胞内蛋白质巯基次磺酸化修饰的特异性检测。
本发明的荧光探针法除适用于检测细胞样本、血浆、组织匀浆中次磺酸化修饰程度,还适用于细胞甚至是动物组织中次磺酸化修饰的动态检测。
附图说明
下面结合附图和实施例对本发明作进一步描述:
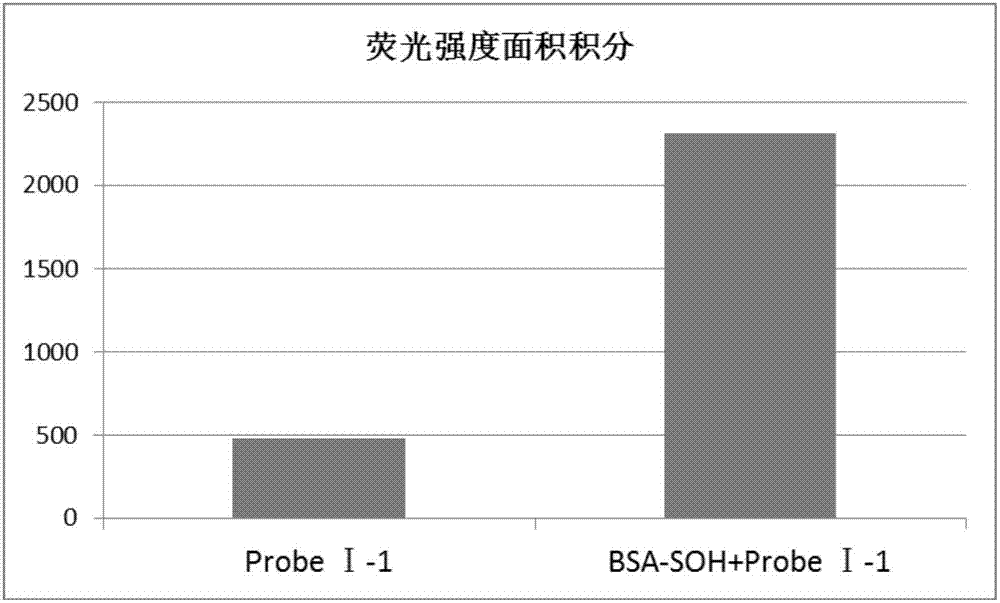
图1是荧光探针分子ⅰ-1与次磺酸化牛血清白蛋白(bsa-soh)反应前后的荧光变化;
图2是荧光探针分子ⅰ-1对次磺酸化牛血清白蛋白(bsa-soh)的选择性;
图3是荧光探针分子ⅰ-1对次磺酸化牛血清白蛋白(bsa-soh)浓度依赖性荧光增强;
图4是荧光探针分子ⅰ-1检测细胞中次磺酸化蛋白;
具体实施方式
本实施例的用于检测次磺酸化蛋白质的荧光探针,具有如下结构通式(ⅰ):
其中,x为化学单键或者为
本实施例中,结构通式(ⅰ)中,所述r为
本实施例的用于检测次磺酸化蛋白质的荧光探针的制备方法,所述用于检测次磺酸化蛋白质的荧光探针经可识别次磺酸的化合物与荧光化合物经缩合反应制得。可识别次磺酸的化合物如氰基乙酸,参与反应的物质添加量以能彻底反应完成为标准添加量,方法简单,易操作。
本实施例中,所述可识别次磺酸的化合物包括带有次磺酸-soh特征识别基团的羧酸或者其衍生物;r只能与次磺酸-soh感应,利用次磺酸-soh与含有亲核性的α-碳原子类化合物间,发生亲核取代反应,设计可与蛋白质中次磺酸化位点特异性反应的荧光探针,这些荧光探针本身在亲水性环境中荧光较弱,与-soh反应后可生成疏水性、具有较强荧光的加合产物,因而可用于蛋白质次磺酸化修饰程度的灵敏检测。
本实施例中,所述可识别次磺酸的化合物为带有次磺酸-soh特征识别基团的羧酸,在咪唑盐酸盐及微量水存在的条件下,以n,n'-羰基二咪唑(cdi)作为缩合剂,经研磨,与溴乙胺或者对氨基苯甲酸发生缩合反应,其化学反应式如下:
本实施例中,所述可识别次磺酸的化合物为带有次磺酸-soh特征识别基团的羧酸,在咪唑盐酸盐及微量水存在的条件下,以n,n'-羰基二咪唑作为缩合剂,经研磨,与8-氨基-1,3,6-萘磺酸二钠盐发生缩合反应,其化学反应式如下:
本实施例中,所述可识别次磺酸的化合物为带有次磺酸-soh特征识别基团的羧酸衍生物,加入三乙胺作为缩合剂和溶剂,经研磨,与8-氨基-1,3,6-萘磺酸二钠盐发生缩合反应,其化学反应式如下:
本实施例中,还包括缩合反应后经萃取分离纯化的步骤;
本发明还公开一种用于检测次磺酸化蛋白质的荧光探针在检测蛋白质巯基次磺酸化修饰中的应用:以定位显色细胞中次磺酸化蛋白的应用为例,可通过以下步骤实现:细胞经过100μm过氧化氢(h2o2)氧化处理30min,用0.05%戊二醛水溶液固定细胞15min,pbs缓冲溶液洗三次,细胞浸润在pbs溶液中,向其中加入式ⅰ所示的荧光探针,使其终浓度为200μm,25℃下避光孵育4小时(或者摇床避光慢速摇匀30min),观察记录细胞荧光强度,本发明提供的荧光探针的特征在于它的荧光基团本身在亲水性生理环境中的荧光量子产率较弱,当与细胞中次磺酸化蛋白的-soh基团特异性快速反应后,荧光基团处于蛋白质疏水结构中,其荧光量子产率大大提高,实现至倍荧光增强,从而实现蛋白质次磺酸化修饰的特异性检测和定量分析。
下面通过具体实施例对本发明做进一步的阐述。
实施例一
荧光探针分子ⅰ-1(结构式:
称取85mg氰基乙酸(85.06,1eq)和178mgn,n'-羰基二咪唑cdi(162.14,1.1eq),50℃在研钵中研磨5分钟,tlc薄层色谱板监测氰基乙酸完全反应,再向研钵中称入384mg8-氨基-1,3,6-萘磺酸二钠盐水合物(427.3,0.9eq)、10.4mg咪唑盐酸盐(104,0.1eq)及100μl水,研磨10分钟,tlc薄层色谱板监测8-氨基-1,3,6-萘磺酸二钠盐完全反应。加入10ml水和3×15ml乙酸乙酯,分液萃取,水层—60℃冷冻干燥,得到黄色固体产物ⅰ-1。hrms(esi-tof)[m+na]+:m/z515.9502。13cnmr(126mhz,d2o)δ111.17,116.77,119.30,119.91,124.64,131.52,133.67,135.54,138.78,139.57,141.75,144.62,170.08。
荧光探针分子ⅰ-1与次磺酸化牛血清白蛋白bsa-soh反应前后的荧光变化:
将探针分子少量溶解在20mmpbs缓冲液中,分别加入pbs缓冲液或次磺酸化牛血清白蛋白的溶液,使探针分子的终浓度为10μm,而待测样品的终浓度为10μm。反应5分钟后,使用荧光分光光度计以280nm激发,记录和计算溶液在发射波长范围下的荧光强度面积积分,进而确定探针分子与反应后荧光强度增强,如图1所示。
荧光探针分子ⅰ-1对次磺酸化牛血清白蛋白bas-soh的选择性:
配置探针分子的pbs溶液,分别加入10μm待测样品的pbs溶液,使探针分子的终浓度为10μm。反应5分钟后,使用荧光分光光度计以280nm激发,记录和计算溶液在发射波长范围下的荧光强度面积积分,计算荧光增强倍数,进而确定探针分子对bsa-soh的选择性,如图2所示。
荧光探针分子ⅰ-1对次磺酸化牛血清白蛋白的浓度依赖性荧光增强:
将探针分子溶解在20mmpbs缓冲液中,分别加入不同浓度的次磺酸化牛血清白蛋白溶液,使探针分子的终浓度为10μm,反应5分钟后使用荧光分光光度计以280nm激发,记录和计算溶液在发射波长范围下的荧光强度面积积分,计算荧光增强倍数,进而确定探针分子对浓度依赖性荧光增强,如图3所示。
荧光探针分子检测细胞中次磺酸化蛋白:
将人肺腺癌细胞a549接种于中号培养皿上,含10%胎牛血清的1640培养液中,置于细胞培养箱中37℃孵育12小时。随后,用pbs冲洗三次,加入h2o2使其终浓度为100μm,放入37℃细胞培养箱,30分钟后取出。然后,加200μl浓度为0.05%的戊二醛水溶液固定细胞,15分钟后,用pbs冲洗1-2次。加入含有荧光探针ⅰ-1的pbs溶液,使其终浓度为100μm,避光放置4个小时。每次用1mlpbs溶液浸洗2次。采用激光共聚焦荧光显微镜观察,拍照。其中采用405nm波长激发。结果表明,荧光探针分子可有效检测到人肺腺癌细胞a549次磺酸化化产物,如图4所示。
实施例二
荧光探针分子ⅰ-2(结构式:
称取85mg氰基乙酸(85.06,1eq)和178mgn,n'-羰基二咪唑cdi(162.14,1.1eq),50℃在研钵中研磨5分钟,tlc薄层色谱板监测氰基乙酸完全反应,再向研钵中称入205mg溴乙胺氢溴酸盐(204.89,1eq)和10.4mg咪唑盐酸盐(104,0.1eq),研磨30分钟,加入10ml水和3×15ml二氯甲烷,收集有机层,干燥浓缩得到中间产物。在研钵中,加入中间产物,2ml三乙胺和384mg8-氨基-1,3,6-萘磺酸二钠盐水合物(427.3,0.9eq),研磨20分钟,10ml水和3×15ml二氯甲烷萃取,分液萃取,水层—60℃冷冻干燥,得到黄色固体产物ⅰ-2。hrms(esi-tof)[m+na]+:m/z558.9416。13cnmr(126mhz,d2o)δ8.34,39.55,46.71,111.02,116.42,119.40,124.60,126.04,131.36,133.78,135.65,137.21,139.97,142.22,169.96。
实施例三
荧光探针分子ⅰ-3(结构式:
称取85mg氰基乙酸(85.06,1eq)和178mgn,n'-羰基二咪唑cdi(162.14,1.1eq),50℃在研钵中研磨5分钟,tlc薄层色谱板监测氰基乙酸完全反应,再向研钵中称入137mg对氨基苯甲酸(137.14,1eq)和10.4mg咪唑盐酸盐(104,0.1eq),研磨30分钟,加入10ml水和3×15ml二氯甲烷,收集水层,水层—60℃冷冻干燥得到中间产物。在研钵中,加入中间产物和178mgn,n'-羰基二咪唑cdi(162.14,1.1eq),50℃在研钵中研磨5分钟,tlc薄层色谱板监测氰基乙酸完全反应,再向研钵中称入384mg8-氨基-1,3,6-萘磺酸二钠盐水合物(427.3,0.9eq)、10.4mg咪唑盐酸盐(104,0.1eq)及100μl水,研磨10分钟,tlc薄层色谱板监测8-氨基-1,3,6-萘磺酸二钠盐完全反应。在研钵中,加入10ml水和3×15ml二氯甲烷萃取,分液萃取,水层—60℃冷冻干燥,得到黄色固体产物ⅰ-3。hrms(esi-tof)[m+na]+:m/z634.9333。13cnmr(126mhz,d2o)δ8.04,46.36,110.91,114.79,116.39,118.76,120.41,124.45,127.77,129.95,130.68,131.17,134.64,135.37,137.25,138.91,139.74,140.69,141.90,144.65,154.10,164.84,169.79,174.72.
实施例四
荧光探针分子ⅰ-4(结构式:
称取156mg3,5-二羰基环已酸(156.14,1eq)和178mgn,n'-羰基二咪唑cdi(162.14,1.1eq),50℃在研钵中研磨5分钟,tlc薄层色谱板监测氰基乙酸完全反应,再向研钵中称入384mg8-氨基-1,3,6-萘磺酸二钠盐水合物(427.3,0.9eq)、10.4mg咪唑盐酸盐(104,0.1eq)及100μl水,研磨10分钟,tlc薄层色谱板监测8-氨基-1,3,6-萘磺酸二钠盐完全反应。加入10ml水和3×15ml乙酸乙酯,分液萃取,水层—60℃冷冻干燥,得到黄色固体产物ⅰ-4。hrms(esi-tof)[m+na]+:m/z586.9218。13cnmr(126mhz,d2o)δ37.56,42.54,99.99,111.26,116.93,118.98,120.05,124.71,131.66,133.35,135.63,138.77,139.54,141.73,144.62,182.66,197.71。
实施例五
荧光探针分子ⅰ-5(结构式:
称取200mg(苯磺酰基)乙酸(200.22,1eq)和178mgn,n'-羰基二咪唑cdi(162.14,1.1eq),50℃在研钵中研磨5分钟,tlc薄层色谱板监测氰基乙酸完全反应,再向研钵中称入384mg8-氨基-1,3,6-萘磺酸二钠盐水合物(427.3,0.9eq)、10.4mg咪唑盐酸盐(104,0.1eq)及100μl水,研磨10分钟,tlc薄层色谱板监测8-氨基-1,3,6-萘磺酸二钠盐完全反应。加入10ml水和3×15ml乙酸乙酯,分液萃取,水层—60℃冷冻干燥,得到黄色固体产物ⅰ-4。hrms(esi-tof)[m+na]+:m/z630.8895。
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照较佳实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
- 还没有人留言评论。精彩留言会获得点赞!