一种用于诊断川崎病的生物标记物及试剂盒与用途的制作方法
本发明涉及分子生物学
技术领域:
,更具体地,涉及用于dna
技术领域:
,特别是指一种用于诊断川崎病的生物标记物及试剂盒与其用途。
背景技术:
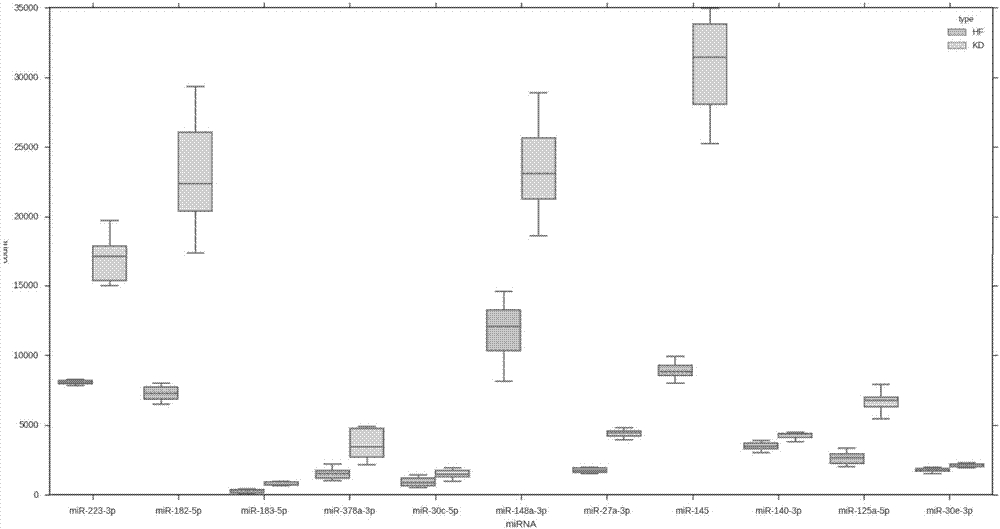
:川崎病(kawasakidisease,kd)于1967年由日本川崎富作首先报告,曾被称为皮肤黏膜淋巴结综合征(mucocutaneouslymphnodesyndrome,mcls),是一种原因未明的急性、自限性全身免疫性血管炎。它主要发病年龄为6个月~4岁,其特征为广泛的中小血管炎,以心血管系统的损害最为严重,主要累及冠状动脉,大约15%~25%未经治疗的儿童最终发展为冠状动脉损害,使其成为发达国家儿童获得性心脏病最常见的原因。研究认为,kd急性期、恢复期均存在长期的血管内皮功能紊乱,成为成人易患冠状动脉粥样硬化的危险因素。2004年美国心脏病协会提出:kd恢复后血管内皮功能持续性障碍,可能是冠心病发生的新的危险因素。川崎病(kd)作为一种急性、自限性的全身性血管炎,主要临床表现为发热、口腔黏膜改变、皮疹、颈部淋巴结肿大、球结膜充血和肢端改变等。其特征为广泛的中、小血管炎症,以心血管系统损害最为严重,组织病理表现包括全血管炎、内皮坏死、单核细胞浸润中、小血管等。如果未及时经正规治疗,25%~30%的患儿会出现冠状动脉病变;而早期应用静脉大剂量丙种球蛋白(ivig)~将冠状动脉瘤的发生率降低到3%~5%左右。由于川崎病的早期最主要的症状是高者热程超过5天,易与颈淋巴结炎、猩红热、荨麻疹、败血症等其他发热性疾病混淆而产生误诊,据相关文献报道,川崎病的早期误诊率可高达26.7%,使误诊患儿不能在川崎病早期及时使用ivig进行联合治疗而导致后期的冠状动脉损伤。血小板作为血液中第二丰富的细胞类型,血小板是由骨髓造血组织中的巨核细胞产生。多功能造血干细胞在造血组织中经过定向分化形成原始的巨核细胞,又进一步成为成熟的巨核细胞。成熟的巨核细胞膜表面形成许多凹陷,伸入胞质之中,相邻的凹陷细胞膜在凹陷深部相互融合,使巨核细胞部分胞质与母体分开。最后这些被细胞膜包围的与巨核细胞胞质分离开的成分脱离巨核细胞,经过骨髓造血组织中的血窦进入血液循环成为血小板。存在于外周血液循环中的血小板,在机体中起着止血和伤口愈合作用。近年来研究发现,血小板已成为全身和局部反应的中心分子,在细胞交流和免疫反应中扮演了重要作用,并且由于血小板没有细胞核,在研究其rna时不会存在rrna的背景干扰。血小板在免疫反应中也起到了信号交流和转移传播的作用,由于川崎病是一种全身性的免疫性疾病,所以研究血小板rna对川崎病的早期诊断有着理论基础和实际意义,而目前关于这方面的研究报道非常少见。技术实现要素:本发明的主要目的就是针对以上现状,提供一种用于诊断川崎病的生物标记物,以克服现有技术中的不足。本发明的第二目的还在于提供一种诊断川崎病的试剂盒与其用途。为实现前述发明目的,本发明采用的技术方案包括:本发明实施例提供了mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p与mir-30e-3p的组合作为诊断川崎病的生物标记物的用途。在一些较为具体的实施方案中,所述的mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p来源于血小板。本发明实施例还提供了一种用于诊断川崎病的生物标记物,其包含mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p。在一些较为具体的实施方案中,所述的mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p来源于血小板。本发明实施例还提供了一种用于诊断川崎病的试剂盒,其包含对患者血小板中mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p的表达量进行定量检测的试剂。在一些较为具体的实施方案中,所述试剂盒包含用于对mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p进行pcr检测的引物组。进一步的,所述引物组中对应于mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p的引物的序列分别如seqidno:1~seqidno:11所示。本发明实施例还提供了生物标记组在制备用于检测受试者中存在川崎病的体外方法中的试剂中的用途,所述的方法包括:测定来源于受试者的血小板的生物标记组中各生物标记的表达水平以获得测定值,所述的生物标记组选自mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p与mir-30e-3p的组合;将所述的测定值与参考值比较,若测定值高于参考值,则确定受试者患有川崎病。优选的,所述的方法包括:提取受试者的血小板中的生物标记组;提供与所述生物标记组中各生物标记一一对应的引物,其中各引物的序列分别如seqidno:1~seqidno:11所示;以及,通过pcr检测方法测得所述测定值。与现有技术相比,本发明的优点包括:1)本发明提供的用于诊断川崎病的生物标记物选取11种mirna来自于第二代高深度测序的结果并结合临床信息综合分析评分所得,联合分析11种生物标志物准确度远远大于单一生物标准物的检测,降低假阳性的发生。2)本发明提供的用于诊断川崎病的试剂盒中含有针对这11种mirnas进行taqman荧光定量pcr检测所用引物,使用者只需取1ml全血分离获得血小板中的rna,使用该试剂盒并配套相应的pcr试剂盒即可获得11种mirnas的含量,并通过ct值计算得到川崎病的患病风险。3)本发明具有取材便利、成本低廉、灵敏度高、稳定性好、易操作等优点,能及时、精准的将川崎病患儿与其他发热性疾病(如麻疹、热疹、肠胃炎、手足口病、疱疹等)患儿区分,提高了川崎病在早期诊断的检出率。因此,本发明对川崎病患儿的快速诊断具有极大的临床应用价值,为进一步研制出在川崎病患儿上使用的快速诊断试剂盒提供了技术保障。附图说明图1是本发明一典型实施例中采集的血液中血小板rna的类型分布示意图。图2是本发明一典型实施例中11种mirnas在kd患儿样本中表达量差异分析示意图。图3是本发明一典型实施例中采用本发明生物标记物的检出结果示意图。图4是本发明一典型实施例中临床样本检测的检出结果示意图。具体实施方式下文将对本发明的技术方案作更为详尽的解释说明。但是,应当理解,在本发明范围内,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。本发明将根据具体事例做进一步的描述,但其仅为例证性的目的而不祈祷限制性作用。在对实例描述前,有必要提供一些备注说明:采用不同厂家、不同批次的试剂会造成实验结果的差异,属于正常现象。在进行小规模实验时,为保证平行实验间的重复性,建议配置试剂后,充分混匀并分装,以保证每次实验试剂的均一性。本发明实施例的一个方面提供了mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p与mir-30e-3p的组合作为诊断川崎病的生物标记物的用途。在一些较为具体的实施方案中,所述的mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p来源于血小板。本发明实施例的另一个方面提供了一种用于诊断川崎病的生物标记物,其包含mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p。在一些较为具体的实施方案中,所述的mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p来源于血小板,为血小板中的mir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p。本发明实施例的另一个方面还提供了一种用于诊断川崎病的试剂盒,其包含对血小板中的mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p的表达量进行定量检测的试剂。在一些较为具体的实施方案中,所述试剂盒包含用于对mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p进行pcr检测的引物组。在一些实施例中,所述引物组中对应于mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p的引物的序列分别如seqidno:1~seqidno:11所示。进一步的,所述的pcr检测采用taqman荧光定量pcr检测。进一步的,所述试剂盒还包括qpcr扩增检测的常规组件,所述qpcr扩增检测的常规组件包括扩增模板、快速优化预混液(2x)、优化mirna引物混合液和无核酸酶超纯水。本发明实施例的另一个方面还提供了生物标记组在制备用于检测受试者中存在川崎病的体外方法中的试剂中的用途,所述的方法包括:测定来源于受试者的血小板的生物标记组中各生物标记的表达水平以获得测定值,所述的生物标记组选自mirnasmir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p与mir-30e-3p的组合;将所述的测定值与参考值比较,若测定值高于参考值,则确定受试者患有川崎病。在一些实施例中,所述的方法包括:提取受试者的血小板中的生物标记组;提供与所述生物标记组中各生物标记一一对应的引物,其中各引物的序列分别如seqidno:1~seqidno:11所示;以及,通过pcr检测方法测得所述测定值。藉由上述技术方案,本发明的用于诊断川崎病的生物标记物选取11种mirna来自于第二代高深度测序的结果并结合临床信息综合分析评分所得,联合分析11种生物标志物准确度远远大于单一生物标准物的检测,降低假阳性的发生。本发明的试剂盒中含有针对这11种mirnas进行taqman荧光定量pcr检测所用引物,使用者只需取1ml全血分离获得血小板中的rna,使用该试剂盒并配套相应的pcr试剂盒即可获得11种mirnas的含量,并通过ct值计算得到川崎病的患病风险。本发明具有取材便利、成本低廉、灵敏度高、稳定性好、易操作等优点,能及时、精准的将川崎病患儿与其他发热性疾病(如麻疹、热疹、肠胃炎、手足口病、疱疹等)患儿区分,提高了川崎病在早期诊断的检出率。因此,本发明对川崎病患儿的快速诊断具有极大的临床应用价值,为进一步研制出在川崎病患儿上使用的快速诊断试剂盒提供了技术保障。以下结合附图和若干实施例对本发明的技术方案作进一步的解释说明。实施例11.用于诊断川崎病的生物标记物筛选筛选方法如下:(1)使用edta抗凝管分别采集20例其他发热性疾病患儿和20例kd患儿血液1ml,4℃冰箱保存,48小时内通过离心分离血小板,分离的血小板使用磷酸盐缓冲液清洗2次后,若不立即使用,可长期保存在液氮中;(2)按照mivanamirnaisolationkit试剂盒的操作说明,提取血小板中的rna,并使用qubit和nanodrop并对其进行浓度和纯度的测定;(3)使用nebnextmirnalibraryprepkit对100ng提取的rna进行mirna文库构建,并切胶回收140bp-350bp的片段,文库构建过程完全遵守nebnextmirnalibraryprepkit的使用说明;(4)mirna文库采用hiseq2500进行sr50高通量测序,测序数据通过cutadapt等信息分析流程得到mirna上调或下调表达差异明显的mirnas,同时统计血小板rna的类型(参见图1);(5)表达差异分析中mir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p在kd患儿样本中均上调(参见图2);(6)血小板中的rna类型包含mrna、trna、mirna、trna、snorna等类型。(7)mir-223-3p、mir-182-5p、mir-183-5p、mir-378a-3p、mir-30c-5p、mir-148a-3p、mir-27a-3p、mir-145、mir-140-3p、mir-125a-5p及mir-30e-3p的表达量在kd患儿中,使用qpcr进行表达量验证。(8)使用advancedmirnaassays对上述20例其他发热性疾病患儿和20例kd患儿中的5例其他发热性疾病患儿和5例kd患儿的血小板rna进行反转录及qpcr反应预混合,反转录使用血小板rna约20ng;(9)取反转录及pre-amp产物5μl,加45μl0.1×te缓冲液进行模板稀释备用;(10)按照下表进行qpcr反应配置:(11)将配置好的预混液加入至96well孔板中,加入5μl稀释后的模板。混合后,500g短暂离心,放入abi7500qpcr仪中;(12)设置qpcr程序如下:(13)点击run,开始运行程序,程序约运行1.5h,运行结束后,统计每个样本的ct值;(14)分析结果可得kd患儿样本在所有mirnas检测中表达量均上调(参见下表),与高通量测序结果一致。controlhf3hf5hf6hf12hf19kd2kd8kd11kd13kd20mir-223-3p8132787179448044810381651501718398151291624015144mir-182-5p6812690577477146797769022805224998227181922325597mir-183-5p294127323341171375717774978681685mir-378a-3p10941092175317121032203037742148435328004885mir-30c-5p75660865797113985361950108315111898992mir-148a-3p13241118518155907411523143312157621012201281862721997mir-27a-3p18841894193819591619179540294427456344944226mir-1458532900390548701854184353205333175348582991328611mir-140-3p33643326346934733125355743134038432344594497mir-125a-5p24413275212833142848226579135344626668167274mir-30e-3p195116881769164819241958192018172046201821592.生物标记物检出率检测(1)使用edta抗凝管分别采集10例其他发热性疾病患儿和10例kd患儿血液1ml,4℃冰箱保存,48小时内通过离心分离血小板,分离的血小板使用磷酸盐缓冲液清洗2次后,若不立即使用,可长期保存在液氮中;(2)按照mivanamirnaisolationkit试剂盒的操作说明,提取血小板中的rna,并使用qubit和nanodrop并对其进行浓度和纯度的测定;(3)使用advancedmirnaassays对血小板rna进行反转录及qpcr反应预混合,反转录使用血小板rna约20ng;(4)取反转录及pre-amp产物5μl,加45μl0.1×te缓冲液进行模板稀释备用,取正常人白细胞样本作阴性对照;(5)按照下表进行qpcr反应配置:(6)将配置好的预混液加入至96well孔板中,加入5μl稀释后的模板。混合后,500g短暂离心,放入abi7500qpcr仪中;(7)设置qpcr程序如下:(8)点击run,开始运行程序,程序约运行1.5h,运行结束后,统计每个样本的ct值;(9)将每个样本所得ct值与阴性样本相减,取2的负幂得到差异值(p);(10)判断标准如下:p≥2.2,判断川崎病样阳性;1.7≤p<2.2,判断疑似川崎;p<1.7,判断川崎阴性;(11)20例患儿中,判断9例患儿川崎阳性,1例疑似川崎,10例其他发热性疾病,检出率95%(疑似川崎按照50%阳性计算)(参见图3)。3.临床样本检测(1)使用edta抗凝管采集50例临床表现症状出现高热48小时以上的患儿血液1ml,4℃冰箱保存,48小时内通过离心分离血小板,分离的血小板使用磷酸盐缓冲液清洗2次后,若不立即使用,可长期保存在液氮中;(2)按照mivanamirnaisolationkit试剂盒的操作说明,提取血小板中的rna,并使用qubit和nanodrop并对其进行浓度和纯度的测定;(3)使用advancedmirnaassays对血小板rna进行反转录及qpcr反应预混合,反转录使用血小板rna约20ng;(4)取反转录及pre-amp产物5μl,加45μl0.1×te缓冲液进行模板稀释备用,取正常人白细胞样本作阴性对照;(5)按照下表进行qpcr反应配置:(6)将配置好的预混液加入至96well孔板中,加入5μl稀释后的模板。混合后,500g短暂离心,放入abi7500qpcr仪中;(7)设置qpcr程序如下:(8)点击run,开始运行程序,程序约运行1.5h,运行结束后,统计每个样本的ct值;(9)将每个样本所得ct值与阴性样本相减,取2的负幂得到差异值(p);(10)判断标准如下:p≥2.2,判断川崎病样阳性;1.7≤p<2.2,判断疑似川崎;p<1.7,判断川崎阴性;(11)50例患儿中,判断33例患儿川崎阳性,5例疑似川崎,12例其他发热性疾病,本发明的诊断结果与临床上的诊断结果(临床指征、超声影像等结果)完全吻合,可见本发明的准确性高(参见图4)。从以上实施例和对应图1-图4可以明显看到,本发明提供的用于诊断川崎病与其他发热性疾病的生物标记物及试剂盒可以有效、准确、及时地将川崎病患儿与其他发热性疾病患儿快速区分,在实施例1中本发明通过高通量测序的方法找寻了川崎病直接相关的生物标志物11个mirnas,并使用taqmanqpcr方法验证了11个mirnas的川崎病特异性表达;在此基础上本发明采用了taqmanqpcr方法对生物标志物的检出率进行了复检,在检测了20例临床样本中,阳性检出率高达95%,并且该检出率会随着样本量的增多逐步升高;最后本案发明人实际检测了50例出现48小时持续高热的患儿样本,检出33例患儿川崎阳性,5例疑似川崎,12例其他发热性疾病,与临床指征及超声影像学结果诊断完全吻合。本发明通过检测血小板中mirnas的表达,较现有的影像学、临床指征用于川崎病早期诊断有着高灵敏、快速、操作简单、稳定性好等优势,较现有使用外泌体mirnas检测川崎病的方法有着取材更加便利、检测背景低的优势。因此,本发明对川崎病患儿的快速诊断具有极大的临床应用价值,为进一步研制出在川崎病患儿上使用的快速诊断试剂盒提供了技术保障。应当理解,上述实施例仅为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。序列表<110>苏州贝斯派生物科技有限公司<120>一种用于诊断川崎病的生物标记物及试剂盒与用途<160>11<170>patentinversion3.5<210>1<211>24<212>rna<213>人工序列<400>1uuuggcaaugguagaacucacacu24<210>2<211>22<212>rna<213>人工序列<400>2uauggcacugguagaauucacu22<210>3<211>22<212>rna<213>人工序列<400>3ucagugcacuacagaacuuugu22<210>4<211>21<212>rna<213>人工序列<400>4uucacaguggcuaaguuccgc21<210>5<211>22<212>rna<213>人工序列<400>5cuuucagucggauguuuacagc22<210>6<211>22<212>rna<213>人工序列<400>6acuggacuuggagucagaaggc22<210>7<211>23<212>rna<213>人工序列<400>7uguaaacauccuacacucucagc23<210>8<211>22<212>rna<213>人工序列<400>8ugucaguuugucaaauacccca22<210>9<211>21<212>rna<213>人工序列<400>9uaccacaggguagaaccacgg21<210>10<211>22<212>rna<213>人工序列<400>10ucccugagacccuaacuuguga22<210>11<211>23<212>rna<213>人工序列<400>11guccaguuuucccaggaaucccu23当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1