白藜芦醇的硅烷基化衍生物,和其用于神经变性、神经或发炎疾病的用途的制作方法
本发明涉及衍生自白藜芦醇的一组化合物,所述化合物具有至少一个硅烷基作为取代基,所述硅烷基又能够被不同基团取代。本发明还涉及这些化合物用于发炎、神经和神经变性疾病的治疗用途。因此,本发明涵盖在药物化学和药理学领域内。
背景技术:
白藜芦醇是酚类化合物。酚类化合物的化学结构由至少一个芳香族环和一个羟基组成。并且在酚类化合物内,白藜芦醇是芪,这组酚类化合物的特征是两个酚环经两个碳原子连接的结构(c6-c2-c6)。白藜芦醇存在于葡萄和其衍生的产品(例如葡萄酒)中以及其他食物中,尽管量小得多,例如花生和一些浆果。在这些食物中,其以游离形式或以白藜芦醇苷(白藜芦醇-3-o-糖苷)形式存在。这种化合物具有延长细胞寿命的抗氧化、消炎和抗肿瘤特性。
白藜芦醇在代表癌发生的三个主要阶段的试验中呈现癌症的化学预防活性:其充当抗氧化剂和抗诱变原,具有消炎作用并且抑制环加氧酶(cox)和氢过氧化物酶,并且诱导人类前髓细胞性白血病的细胞分化。此外,如上文所指出,白藜芦醇与红葡萄酒的心血管效用的相关性已得到充分研究。也已经提出白藜芦醇的神经学用途。
考虑到白藜芦醇呈现的多种有益生理学作用,已经有很多项目聚焦于获得改善其健康相关特性的这种分子的衍生物。文献国际免疫药理学(int.immunopharmacology)25(2015)528-537探究了各种白藜芦醇衍生物的消炎特性和其用作神经炎症抑制剂的潜在性。
医药化学杂志(j.med.chem)2010年7月8日;53(13):5033-5043描述了硫酸化白藜芦醇衍生物的合成和其对各种生理学活性的影响,例如抑制tnf-α或环加氧酶活性。
文献wo2011/073482描述了含有糖类取代基的白藜芦醇衍生物,其具有调节炎症、尤其肠病变(例如大肠急躁症或克罗恩氏病(crohn'sdisease))的能力。
技术实现要素:
在第一方面中,本发明涉及式(i)化合物的用途:
其中r1、r2和r3独立地选自h、sir4r5r6基团、-nh(co)r7基团,或碳水化合物,
其中r4、r5和r6独立地选自直链或分支c1-c6烷基或苯基且r7是直链或分支c1-c12烷基,
限制条件为r1、r2和r3中的至少一个是sir4r5r6基团,
其用于制造供治疗或预防发炎、神经或神经变性疾病的药剂。
在一个优选实施例中,r1和r2是sir4r5r6基团。在一个更优选实施例中,r3是h。
在另一个更优选实施例中,r3是-nh(co)r7。
在另一个更优选实施例中,r3是以下碳水化合物:
其中r8是选自h或-c(o)-r9,其中r9是c1-c22烷基或c2-c22烯基。
在一个更优选实施例中,当r1和r2是sir4r5r6基团时,r4和r5是甲基,并且r6是叔丁基。在另一个更优选实施例中,r4、r5和r6是乙基。在另一个更优选实施例中,r4、r5和r6是异丙基。
在一个优选实施例中,r1和r3是sir4r5r6基团。
在一个更优选实施例中,r2是h。
在另一个更优选实施例中,r2是-nh(co)r7。
在另一个更优选实施例中,r2是以下碳水化合物:
其中r8是选自h或-c(o)-r9,其中r9是c1-c22烷基或c2-c22烯基。
在一个更优选实施例中,当r1和r3是sir4r5r6基团时,r4和r5是甲基,并且r6是叔丁基。在另一个更优选实施例中,r4、r5和r6是乙基。在另一个更优选实施例中,r4、r5和r6是异丙基。
在另一个更优选实施例中,r1、r2和r3是sir4r5r6基团。
在一个更优选实施例中,当r1、r2和r3是sir4r5r6基团时,r4和r5是甲基,并且r6是叔丁基。在另一个更优选实施例中,r4、r5和r6是乙基。在另一个更优选实施例中,r4、r5和r6是异丙基。
在另一个优选实施例中,式(i)化合物选自以下群组:
在一个优选实施例中,神经或神经变性疾病选自阿尔茨海默氏病(alzheimer'sdisease)、帕金森氏病(parkinson'sdisease)、亨廷顿氏病(huntington'sdisease)、多发性硬化症、肌肉萎缩性侧索硬化症、额颞叶型痴呆症、局部缺血和癫痫症。
本发明的另一个方面涉及式(i')化合物:
其中r1、r2和r3独立地选自h、sir4r5r6基团、-nh(co)r7基团,或碳水化合物,
其中r4、r5和r6独立地选自直链或分支c1-c6烷基或苯基且r7是直链或分支c1-c12烷基,
限制条件为r1、r2和r3中的至少一个是sir4、r5、r6基团且其不是以下化合物之一:
-(e)-(5-(4-(三甲基硅烷氧基)苯乙烯基)-1,3-亚苯基)双(氧基)双(三甲基硅烷),
-(e)-4-(3,5-双(三异丙基硅烷氧基)苯乙烯基)苯酚,
-(e)-3-(叔丁基二甲基硅烷氧基)-5-(4-(叔丁基二甲基硅烷氧基)苯乙烯基)苯酚,
-(e)-4-(3,5-双(叔丁基二甲基硅烷氧基)苯乙烯基)苯酚,
-(e)-3-(叔丁基二甲基硅烷氧基)-5-(4-羟基苯乙烯基)苯酚,
-(e)-5-(4-(叔丁基二甲基硅烷氧基)苯乙烯基)苯-1,3-二醇,
-(e)-(5-(4-(叔丁基二甲基硅烷氧基)苯乙烯基)-1,3-亚苯基)双(氧基)双(叔丁基二甲基硅烷)。
在一个优选实施例中,r1和r2是sir4r5r6基团。
在一个更优选实施例中,r3是h。
在另一个更优选实施例中,r3是-nh(co)r7。
在另一个更优选实施例中,r3是以下碳水化合物:
其中r8是选自h或-c(o)-r9,其中r9是c1-c22烷基或c2-c22烯基。
在一个更优选实施例中,当r1和r2是sir4r5r6基团时,r4和r5是甲基,并且r6是叔丁基。在另一个更优选实施例中,r4、r5和r6是乙基。在另一个更优选实施例中,r4、r5和r6是异丙基。
在一个优选实施例中,r1和r3是sir4r5r6基团。
在一个更优选实施例中,r2是h。
在另一个更优选实施例中,r2是-nh(co)r7。
在另一个更优选实施例中,r2是以下碳水化合物:
其中r8是选自h或-c(o)-r9,其中r9是c1-c22烷基或c1-c22烯基。
在一个更优选实施例中,当r1和r3是sir4r5r6基团时,r4和r5是甲基,并且r6是叔丁基。在另一个更优选实施例中,r4、r5和r6是乙基。在另一个更优选实施例中,r4、r5和r6是异丙基。
在另一个优选实施例中,r1、r2和r3是sir4r5r6基团。
在一个更优选实施例中,当r1、r2和r3是sir4r5r6基团时,r4和r5是甲基,并且r6是叔丁基。在另一个更优选实施例中,r4、r5和r6是乙基。在另一个更优选实施例中,r4、r5和r6是异丙基。
在取代基是sir4r5r6基团的另一个更优选实施例中,r4和r5苯基,并且r6是叔丁基。并且在另一个更优选实施例中,r4、r5和r6是甲基。
在另一个优选实施例中,式(i')化合物选自以下群组:
本发明的另一个方面涉及上述式(i')化合物用于制造药剂的用途。
本发明的另一方面涉及一种医药组合物,其包含如上文所述的式(i')化合物。
本发明的另一方面涉及一种治疗发炎、神经或神经变性疾病的方法,其包含向有需要的患者投与治疗有效量的式(i)或(i')化合物。
在本说明书所使用的含义中,术语“治疗有效量”是指足以产生所期望作用、减轻疾病症状的活性化合物的量。剂量不应按导致非所需副作用的比例使用,所述副作用的临床评估使得其不利且在治疗上是无法治疗的。剂量通常根据患者的年龄、状况、性别和疾病程度以及施药途径和频率而变,并且能基于各种情况来确定。
在本发明中,术语“烷基”是指具有1到22个,优选1到12个并且更优选1到6个碳原子的直链或分支烃链基团,并且其通过单键结合到分子的其余部分,例如丙基、乙基、甲基、异丙基、十一烷酰基、十七烷酰基、十八烷酰基等。这些烷基可以任选地在一个或多个位置被一个或多个基团(例如羟基、胺、酰胺、氧代、氰基、卤素、芳基等)取代。
在本发明中,术语“烯基”是指具有2到22个碳原子且不饱和度在1与6之间(取决于碳数目)的不饱和直链或分支脂肪族链,包括(但不限于)乙烯基、烯丙基、油烯基、亚油烯基、二十碳五烯酰基、二十二碳六烯酰基等。这些烷基可以任选地在一个或多个位置被一个或多个基团(例如羟基、胺、酰胺、氧代、氰基、卤素、芳基等)取代。
由式(i)和(i')表示的本发明化合物,更具体地说,属于上述此通式的特定化合物可以包括异构体,这取决于多个键的存在(例如z、e),包括光学异构体或对映异构体,这取决于手性中心的存在。个别异构体、对映异构体或非对映异构体和其混合物落入本发明的范围内。个别对映异构体或非对映异构体以及其混合物可以使用常规技术分离。
本发明化合物可以呈游离化合物或溶剂化物的结晶形式,并且希望两种形式均落入本发明的范围内。在此意义上,如本文所用,术语“溶剂化物”包括药学上可接受的溶剂化物,即,能够用于制造药剂的式(i)或(i')化合物的溶剂化物;与药学上不可接受的溶剂化物,其可以用于制备药学上可接受的溶剂化物或盐。药学上可接受的溶剂合物的性质并非关键,只要其是药学上可接受的。在一个特定实施例中,溶剂化物是水合物。溶剂化物可以通过所属领域的技术人员熟知的常规溶剂化方法获得。
用于治疗时,式(i)或(i')化合物、其异构体、盐或溶剂化物优选呈药学上可接受的形式或实质性纯形式,即,其具有药学上可接受的纯度水平,不包括正常医药添加剂,例如稀释剂和载体,且不包括在正常给药水平下视为毒性的物质。活性物质的纯度水平优选大于50%,更优选大于70%,甚至更优选大于90%。在一个优选实施例中,式(i)或(i')化合物或其盐或溶剂化物的含量大于95%。
除非另外指明,否则本发明的化合物还包括不同之处仅为存在一个或多个同位素富集原子的化合物。举例来说,除氢被氘或被氚取代或碳被13c或14c富集的碳或15n富集的氮取代之外,具有所述结构的化合物属于本发明的范畴内。
用于治疗用途的式(i)或(i')化合物是在药学上可接受的稀释剂中制备为固体形式或水性悬浮液形式。这些制剂可以通过任何适当施药途径施用,为此目的,将制剂调配成适于所选施药途径的医药形式。举例来说,将式(i)或(i')化合物与赋形剂(例如淀粉或乳糖或佐剂,例如环糊精)以及所属领域的技术人员已知的用于制备固体或液体调配物的任何类型的药物载体合并。在一个特定实施例中,本发明提供的式(i)或(i')化合物是通过口服、局部、直肠或肠胃外(包括皮下、腹膜内、皮内、肌肉内、静脉内等)施用。药物施用的不同医药形式和为了获得其而必需的赋形剂的评述可以见于例如“tratadodefarmaciagalénica”[“草本制剂药剂学论文集”],c.faulíitrillo,1993,luzán5,s.a.ediciones,madrid,或西班牙、欧洲或美国药典的其它惯用或类似出版物中。
本发明中所述的化合物和其药学上可接受的盐和溶剂化物以及含有其的医药组合物能结合其它额外药物使用,以便提供组合疗法。这些额外药物可以是相同药物组合物的一部分,或可替代地,其可以单独组合物的形式提供,以便与包含式(i)或(i')化合物或其异构体、溶剂化物或药学上可接受的盐的医药组合物同时或非同时施用。
在通篇说明书和权利要求书中,表述“包含”和其变化形式不希望排除其它技术特点、添加剂、组分或步骤。所属领域的技术人员根据说明书且部分地根据本发明的实施将显而易知本发明的其它目标、优点和特点。以下实例和附图是为了说明而提供且不希望限制本发明的范围。
附图说明
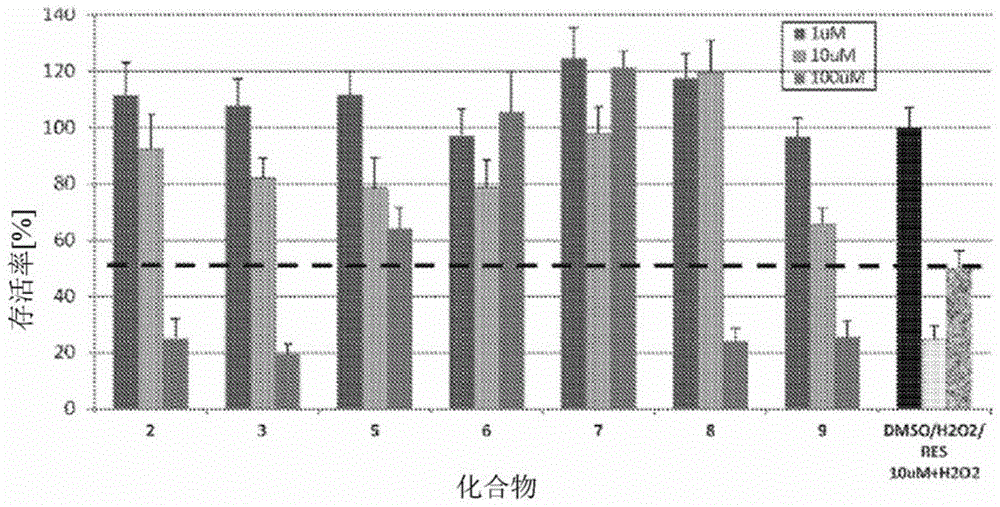
图1.h2o2损伤且用不同化合物2-9处理之后,神经母细胞瘤sh-sy5y的细胞存活率。对照物是dmso:1%dmso;h2o2:含h2o2的1%dmso;res10μm+h2o2:白藜芦醇/含h2o2的1%dmso。
图2.h2o2损伤且用不同化合物10-11处理之后,神经母细胞瘤sh-sy5y的细胞存活率。对照物是dmso:1%dmso;h2o2:含h2o2的1%dmso;res10μm+h2o2:白藜芦醇/含h2o2的1%dmso。
图3.h2o2损伤且用不同化合物12-13处理之后,神经母细胞瘤sh-sy5y的细胞存活率。对照物是dmso:1%dmso;h2o2:含h2o2的1%dmso;res10μm+h2o2:白藜芦醇/含h2o2的1%dmso。
图4.h2o2损伤且用不同化合物14-15处理之后,神经母细胞瘤sh-sy5y的细胞存活率。对照物是dmso:1%dmso;h2o2:含h2o2的1%dmso;res10μm+h2o2:白藜芦醇/含h2o2的1%dmso。
图5.h2o2损伤且用不同化合物16-20处理之后,神经母细胞瘤sh-sy5y的细胞存活率。对照物是dmso:1%dmso;h2o2:含h2o2的1%dmso;res10μm+h2o2:白藜芦醇/含h2o2的1%dmso。
图6.用lps产生炎症且用不同化合物2-9处理之后,raw巨噬细胞的细胞存活率。对照物是dmso:1%dmso;单独lps:lps(100ng/ml);lps+res10μm:lps(100ng/ml)+白藜芦醇。
图7.用lps产生炎症且用不同化合物10-11处理之后,raw巨噬细胞的细胞存活率。对照物是dmso:1%dmso;单独lps:lps(100ng/ml);lps+res10μm:lps(100ng/ml)+白藜芦醇。
图8.用lps产生炎症且用不同化合物12-13处理之后,raw巨噬细胞的细胞存活率。对照物是dmso:1%dmso;单独lps:lps(100ng/ml);lps+res10μm:lps(100ng/ml)+白藜芦醇。
图9.用lps产生炎症且用不同化合物14-15处理之后,raw巨噬细胞的细胞存活率。对照物是dmso:1%dmso;单独lps:lps(100ng/ml);lps+res10μm:lps(100ng/ml)+白藜芦醇。
图10.用lps产生炎症且用不同化合物16-20处理之后,raw巨噬细胞的细胞存活率。对照物是dmso:1%dmso;单独lps:lps(100ng/ml);lps+res10μm:lps(100ng/ml)+白藜芦醇。
图11.用lps使raw巨噬细胞发炎且用不同化合物2-9处理之后,培养基中的tnf-α浓度。
图12.用lps使raw巨噬细胞发炎且用不同化合物2-9处理之后,培养基中的no浓度。
图13.用lps使raw巨噬细胞发炎且用不同化合物2-9处理之后,培养基中的il6浓度。
图14.关于化合物res、6、8和9控制的ache活性。进行anova统计学检验,随后进行邓奈特多项比较试验(dunnett'smultiplecomparisontest)。当相对于对照物,#p<0.05;相对于对照物+ptz,*p<0.05,**p<0.01时,认为是显著的。
图15.关于化合物res、11、14、15和17控制的ache活性。进行anova统计学检验,随后进行邓奈特多项比较试验。当相对于对照物,#p<0.05;相对于对照物+ptz,*p<0.05,**p<0.01时,认为是显著的。
图16:实例6中进行的实验的设计示意图。
图17:a)用化合物res和15处理的各组小鼠的运动能力评估(四种运动参数的总和);b)用化合物res和15处理的各组小鼠在第5天的旋杆时间(秒);c)用化合物res和15处理的各组小鼠在第5天的平均体重;d)用化合物res和15处理的各组小鼠血浆中的介白素il-6含量。
图18:a)用化合物15和eae-t对照物预防性处理的各组小鼠的运动能力评估;b)用化合物res和不含t的eae对照物预防性处理的各组小鼠的运动能力评估;c)用化合物15和eae-t对照物治疗性处理的各组小鼠的运动能力评估;b)用res化合物和不含t的eae对照物治疗性处理的各组小鼠的运动能力评估。
具体实施方式
实例
本发明人将借助于证明本发明产物有效性而执行的测试来说明本发明。
实例1:白藜芦醇的硅烷基化衍生物的合成
硅烷化通用方法.
在搅拌下将白藜芦醇(1eq.)和咪唑(2.5eq.)添加到具有dmf(3ml/mmol白藜芦醇)的圆底烧瓶中并且冷却到0℃。相应的氯化硅烷(1,4-1,55eq.)然后分两批逐滴添加,第一半在0小时添加且第二半在3小时添加。在室温下搅拌反应物总共6小时。然后过滤反应混合物,在水中稀释,并且用乙酸乙酯(3×20ml)萃取。合并的有机相用mgso4脱水,过滤,浓缩至干燥,并且通过硅胶柱色谱提纯,其中洗脱是用己烷/乙酸乙酯混合物进行。
叔丁基二甲基硅烷基白藜芦醇衍生物系列.
依循通用方法,使用白藜芦醇(830mg,3.64mmol)和氯化叔丁基二甲基硅烷(849.55mg,5.64mmol),通过使用己烷/乙酸乙酯梯度(8:1到2:1)的柱色谱提纯反应混合物之后,除单硅烷化衍生物之外,还获得化合物1、2和3。
3,4',5-o-三-叔丁基二甲基硅烷基白藜芦醇,化合物1。产率=5.8%;rf=0.9(己烷:乙酸乙酯-7:3)。
3,4',-o-三-叔丁基二甲基硅烷白藜芦醇,化合物2。产率=22.1%;rf=0.65(己烷:乙酸乙酯-7:3)。
3,5,-o-三-叔丁基二甲基硅烷基白藜芦醇,化合物3。产率=6.4%;rf=0.55(己烷:乙酸乙酯-7:3)。
三异丙基硅烷基白藜芦醇衍生物系列.
依循通用方法,使用白藜芦醇(816mg,3.57mmol)和氯化三异丙基硅烷(1.19,5.54mmol),通过使用己烷/乙酸乙酯梯度(10:1到1:1)的柱色谱提纯反应混合物之后,除单硅烷化衍生物之外,还获得化合物4、5和6。
3,4',5-o-三-三异丙基硅烷基白藜芦醇,化合物4。产率=19.4%;rf=0.9(己烷:乙酸乙酯-3:1)。1hrmn(400mhz,cdci3):δ=7.47(d,j=8.3hz,2h),7.05(d,j=16.2hz,1h,ch),6.95(dd,j=12.4,6.4hz,3h,ch和h),6.74(s,2h,h2和h6),6.44(s,1h,h4),1.41-1.33(m,9h,ch-si),1.29-1.16(m,54h,ch3)。13crmn(101mhz,cdci3):δ=157.10,155.96,139.44,130.45,128.39,127.73,126.83,120.17,111.26,110.94,18.02,12.78。
3,4',-o-二-三异丙基硅烷基白藜芦醇,化合物5。产率=26.1%;rf=0.65(己烷:乙酸乙酯-3:1)。1hrmn(400mhz,cdci3):δ=7.34(d,j=8.2hz,2h),6.96(d,j=16.2hz,1h),6.83(t,j=12.0hz,3h),6.64(s,1h),6.55(s,1h),6.33(s,1h),1.30-1.22(m,6h),1.11(dd,j=16.0,7.4hz,36h)。13crmn(101mhz,cdci3):δ=158.14,157.12,155.68,139.63,130.56,127.98,127.47,126.57,119.77,109.57,106.15,106.06,17.40,17.37,17.10,12.62,12.59,12.32。tofms-es,质量计算值:c32h51o3si2[m-h]=539.3377,质量测量值:[m-h]=539.3390。
3,5,-o-二-三异丙基硅烷基白藜芦醇,化合物6。产率=8.7%;rf=0.5(己烷:乙酸乙酯-3:1)。
三乙基硅烷基白藜芦醇衍生物系列.
依循通用方法,使用白藜芦醇(809mg,3.54mmol)和氯化乙基硅烷(1.19,5.49mmol),通过使用己烷/乙酸乙酯梯度(10:1到1:1)的柱色谱提纯反应混合物之后,除单硅烷化衍生物之外,还获得化合物7、8和9。
3,4',5-o-三-三乙基硅烷基白藜芦醇,化合物7。产率=3.8%;rf=0.95(己烷:乙酸乙酯-3:1)。1hrmn(400mhz,cdci3):δ=7.40(d,j=8.5hz,2h),6.98(d,j=16.2hz,1h),6.90-6.82(m,3h),6.64(d,j=2.0hz,2h),6.31(t,j=2.0hz,1h),1.04(td,j=7.8,2.8hz,26h),0.78(q,j=7.9hz,18h)。13crmn(101mhz,cdci3):δ=156.61,155.45,139.48,130.60,128.44,127.73,126.76,120.17,111.41,110.93,6.66,5.03。质量计算值:c32h55o3si3[m+h]=571.3459,质量测量值:[m+h]=571.3460。
3,4',-o-三-三乙基硅烷基白藜芦醇,化合物8。产率=14.9%;rf=0.6(己烷:乙酸乙酯-3:1)。1hrmn(400mhz,cdci3):δ=7.40(d,j=8.6hz,2h),6.98(d,j=16.2hz,1h),6.91-6.82(m,3h),6.62(s,1h),6.61(s,1h),6.32(s,1h),1.09-1.02(m,18h),0.80(q,j=7.9hz,12h)。13crmn(101mhz,cdci3):δ=156.92,156.69,155.45,139.94,130.58,128.82,127.83,126.47,120.25,110.96,106.52,106.40,6.67,6.64,5.03。tofms-es+,质量计算值:c26h41o3si2[m+h]=457.2594,质量测量值:[m+h]=457.2593。
3,5,-o-三-三乙基硅烷基白藜芦醇,化合物9。产率=6.8%;rf=0.5(己烷:乙酸乙酯-3:1)。1hrmn(400mhz,cdci3):7.37(d,j=8.3hz,2h),6.96(d,j=16.2hz,1h),6.82(t,j=12.6hz,3h),6.63(s,2h),6.25(s,1h),1.02(t,j=7.9hz,18h),0.76(q,j=7.9hz,12h)。13crmn(101mhz,cdci3):δ=157.11,156.55,140.04,128.84,128.66,127.64,127.55,125.16,115.19,110.99,110.08,48.34,48.13,47.92,47.70,47.49,47.28,47.06,5.77,4.66。tofms-es+,质量计算值:c26h41o3si2[m+h]=457.2594,质量测量值:[m+h]=457.2586。
三异丙基硅烷基和乙基碳酰胺白藜芦醇衍生物.
将异氰酸乙酯(1.5eq.)和三乙胺(2eq.)添加到3,4'-二-三异丙基硅烷基白藜芦醇或3,5-二-三异丙基硅烷基白藜芦醇(1eq.)于二氯甲烷中的溶液中。在室温下反应1小时之后,浓缩反应物且在色谱柱上提纯,其中洗脱是用己烷:乙酸乙酯(2:1到0:1)进行。
氨基甲酸3,4',-o-二-三异丙基硅烷基-5-乙酯白藜芦醇,化合物10。产率=80.2%。rf=0.9(己烷:乙酸乙酯-5:1)。1hrmn(300mhz,cdci3):δ=7.39(d,j=8.5hz,2h),7.02(d,j=16.2hz,1h),6.89(dd,j=14.6,5.9hz,5h),6.60(s,1h),3.40-3.26(m,2h),1.30(ddd,j=10.6,7.4,3.7hz,9h),1.15(dd,j=7.0,3.1hz,36h)。13crmn(75mhz,cdci3):δ=157.04,156.29,152.30,139.75,130.38,129.38,128.01,126.25,120.39,115.12,112.30,36.38,18.21,18.18,17.97,15.40,12.95,12.93,12.57。tofms-es+,质量计算值:c35h57no4si2[m+h]=612.3904,质量测量值:[m+h]=612.3907。
氨基甲酸3,5,-o-二-三异丙基硅烷基-4-乙酯白藜芦醇,化合物11。产率=85.6%。rf=0.9(己烷:乙酸乙酯-5:1)。1hrmn(300mhz,cdci3):δ=7.51(d,j=8.0hz,2h),7.15(d,j=8.0hz,2h),7.01(d,j=16.4hz,1h),6.93(d,j=16.1hz,1h),6.67(s,2h),6.38(s,1h),3.41-3.28(m,2h),1.32-1.22(m,9h),1.15(d,j=7.2hz,36h)。rmnof13c(75mhz,cdci3):δ=157.31,157.25,139.15,128.14,128.00,127.59,121.99,116.20,116.04,112.17,111.61,111.38,45.95,36.41,18.20,12.95。tofms-es+,质量计算值:c35h57no4si2[m+h]=612.3904,质量测量值:[m+h]=612.3900。
三异丙基硅烷基葡糖基白藜芦醇衍生物系列.
在搅拌和惰性氩气气氛下,将3,4'-二-三异丙基硅烷基白藜芦醇或3,5-二-三异丙基硅烷基白藜芦醇(1eq.)溶解于15ml无水二氯甲烷中并且添加全乙酰基葡萄糖三氟乙酰亚胺酯(1.5eq.)和醚合三氟化硼(0.1eq.)。反应30分钟之后,添加5ml三乙胺,浓缩且添加到硅胶提纯柱中,其中洗脱是用己烷和乙酸乙酯(5:1)的混合物进行。将所得产物溶解于二氯甲烷、水和甲醇的混合物(5ml,2:1:2)中,并且添加碳酸氢钠(3eq.)。葡萄糖单元中的乙酸酯单元脱除保护基之后(24-48小时),浓缩反应物且通过柱色谱提纯,其中洗脱是用己烷:乙酸乙酯(1:1到1:3)进行。
3,4'-o-二-三异丙基硅烷基-5-葡糖基白藜芦醇,化合物12。产率=70.6%。rf=0.05(己烷:乙酸乙酯-1:3)。1hrmn(500mhz,cd3od):δ=7.43(d,j=8.6hz,2h),7.05(d,j=16.3hz,1h),6.98-6.89(m,2h),6.87(d,j=8.6hz,2h),6.70(s,1h),6.55(t,j=2.0hz,1h),4.92-4.88(m,1h),3.94-3.88(m,1h),3.75(dd,j=11.9,4.8hz,1h),3.52-3.38(m,4h),1.36-1.23(m,6h),1.18-1.10(m,36h)。13crmn(126mhz,cd3od):δ=158.94,156.93,155.80,139.83,130.51,128.55,127.51,126.04,119.69,111.96,107.30,107.07,101.13,76.86,76.59,73.48,69.90,61.01,17.05,16.99,12.53,12.51。tofms-es+,质量计算值:c38h62o8si2[m+na]=725.3881,质量测量值:[m+na]=725.3682。
3,5-o-二-三异丙基硅烷基-4'-葡糖基白藜芦醇,化合物13。产率=75.3%。rf=0.05(己烷:乙酸乙酯-1:3)。1hrmn(500mhz,cd3od):δ=7.48(d,j=8.7hz,2h),7.09(d,j=8.7hz,2h),6.95(q,j=16.3hz,3h),6.66(d,j=2.0hz,2h),6.32(t,j=2.1hz,1h),4.96-4.90(m,1h),3.91(dd,j=12.1,1.9hz,1h),3.73(dd,j=12.1,5.3hz,1h),3.51-3.47(m,2h),3.45(dd,j=5.0,1.7hz,1h),3.44-3.38(m,1h),1.31-1.23(m,6h),1.14(d,j=7.3hz,36h)。13crmn(126mhz,cd3od):δ=157.41,156.96,139.63,131.54,128.05,127.37,126.65,116.54,110.93,110.28,100.83,76.75,76.57,73.49,69.94,61.10,17.05,12.55.tofms-es+,质量计算值:c38h62o8si2[m+na]=725.3881,质量测量值:[m+na]=725.3907。
三异丙基硅烷基辛酰基-葡糖基白藜芦醇衍生物系列.
将3,4'-o-二-三异丙基硅烷基-5-葡糖基白藜芦醇或3,5-o-二-三异丙基硅烷基-4'-葡糖基白藜芦醇(1eq.)溶解于甲基叔丁基醚和辛酸乙烯酯(3eq.)和酶lypozymetl
3,4'-o-二-三异丙基硅烷基-5-(-6-辛酰基)葡糖基白藜芦醇,化合物14。产率=75.3%。rf=0.05(己烷:乙酸乙酯-1:3)。1hrmn(500mhz,cdci3):δ=1hnmr(500mhz,cdcl3)δ=7.37(d,j=8.5hz,2h),7.12(d,j=8.5hz,1h),6.98(d,j=16.1hz,2h),6.87(d,j=8.5hz,2h),6.75(s,1h),6.73(s,1h),4.94-4.87(m,1h),4.75-4.70(m,1h),4.59-4.48(m,2h),3.69-3.60(m,3h),1.28-1.25(m,18h),1.15-1.07(m,36h),0.91-0.89(m,3h)。13crmn(126mhz,cdci3):δ=171.07,139.75,130.16,127.72,126.19,120.16,119.68,115.09,112.90,109.58,107.50,106.00,104.78,102.13,100.89,66.80,60.38,45.71,38.73,34.00,31.91,30.40,29.69,29.35,28.91,24.47,23.78,22.68,21.03,20.82,17.94,17.89,17.86,14.18,14.10,12.67,12.62,12.54,10.96,8.76。tofms-es-,质量计算值:c46h76o9si2[m-h]=827.4950,质量测量值:[m-h]=827.4922。
3,5-o-二-三异丙基硅烷基-4'-(6-辛酰基)葡糖基白藜芦醇,化合物15。产率=15.5%。rf=0.07(己烷:乙酸乙酯-1:2)。1hrmn(300mhz,cdci3):δ7.45(d,j=8.5hz,2h),7.07(d,j=8.4hz,2h),6.93(q,j=16.2hz,2h),6.66(s,2h),6.37(s,1h),4.96(d,j=6.0hz,1h),4.43(m,2h),3.77-3.55(m,4h),2.36(t,j=7.5hz,2h),1.63(d,j=6.8hz,2h),1.29-1.24(m,8h),1.14(d,j=7.0hz,36h),0.92-0.84(m,3h)。13crmn(75mhz,cdci3):δ=174.78,157.28,139.28,132.63,127.93,117.30,111.52,74.32,73.59,34.47,31.88,29.97,29.36,29.17,25.12,22.84,18.18,14.29,12.94。tofms-es+,质量计算值:c46h76o9si2[m+na]=851.4926,质量测量值:[m+na]=851.4966。
具有酰基的三乙基硅烷基白藜芦醇衍生物系列.
将3,5-o-三乙基硅烷基白藜芦醇(9)(1eq.)溶解于叔丁醇中,且添加相应脂肪酸的乙烯基酯(6eq.)和novozyme
3,5-o-三乙基硅烷基-4'-丙酰基白藜芦醇,化合物16。产率=34.0%。rf=0.35(己烷:乙酸乙酯-8:1)。1hrmn(400mhz,cdci3):δ=7.37(d,j=8.3hz,2h),6.94(d,j=16.2hz,1h),6.87-6.73(m,3h),6.60(d,j=2.3hz,2h),6.28(t,j=2.1hz,1h),2.33(q,2h),1.66(t,3h),1.01(t,j=7.9hz,18h),0.75(q,j=7.9hz,12h)。13crmn(101mhz,cdci3):δ=180.10(co),156.55(2xcq),155.26(cq),139.39(cq),130.20(cq),128.24(芳香族ch),127.91(2x芳香族ch),126.60(芳香族ch),115.56(2x芳香族ch),111.38(2x芳香族ch),110.93(芳香族ch),29.67(ch2co),14.06(ch3ch2co),6.60(6xch2si),5.00(6xch3ch2si)。
3,5-o-三乙基硅烷基-4'-丁酰基白藜芦醇,化合物17。产率=39.0%。rf=0.29(己烷:乙酸乙酯-8:1)。1hrmn(400mhz,cdci3):δ=7.37(d,j=8.0hz,2h),6.93(d,j=16.2hz,1h),6.87-6.76(m,3h),6.60(d,j=2.2hz,2h),6.27(t,j=2.1hz,1h),2.34(t,2h),1.66(m,2h),1.00(t,j=7.9hz,18h),0.94(t,3h),0.74(q,j=7.9hz,12h)。13crmn(101mhz,cdci3):δ=179.26(co),156.55(2xcq),155.32(cq),139.40(cq),130.14(cq),128.25(芳香族ch),127.91(2x芳香族ch),126.56(芳香族ch),115.57(2x芳香族ch),111.38(2x芳香族ch),110.91(芳香族ch),29.65(ch2co),22.66(ch2ch3),14.06(ch3),6.60(6xch2si),4.99(6xch3ch2si)。
3,5-o-三乙基硅烷基-4'-己酰基白藜芦醇,化合物18。产率=66.0%。rf=0.29(己烷:乙酸乙酯-8:1)。1hrmn(400mhz,cdci3):δ=7.36(d,j=8.0hz,2h),6.93(d,j=16.2hz,1h),6.85-6.76(m,3h),6.59(d,j=2.2hz,2h),6.26(t,j=2.2hz,1h),2.33(t,j=7.5hz,2h),1.70-1.56(m,2h),1.32(m,2h),1.00(t,j=7.9hz,18h),0.92-0.84(m,3h),0.79-0.69(m,12h)。13crmn(101mhz,cdci3):δ=180.26(co),156.54(2xcq),155.39(cq),139.41(cq),130.07(cq),128.28(芳香族ch),127.88(2x芳香族ch),126.49(芳香族ch),115.57(2x芳香族ch),111.36(2x芳香族ch),110.88(芳香族ch),34.02(ch2co),31.16(ch2ch2),24.33(ch2ch2),22.24(ch2ch3),13.80(ch3),6.58(6xch2si),4.98(6xch3ch2si)。
3,5-o-三乙基硅烷基-4'-辛酰基白藜芦醇,化合物19。产率=63.0%。rf=0.25(己烷:乙酸乙酯-8:1)。1hrmn(400mhz,cdci3):δ=7.36(d,j=8.3hz,2h),6.93(d,j=16.3hz,1h),6.87-6.72(m,3h),6.59(d,j=2.2hz,2h),6.26(t,j=2.2hz,1h),2.33(t,j=7.5hz,2h),1.62(q,j=7.4hz,2h),1.29(m,8h),1.00(t,j=7.9hz,18h),0.86(t,j=6.6hz,3h),0.74(q,j=7.9hz,12h)。13crmn(101mhz,cdci3):δ=180.38(co),156.54(2xcq),155.43(cq),139.40(cq),130.04(cq),128.27(charom),127.87(2xcharom),126.48(charom),115.56(2xcharom),111.34(2xcharom),110.87(charom),34.07(ch2co),31.58(ch2ch2),28.97(ch2ch2),28.85(ch2ch2),24.64(ch2ch2),22.54(ch2ch3),13.98(ch3),6.58(6xch2si),4.98(6xch3ch2si)。
3,5-o-三乙基硅烷基-4'-癸酸白藜芦醇,化合物20。产率=89.0%。rf=0.25(己烷:乙酸乙酯-8:1)。1hrmn(400mhz,cdci3):δ=7.36(d,j=8.2hz,2h),6.93(d,j=16.2hz,1h),6.88-6.74(m,3h),6.59(d,j=2.2hz,2h),6.26(t,j=2.2hz,1h),2.33(t,j=7.5hz,2h),1.62(q,j=7.4hz,2h),1.41-1.18(m,12h),1.00(t,j=7.9hz,18h),0.86(t,j=6.8hz,3h),0.74(q,j=7.8hz,12h)。13crmn(101mhz,cdci3):δ=180.43(co),156.54(2xcq),155.48(cq),139.42(cq),,130.00(cq),128.30(芳香族ch),127.86(2x芳香族ch),126.44(芳香族ch),115.57(2x芳香族ch),111.34(2x芳香族ch),110.86(芳香族ch),34.08(ch2co),31.82(ch2ch2),29.35(ch2ch2),29.21(ch2ch2),29.20(ch2ch2),29.02(ch2ch2),24.64(ch2ch2),22.62(ch2ch3),14.02(ch3),6.57(6xch2si),4.98(6xch3ch2si)。
实例2:存活率和神经保护分析.
在胶原蛋白(100ng/ml)预处理的皮氏培养皿中培养sh-sy5y神经母细胞瘤细胞系,所述培养皿含有补充有青霉素/链霉素和10%失活胎牛血清的f12培养基。
在胶原蛋白预处理的96孔板中如下准备神经元细胞存活率分析:以100μl体积每孔接种20,000个细胞且培育细胞24小时后,添加化合物。将待测试的化合物溶解于dmso中并且按照三种不同浓度(1、10和100μm)添加,以便测定其毒性。将每个孔中的dmso最终百分比调节到1%。添加化合物之后的第24小时,借助于mtt分析,根据制造商方法来评估细胞存活率。计算若干独立实验的至少八个不同测量值的平均值和标准差。
为了进行神经保护分析,按照与细胞存活率分析相同的方式培养神经元并且接种。将待测试的化合物溶解于dmso中并且按照三种不同浓度(1、10和100μm)添加,并且在培育10分钟之后,将过氧化氢(100μm)添加到培养基中。将每个孔中的dmso最终百分比调节到1%。添加化合物之后的第24小时,借助于mtt分析,根据制造商方法来评估细胞存活率。计算若干独立实验的至少八个不同测量值的平均值和标准差。添加本发明化合物和h2o2之后,通过将神经元存活率实验的结果相对于各实验的阳性对照组(神经元+h2o2)归一化来计算神经元恢复率。
观察到res10μm对照组的细胞存活率恢复到最多50%(图1到5,由虚线指示)。相比之下,本发明的许多硅烷基化衍生物在1μμ到100μμ的浓度下使存活率恢复80%到120%。有些在100μμ下似乎呈现毒性。
实例3:炎症分析.
用p75和补充有青霉素/链霉素和10%失活胎牛血清的高葡萄糖dmem培养raw264.7巨噬细胞。
在96孔板中如下准备raw巨噬细胞的细胞存活率分析:以100μl体积每孔接种25,000个细胞并且培育细胞4小时,随后添加化合物。将待测试的化合物溶解于dmso中并且按照三种不同浓度(1、10和100μm)添加,以便测定其毒性。将每个孔中的dmso最终百分比调节到1%。添加化合物之后的第24小时,借助于mtt分析,根据制造商方法来评估细胞存活率。计算若干独立实验的至少八个不同测量值的平均值和标准差。
为了测试因添加lps而引起的损伤缓解,根据上述程序培养raw264.7巨噬细胞。将待测试的化合物溶解于dmso中并且按照三种不同浓度(1、10和100霱)添加,并且在培育10分钟之后,将lps(100ng/ml)添加到培养基中。将每个孔中的dmso最终百分比调节到1%。添加化合物之后的第24小时,借助于mtt分析,根据制造商方法来评估细胞存活率。计算若干独立实验的至少八个不同测量值的平均值和标准差。
在此分析中,观察到10μm白藜芦醇对照组恢复到最多62%的细胞存活率(图6到10,虚线所示)。相比之下,本发明的若干硅烷基化衍生物在1μμ到100μμ的浓度下使细胞存活率得到更大的恢复。有些在100μμ下似乎呈现毒性。
实例4:在使用lps的分析中测量炎症参数
为了测定细胞因子的产生,将5×105个raw264.7巨噬细胞接种于24孔板(每孔0.5ml)中。然后添加待测试的化合物(10μm),且通过或不通过添加lps(1μg/ml)到培养基中来刺激刺激巨噬细胞。24小时之后,使用得自bdpharmingen和prepotech的捕捉抗体和生物素标记的抗体,依循已知方案,通过elisa测量上清液中的il-6和tnf-α含量。根据已确立的方案,使用格瑞斯试剂(griessreagent),通过测定培养基中的亚硝酸盐浓度来间接测量24小时时上清液中的no含量。每个测量值最少进行两个独立实验且每个实验重复三次。数值按照平均值±标准差表示。
在前述分析中,用res或用本发明化合物中的一些(2、3、5、6、8和9)处理之后,通过elisa测量各种炎症参数的水平(tnf-α、no和il-6)。
观察到res10μm的控制使炎症参数(tnf-α、no和il-6)显著减小(分别为图11、12和13,如粗体条形图所示)。相比之下,本发明的若干硅烷基化衍生物改善res且甚至进一步降低这些参数。
实例5:评估各种硅烷基化化合物在戊烯四唑(ptz)诱导的斑马鱼幼体神经变性模型中的神经保护能力。
此分析的目标是分析白藜芦醇的各种衍生物在神经毒素戊烯四唑(ptz)诱导的神经毒性模型中的保护作用。作为实验模型,使用斑马鱼(daniorerio)研究化合物对生育后(dpf)第5天的幼体中的乙酰胆碱酯酶活性(ache)的影响。
对斑马鱼中枢神经系统(cns)的研究表明,在发育24小时时,胚脑已经分节并且已经具有一些结构,例如神经管、脊索和体节(肌肉,和骨骼前体)。生育后第5天时(5dpf),动物已形成有感觉器官,例如眼和耳石。另外,心脏、肝脏、肾脏和胰腺以及循环、消化和神经系统均具有完全功能。此时,动物能够对视觉、嗅觉和机械刺激作出反应且开始搜索食物。
将斑马鱼胚接种于培养皿中的50ml稀释水(ad)中且生长到5dpf(幼体期)。仅使用不展现任何外部异常类型的那些幼体进行分析。接着,使用巴斯德移液管(pasteurpipette)将幼体转移到24孔微量培养板中,使得每个孔含有五个幼体,每种条件重复十次。首先,对5dpf幼体进行预处理。为此,将幼体在26±1℃下在体积2ml的ad(作为两个对照组(对照物和对照物+ptz))、20μm毒扁豆碱(phys)(毒扁豆碱是phys组的酶ache的商用抑制剂)和10μm浓度的测试化合物中培育1小时。然后更换培养基,并且将幼体和化合物与5mmptz的组合一起在26±1℃下培育6小时。这个培育期之后,检查所有幼体,且确定幼体的全身状态完全正常而无任何可见的异常或反常行为。最后,处理幼体以便分析ache活性。
为了测定ache水平,一旦完成实验期,即根据已确立的技术研究方案进行幼体处理。对幼体进行机械均质化,且将样品离心以获得上清液,所述上清液用于测定ache酶含量与所施处理的关系。另外,根据已确立的技术研究方案测定各实验组的总蛋白质。最后,对照组中所测定的ache水平取作参考测量值且视为100%。
此分析的结果表明,硅烷基化衍生物9(3,5-二-三乙基硅烷基白藜芦醇)和15(3,5-o-二-三异丙基硅烷基-4'-(6-辛酰基)葡糖基白藜芦醇)显著地阻止ptz诱导5dpf幼体中的ache活性减少,从而展现明显的神经保护作用(参见图14和15)。硅烷基化衍生物8、14和17展示较低的神经保护作用,类似于针对白藜芦醇(res)所观察到的作用。
实例6:用亨廷顿氏病动物模型测试化合物15
化合物15作为一种可能的疗法在小鼠亨廷顿氏病模型中探究。化合物白藜芦醇(res)作为参考物添加。
在这个模型中,将增加量的3-硝基-丙酸(3np)注射到小鼠中,从而产生表型在机械方式上和病理学上非常类似于亨廷顿氏病表型的病灶。一旦引起损伤,则用res、化合物15或媒剂处理小鼠,并且我们基于不同参数研究其对小鼠的影响。在行为研究(旋杆测试)中,评估运动能力(按照若干参数(例如小鼠全身肌张力障碍、翻转能力和探索能力)正常0到无能力4的量表列表),监测体重,且随后获取测量值,例如血浆或脑中的促炎性细胞因子抑制的测量值。
实验设计展示于图16中。#=行为研究和旋杆测试;φ化合物施用;w=小鼠周龄;d=实验天数。
结果展示于图17中。在所有情况下,观察化合物15怎样才能够改善3np引起的表型,改善是通过降低运动神经病灶的严重程度或促炎性细胞因子(例如il-6)的含量或增加动物体重。化合物15与res之间的差异不大,可能是因为这个动物模型短暂并且极具侵害性。测试化合物15在神经元、运动神经和炎症损伤较慢且更具渐进性的模型中是合理的,因为其更接近患者的现实,且因为治疗在更具渐进性的模型中的效率可能高得多。
实例7:对化合物15在动物多发性硬化症模型中进行测试
化合物15作为一种可能的疗法在小鼠多发性硬化症模型中探究。化合物白藜芦醇(res)作为参考物添加。实验过敏性脑脊髓炎模型eae用作多发性硬化症的动物模型。
在这个模型中,向小鼠注射髓鞘少突胶质细胞糖蛋白(mog,mog35-55,是对应于mog糖蛋白的位置35到55序列的21胺基酸肽)和病毒百日咳(百日咳毒素,ptx)以便诱发疾病。诱导之后的第2天,再次给予新剂量的病毒,原因是有些小鼠不呈现eae症状。一旦引起损伤,则用res、化合物15或媒剂处理小鼠,并且我们基于正常0到无能力4量表的不同运动神经参数来研究其对小鼠的影响。
实验设计如下所示:
实验组:
-不含吐温-80乳化剂的媒剂(不含t的对照eae)
-含有吐温-80乳化剂的媒剂(eae-t对照物)
-预防性res(不含吐温-80乳化剂)(res-prev)
-治疗性res(无吐温-80乳化剂)(res-terap)
-预防性化合物15(含有吐温-80乳化剂)(化合物15-prev)
-治疗性化合物15(含有吐温-80乳化剂)(化合物15-terap)
-预防性疗法(治疗前.prev):诱导之后的第5天开始(腹膜内)施用化合物(白藜芦醇、化合物15,和媒剂,含有或不含有吐温-80)。注射250μl所讨论的化合物(20mg/kg),一周两次且所述疗法维持3周。然后停止治疗,但小鼠状态另外监测3周(总共47天)。
-治疗性疗法(治疗.terap):诱导之后的第12天开始(腹膜内)施用化合物(白藜芦醇、化合物15,和媒剂,含有或不含有吐温-80)。注射250μl所讨论的化合物(20mg/kg),一周两次且所述疗法维持2周。然后停止治疗,但小鼠状态另外监测3周(总共47天)。
进行预防性疗法(参见图18a和18b)时,观察到化合物15对运动能力不具有较大影响(a)。另一方面,通过这种预防性疗法,res确实减小对运动水平的损害(b)。
进行治疗性疗法(参见图18c和18d)时,相较于对照组,观察到化合物15使小鼠运动能力的临床分类改善,尤其在测试的第20-30天之间(施用化合物的第二周)。还惊人的是,当药物施用已中断时,临床分类的这种改善在第30到47天期间得到维持。相比之下,小鼠就治疗模式中施用res时所产生的损伤而言似乎未改善。
还应该强调,吐温-80乳化剂本身似乎具有药理学作用(参见预防性治疗组的控制情况,a相对于b),其至少部分地遮蔽化合物15在减少多发性硬化症模型损伤中的可能影响。
重要的是注意到,施用20mg/kg的每种化合物(res和化合物15),但鉴于两种化合物的分子量存在较大差异(mw化合物15=3xmwres),因此施用剂量并非相当的。因此,res的
- 还没有人留言评论。精彩留言会获得点赞!