一种水溶性强酸可变色的偶氮-蒽醌类pH探针及其制备和应用的制作方法
本发明属于ph探针及其制备和应用领域,特别涉及一种水溶性强酸可变色的偶氮-蒽醌类ph探针及其制备和应用。
背景技术:
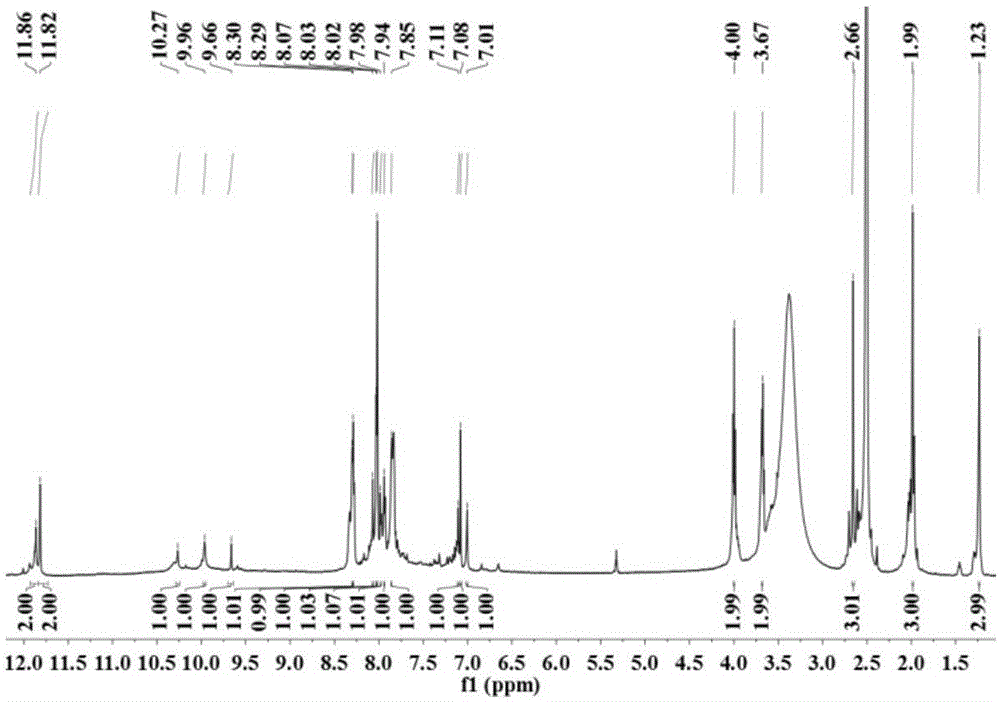
:ph值作为酸度的衡量指标,其快速准确的测量在生物工程、环境监测,生态保护、医疗诊断等过程中都显得尤为重要。ph试纸测量法,电极法和传感器是目前测定ph值的主要方法。其中,ph试纸测量法,存在主观因素带来的误差。电极法虽然在准确度上有了较大的提高,但易受电化学干扰、金属离子干扰,易机械损伤,存在强酸强碱测定时误差大,以及不适于活体ph值检测等缺陷。荧光探针类的光化学传感器是目前研究的最多的一类ph值测定方法,因具有选择性好、灵敏度高、试样量小等特点而广受研究者的青睐,但是,荧光传感器测量法对ph的检测需要复杂的光学器件,且易受环境的干扰,此类ph值传感器很难完成实时检测。目前大多说传感器均是可用于监测弱酸到弱碱性环境,适用于强酸性环境监测的传感器较少,现有的检测方法无论是荧光探针方法、ph试纸测量法,ph计测量法在强酸性溶液中都存在一系列问题,例如检测不灵敏,误差大,操作麻烦等。因此,发展一类简便可行,可实现实时检测的强酸性ph探针仍是一个重要的研究方向。技术实现要素:本发明所要解决的技术问题是提供一种水溶性强酸可变色的偶氮-蒽醌类ph探针及其制备和应用,克服了现有技术中如ph试纸、电极法存在的误差大及荧光探针类传感器不能实时监测的缺陷,该方法无需借助复杂光学器件,直接通过肉眼观察便可快速检测溶液的ph值,且制备工艺简单,成本廉价。本发明的一种如下通式的水溶性强酸可变色的偶氮-蒽醌类ph探针,式中,其中n、x、y为0,1,2或3。所述为:本发明的一种所述水溶性强酸可变色的偶氮-蒽醌类ph探针的制备方法,包括:(1)将打浆均匀的三聚氯氰中加入p-3r色基溶液,在0~10℃,ph值小于6.0的条件下,反应2~4h,得到一次缩合液;其中,p-3r色基为1-氨基-2-磺酸-4-(3-氨基-2,4,6-三甲基-5-磺酸苯氨基)蒽醌钠盐,三聚氯氰与p-3r色基的摩尔比为1:0.98~1:1;(2)将2,4-二氨基苯磺酸加入一次缩合液中,调整反应液ph值至2.5~4.5,升温至25℃~45℃,反应3-5h,得到二次缩合液;其中,2,4-二氨基苯磺酸与三聚氯氰的摩尔比为0.98:0.99~0.98:1;(3)将芳香族伯胺溶于水,得到芳香族伯胺溶液,加入酸,搅拌,在1h内滴入亚硝酸钠溶液,滴完后-5~0℃条件下反应1-2h,得到重氮盐;其中芳香族伯胺溶液质量分数为10%~30%,芳香族伯胺与步骤(1)中p-3r色基的摩尔比为0.98:0.99~0.98:1;(4)将步骤(2)中的二缩液降温至5℃以下,然后加入(3)中的重氮盐,调节ph值1.5~5.5,在0~5℃下反应2-4h,然后再在室温条件下反应2~3h,达到偶合终点;进行盐析、提纯,得到水溶性强酸可变色的偶氮-蒽醌类ph探针。上述制备方法的优选方式如下:所述步骤(1)中打浆均匀的三聚氯氰为:质量百分浓度为15-25%的三聚氯氰溶液,在0-2℃条件下于冰水中打浆0.1-0.5h。所述步骤(1)中p-3r色基溶液的质量分数为10%~20%,并调节ph值为5.8~6.5。所述步骤(3)中芳香族伯胺为中的一种,其中n、x、y为0,1,2或3。所述当芳香族伯胺中的r2基团为吸电子基,如-no2、-so3na、-so2ch2ch2oso3na时,重氮化时所用的酸为浓硫酸,芳香族伯胺、浓硫酸与亚硝酸钠的摩尔比为0.98:0.98:1.01-0.98:1.5:1.01。当r2为供电子基och3和ch3时,重氮化时所用的酸为浓盐酸,芳香族伯胺、浓盐酸与亚硝酸钠的摩尔比为0.98:0.98:1.01-0.98:2:1.01。所述步骤(4)中盐析为按反应结束时总液量的10%称取kcl进行盐析,抽滤烘干;提纯为:将盐析所得染料分散于无水乙醇与蒸馏水的混合物中,进行重结晶,快速抽滤,滤去盐及有机小分子,得到滤饼,真空干燥得成品;其中无水乙醇与水的体积比为2:1。本发明提供一种所述水溶性强酸可变色的偶氮-蒽醌类ph探针在探测酸性环境中ph的应用,直接通过裸眼识别溶液颜色的变化快速检测出ph值。本发明还提供一种所述水溶性强酸可变色的偶氮-蒽醌类ph探针在生物工程、环境监测,生态保护、医疗诊断中的应用。有益效果(1)本发明探针可用于检测的强酸溶液的ph,ph探针的检测线为0.5-4,与现有的检测方法相比,在强酸性条件下例如小于2以下,检测准确,信号明确,本发明的用作ph探针的偶氮-蒽醌类水溶性化合物制备工艺简单,成本低;(2)本发明的用作ph探针的偶氮-蒽醌类水溶性化合物检测溶液ph时无需借助复杂光学器件,直接通过肉眼观察便可快速检测溶液的ph值,既保留了传统比色检测简便、易读的优点,又实现了大多数荧光探针无法达到的实时检测的效果;(3)本发明的用作ph探针的偶氮-蒽醌类水溶性化合物用于强酸溶液的ph值的检测;(4)本发明的用作ph探针的偶氮-蒽醌类水溶性化合物用于溶液ph检测时具有可逆性;(5)本发明的用作ph探针的苯并噻唑类水溶性化合物用于溶液ph检测时几乎不受金属离子的影响。附图说明图1是结构式为实施例1中探针的核磁共振氢谱图;图2是结构式为实施例2中探针的核磁共振氢谱图;图3是结构式为实施例3中探针的核磁共振氢谱图;图4是结构式为实施例4中探针的核磁共振氢谱图;图5是实施例6中探针在不同ph的水溶液中的紫外吸收光谱图;插图为肉眼观察不同ph值溶液的颜色的照片;图6为实施例7中探针在不同ph的水溶液中的紫外吸收光谱图;插图为肉眼观察不同ph值溶液的颜色的照片;图7为实施例8中探针在不同ph的水溶液中的紫外吸收光谱图;插图为肉眼观察不同ph值溶液的颜色的照片;图8为实施例9中探针在不同ph的水溶液中的紫外吸收光谱图;插图为肉眼观察不同ph值溶液的颜色的照片。具体实施方式下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。实施例1结构如下的偶氮-蒽醌类ph探针的合成工艺:(1)一缩物的制备:18.6g(0.1mol)三聚氯氰配置成20%(质量百分浓度)的溶液,在0~2℃条件下于冰水浴中打浆0.5h。准确称取52.61g(0.099mol)1-氨基-2-磺酸-4-(3-氨基-2,4,6-三甲基-5-磺酸苯氨基)蒽醌单钠盐配成15%的溶液,调节ph值为5.8~6.5,溶解液为蓝色澄清溶液,在0~5℃条件下1h内滴加到打浆均匀的三聚氯氰中,滴加完毕后保持温度5℃,ph值4~4.5反应3h,薄层色谱法检测一缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:3)。(2)二缩物的制备:准确称取18.42g(0.098mol)2,4-二氨基苯磺酸干粉,一次加入到步骤(1)制备好的一次缩合液中,调整反应液ph值至2.5~3.5,升温至25℃~30℃,反应3~5h,薄层色谱法(tlc)检测二缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:4),得到蓝色二次缩合液,反应结束后降温至5℃备用。(3)重氮盐的制备:准确称取27.54g(0.098mol)4-硫酸乙酯砜基苯胺,配置成质量分数为20%的水溶液,搅拌0.5h至混合均匀后降温至0~5℃,一次性加入9.8g(0.098mol)质量分数为37.5%的浓盐酸,搅拌10min,之后在1h内缓慢滴入6.969g(0.101mol)亚硝酸钠水溶液,滴完后-5~0℃条件下反应2h,反应完后用氨基磺酸消除过量的亚硝酸。(4)偶合反应:将步骤(2)中的二缩液降温至5℃以下,然后加入(3)中制备好的重氮盐,调节ph值1.5~5.5,在0~5℃下反应4h,然后再在室温条件下反应2~3h,薄层色谱法(tlc)检测偶合反应终点(展开剂为:正丁醇:乙醇:水=7:2:3),将得到的产物在65℃温度下烘干。(5)盐析:按反应结束时总液量的10%称取kcl进行盐析,抽滤烘干得偶氮-蒽醌ph探针粗品,得到染料的产率为82.14%。(6)提纯:将盐析所得染料分散于无水乙醇与蒸馏水的混合物中,进行重结晶,快速抽滤,滤去盐及有机小分子,得到滤饼,真空干燥得ph探针纯品。其核磁共振氢谱见图1,1hnmr(dmso,δh,ppm):11.86(s,2h,-nh2),11.82(s,2h,-nh2),10.27(s,1h,-nh),9.96(s,1h,-nh),9.66(s,1h,-nh),8.30(d,1h,ar-h),8.29(d,1h,ar-h),8.07(s,1h,ar-h),8.03(s,1h,ar-h),8.02(d,1h,ar-h),7.98(d,1h,ar-h),7.94(d,1h,ar-h),7.85(t,1h,ar-h),7.11(s,1h,ar-h),7.08(s,1h,ar-h),7.01(s,1h,ar-h),4.00(t,2h,-ch2-),3.67(t,2h,-ch2-),2.66(s,3h,-ch3),1.99(s,3h,-ch3),1.23(s,3h,-ch3)。实施例2结构如下的偶氮-蒽醌类ph探针的合成工艺:(1)一缩物的制备:18.6g(0.1mol)三聚氯氰配置成20%(质量百分浓度)的溶液,在0~2℃条件下于冰水浴中打浆0.5h。准确称取52.61g(0.099mol)1-氨基-2-磺酸-4-(3-氨基-2,4,6-三甲基-5-磺酸苯氨基)蒽醌单钠盐配成15%的溶液,调节ph值为5.8~6.5,溶解液为蓝色澄清溶液,在0~5℃条件下1h内滴加到打浆均匀的三聚氯氰中,滴加完毕后保持温度5℃,ph值4~4.5反应3h,薄层色谱法检测一缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:3)。(2)二缩物的制备:准确称取18.42g(0.098mol)2,4-二氨基苯磺酸干粉,一次加入到步骤(1)制备好的一次缩合液中,调整反应液ph值至2.5~3.5,升温至25℃~30℃,反应3~5h,薄层色谱法(tlc)检测二缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:4),得到蓝色二次缩合液,反应结束后降温至5℃备用。(3)重氮盐的制备:准确称取16.95g(0.098mol)对氨基苯磺酸,配置成质量分数为25%的水溶液,搅拌0.5h至混合均匀后降温至0~5℃,一次性加入9.8g(0.098mol)质量分数为37.5%的浓盐酸,搅拌10min,之后在1h内缓慢滴入6.969g(0.101mol)亚硝酸钠水溶液,滴完后-5~0℃条件下反应2h,反应完后用氨基磺酸消除过量的亚硝酸。(4)偶合反应:将步骤(2)中的二缩液降温至5℃以下,然后加入(3)中制备好的重氮盐,调节ph值1.5~5.5,在0~5℃下反应4h,然后再在室温条件下反应2~3h,薄层色谱法(tlc)检测偶合反应终点(展开剂为:正丁醇:乙醇:水=7:2:3),将得到的产物在65℃温度下烘干。(5)盐析:按反应结束时总液量的10%称取kcl进行盐析,抽滤烘干得偶氮-蒽醌ph探针粗品,得到染料的产率为84.67%。(6)提纯:将盐析所得染料分散于无水乙醇与蒸馏水的混合物中,进行重结晶,快速抽滤,滤去盐及有机小分子,得到滤饼,真空干燥得ph探针纯品,其核磁共振氢谱见图2,1hnmr(dmso,δh,ppm):11.86(s,2h,-nh2),11.83(s,2h,-nh2),10.26(s,1h,-nh,9.95(s,1h,-nh),9.68(s,1h,-nh),8.32(s,1h,ar-h),8.30(s,1h,ar-h),8.29(d,1h,ar-h),8.05(d,1h,ar-h),8.00(s,1h,ar-h),7.95(s,1h,ar-h),7.84(t,1h,ar-h),7.79(t,1h,ar-h),7.75(d,1h,ar-h),7.10(s,1h,ar-h),7.00(s,1h,ar-h),2.67(s,3h,-ch3),2.00(s,3h,-ch3),1.23(s,3h,-ch3)。实施例3结构如下的偶氮-蒽醌类ph探针的合成工艺:(1)一缩物的制备:18.6g(0.1mol)三聚氯氰配置成20%(质量百分浓度)的溶液,在0~2℃条件下于冰水浴中打浆0.5h。准确称取52.61g(0.099mol)1-氨基-2-磺酸-4-(3-氨基-2,4,6-三甲基-5-磺酸苯氨基)蒽醌单钠盐配成15%的溶液,调节ph值为5.8~6.5,溶解液为蓝色澄清溶液,在0~5℃条件下1h内滴加到打浆均匀的三聚氯氰中,滴加完毕后保持温度5℃,ph值4~4.5反应3h,薄层色谱法检测一缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:3)。(2)二缩物的制备:准确称取18.42g(0.098mol)2,4-二氨基苯磺酸干粉,一次加入到步骤(1)制备好的一次缩合液中,调整反应液ph值至2.5~3.5,升温至25℃~30℃,反应3~5h,薄层色谱法(tlc)检测二缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:4),得到蓝色二次缩合液,反应结束后降温至5℃备用。(3)重氮盐的制备:准确称取9.128g(0.098mol)苯胺液体,搅拌下一次性加入10g(0.1mol)质量分数为37.5%的浓盐酸,降温至0~5℃搅拌10min至混合均匀后,在1h内缓慢滴入6.969g(0.101mol)亚硝酸钠水溶液,滴完后-5~0℃条件下反应2h,反应完后用氨基磺酸消除过量的亚硝酸。(4)偶合反应:将步骤(2)中的二缩液降温至5℃以下,然后加入(3)中制备好的重氮盐,调节ph值1.5~5.5,在0~5℃下反应4h,然后再在室温条件下反应2~3h,薄层色谱法(tlc)检测偶合反应终点(展开剂为:正丁醇:乙醇:水=7:2:3),将得到的产物在65℃温度下烘干。(5)盐析:按反应结束时总液量的10%称取kcl进行盐析,抽滤烘干得偶氮-蒽醌ph探针粗品,得到染料的产率为85.02%。(6)提纯:将盐析所得染料分散于无水乙醇与蒸馏水的混合物中,进行重结晶,快速抽滤,滤去盐及有机小分子,得到滤饼,真空干燥得ph探针纯品,其核磁共振氢谱见图3,1h-nmr(dmso,δh,ppm):11.87(s,2h,-nh2),11.83(s,1h,-nh2),11.18(s,1h,-nh),10.27(s,1h,-nh),9.64(s,1h,-nh),8.40(s,1h,ar-h),8.38(s,1h,ar-h),8.30(t,1h,ar-h),8.29(d,1h,ar-h),8.09(s,1h,ar-h),8.05(d,1h,ar-h),7.96(s,1h,ar-h),7.86(d,1h,ar-h),7.85(d,1h,ar-h),7.14(t,1h,ar-h),7.10(s,1h,ar-h),6.60(s,1h,ar-h)2.66(s,3h,-ch3),2.00(s,3h,-ch3),1.23(s,3h,-ch3).实施例4结构如下的偶氮-蒽醌类ph探针的合成工艺:(1)一缩物的制备:18.6g(0.1mol)三聚氯氰配置成20%(质量百分浓度)的溶液,在0~2℃条件下于冰水浴中打浆0.5h。准确称取52.61g(0.099mol)1-氨基-2-磺酸-4-(3-氨基-2,4,6-三甲基-5-磺酸苯氨基)蒽醌单钠盐配成15%的溶液,调节ph值为5.8~6.5,溶解液为蓝色澄清溶液,在0~5℃条件下1h内滴加到打浆均匀的三聚氯氰中,滴加完毕后保持温度5℃,ph值4~4.5反应3h,薄层色谱法检测一缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:3)。(2)二缩物的制备:准确称取18.42g(0.098mol)2,4-二氨基苯磺酸干粉,一次加入到步骤(1)制备好的一次缩合液中,调整反应液ph值至2.5~3.5,升温至25℃~30℃,反应3~5h,薄层色谱法(tlc)检测二缩反应终点(展开剂为:正丁醇:乙醇:水=8:2:4),得到蓝色二次缩合液,反应结束后降温至5℃备用。(3)重氮盐的制备:准确称取9.128g(0.098mol)对甲苯胺晶体,搅拌下一次性加入10g(0.1mol)质量分数为37.5%的浓盐酸,,降温至0~5℃搅拌10min至混合均匀后,在1h内缓慢滴入6.969g(0.101mol)亚硝酸钠水溶液,滴完后-5~0℃条件下反应2h,反应完后用氨基磺酸消除过量的亚硝酸。(4)偶合反应:将步骤(2)中的二缩液降温至5℃以下,然后加入(3)中制备好的重氮盐,调节ph值1.5~5.5,在0~5℃下反应4h,然后再在室温条件下反应2~3h,薄层色谱法(tlc)检测偶合反应终点(展开剂为:正丁醇:乙醇:水=7:2:3),将得到的产物在65℃温度下烘干。(5)盐析:按反应结束时总液量的10%称取kcl进行盐析,抽滤烘干得偶氮-蒽醌ph探针粗品,得到染料的产率为86.29%。(6)提纯:将盐析所得染料分散于无水乙醇与蒸馏水的混合物中,进行重结晶,快速抽滤,滤去盐及有机小分子,得到滤饼,真空干燥得ph探针纯品,其核磁共振氢谱见图4,1h-nmr(dmso,δh,ppm):11.89(s,2h,-nh2),11.87(s,1h,-nh2),10.23(s,1h,-nh),9.91(s,1h,-nh),9.65(s,1h,-nh),8.31(s,1h,ar-h),8.30(d,1h,ar-h),8.04(t,1h,ar-h),7.97(s,1h,ar-h),7.87(s,1h,ar-h),7.85(d,1h,ar-h),7.74(d,1h,ar-h),7.35(d,1h,ar-h),7.22(s,1h,ar-h),7.13(t,1h,ar-h),7.05(s,1h,ar-h),2.55(s,3h,-ch3),2.38(s,3h,-ch3),2.04(s,3h,-ch3),1.23(s,3h,-ch3).实施例5将实施例1、2、3、4中的ph探针分别配置成浓度为5×10-5mol/l的水溶液,ph均调整为1.0,测定各个探针的最大吸收波长,结果如下表所示:实施例1实施例2实施例3实施例4λmax/nm490/588/626506/588/626528/588/626552/588/626实施例6探针在不同ph水溶液中的吸收光谱:分别配置含有实施例1中探针的不同ph值(ph为0.8、1.0、1.2、1.4、1.6、1.8、2.0、2.5、3.0、4.0)的缓冲溶液,探针的浓度为5×10-5mol/l。测定各个不同ph值下溶液的紫外可见吸收光谱,结果如图5所示,随着ph值的变化,紫外可见吸收光谱一直在发生变化,最大吸收波长也在发生改变,表明颜色在随ph值随时改变,通过肉眼也可以观察到不同ph值溶液的颜色的变化,用相机拍照,照片如插图所示。实施例7探针在不同ph水溶液中的吸收光谱:分别配置含有实施例2中探针的不同ph值(ph为0.8、1.0、1.2、1.4、1.6、1.8、2.0、2.5、3.0、4.0)的缓冲溶液,探针的浓度为5×10-5mol/l。测定各个不同ph值下溶液的紫外吸收光谱,结果如图6所示,随着ph值的变化,紫外可见吸收光谱一直在发生变化,最大吸收波长也在发生改变,表明颜色在随ph值随时改变,通过肉眼也可以观察到不同ph值溶液的颜色的变化,肉眼观察不同ph值溶液的颜色并用相机拍照,照片如插图所示。实施例8探针在不同ph水溶液中的吸收光谱:分别配置含有实施例3中探针的不同ph值(ph为0.8、1.0、1.2、1.4、1.6、1.8、2.0、2.5、3.0、4.0)的缓冲溶液,探针的浓度为5×10-5mol/l。测定各个不同ph值下溶液的紫外吸收光谱,结果如图7所示,随着ph值的变化,紫外可见吸收光谱一直在发生变化,最大吸收波长也在发生改变,表明颜色在随ph值随时改变,通过肉眼也可以观察到不同ph值溶液的颜色的变化,肉眼观察不同ph值溶液的颜色并用相机拍照,照片如插图所示。实施例9探针在不同ph水溶液中的吸收光谱:分别配置含有实施例4中探针的不同ph值(ph为0.8、1.0、1.2、1.4、1.6、1.8、2.0、2.5、3.0、4.0)的缓冲溶液,探针的浓度为5×10-5mol/l。测定各个不同ph值下溶液的紫外吸收光谱,结果如图8所示,随着ph值的变化,紫外可见吸收光谱一直在发生变化,最大吸收波长也在发生改变,表明颜色在随ph值随时改变,通过肉眼也可以观察到不同ph值溶液的颜色的变化,肉眼观察不同ph值溶液的颜色并用相机拍照,照片如插图所示。实施例10探针对氢离子的选择具有可逆性:用0.10mol/l的氢氧化钠和0.10mol/l的盐酸溶液分别将实施例1中ph为1.0、4.0的含探针浓度为5×10-5mol/l的缓冲溶液调整ph为4.0、1.0,发现ph从1.0调至4.0,溶液颜色由橙红色变为绿色,ph从4.0调至1.0,溶液颜色由绿色变为橙红色。实施例11探针对氢离子的选择:在ph为1.0的含实施例2中探针浓度5×10-5mol/l的缓冲溶液中,分别滴加4.00×10-5mol/l的钙、铁、镁等常见金属离子,肉眼观察溶液颜色发现无变化,由此可见,这些常见的金属离子对探针裸眼显色识别氢离子的特性影响很小。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1