一种偶氮苯基硫脲衍生物的有机凝胶化合物及制备方法、有机凝胶及应用与流程
本发明属于超分子化学
技术领域:
,具体涉及一种偶氮苯基硫脲衍生物的有机凝胶化合物及制备方法、有机凝胶及应用。
背景技术:
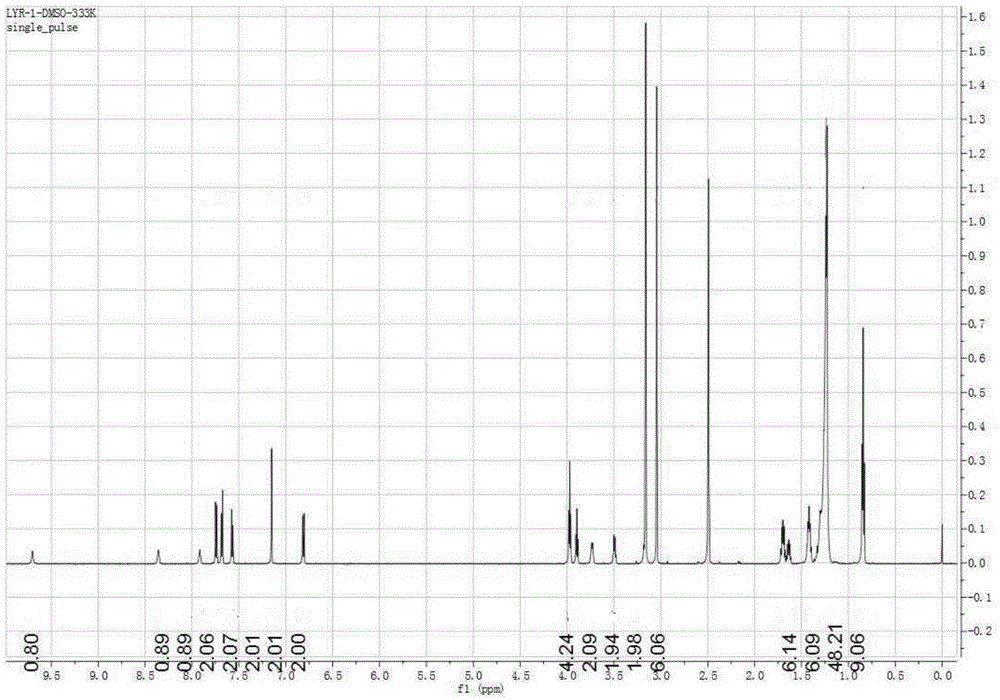
:铜是一种存在于动物和人类机体的基本微量元素,它作为一些酶和蛋白质的辅助因子,参与了广泛的代谢过程。但高含量的铜对生命健康会产生严重的危害,导致体内器官的生化紊乱、生理功能障碍及多种病理变化。汞是唯一在常温下呈液态且易流动的金属,主要用于科学仪器、汞锅炉、汞泵及汞气灯中,在医药上也广泛应用,长期以来,汞产品在人们的生活中随处可见。环境中的汞能被动植物富集,经生物转化作用转变成毒性更大的有机汞,各种形式的汞可通过水体及食物链进入人体,对人体产生毒性作用,长时间暴露在高汞环境中,可以导致脑损伤和死亡。因此,环境中的痕量汞检测极为重要。铁是人体必需的元素之一,对人体的新陈代谢和身体健康具有重要作用,血液中铁的含量不足,就会造成缺铁性贫血。水中含铁虽不会妨害人体健康,但含铁量高的水在管道内易生长铁细菌,增加水的浑浊度,使水产生特殊的色、臭、味,因此饮起来很不可口,有一种铁锈味。同时水体中铁含量的高低对工农业生产和日常生活也有着重要影响。另外,铁离子在化工生产医药食品卫生等行业都起着一定的作用,所以,测定铁离子的含量是很有价值的。挥发性酸又称气态酸,如盐酸和三氟乙酸均具有较强的挥发性。这类酸通常用作医药、农药中间体、生化试剂、有机合成试剂。三氟乙酸用于合成含氟化合物、杀虫剂和染料;是酯化反应和缩合反应的催化剂;羟基和氨基的保护剂,用于糖和多肽的合成;还用作选矿剂、用于有机合成。但这类酸对眼睛、粘膜、呼吸道和皮肤有强烈刺激作用,吸入后可能引起咽喉、支气管的痉挛、炎症、水肿,化学性肺炎、肺水肿而死亡,症状有烧灼感、咳嗽、喘息、气短、喉炎、头痛、恶心和呕吐,还可致皮肤灼伤。有机胺是大气中普遍存在的一类痕量化合物,有比无机氨更强的碱性,也是很重要的含氮有机化合物之一。目前大气中已被识别出来的有机胺大约有150种,主要成分有甲胺、二甲胺、三甲胺、乙胺、二乙胺、丙胺、苯胺等24种,有机胺通畅嗅觉阈值低,当在空气中达到一定浓度时,不仅嗅觉上令人厌恶,还会对人体健康造成损害。因此,灵敏检测铜离子、铁离子、汞离子、气态酸及有机胺具有重要的实际意义,同时也具有环保的价值。现有技术中常采用仪器分析的方法实现对上述铜离子、铁离子、汞离子、气态酸及有机胺进行检测,检测方法及过程相对繁琐。小分子凝胶作为一类新型的功能材料,是介于液相和固相之间的软材料。这类材料通常含有构造基团和功能基团,通过构造基团之间的非共价键相互作用形成不同尺寸的微纳米网络结构,从而将大量的溶剂分子固定在网络中;而功能基团的引入可以使凝胶对外界刺激例如光、热、ph、生物分子、超声、金属离子等做出灵敏的响应,并引起体系光学、电学性能、分子构象、甚至化学性质的变化,从而使材料具有信息存储、传递和处理的能力。现有技术中已经有关于将小分子凝胶用于金属或气态酸的检测,若能够开发一种新的有机凝胶化合物可同时用于hg2+、cu2+、fe3+、挥发性酸以及有机胺的检测,将具有非常好的应用前景。技术实现要素:本发明的目的在于提供一种偶氮苯基硫脲衍生物的有机凝胶化合物,该有机凝胶化合物可用于检测hg2+、cu2+、fe3+、挥发性酸以及有机胺。本发明的第二个目的在于提供一种偶氮苯基硫脲衍生物的有机凝胶化合物的制备方法。本发明的第三个目的在于提供一种有机凝胶。本发明的第四个目的在于提供一种偶氮苯基硫脲衍生物的有机凝胶化合物在检测挥发性酸中的应用。为实现以上目的,本发明的技术方案是:一种偶氮苯基硫脲衍生物的有机凝胶化合物,具有式ⅰ所示的结构:上述有机凝胶化合物的制备方法,包括以下步骤:将4-二甲氨基偶氮苯-4'-硫代异氰酸酯、n-(2-胺乙基)-3,4,5-三(十二烷氧基)苯甲酰胺、无水四氢呋喃混合后搅拌回流10~13h,然后减压蒸出四氢呋喃,将剩余的产物过柱提纯即得。所述4-二甲氨基偶氮苯-4'-硫代异氰酸酯与n-(2-胺乙基)-3,4,5-三(十二烷氧基)苯甲酰胺的摩尔比为1:1;所述回流的温度为90~95℃。一种有机凝胶,由包括以下步骤的制备方法制得:将上述偶氮苯基硫脲衍生物的有机凝胶化合物于有机溶剂中加热至溶解,然后冷却至室温,即得,所述有机溶剂为正己烷、石油醚、二甲基亚砜、乙腈、乙醇中的任意一种。所述加热至溶解的加热温度在80℃以上。所述偶氮苯基硫脲衍生物的有机凝胶化合物在正己烷中的临界凝胶浓度为1.9mg/ml。所述偶氮苯基硫脲衍生物的有机凝胶化合物在石油醚中的临界凝胶浓度为1.8mg/ml。所述偶氮苯基硫脲衍生物的有机凝胶化合物在二甲基亚砜中的临界凝胶浓度为12.5mg/ml。所述偶氮苯基硫脲衍生物的有机凝胶化合物在乙腈中的临界凝胶浓度为12.5mg/ml。所述偶氮苯基硫脲衍生物的有机凝胶化合物在乙醇中的临界凝胶浓度为25.0mg/ml。所述偶氮苯基硫脲衍生物的有机凝胶化合物在检测hg2+、cu2+、fe3+、挥发性酸或有机胺中的应用。上述临界凝胶浓度指形成凝胶的最低浓度。所述挥发性酸为三氟乙酸、硝酸、盐酸中的任意一种。所述有机胺为三乙胺、三丙胺、氨水、二乙胺中的任意一种。本发明偶氮苯基硫脲衍生物的有机凝胶化合物中存在偶氮基团、硫脲基团、酰胺基团,具有金属离子传感特性。本发明偶氮苯基硫脲衍生物的有机凝胶化合物对汞离子的检测主要是通过分子内环化反应,在分子环化反应过程中失去了h2s,进而使得其紫外可见吸收光谱发生改变。本发明偶氮苯基硫脲衍生物的有机凝胶化合物对铁离子及铜离子的检测机理相同,均为铜离子或铁离子与化合物1中的氮氮双键发生配位,使得化合物1原来的吸收光谱发生了改变。本发明的偶氮苯基硫脲衍生物的有机凝胶化合物还可用于检测挥发性酸及有机胺,检测挥发性酸是通过酸中的质子与端位的氨基反应生成季铵盐,溶液的颜色发生了变化,当检测有机胺时是通过酸碱反应,溶液或固体的颜色恢复原貌。本发明的偶氮苯基硫脲衍生物的有机凝胶化合物可实现对hg2+、cu2+、fe3+、挥发性酸以及有机胺的检测,且检测方法简单快捷,无需采用仪器通过肉眼即可进行判别。附图说明图1为式ⅰ所示偶氮苯基硫脲衍生物的有机凝胶化合物的1hnmr谱图;图2为式ⅰ所示偶氮苯基硫脲衍生物的有机凝胶化合物的13cnmr谱图;图3为偶氮苯基硫脲衍生物的有机凝胶化合物在不同溶剂中形成的有机凝胶的形貌示意图;图4为偶氮苯基硫脲衍生物的有机凝胶化合物在不同溶剂中形成的干凝胶的sem图;图5为化合物1的乙腈溶液加入不同金属离子后的形貌示意图;图6为化合物1的乙腈溶液及加入不同金属离子后的紫外可见吸收光谱图;图7为分别加入hg2+,fe3+,cu2+后的化合物1的乙腈溶液的紫外可见吸收光谱图;图8为加入三氟乙酸以及加入三乙胺后的化合物1的乙腈溶液的紫外可见吸收光谱图及相应的线性曲线;图9为不同气态酸对胶片1的形貌的影响示意图;图10为不同有机胺对深棕色的胶片1的形貌的影响示意图;图11为采用不同浓度的三乙胺对深棕色的胶片1对进行处理后的紫外可见吸收光谱图及相应的线性曲线示意图。具体实施方式实施例1本实施例偶氮苯基硫脲衍生物的有机凝胶化合物,具有式ⅰ所示的结构:本实施例偶氮苯基硫脲衍生物的有机凝胶化合物的制备路线如下:具体制备方法包括以下步骤:将1.0g(3.54mmol)4-二甲氨基偶氮苯-4'-硫代异氰酸酯、2.54g(3.54mmol)n-(2-胺乙基)-3,4,5-三(十二烷氧基)苯甲酰胺在100ml无水四氢呋喃中混匀,之后于90℃回流12h,然后减压蒸出四氢呋喃,将剩余的产物过硅胶柱提纯,洗脱剂为甲醇/二氯甲烷(1/1200,v/v),最终得黄色粉末,即为式ⅰ所示化合物,收率70.5%,1hnmr(600mhz,dmso-d6):9.70(s,1h),8.36(s,1h),7.92(s,1h),7.75(d,j=9.0hz,2h),7.69(d,j=9.0hz,2h),7.58(d,j=9.0hz,2h),7.15(s,2h),6.82(d,j=9.0hz,2h),3.99(t,j=6.6hz,4h),3.91(t,j=6.6hz,2h)3.74(d,j=3.6hz,2h),3.50(d,j=3.6hz,2h),3.04(s,6h),1.72-1.62(m,6h),1.43-1.39(m,6h),1.30-1.23(m,48h),0.84(t,j=6.6hz,9h);13cnmr(150mhz,dmso-d6):181.3,166.7,152.9,152.8,149.4,143.4,141.1,140.7,129.8,1249.,123.4,122.8,112.1,106.8,73.1,69.3,44.2,31.8,30.3,29.5,29.3,29.2,26.1,22.5,14.3.hrmscalculatedforc60h99n6o4s[m+h]+999.7449,found:999.7474.上述偶氮苯基硫脲衍生物的有机凝胶化合物的制备方法中,回流温度还可以为95℃,回流时间为10h。式ⅰ所示化合物的1hnmr谱如图1所示,式ⅰ所示化合物的13cnmr谱如图2所示。实施例2将实施例1制备的偶氮苯基硫脲衍生物的有机凝胶化合物(简称化合物1)和有机溶剂于密封小瓶子中,加热至溶剂沸点(80℃以上)左右,使偶氮苯基硫脲衍生物的有机凝胶化合物溶解,然后静置冷却至25℃,观察其在不同溶剂中的成凝胶能力。凝胶都是热力学可逆的,加热后变成可流动的溶胶,具体凝胶性能见表1。表1偶氮苯基硫脲衍生物的有机凝胶化合物在不同溶剂中的成胶状态有机溶剂凝胶状态有机溶剂凝胶状态dmfs1,4-二氧六环s正己烷g(1.9)乙腈g(12.5)甲醇p乙醇g(25.0)丙酮p乙酸乙酯p石油醚g(1.8)甲苯s二甲基亚砜g(12.5)四氢呋喃s二氯甲烷s氯仿s注释:其中g表示凝胶,pg表示部分凝胶,s表示溶解,ni表示不溶;括号内为最小成胶浓度,单位mg/ml。由表1可知,本发明的偶氮苯基硫脲衍生物的有机凝胶化合物在正己烷、石油醚、二甲基亚砜、乙腈、乙醇溶剂中能够形成有机凝胶。偶氮苯基硫脲衍生物的有机凝胶化合物在石油醚、正己烷、二甲基亚砜、乙醇、乙腈溶剂中形成的有机凝胶稳定性好,为黄色不透明物,可以放置几个月,其形貌如图3所示,其中图3中a)为在石油醚溶剂中形成的有机凝胶,b)为在正己烷溶剂中形成的有机凝胶,c)为在dmso溶剂中形成的有机凝胶,d)为在乙醇溶剂中形成的有机凝胶,e)为在乙腈溶剂中形成的有机凝胶。将上述形成的有机凝胶分别用相应的有机溶剂稀释后分散在云母板上,进行冷冻干燥,形成干凝胶,然后分别进行扫描电镜测试,结果如图4所示,图4中a)、b)、c)、d)、e)分别为在石油醚、正己烷、二甲基亚砜、乙醇、乙腈溶剂中的干凝胶的sem图,由图4中a)、b)可知,在正己烷和石油醚溶剂中形成的有机凝胶为纳米纤维形成的多孔网络结构,所述纳米纤维的宽为300nm,长度为十几微米;相比在乙醇和乙腈中形成的有机凝胶,在正己烷和石油醚中形成的纳米纤维凝胶分散更为均匀;由图4d)、4e)可知,在乙醇和乙腈中形成的有机凝胶的纳米纤维结构的宽为300~400nm,长为十几个微米。上述的纳米纤维结构倾向于堆叠并缠绕成一个节点,就像池塘里有许多个小蝌蚪;如图4c)所示,在二甲基亚砜溶剂中形成的有机凝胶呈现出不规则的微米带,宽为1-3μm,长为几十微米。实验例1式ⅰ所示的偶氮苯基硫脲衍生物的有机凝胶化合物(化合物1)对金属离子的检测研究,分别选取ag+,cd2+,fe2+,k+,mg2+,mn2+,na+,ni2+,pb2+,zn2+,hg2+,fe3+,cu2+进行实验。向化合物1的乙腈溶液(c=10-4m)中添加不同的金属离子ag+,cd2+,fe3+,k+,mg2+,mn2+,na+,ni2+,pb2+,zn2+,hg2+,fe3+,cu2+,如图5a所示,加入fe3+后溶液由黄色变为酒红色,加入hg2+后溶液由黄色变为鲜红色,加入cu2+之后溶液由黄色变为姜黄色,而加入其它金属离子后,颜色无明显变化;如图5b所示为fe3+和cu2+的乙腈溶液,均为无色,作为对照,以排除fe3+和cu2+颜色本来带来的影响,由图5可知,化合物1对hg2+,fe3+,cu2+具有选择性。为了进一步证明化合物1对hg2+,fe3+,cu2+的选择性,对化合物1的乙腈溶液及加入ag+,cd2+,fe3+,k+,mg2+,mn2+,na+,ni2+,pb2+,zn2+,hg2+,fe3+,cu2+后的化合物1的乙腈溶液进行紫外可见检测,结果如图6所示,由图6可知,化合物1的乙腈溶液的紫外可见吸收光谱在261nm和423nm处有两个吸收峰,对应的摩尔吸收系数分别为3.11×104和3.52×104m-1cm-1,加入1.0eq的hg2+后,在531nm处出现了新的吸收峰,在261nm处的吸收峰红移9nm至270nm,在423nm处的吸收峰红移25nm至448nm;当加入1.0eq.的fe3+时,549nm处出现了新的吸收峰,270nm和448nm处的两个吸收峰蓝移至248nm和421nm。其它金属离子加入到化合物1的乙腈溶液中,紫外吸收光谱的吸收峰的吸光度有所变化,但是峰位置没有明显的移动。化合物1对hg2+,fe3+,cu2+的检测能力通过紫外可见吸收光谱的变化进行研究。如图7a,加入hg2+前,化合物1的溶液在261nm和423nm处存在两个吸收峰,随着hg2+滴定量的增加,423nm处的吸光度逐渐衰减,而在541nm出现一新的吸收峰并且逐渐增强,在475nm处出现的等吸光度点体现了hg2+和化合物1的反应;当hg2+的加入量为1.2eq时,261nm和423nm处的两个吸收峰的吸光度达到最小值。如图7a′,541nm处的吸光度与423nm处的吸光度的比值与hg2+的加入量之间呈线性关系,线性系数r=0.9931,化合物1对hg2+的最小检测限为9.22×10-9mol/l。化合物1对汞离子的检测主要是通过分子内环化反应,在分子环化反应过程中失去了h2s,加入汞离子后化合物1的结构发生了如下改变:如图7b,随着fe3+滴定量的增加,423nm处的吸光度逐渐降低,549nm处出现新的吸收峰且吸光度逐渐增加,在549nm处出现的等吸光度点说明fe3+和化合物1反应生成了复合物;如图7b′,549nm处的吸光度与423nm处的吸光度的比值与fe3+的加入量之间呈线性关系,线性系数r=0.9941,化合物1对fe3+的最小检测限为1.39×10-9mol/l。化合物1对铁离子的检测主要是通过铁离子与偶氮苯中的氮氮双键的配位作用,使得原来的吸收光谱发生了变化,实现了对铁离子的肉眼识别。如图7c,随着cu2+滴定量的增加,423nm处的吸光度逐渐降低,在500nm和900nm之间出现新的吸收峰且吸光度逐渐增加,随着铜离子的滴定,吸收峰发生了26nm的红移从423nm红移至449nm;如图7c′,600nm处的吸光度与423nm处的吸光度的比值与cu2+的加入量之间呈线性关系,线性系数r=0.9946,化合物1对cu2+的最小检测限为5.99×10-9mol/l。化合物1对铜离子的检测主要是通过铜离子与偶氮苯中的氮氮双键的配位作用,使得原来的吸收光谱发生了变化,实现了对铜离子的肉眼识别。上述化合物1对铁离子及铜离子的检测机理相同,均为铜离子或铁离子与化合物1中的氮氮双建发生配位,使得化合物1原来的吸收光谱发生了改变,其中铜离子或铁离子与化合物1的配位作用如下所示:其中,m为cu2+或fe3+。实验例2式ⅰ所示的偶氮苯基硫脲衍生物的有机凝胶化合物(化合物1)对挥发性酸及有机胺的检测研究,以三氟乙酸和三乙胺为例进行研究。向式ⅰ所示的偶氮苯基硫脲衍生物的有机凝胶化合物(化合物1)的乙腈溶液(c=10-5m)中加入三氟乙酸,如图8a所示,随着三氟乙酸的加入,423nm处的吸收峰逐渐减弱,在548nm处出现新的吸收峰并且该处的吸光度逐渐增大,在479nm处出现等吸光度点。加入三氟乙酸后,化合物1的乙腈溶液由黄色逐渐转变为紫色,当三氟乙酸的加入量为450eq时,423nm和548nm处的吸光度变化都达到极限,479nm为等吸光度点。如图8a′所示,548nm处的吸光度和423nm处的吸光度之比与三氟乙酸加入量之间为线性关系,线性系数r=0.9966,化合物1对三氟乙酸的最低检测限为3.1×10-9mol/l。化合物1检测气态酸的原理为:通过酸中的质子与化合物1中端位的氨基反应生成季铵盐,使得化合物1溶液的颜色发生了变化。理论上,加入有三氟乙酸的化合物1的溶液通过酸碱反应能够进一步检测有机胺。如图8b所示,向加入有三氟乙酸的化合物1的乙腈溶液中加入三乙胺,溶液颜色由紫色转变为黄色,随着三乙胺的加入(直至250eq),548nm处的吸收峰逐渐减弱,423nm处的吸收峰逐渐恢复,在479nm处存在等吸光度点。如图8b′所示,423nm处的吸光度与528nm处的吸光度的比值与三乙胺的加入量成线性关系,线性系数r=0.9927,三乙胺的最低检测限为2.77×10-9mol/l。上述检测气态挥发性酸是通过酸中的质子与端位的氨基反应生成季铵盐,溶液的颜色发生了变化,当检测有机胺时是通过酸碱反应,溶液或固体的颜色又转变回来,其中化合物1的结构变化如下所示。将化合物1溶解在二氯甲烷中然后铺在石英石板材上制备胶片1以减少化合物1的使用量。检测胶片1对挥发性酸和有机胺的选择性。实验证明,如图9所示,胶片1在三氟乙酸、盐酸或硝酸2~30s的激发下颜色由黄色迅速变为深棕色;由于甲酸、乙酸、丙酸的活性较弱,胶片1对其不敏感,胶片1的颜色未发生变化。用对挥发性酸响应后的深棕色胶片1来检测其对有机胺的灵敏性。如图10所示,采用三乙胺、三丙胺、氨水、二乙胺响应深棕色的胶片1,胶片颜色由深棕色转变成黄色,乙二胺、苯胺具有弱的挥发性和碱性不能够使得胶片1颜色由深棕色恢复为黄色。胶片1受三氟乙酸浓度的影响通过紫外可见光谱来研究。如图11a所示,胶片1在399nm处有最大吸收峰,胶片1在三氟乙酸气氛中颜色由黄色转变成深棕色,随着三氟乙酸的浓度由3ppm增大到33ppm,399nm处的吸收峰逐渐衰减,在530nm处出现新的吸收峰并且逐渐增强。并且530nm处的吸光度与399nm处的吸光度的比值与三氟乙酸的浓度之间为线性关系,线性曲线如图11b所示,线性系数r=0.9986,胶片1对三氟乙酸的最低检测限为0.0848ppb。对本领域的技术人员来说,可根据以上描述的技术方案以及构思,做出其它各种相应的改变以及形变,而所有的这些改变以及形变都应该属于本发明权利要求的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1