一种丙谷二肽的分离提纯方法与流程
本发明涉及丙谷二肽的生产技术领域,具体来说,涉及一种丙谷二肽的分离提纯方法。
背景技术:
丙谷二肽,学名n-(2)-l-丙氨酰-l-谷氨酰胺,是l-谷氨酰胺的一种改性化合物,相对分子质量为217.22,易溶于水。l-谷氨酰胺是机体内含量非常丰富的一种氨基酸,是人体多种组织代谢的参与体,人体缺乏l-谷氨酰胺会引发多种疾病。由于l-谷氨酰胺溶解度低且不稳定,因此l-谷氨酰胺的肠外应用受到了限制。丙谷二肽可在体内分解为l-谷氨酰胺和l-丙氨酸,这一特性使经由肠外营养输液补充l-谷氨酰胺成为可能。丙谷二肽分解释放出的氨基酸作为营养物质各自储存在身体的相应部位并随机体的需要进行代谢。
由于丙谷二肽药用价值的特殊性,就像生理盐水、葡萄糖一样,将成为救护病人的必需品。而目前工业上制造丙谷二肽的方法主要有化学合成法和酶促合成法。由于化学合成法合成路线长,过程控制点要求高,收率低,因此酶促合成法逐渐成为工业化生产的主要方法。通过酶促合成法得到的丙谷二肽反应液后,再经过后续的提取纯化工艺得到产品,其主要方法流程如附图1所示,该工艺在进行活性炭吸附时会产生固废,另外经过两次结晶后,产品的收率低,产品纯度低,导致处理成本较大。
目前味之素株式会社也在采用酶促合成的方法合成丙谷二肽,但是在后期的纯化中不能去除因酶促反应产生的三肽、四肽及多肽杂质,所以不能够用作医药级别原料药的使用,只能当做食品级二肽使用。针对这一技术问题,我们进行了大量的实验,令人惊奇的发现,在纯化过程中加入酸性物质可以有效的去除丙谷二肽中的三肽、四肽及其他多肽杂质。
技术实现要素:
针对相关技术中的问题,本发明提出一种丙谷二肽的分离提纯方法,以克服现有相关技术所存在的上述技术问题。
本发明的技术方案是这样实现的:
一种丙谷二肽的分离提纯方法,包括以下步骤:
将陶瓷膜过滤除酶;然后将丙谷二肽酶反应液通过陶瓷膜过滤设备过滤,脱除反应液中残留的酶蛋白,得陶瓷膜透析液。
采用电渗析的方法脱盐:将陶瓷膜过滤液进入电渗析设备进行脱盐,把丙谷二肽和无机盐进行分离,得丙谷二肽溶液。
采用反渗透膜设备浓缩:将脱盐后的丙谷二肽溶液进入反渗透设备进行浓缩,得原体积的30-40%的浓缩液。
采用减压浓缩的设备对上步的浓缩液进行进一步的浓缩至反渗透原体积45%。
析晶:将上步的浓缩液加入3倍量的甲醇析晶,得粗品。
多肽杂质去除纯化:将粗品溶解于3倍量的水中,再加入0.1-50%的酸性物质,30-80℃加热搅拌,加入6倍水量的甲醇析晶得纯化的精制品,纯度大于99.7%;单个杂质小于0.1%。因为多肽的溶解度取决于其物理特性,氨基酸可分类为酸性、碱性、极性、非极性、疏水性。丙谷二肽在酶催化反应中会形成三肽、四肽及其它的多肽杂质,三肽杂质为丙氨酰丙氨酰谷氨酰胺,四肽杂质为丙氨酰丙氨酰丙氨酰谷氨酰胺。随着肽链的不断增加,其疏水基团(-ch3)在不断的增加,使其在水中的溶解性越来越差,使得在纯化过程中,随着甲醇的加入,三肽和四肽杂质更容易的析出,造成难以去除的现象。三肽四肽的结构上有1个末端-cooh和2个末端-nh2,从其在水中电离的电荷量来看,应该是碱性的,所以在纯化过程中加入酸性物质,可以很好的增加三肽四肽及其它多肽的溶解性,有利于纯化去除。
进一步,所述陶瓷膜过滤设备采用的陶瓷膜的孔径为20-100nm,其中,温度为30-50℃之间,压力为0.15-0.5mpa,可以有效的去除反应液中的酶。
进一步,所述减压浓缩是温度控制在30-80℃,优选50-65℃;减压浓缩至反渗透原体积45%。
进一步,所述析晶是控制甲醇的加入量为1-10倍。
进一步,所述析晶是控制甲醇的加入量为3-5倍。
进一步,所述纯化是加水溶解粗品的水的加入量为粗品质量的1-10倍;加入的酸性物质为无机酸(如盐酸、硫酸等)和有机酸(如一元羧酸甲酸、二元羧酸草酸、三元羧酸柠檬酸等,及其它多元羧酸)及它们的复合酸以及酸性氧化物(如so2)、酸式盐(如nahso4);其加入的量为所纯化物质的0.1%-50%。
进一步,所述纯化是加水溶解粗品的水的加入量为粗品质量的2-5倍;加入的酸性物质为柠檬酸、盐酸和硫酸;其加入的量为所需纯化物质量的1-5%。
本发明有益效果为:本发明通过以上一系列工艺流程步骤,从而降低了生产成本,简化了生产工艺、缩短了生产周期、提高总收率,并且具有产品纯度高等优点;解决生物酶法合成丙谷二肽过程中三肽、四肽及多肽等难以去除的难题;使得生物酶法合成的丙谷二肽能够达到制药原料药的纯度;具有很好的工业化前景。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
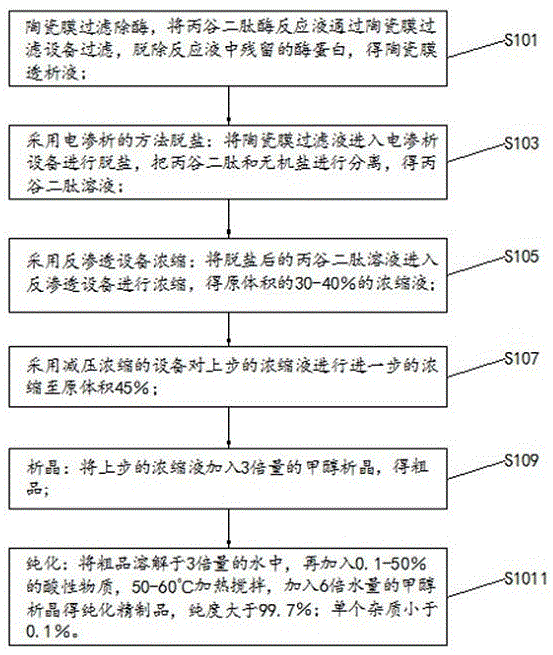
图1是根据本发明实施例的一种丙谷二肽的分离提纯方法的步骤流程图;
图2是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品的hplc图;
图3是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品未加酸性物质处理所得丙谷二肽成品的hplc图;
图4是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经5%柠檬酸处理所得丙谷二肽成品的hplc图;
图5是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经5%磷酸酸处理所得丙谷二肽成品的hplc图;
图6是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经5%盐酸处理所得丙谷二肽成品的的hplc图;
图7是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经5%硫酸处理所得丙谷二肽成品的的hplc图;
图8是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经30%柠檬酸处理所得丙谷二肽成品的的hplc图;
图9是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经45%柠檬酸处理所得丙谷二肽成品的的hplc图;
图10是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经硝酸酸处理所得丙谷二肽成品的的hplc图;
图11是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经甲酸处理所得丙谷二肽成品的hplc图;
图12是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经草酸处理所得丙谷二肽成品的的hplc图;
图13是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经酒石酸处理所得丙谷二肽成品的的hplc图;
图14是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经琥珀酸处理所得丙谷二肽成品的的hplc图;
图15是根据本发明实施例的一种丙谷二肽的分离提纯方法的丙谷二肽粗品经乙酸处理所得丙谷二肽成品的的hplc图。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员所获得的所有其他实施例,都属于本发明保护的范围。
根据本发明的实施例,提供了一种丙谷二肽的分离提纯方法。
如图1~13所示,根据本发明实施例的丙谷二肽的分离的提纯方法,步骤如下:
步骤s101,将陶瓷膜过滤除酶;然后将丙谷二肽酶反应液通过陶瓷膜过滤设备过滤,脱除反应液中残留的酶蛋白,得陶瓷膜过滤液;
步骤s103,采用电渗析的方法脱盐:将陶瓷膜过滤液进入电渗析设备进行脱盐,把丙谷二肽和无机盐进行分离,得丙谷二肽溶液;
步骤s105,采用反渗透膜设备浓缩:将脱盐后的丙谷二肽溶液进入反渗透设备进行浓缩,得原体积的30-40%的浓缩液;
步骤s107,采用减压浓缩的设备对上步的浓缩液进行进一步的浓缩至反渗透原体积45%;
步骤s109,析晶:将上步的浓缩液加入3倍量的甲醇析晶,得粗品;
步骤s1011,纯化:将粗品溶解于3倍量的水中,再加入0.1-50%的酸性物质,50-60℃加热搅拌,加入6倍水量的甲醇析晶得纯化的精制品,纯度大于99.7%;单个杂质小于0.1%。
在一个实施例中,制得的丙谷二肽酶反应液中,取丙谷二肽浓度为65g/l,氯化钠质量分数3.7%的转化液10l;经50nm陶瓷膜过滤后,电渗析设备,所述电渗析设备是利用膜的选择透过性对水中的物质进行分离而达到除盐等预期目的的一种水处理设备,控制电压为37v进行电渗析,控制渗析液的电导率为8000时,停止渗析;将脱盐后的渗析液透过反渗透膜浓缩,所述反渗透膜原理是在高于溶液渗透压的作用下,依据其他物质不能透过半透膜而将这些物质和水分离开来;所选的反渗透膜可以截留分子量大于100的物质,而能透过水,待浓缩至原体积的40%时停止浓缩;再将此浓缩液在50-65℃的条件下进行减压浓缩至原体积的45%,加三倍体积的甲醇析晶得粗品,粗品的纯度为97.55%(hplc图见图2);将所得粗品加入3倍质量的水溶解,加热60℃搅拌,30min后加6倍体积的甲醇析晶,过滤,65℃减压干燥。得精制品500克。纯度为:99.10%(hplc图见图3)。
在一个实施例中,制得的丙谷二肽酶反应液中,取丙谷二肽浓度为65g/l,氯化钠质量分数3.7%的转化液10l;经50nm陶瓷膜过滤后,上电渗析设备,控制电压为37v进行电渗析,控制渗析液的电导率为8000时,停止渗析;将脱盐后的渗析液透过反渗透膜浓缩,待浓缩至原体积的40%时停止浓缩;再将此浓缩液在50-65℃的条件下进行减压浓缩至原体积的45%,加三倍体积的甲醇析晶得粗品,粗品的纯度为97.55%(hplc图见图2);将所得粗品加入3倍质量的水溶解,再加入5%的一水柠檬酸加热60℃搅拌,30min后加6倍体积的甲醇析晶,过滤,65℃减压干燥。得精制品510克。纯度为:99.83%(hplc图见图4)。
在一个实施例中,制得的丙谷二肽酶反应液中,取丙谷二肽浓度为65g/l,氯化钠质量分数3.7%的转化液10l;经50nm陶瓷膜过滤后,上电渗析设备,控制电压为37v进行电渗析,控制渗析液的电导率为8000时,停止渗析;将脱盐后的渗析液透过反渗透膜浓缩,待浓缩至原体积的40%时停止浓缩;再将此浓缩液在50-65℃的条件下进行减压浓缩至原体积的45%,加三倍体积的甲醇析晶得粗品,粗品的纯度为97.55%(hplc图见图2);将所得粗品加入3倍质量的水溶解,再加入5%的磷酸加热60℃搅拌,30min后加6倍体积的甲醇析晶,过滤,65℃减压干燥。得精制品508克。纯度为:99.55%(hplc图见图5)。
在一个实施例中,制得的丙谷二肽酶反应液中,取丙谷二肽浓度为65g/l,氯化钠质量分数3.7%的转化液10l;经50nm陶瓷膜过滤后,上电渗析设备,控制电压为37v进行电渗析,控制渗析液的电导率为8000时,停止渗析;将脱盐后的渗析液透过反渗透膜浓缩,待浓缩至原体积的40%时停止浓缩;再将此浓缩液在50-65℃的条件下进行减压浓缩至原体积的45%,加三倍体积的甲醇析晶得粗品,粗品的纯度为97.55%(hplc图见图2);将所得粗品加入3倍质量的水溶解,再加入5%的盐酸加热60℃搅拌,30min后加6倍体积的甲醇析晶,过滤,65℃减压干燥。得精制品505克。纯度为:99.74%(hplc图见图6)。
在一个实施例中,制得的丙谷二肽酶反应液中,取丙谷二肽浓度为65g/l,氯化钠质量分数3.7%的转化液10l;经50nm陶瓷膜过滤后,上电渗析设备,控制电压为37v进行电渗析,控制渗析液的电导率为8000时,停止渗析;将脱盐后的渗析液透过反渗透膜浓缩,待浓缩至原体积的40%时停止浓缩;再将此浓缩液在50-65℃的条件下进行减压浓缩至原体积的45%,加三倍体积的甲醇析晶得粗品,粗品的纯度为97.55%(hplc图见图2);将所得粗品加入3倍质量的水溶解,再加入5%的硫酸酸加热60℃搅拌,30min后加6倍体积的甲醇析晶,过滤,65℃减压干燥。得精制品509克。纯度为:99.80%(hplc图见图7)。
在一个实施例中,制得的丙谷二肽酶反应液中,取丙谷二肽浓度为65g/l,氯化钠质量分数3.7%的转化液10l;经50nm陶瓷膜过滤后,上电渗析设备,控制电压为37v进行电渗析,控制渗析液的电导率为8000时,停止渗析;将脱盐后的渗析液透过反渗透膜浓缩,待浓缩至原体积的40%时停止浓缩;再将此浓缩液在50-65℃的条件下进行减压浓缩至原体积的45%,加三倍体积的甲醇析晶得粗品,粗品的纯度为97.55%(hplc图见图2);将所得粗品加入3倍质量的水溶解,再加入30%的一水柠檬酸加热60℃搅拌,30min后加6倍体积的甲醇析晶,过滤,65℃减压干燥。得精制品512克。纯度为:99.76%(hplc图见图8)。
在一个实施例中,制得的丙谷二肽酶反应液中,取丙谷二肽浓度为65g/l,氯化钠质量分数3.7%的转化液10l;经50nm陶瓷膜过滤后,上电渗析设备,控制电压为37v进行电渗析,控制渗析液的电导率为8000时,停止渗析;将脱盐后的渗析液透过反渗透膜浓缩,待浓缩至原体积的40%时停止浓缩;再将此浓缩液在50-65℃的条件下进行减压浓缩至原体积的45%,加三倍体积的甲醇析晶得粗品,粗品的纯度为97.55%(hplc图见图2);将所得粗品加入3倍质量的水溶解,再加入45%的一水柠檬酸加热60℃搅拌,30min后加6倍体积的甲醇析晶,过滤,65℃减压干燥。得精制品508克。纯度为:99.73%(hplc图见图9)。
对比例:
为了比较不同的酸性物质对丙谷二肽的纯化效果,我们对可以采购到酸性物质进行试验,试验的过程与上述实施例相同,只是加入的酸性物质不同,结果见下表:
经试验,加入酸性物质对丙谷二肽的纯化都有一定程度的有益作用。
综上所述,借助于本发明的上述技术方案,本发明通过以上一系列工艺流程步骤,从而降低了生产成本,简化了生产工艺、缩短了生产周期、提高总收率,并且具有产品纯度高等优点;解决生物酶法合成丙谷二肽过程中三肽和四肽及多肽等难以去除的难题;使得生物酶法合成的丙谷二肽能够达到制药原料药的纯度;具有很好的工业化前景。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!