植物生产口服重组人粒细胞集落刺激因子的制作方法
本发明涉及生物技术领域,特别涉及植物生产口服重组人粒细胞集落刺激因子。
背景技术:
人粒细胞集落刺激因子(g-csf)是由单核细胞、纤维母细胞、内皮细胞产生的一种分子量约为20kd的糖蛋白类调节因子,其等电点约为6.0。g-csf作用于骨髓中性粒细胞系造血前体细胞,促进其增殖、分化、成熟和释放。成熟人体内g-csf有177个氨基酸(a)型和174个氨基酸(b)型两种异构体,b型分子的螺旋含量很高,晶体构型含有四个a螺旋,属于长链螺旋细胞因子家族。鉴于b型的生物学活性及稳定性均显著高于a型,b型分子深受研究者的推崇。重组人g-csf已广泛用于骨髓移植和肿瘤的治疗,此外,重组人粒细胞集落刺激因子还被用于治疗急性白血病、再生障碍性贫血等疾病。g-csf在辅助肿瘤治疗方面的作用主要是增加白细胞数目,降低化疗和放疗的风险。目前已有多种以b型为基础的重组人粒细胞制剂被批准上市,如非格司亭(filgrastim),来格司亭(lenograstim),那托司亭(nartograstim)。其中非格司亭和那托司亭为大肠杆菌表达的非糖基化形式的重组人g-csf,而来格司亭是ch0细胞表达的带糖基化修饰的g-csf。非格司亭氨基酸序列即在天然g-csf的n端附加一个蛋氨酸,那托司亭为非格司亭的突变体,共涉及天然g-csf中5个氨基酸的定点突变。
目前已知的制备gm-csf的方法主要有二种:(1)利用真核细胞来表达。例如用酵母细胞、用cos-1动物细胞来表达、用cho细胞、或用昆虫细胞进行表达。
利用真核细胞表达蛋白的最大优点是表达的蛋白可以部分或完全糖基化,因而更接近天然蛋白构型。但其缺点是表达量普遍较低,而生产成本很高、生产工艺复杂。(2)利用大肠杆菌制备gm-csf。既然糖基化对gm-csf的生物学活性并无意义,那么用大肠杆菌(e.coli)表达gm-csf就十分合适。目前大部分重组gm-csf均是来源于e.coli。大肠杆菌制备gm-csf的优点是低成本和高表达。目前使用大肠杆菌制备gm-csf时,均采用胞浆表达法,所表达的gm-csf在大肠杆菌胞浆中以不溶性的包含体(inclusionbodies)形式存在。这种表达体系的缺点主要表现在以下两个方面:(a)在纯化过程中必须使用变性剂或去污剂,需要变性和复性的过程,这给下游的纯化工作带来困难,同时也降低了产品的最终得率;(b)这种表达体系更大的缺点是使表达的gm-csf的n端比天然gm-csf多了一个甲硫氨酸残基(met)。因此在体内应用时可能会刺激机体产生抗体,从而影响疗效并加大了副作用。
因此,提供一种方便高效地生产gm-csf的方法具有重要的现实意义。
技术实现要素:
有鉴于此,本发明提供植物生产口服重组人粒细胞集落刺激因子的应用。本发明利用植物尤其是生菜作为重组蛋白生产的高效平台技术,表达了重组人粒细胞集落刺激因子。并且制成口服重组人粒细胞集落刺激因子。本发明对具有降糖作用的活性多肽进行结构改造和修饰,使其获得可通过肠道进行吸收并在体内达到有效治疗浓度的特性,并通过植物来生产该活性物质。
为了实现上述发明目的,本发明提供以下技术方案:
本发明提供了植物作为宿主生产重组人粒细胞集落刺激因子的应用;所述植物选自生菜、菠菜、番茄、萝卜、白菜、玉米、大豆、小麦或烟草;所述植物的器官选自种子、叶、根茎或整株植物。
在上述研究的基础上,本发明提供了一种表达载体,包括重组人粒细胞集落刺激因子的核苷酸序列以及叶绿体表达载体。
在本发明的一些具体实施方案中,所述重组人粒细胞集落刺激因子的序列为将重组人粒细胞集落刺激因子的密码子优化为植物偏好的密码子,获得优化序列。
在本发明的一些具体实施方案中,所述优化序列如seqidno.2所示;所述重组人粒细胞集落刺激因子的氨基酸序列如seqidno.1所示。
在本发明的一些具体实施方案中,其构建方法包括如下步骤:
步骤1:将重组人粒细胞集落刺激因子的密码子优化为植物偏好的密码子,获得优化序列;
步骤2:将步骤1获得的所述优化序列克隆到puc57载体中,获得puc57-csf。
本发明还提供了所述的表达载体在表达重组人粒细胞集落刺激因子中的应用。
本发明还提供了一种植物作为宿主表达重组人粒细胞集落刺激因子的方法,将所述的表达载体用基因枪轰击叶片,在植物叶绿体中表达后获得再生植株,将植物叶片冻干粉碎,灌装胶囊,制成重组人粒细胞集落刺激因子。
在本发明的一些具体实施方案中,所述植物选自生菜、菠菜、番茄、萝卜、白菜、玉米、大豆、小麦或烟草;所述植物的器官选自种子、叶、根茎或整株植物。
在本发明的一些具体实施方案中,所述基因枪轰击包括如下步骤:
步骤1:准备转化用载体
步骤2:准备微粒子弹;
步骤3:基因枪轰击;
步骤4:转换后培养、再生为植株。
本发明通过植物叶绿体表达技术是利用基因枪轰击、同源重组的方式将含有目标蛋白的质粒转移到植物叶绿体中,获得该基因植物叶绿体中高效表达的技术。与动物细胞表达系统相比,植物表达系统的成本非常低,仅为其千分之一到千分之二。
本发明利用植物叶片,生产口服重组人粒细胞集落刺激因子。该降糖产品不需要注射,减轻病患的痛苦,同时这一产品为长效降糖产品,病患可以做到一周用药一次。生菜不含有植物有毒物质,而且本产品不需蛋白纯化流程,可以大大缩短生产周期和生产成本。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
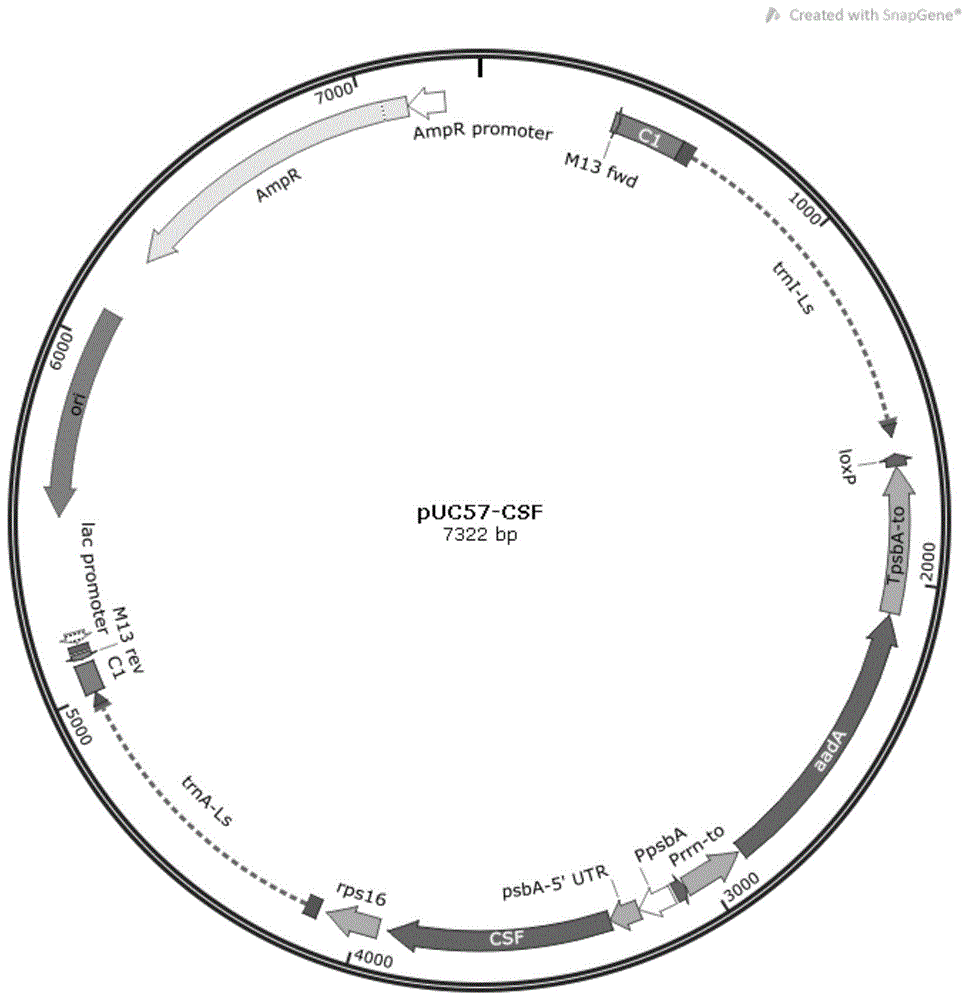
图1示载体puc57-csf示意图;
图2示western-blot结果;
图3示生菜表达g-csf能显著改善mptp诱导的小鼠行为异常。
具体实施方式
本发明公开了植物作为宿主在表达重组人粒细胞集落刺激因子的应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
本发明提供了植物作为宿主在表达重组人粒细胞集落刺激因子的应用。优选的,所述植物选自生菜、菠菜、番茄、萝卜、白菜、玉米、大豆、小麦或烟草;所述植物的器官选自种子、叶、根茎或整株植物。本发明还提供了一种表达载体,包括重组人粒细胞集落刺激因子序列以及载体。
在本发明的一些具体实施方案中,所述重组人粒细胞集落刺激因子密码子优化为植物偏好的密码子。
在本发明的一些具体实施方案中,所述优化的重组人粒细胞集落刺激因子的氨基酸序列如seqidno.1所示;所述优化的重组人粒细胞集落刺激因子的核苷酸序列如seqidno.2所示。
在本发明的一些具体实施方案中,所述载体为植物叶绿体载体。
在本发明的一些具体实施方案中,所述表达载体的构建方法包括如下步骤:
步骤1:将重组人粒细胞集落刺激因子的密码子优化为植物偏好的密码子;
步骤2:由金斯瑞进行基因合成克隆到puc57载体中,获得puc57-csf克隆载体;
具体的,为了提供外源蛋白在植物中的高效表达,本发明将重组人粒细胞集落刺激因子氨基酸序列利用反翻译软件(https://www.ebi.ac.uk/tools/st/emboss_backtranseq/)得到核苷酸序列,并将其密码子优化为植物偏好的密码子,由金斯瑞公司(南京,中国)合成。并由金斯瑞克隆到puc57载体中,获得puc57-csf载体(图1)。
本发明还提供了所述的表达载体在表达重组人粒细胞集落刺激因子中的应用。
将本发明提供的表达载体用基因枪轰击植物叶片,再生为植株后收获植物叶片并制成口服重组人粒细胞集落刺激因子。
本发明提供的植物作为宿主在表达重组人粒细胞集落刺激因子中的应用中所用原料及试剂均可由市场购得。
下面结合实施例,进一步阐述本发明:
实施例1叶绿体表达载体的构建
为了将外源蛋白在植物中的高效表达,将重组人粒细胞集落刺激因子氨基酸序列利用反翻译软件(https://www.ebi.ac.uk/tools/st/emboss_backtranseq/)得到核苷酸序列,并将其密码子优化为植物偏好的密码子,由金斯瑞公司(南京,中国)合成。
实施例2转化材料准备
将植物种子用无菌水浸泡过夜,用70%乙醇浸泡1分钟后用无菌水冲洗1次;再用2%naclo(加0.1%tween-20)处理15分钟,每5分钟轻柔混匀1次,无菌水冲洗4-5次;用无菌滤纸吸干后种植于1/2ms培养基上(含3%蔗糖、0.7%琼脂粉、ph值为5.8),置于光照培养箱中25℃,16h光照8h黑暗培养,约3周可用于转化。
实施例3基因枪准备
称取50-60mg金粉(0.6μm)于干燥的1.5ml灭菌ep离心管。加入1ml无水乙醇,涡旋2分钟。加入1ml无菌水,涡旋1分钟,室温放置1分钟,10,000rpm离心2分钟,去上清。加入1ml50%甘油,重悬金粉,-20℃冻存。甘油保存状态的金粉悬液涡旋5分钟使金粉重悬。取50μl金粉悬液于无菌1.5ml离心管,涡旋1分钟。加入10μg质粒dna,涡旋30秒。加入50μl2.5mcacl2,涡旋30秒。加入20μl0.1m亚精胺,混合物涡旋5分钟,冰上静置2分钟。加60μl预冷的无水乙醇,手指轻弹使之重悬,14,000rpm离心10秒,去上清,重复一次。加入50μl无水乙醇重悬,备用。
实施例4基因枪轰击
根据样品数量取一定数量的载体膜、可裂膜、阻挡网(注意:载体膜、可裂膜需每枪更换,阻挡网同一个样品可共用)于无水乙醇中浸泡15分钟,用无菌水冲洗2次,自然晾干,备用。将晾干的载体膜放入无菌铁环中,压平。将制备好的子弹涡旋充分混匀,取10μl子弹于载体膜中央,自然晾干。把微粒发射装置移出轰击室,旋下盖子,加入阻挡网,把微粒载片安装在固定槽中(有微粒的一面朝下),旋上盖子,将微粒发射装置放回轰击室。
实施例5转化后培养及筛选
1.暗培养:将轰击后的生菜叶片剪下,切成10~20mm2的叶盘置于rmol培养基(不加抗生素)中25℃暗培养2天。
2.筛选培养:将暗培养结束的材料转移至筛选培养基(抗生素浓度为50μg/ml)中进行筛选培养。
3.生根培养:将芽转移至生根培养基(抗生素浓度为100μg/ml)中诱导生根。
实施例6westernblot检测目的蛋白表达情况
采用液氮研磨、变性裂解提取植物蛋白,将裂解上清和5×上样缓冲液(使用前加入β-巯基乙醇至终浓度为5%)按4:1的比例混合(如200μl蛋白裂解上清与50μl5×上样缓冲液混合),混匀,95℃加热6min,同时处理阴性对照及阳性对照;电泳电压积层胶80v,分离胶120v,待目的蛋白跑至分离胶中间位置后,停止电泳,回收下槽电泳液,拆开电泳装置,按照负极(黑色)、海绵、滤纸、凝胶、pvdf膜(事先用甲醇活化15s、ddh2o洗涤后浸泡于1×转移缓冲液中)或nc膜(不需活化)、滤纸、海绵、正极(透明)的顺序放置,排气泡后组装,放入电泳槽(注黑色对应电泳槽黑色一面放入),加满转移缓冲液,将整个电泳槽放入冰水混合液中,90v电泳1.0h;电泳快结束时配制5%脱脂奶粉(封闭液),将转移后的膜放入封闭液中室温封闭至少1h,4℃孵育一抗过夜(一抗稀释于5%脱脂奶粉中,稀释比参考说明书);使用pbst或tbst洗涤15min×3次,室温孵育二抗1~2h,pbst或tbst洗涤15min×3次,采用dab试剂盒进行显色,拍照,分析目的蛋白表达情况:如图1所示,非表达生菜没有目的蛋白检出,表达植株能检出目的蛋白条带,大小符合预期,证明csf已经在生菜叶片中表达。
实施例7重组人粒细胞集落刺激因子活性检测
1-甲基-4-苯基-1,2,3,6-四氢吡啶(mptp),可以特异性的损伤多巴胺能神经元,出现类似帕金森氏病(pd)的症状。实验选取c57/bl6j小鼠,雄性,20-22g,12-14周,动物饲养于室温24±2℃的环境中,维持光-暗12小时循环交替。30只小鼠随机分成3组,每组10只,分别为溶剂对照组、mptp模型组、mptp+生菜表达csf组。mptp以30mg/kg的剂量腹腔注射,连续注射5天,csf为40ug/kg口服给药(从第7天起)连续5天。溶剂对照组为生理盐水。第12天对小鼠进行行为学评价。
将小鼠向上轻柔的放在粗糙的杆顶(直径8mm,高55cm)。小鼠从头向上调整至完全向下的时间记录为t1,小鼠从向下运动至四肢全部到达杆底的时间记录为t2。每只小鼠重复检测5次取平均值。
表1数据表明结果表明,生菜表达g-csf能显著改善mptp诱导的小鼠行为异常。如图3。
表1csf改善mptp效果时长
*示与对照相比p≤0.05。
实施例8动物毒性试验
将7周大小的实验用小白鼠随机分为三个治疗组,每组10只,分别接收含有降糖蛋白(按照体重喂食500ng/g)(本发明得到的重组人粒细胞集落刺激因子),及不含降糖蛋白两种实验胶囊中的一种,接受相同的实验饮食。连续喂食10天,每次喂食后实进行观察,每天需要连续观察6小时以上,并没有看小鼠处于兴奋状态还是抑制状态,没有出现行动迟缓等现象,也没有出现腹泻等情况。证明重组人粒细胞集落刺激因子口服安全性高。
实施例9
实验组1:本发明提供的植物生产重组人粒细胞集落刺激因子;
对照组1:利用酵母细胞生产重组人粒细胞集落刺激因子;
实验组2:利用烟叶生产重组人粒细胞集落刺激因子;
表2重组人粒细胞集落刺激因子
*示与对照组1相比p≤0.05;**示与对照组1相比p≤0.01;
#示与实验组2相比p≤0.05;##示与实验组2相比p≤0.01;
由表2可知,实验组1与对照组1的动物系统相比,本发明提供的生菜瞬时表达重组人粒细胞集落刺激因子,简化了蛋白纯化的难易程度,极显著(p≤0.01)降低了生产成本。
实验组1与实验组2的烟叶系统相比,生菜瞬时表达重组人粒细胞集落刺激因子,简化了蛋白纯化的难易程度,显著(p≤0.05)降低了生产成本。
实验组2与对照组相比,烟叶瞬时表达重组人粒细胞集落刺激因子比动物系统简化了蛋白纯化的难易程度,显著(p≤0.05)降低了生产成本。
综合上述试验结果表明,植物系统尤其是生菜系统是更加经济、高效的表达平台。能够快速瞬时表达重组蛋白质,可以在短时间内大规模生产重组人粒细胞集落刺激因子。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
序列表
<110>王跃驹
<120>植物生产口服重组人粒细胞集落刺激因子
<130>mp1909370
<160>2
<170>siposequencelisting1.0
<210>1
<211>207
<212>prt
<213>recombinanthumangranulocytecolony-stimulatingfactor
<400>1
metalaglyproalathrglnserprometlysleumetalaleugln
151015
leuleuleutrphisseralaleutrpthrvalglnglualathrpro
202530
leuglyproalaserserleuproglnserpheleuleulyscysleu
354045
gluglnvalarglysileglnglyaspglyalaalaleuglnglulys
505560
leuvalserglucysalathrtyrlysleucyshisproglugluleu
65707580
valleuleuglyhisserleuglyileprotrpalaproleuserser
859095
cysproserglnalaleuglnleualaglycysleuserglnleuhis
100105110
serglyleupheleutyrglnglyleuleuglnalaleugluglyile
115120125
serprogluleuglyprothrleuaspthrleuglnleuaspvalala
130135140
aspphealathrthriletrpglnglnmetglugluleuglymetala
145150155160
proalaleuglnprothrglnglyalametproalaphealaserala
165170175
pheglnargargalaglyglyvalleuvalalaserhisleuglnser
180185190
pheleugluvalsertyrargvalleuarghisleualaglnpro
195200205
<210>2
<211>624
<212>dna
<213>recombinanthumangranulocytecolony-stimulatingfactor
<400>2
atggccggccccgccacccagagccccatgaagctgatggccctgcagctgctgctgtgg60
cacagcgccctgtggaccgtgcaggaggccacccccctgggccccgccagcagcctgccc120
cagagcttcctgctgaagtgcctggagcaggtgaggaagatccagggcgacggcgccgcc180
ctgcaggagaagctggtgagcgagtgcgccacctacaagctgtgccaccccgaggagctg240
gtgctgctgggccacagcctgggcatcccctgggcccccctgagcagctgccccagccag300
gccctgcagctggccggctgcctgagccagctgcacagcggcctgttcctgtaccagggc360
ctgctgcaggccctggagggcatcagccccgagctgggccccaccctggacaccctgcag420
ctggacgtggccgacttcgccaccaccatctggcagcagatggaggagctgggcatggcc480
cccgccctgcagcccacccagggcgccatgcccgccttcgccagcgccttccagaggagg540
gccggcggcgtgctggtggccagccacctgcagagcttcctggaggtgagctacagggtg600
ctgaggcacctggcccagccctga624
- 还没有人留言评论。精彩留言会获得点赞!