一种MAPK6P2基因的靶向抑制剂及其用途的制作方法
本发明属于生物医药技术领域,具体涉及一种mapk6p2基因的靶向抑制剂及其用途。
背景技术:
胶质瘤是最常见的原发性中枢神经系统肿瘤,年发病率为3~8人/10万人,构成比占所有恶性中枢神经系统肿瘤的45.2%和所有原发性恶性中枢神经系统肿瘤的80%。按照目前的治疗标准,即先进行最大安全范围的手术切除,再进行术后放疗,同时辅以化疗如替莫唑胺等,以及抗血管生成药物治疗。但胶质瘤中组织病理学诊断中的低分化、高分级的患者预后较差,iv级胶质瘤患者的中位生存期仅为12~18个月。近年来在针对胶质瘤发病机制的研究中,假基因在转录和转录后等水平上对胶质瘤细胞生物学行为的调控作用受到越来越多研究者高度重视。因此深入研究假基因调控胶质瘤细胞生物学行为的作用与机制,可能为胶质瘤分子治疗提供新靶标。
假基因又称伪基因,与正常基因相似,但丧失基因功能的dna序列。以往认为它是基因家族在进化过程中形成的无功能的残留物,一般情况不被转录,因此没有明确生理意义,往往存在于真核生物的多基因家族中。近期研究表明,假基因与非编码rna的功能相似,在转录和转录后等水平上发挥重要的分子调控作用,并且参与多种恶性肿瘤的发生和发展的调节作用,在人呼吸系统、消化系统和神经系统等多种系统肿瘤中发挥重要调节作用。
mapk6p2基因定位于21q21.1,其亲本基因mapk6定位于人染色体15q21.2。编码核苷酸序列长为4036bp。目前尚未检索到mapk6p2在胶质瘤中相关的研究报道。rna干扰技术的原理是利用dicer酶切割rna分子,形成rna沉默复合体,靶向结合目标rna分子进而降解rna分子的过程,可在医学应用中起治疗作用。其中shrna是一种茎环间隔的两个短反向互补序列组成的人工rna,作为一种常用的rna干扰工具,shrna和靶基因mrna结合发挥作用。由于sirna存在脱靶效应,或影响对正常基因表达,因而目前shrna技术更为安全和可靠。
目前,mapk6p2在肿瘤发生发展中的作用以及相关机制尚未见报道,关于mapk6p2在胶质瘤基因治疗方面的应用目前还不明确。因此,研制一种mapk6p2相关的药物成为目前亟待解决的问题。
技术实现要素:
鉴于现有技术存在的问题,本发明的目的在于提供一种mapk6p2基因的靶向抑制剂及其用途。经本发明实验证明mapk6p2基因在胶质瘤在组织中高表达,通过抑制mapk6p2基因的表达从而抑制胶质瘤细胞增殖、迁移和侵袭能力。本发明利用rna干扰技术研制一种mapk6p2基因的靶向抑制剂,该抑制剂可与mapk6p2基因特异性结合,使mapk6p2基因沉默,从而抑制胶质瘤细胞增殖、迁移和侵袭能力,达到治疗胶质瘤的目的。mapk6p2基因的靶向抑制剂在胶质瘤基因治疗与分子靶向治疗领域发挥重要作用,为临床治疗胶质瘤提供新的靶向治疗药物。
为了实现上述目的,本发明采用以下技术方案。
一种mapk6p2基因的靶向抑制剂,该抑制剂的靶向序列为:5’-gcgagtgaagttaaccattac-3’(seqidno.1)。
进一步地,所述的mapk6p2基因的靶向抑制剂能够抑制mapk6p2基因表达的shrna序列,所述shrna模板序列包括正义链和反义链,所述正义链和反义链分别为:
正义链:
5’-caccgcgagtgaagttaaccattacttcaagagagtaatggttaacttcactcgcttttttg-3’(seqidno.2)。
反义链:
5’-gatccaaaaaagcgagtgaagttaaccattactctcttgaagtaatggttaacttcactcgc-3’(seqidno.3)。
进一步地,获得一种转录上述的shrna的转录产物,序列为:
5’-gcgagtgaagttaaccattacttcaagagagtaatggttaacttcactcgctt-3’(seqidno.4)。
优选地,该抑制剂的剂型为注射制剂。
优选地,该抑制剂为任何药物治疗学上可接受的的剂型。
优选地,该抑制剂为任何药物治疗学上可接受的的剂量。
所述的mapk6p2基因的靶向抑制剂在制备用于治疗人脑胶质瘤药物中的应用。
与现有技术相比,本发明的有益效果如下。
1)本发明提供的mapk6p2基因的靶向抑制剂特异性强,沉默效率高,脱靶率低,抑制mapk6p2基因的表达。
2)本发明涉及通过mapk6p2基因的抑制剂抑制人mapk6p2基因的表达,从而抑制胶质瘤细胞增殖、迁移和侵袭能力,为胶质瘤的基因治疗提供全新的治疗方法。
3)本发明提供的mapk6p2基因的抑制剂的靶向治疗能显著降低传统治疗药物的耐药问题。
4)本发明提供的mapk6p2基因的抑制剂已在体外细胞学水平上进行应用研究,实验证明mapk6p2基因的抑制剂的靶向治疗效果确切,并且无不良反应发生。
附图说明
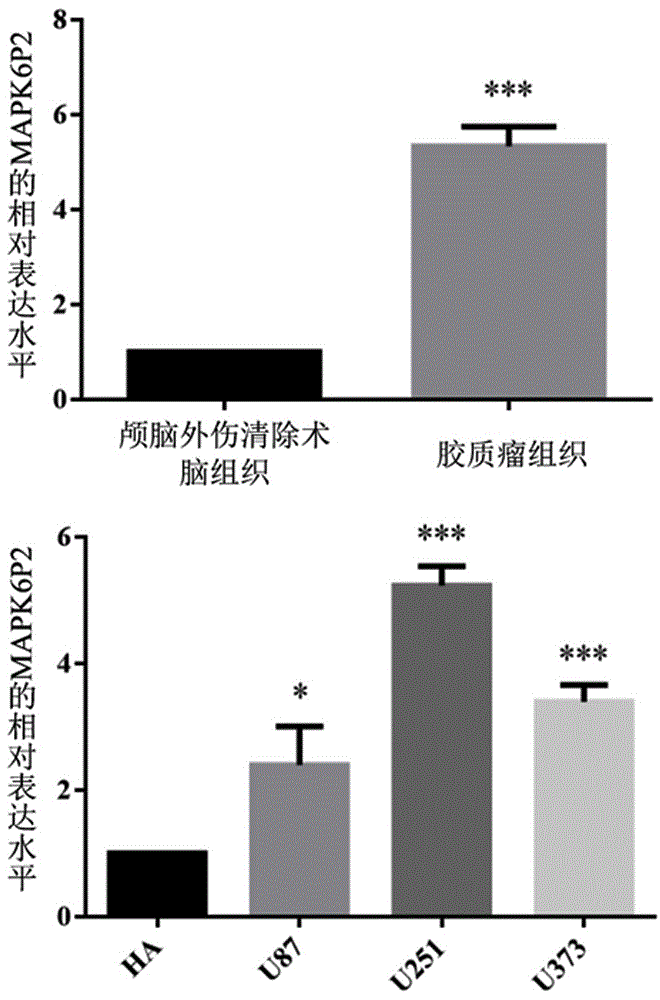
图1是应用realtimepcr检测mapk6p2基因在胶质瘤组织和细胞中的表达水平显著增高的柱状图。
图2是应用realtimepcr检测应用mapk6p2基因抑制剂后,胶质瘤细胞中的mapk6p2表达水平显著下调的柱状图。
图3是cck-8细胞活力法检测应用mapk6p2基因抑制剂后,抑制胶质瘤细胞增殖能力的统计图。
图4是transwell细胞迁移实验检测应用mapk6p2基因抑制剂后,抑制胶质瘤细胞迁移能力的照片和统计图。
图5是transwell细胞侵袭实验检测应用mapk6p2基因抑制剂后,抑制胶质瘤细胞侵袭能力的照片和统计图。
具体实施方式
下面结合具体实施例和附图详细介绍本发明的技术方案和技术效果。未注明具体条件的实验方法,通常按照常规条件,例如教科书和实验指南中所述的条件,或按照制造厂商所建议的条件,为本领域普通技术人员熟知或易于获知,以下实施例仅为本发明的优选实施例,并不限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
实施例一shrna的设计与干扰载体的制备及mapk6p2基因抑制剂应用。
一、细胞培养。
人胶质瘤细胞系u87、u251、u373和人星形胶质细胞(ha)购自上海研究院生命科学细胞资源中心。在100mm细胞培养皿中用含10%胎牛血清的dmem高糖培养液(星形胶质细胞培养基am)培养u87、u251、u373和ha细胞,每2天更换一次培养液,约2-3天细胞可长至单层。
二、实时定量pcr检测mapk6p2的表达。
1.trizol法提取细胞中的总rna。
冷pbs洗涤收集的细胞,加入1mltrizol试剂吹打数次,镜下观察细胞成油滴状(充分裂解),后移入1.5mlep管中,静置5分钟,使其充分裂解;样品中加入0.2ml氯仿,手动剧烈震荡室温下静置3分钟;于4℃12000g离心15分钟,取上层水相到新的ep管中,再加入0.5ml异丙醇,上下颠倒混匀,室温下静置10分钟;4℃12000g离心15分钟后弃上清,加入1ml75%乙醇;4℃7500g离心5分钟,干燥15分钟后加入40μldepc水,样品可冻存于-80℃冰箱。
2.一步染料法qrt-pcr检测mapk6p2的表达。
测定ct值,以b-actin为内参照,以2^(-△△ct)计算mapk6p2的相对表达量。检测mapk6p2基因在胶质瘤组织和细胞中的表达水平显著增高的统计图,如图1所示。
三、mapk6p2基因抑制剂的制备和应用。
设计mapk6p2基因的干扰序列,选定靶向人mapk6p2基因并特异性抑制mapk6p2基因表达的抑制剂靶向序列如下:5’-gcgagtgaagttaaccattac-3’。
在ncbi的同原序列比对分析nucleotideblast中输入gcgagtgaagttaaccattac序列进行比对分析,结果表明该序列和人的其它mrna基因没有高度同源性,可作特异性干扰mapk6p2基因的特异性序列。进一步设计该靶向抑制剂的shrna序列,如下,包括正义链和反义链。
此shrna正义链序列为:
5’-caccgcgagtgaagttaaccattacttcaagagagtaatggttaacttcactcgcttttttg-3’。
此shrna反义链序列为:
5’-gatccaaaaaagcgagtgaagttaaccattactctcttgaagtaatggttaacttcactcgc-3’。
所述的shrna的转录产物,序列为:
5’-gcgagtgaagttaaccattacttcaagagagtaatggttaacttcactcgctt-3’。
序列信息设计并合成相应质粒,作为mapk6p2基因抑制剂。
mapk6p2基因抑制剂转染:sh-nc、sh-mapk6p2的质粒u6/gfp/neo,使mapk6p2表达沉默,不含有mapk6p2序列或shrna的空质粒为实验阴性对照;应用24孔培养板培养胶质瘤细胞,当细胞生长达到80%左右时进行转染;配置转染需要的质粒、opti-mem®ⅰ和ltxandplusreagent(lifetechnologies)转染试剂。a管:一个孔按照1μg质粒dna溶解于50µlopti-mem®ⅰ+1µlp3000,放置5min,b管:孔按照1µlltxandplus溶解于50µlopti-mem®ⅰ中;将a、b两管混匀后静置5min;吸出培养液,每孔加入转染混合液100µl,再加入ebm-2培养液400µl;48h后用含有浓度为0.4mg/ml抗生素g418的培养基进行筛选,不断增加g418的浓度,大约4周后得到能够稳定沉默mapk6p2的胶质瘤细胞系。在后续实验中分为3组,分别是:不加任何处理的空白对照组(control);转染mapk6p2沉默空质粒的阴性对照组(sh-nc);转染mapk6p2沉默质粒的实验组(sh-mapk6p2)。mapk6p2基因抑制剂后,胶质瘤细胞中的mapk6p2表达水平显著下调的统计图,如图2所示。
实施例2应用mapk6p2基因抑制剂显著抑制胶质瘤的恶性生物学行为。
一、cck-8细胞活力法检测mapk6p2基因抑制剂对胶质瘤细胞增殖能力的影响。
u251细胞用胰蛋白酶消化,分别用正常培养液制成单细胞悬液。计数细胞,以2000个/孔的浓度接种于96孔细胞培养板。每组设5个复孔,每孔共计200µl。24h后加入10µlcck-8。2小时后用酶标仪测定波长450nm时各孔光吸收值。cck-8细胞活力法检测应用mapk6p2基因抑制剂后,抑制u251细胞增殖的统计图,如图3所示。
二、transwell细胞迁移实验检测mapk6p2基因抑制剂对胶质瘤细胞迁移能力的影响。
检测细胞迁移能力:在24孔板中各孔添加600µl含有血清的培养液,之后放上transwell小室;将不同组的u251细胞用胰酶消化后轻轻吹散后离心,加入不含血清的培养液将细胞进行重悬,各个小室里添加100µl细胞悬液,均匀地铺在上室,大概有105个细胞。放置于37℃细胞培养箱中培养24h;24h后拿出小室,使用棉签轻轻把上室里面擦干净,使用pbs清洗小室并晾干。之后配置固定液,根据甲醇∶冰乙酸=3∶1的配比进行配置,即750µl的甲醇+250µl的冰乙酸吹打混匀;把小室浸没到固定液中固定细胞30min;使用pbs清洗小室并晾干,把吉姆约200µl萨染料铺于倒置小室底部,染色至少30min;使用pbs清洗小室两次,放于倒置显微镜下,在400×镜下观察,随机选择5个视野进行细胞个数统计,体现细胞迁移能力。transwell细胞迁移实验检测应用mapk6p2基因抑制剂后,u251细胞迁移数目显著减少,如图4所示。
三、transwell细胞侵袭实验检测mapk6p2基因抑制剂对胶质瘤细胞侵袭能力的影响。
检测细胞侵袭能力:在24孔板中各孔添加600µl含有血清的培养液,之后放上transwell小室,在小室中加入50µl的matrigel胶原液,37℃细胞培养箱中培养30mins;将不同组的u251细胞用胰酶消化后轻轻吹散后离心,加入不含血清的培养液将细胞进行重悬,各个小室里添加100µl细胞悬液,均匀地铺在上室,大概有105个细胞。放置于37℃细胞培养箱中培养24h;24h后拿出小室,使用pbs清洗小室并晾干。之后配置固定液,根据甲醇∶冰乙酸=3∶1的配比进行配置,即750µl的甲醇+250µl的冰乙酸吹打混匀;把小室浸没到固定液中固定细胞30min;使用pbs清洗小室并晾干,把吉姆约200µl萨染料铺于倒置小室底部,染色至少30min;使用pbs清洗小室两次,放于倒置显微镜下,在400×镜下观察,随机选择5个视野进行细胞个数统计,体现细胞侵袭能力。transwell细胞侵袭实验检测应用mapk6p2基因抑制剂后,抑制u251细胞迁移数目显著减少,如图5所示。
统计学方法:以上所有的实验都单独重复进行三次,数据均以平均值±标准差表示。多组数据间利用统计软件spss19.0,使用单因素方差分析(anova)法进行分析,明确组间是否存在差异,当p值<0.05视为有统计学意义。ic50应用graphpad软件进行计算。
序列表
<110>中国医科大学附属盛京医院
<120>一种mapk6p2基因的靶向抑制剂及其用途
<130>4
<160>4
<170>patentinversion3.3
<210>1
<211>21
<212>dna
<213>人工序列
<400>1
gcgagtgaagttaaccattac21
<210>2
<211>62
<212>dna
<213>人工序列
<400>2
caccgcgagtgaagttaaccattacttcaagagagtaatggttaacttcactcgcttttt60
tg62
<210>3
<211>62
<212>dna
<213>人工序列
<400>3
gatccaaaaaagcgagtgaagttaaccattactctcttgaagtaatggttaacttcactc60
gc62
<210>4
<211>51
<212>dna
<213>人工序列
<400>4
gcgagtgaagttaaccattacttcaagagagtaatggttaacttcactcgctt53
- 还没有人留言评论。精彩留言会获得点赞!