一种新型杂多钽酸盐及其制备方法和应用与流程
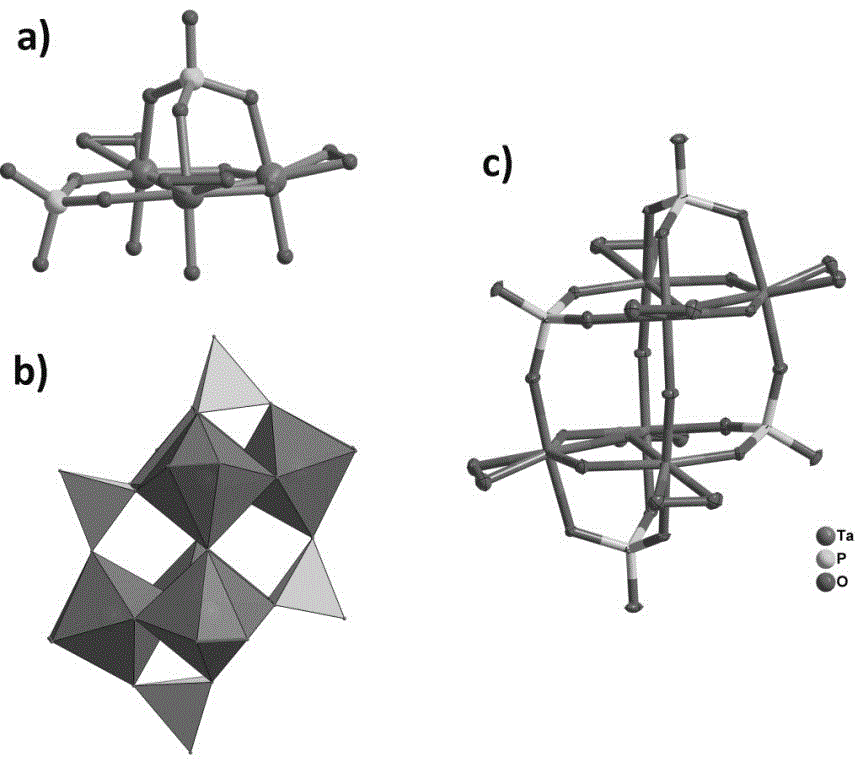
本发明属于多酸化学新材料技术领域,具体涉及一种新型杂多钽酸盐及其制备方法和应用。
背景技术:
多酸通常是由前过渡金属离子通过氧原子连接形成的一类多核配合物,在催化、材料、磁学、药物、纳米科学等领域扮演着越来越重要的角色。根据其是否包含杂原子,多酸可以分为同多酸(Isopolyoxometalate)和杂多酸(Heteropolyoxometalate)两大类。由同种无机含氧酸根离子缩合得到的是同多阴离子,如 [W6O19]2-;由不同种类的无机含氧酸根离子缩合得到的是杂多阴离子,如 [PW12O40]3-,其中,P 为杂原子(Hetero atom),又称中心原子,W 为配原子(Addenda atom),又称多原子。根据其多原子的不同,多酸又可以分为多钨氧酸盐(Polyoxotungstate)、多钼氧酸盐(Polyoxomolybdate)、多钒氧酸盐(Polyoxovanadate)、多铌氧酸盐(Polyoxoniobate)和多钽氧酸盐(Polyoxotantalate)。(参见Müller A, Peters F, Pope M T, Gatteschi D, Chem. Rev., 1998, 98, 239−271; Long D-L, Burkholder E, Cronin L, Chem. Soc. Rev., 2007, 36, 105−121; Long D-L, Tsunashima R, Cronin L, Angew. Chem. Int. Ed., 2010, 49, 1736–1758; Li F-Y, Xu L, Dalton Trans., 2011, 40, 4024–4034; Du D-Y, Yan L-K, Su Z-M, Li S-L, Lan Y-Q, Wang E-B, Coord. Chem. Rev., 2013, 257, 702–717; Miras H N, Vilà-Nadal L, Cronin L, Chem. Soc. Rev., 2014, 43, 5679−5699;Yin P, Wu B, Mamontov E,Daemen L L,Cheng Y, Li T, Seifert S, Hong K, Bonnesen P V, Keum J K, Ramirez-Cuesta A J, J. Am. Chem. Soc., 2016, 138, 2638−2643; Gong Q, Wang Y, Hu Q, Zhou J, Feng R, Duchesne P N, Zhang P, Chen F, Han N, Li Y, Jin C, Li Y, Lee S-T, Nat. Commun., 2016, DOI: 10.1038/ncomms13216.)。
虽然镧系收缩使铌和钽的原子半径、离子半径很接近,二者具有相似的化学性质,都可以形成典型的 Lindqvist 结构阴离子,[M6O19]8-(M = Nb、Ta)。但相对于铌来说,钽元素的化学惰性更强,尽管国内外多酸化学家在该领域付出了很大努力,然而到目前为止,钽多酸盐(Polyoxotantalate,POTa)依然主要局限于 [Ta6O19]8– 阴离子及其少量的简单衍生物。从结构上看,已报到的这些POTas可以分为同多钽氧酸六钽酸盐(Lindqvist I, Aronsson B, Ark. Foer Kemi, 1954, 7, 49–52; Nelson W H, Inorg. Chem., 1963, 2, 985–992; Shen L, Xu Y-Q, Gao Y-Z, Cui F-Y, Hu C-W, J. Mol. Struct., 2009, 934, 37–43; Abramov P A, Abramova A M, Peresypkina E V, Gushchin A L, Adonin S A, Sokolov M N, J. Struct. Chem., 2011, 52, 1012–1017; Matsumoto M, Ozawa Y, Yagasaki A, Inorg. Chem. Commun., 2011, 14, 115–117, Guo G-L, Xu Y-Q, Chen B-K, Lin Z-G, Hu C-W, Inorg. Chem. Commun., 2011, 14, 1448–1451; Matsumoto M, Ozawa Y, Yagasaki A, Inorg. Chem., 2012, 51, 5991–5993.)和钽十氧酸盐(Matsumoto M, Ozawa Y, Yagasaki A, Zhe Y, Inorg. Chem., 2013, 52, 7825–7827.)、基于Ta6O19的有机金属衍生物(Besserguenev A V, Dickman M H, Pope M T, Inorg. Chem., 2001, 40, 2582–2586; Abramov P A, Sokolov M N, Floquet S, Haouas M, Taulelle F, Cadot E, Peresypkina E V, Virovets A V, Vicent C, Kompankov N B, Zhdanov A A, Shuvaeva O V, Fedin V P, Inorg. Chem., 2014, 53, 12791–12798; Abramov P A, Sokolov M N, Virovets A V, Floquet S, Haouas M, Taulelle F, Cadot E, Vicent C, Fedin V P, Dalton Trans, 2015, 44, 2234–2239; Abramov P A, Vicent C, Kompankov N B, Gushchin A L, Sokolov M N, Eur. J.Inorg. Chem., 2016, 154–160.)、钽取代多钨氧酸盐(Li S, Liu S, Liu S, Liu Y, Tang Q, Shi Z, Ouyang S, Ye J, J. Am. Chem. Soc., 2012, 134, 19716–19721; Huang P, Qin C, Zhou Y, Hong Y-M, Wang X-L, Su Z-M, Chem. Commun., DOI: 10.1039/c6cc07649a; Huang P, Han X-G, Li X-L, Qin C, Wang X-L, Su Z-M, CrystEngComm, 2016, DOI: 10.1039/c6ce01953f.)和钛取代的同多钽酸盐(Son J-H, Casey W H, Chem.- Eur. J., 2016, 22, 14155–14157.)。2012 年,日本的 Yagasaki 和 Ozawa 教授合作得到了一例通过氢键键合的四聚钽酸盐化合物, TBA14[H18(Ta6O19)4]·2THF·22H2O(THF = 四氢呋喃,参见Matsumoto M, Ozawa Y, Yagasaki A, Inorg. Chem., 2012, 51, 5991–5993.);同年,我国刘术侠教授课题组成功得到了结构新颖的钽取代多钨氧酸盐,K5Na4[P2W15O59(TaO2)3]·17H2O、Cs3K3.5H0.5[SiW9(TaO2)3O37]·9H2O、Cs10.5K4H5.5[Ta4O6(SiW9Ta3O40)4]·30H2O和K8Na8H4[P8W60Ta12(H2O)4(OH)8O236]·42H2O,并对该系列化合物的光催化产氢性能进行了研究(参见Li S, Liu S, Liu S, Liu Y, Tang Q, Shi Z, Ouyang S, Ye J, J. Am. Chem. Soc., 2012, 134, 19716–19721.)。2016年,苏忠民教授课题组报道了基于Keggin、Wells-Dawson型钽取代多钨氧酸盐过渡、稀土金属衍生物,Cs5K2[(Si2W18Ta6O78)Cr(H2O)4]·8H2O和Cs3K4H2[(Si2W18Ta6O78)FeCl2(H2O)2]·15H2O、Cs16K16Na4[Ta18P12W90(OH)6(H2O)2O360]·24H2O和 Cs26K2H2[Yb2Ta18P12W90(OH)6(H2O)16O360]·52H2O(参见Huang P, Qin C, Zhou Y, Hong Y-M, Wang X-L, Su Z-M, Chem. Commun.,DOI: 10.1039/c6cc07649a; Huang P, Han X-G, Li X-L, Qin C, Wang X-L, Su Z-M, CrystEngComm, 2016, DOI: 10.1039/c6ce01953f.)。最近美国Casey教授采用水热合成法得到了两例钛取代的钽酸盐TMA8Ti2Ta8O28·21H2O和TMA10Ti12Ta6O44·39H2O,这是目前唯一的两例过渡金属取代同多钽氧簇(参见Son J-H, Casey W H, Chem.- Eur. J., 2016, 22, 14155–14157.)。综上所述可知,多钽酸盐仍然处于萌芽阶段,与其有关的研究还很少,而且到目前为止还未见杂多钽酸盐的报道。
技术实现要素:
本发明的目的是提供一种新型杂多钽酸盐及其制备方法和应用。
为实现上述目的,本发明采用的技术方案是,一种新型杂多钽酸盐,其化学式为K3[H3P4(TaO2)6(OH)4O20]·12H2O,该杂多钽酸盐属于单斜晶系,空间群为P21/c,晶胞参数为:a= 12.6862(10) Å,b = 9.9322(8) Å,c = 16.8359(13) Å;β = 105.3940(10)°。
所述新型杂多钽酸盐采用常规水溶液法制备,具体步骤为:
(1)按照本领域常规方法合成六钽酸钾盐K8[Ta6O19]·16H2O前驱体(具体参考文献Nelson W H, Tobias R S, Inorg. Chem., 1963, 2 , 985–992)。
(2)将K8[Ta6O19]·16H2O溶解在双氧水溶液中,室温搅拌至澄清,然后加入磷酸溶液(本领域技术人员可以通过常规技术来确定磷酸溶液的用量),接着用氢氧化钠溶液调pH至2.1-2.7,在80-90℃反应3-4小时,冷却至室温,加入固体氯化钾并在室温下搅拌25~35min,过滤除去沉淀后放置8-10天,得晶体,晶体经后处理(洗涤、干燥)即得。其中,K8[Ta6O19]·16H2O、H3PO4和KCl的物质的量比为1:(20-26): 10。
优选的,上述方法步骤(2)中,所述磷酸溶液的浓度为3 mol/L;所述双氧水溶液的使用是本领域的常规技术,本领域技术人员也可以根据需要选择合适浓度的双氧水溶液;所述氢氧化钠溶液的浓度为1 mol/L或2 mol/L。
本发明以双氧水为介质,一方面双氧水可以有效的防止六钽酸钾的水解,另一方面在酸性条件下六钽酸钾能形成钽过氧活性基团。加入磷酸以后,在加热条件下随着部分铌过氧键的断裂同时形成P-O-Ta键,从而形成杂多磷钽酸盐。
本发明新型杂多钽酸盐的结构描述如下:化合物分子包含三个K+ 离子、一个[H3P4(TaO2)6(OH)4O20]3- 聚阴离子和十二个个结晶水。X-射线单晶衍射分析结果表明,[P4(TaO2)6O24]10- (1a) 阴离子单元是由两个 [P2(TaO2)3O14]14- (P2Ta3) 亚单元通过四个氧原子共角连接而成。其中,每个磷原子与三个 m2-桥氧和一个端氧原子配位形成四面体构型,每个钽原子与四个 m2-桥氧,一个 m3-桥氧和一个端位的过氧单元配位形成扭曲的 TaO7五角双锥构型。在多阴离子1a中,Ta-Operoxo的平均键长为1.95 Å,Operoxo-Ta-Operoxo的平均键角为 44.88°,Operoxo-Operoxo的平均距离是 1.49 Å,与过氧化氢单晶结构中所观察到过氧键的键长(1.49 Å)一致(参见Abrahams S C, Collin R L, Lipscomb W N, Acta Crystallogr. 1951, 4, 15–20.)。键价计算(参见Brown I D, Altermatt D, Acta Crystallographica, 1985, B41, 244–247.)表明,1a中所有 P、Ta 中心的价态都是 +5 价,而 O4、O10、O16 和 O18 的价键值分别为 -1.38、-1.32、-1.38 和-1.32。一般来说,单质子化的价键值在 -1.0 左右,考虑到这些数值较高,我们认为这些氧原子介于单质子化和非质子化之间。因此,1a 阴离子应该写为[P4(TaO2)6(OH)4O20]6-。元素分析结果表明化合物1 含有三个钾抗衡阳离子,从电荷平衡的角度分析,化合物1 仍需要添加三个质子来平衡电荷,但这些质子的位置不能通过 X-射线衍射精确地确定,可能局部离域在多阴离子上,这种现象在多酸化学中是非常常见的(参见Bontchev R P, Nyman M, Angew. Chem. Int. Ed, 2006,45, 6670–6672 ; Niu J, Ma P, Niu H, Li J, Zhao J, Song Y, Wang J, Chem. Eur. J, 2007,13, 8739–8748 ; Zheng S T, Zhang J, Clemente-Juan J M, Yuan D-Q, Yang G-Y, Angew Chem Int Ed, 2009,48, 7176–7179.)。据我们所知,这是到目前为止首例杂多钽酸盐。XRD结果表明,本发明新型杂多钽酸盐样品纯度高,用于光催化降解有机染料的产品是纯净的。
多酸在光照的条件下可以有效的催化降解有机污染物。(参见Wu Q, Chen W-L, Liu D, Liang C, Li Y-G, Lin S-W, Wang E-B, Dalton Trans, 2011, 56–61; Chen C, Zhao W, Lei P, Zhao J, Serpone N, Chem. Eur. J, 2004,10, 1956–1965.)通过紫外光谱跟踪催化剂降解罗丹明B(RhB)溶液的效率来检测其催化活性的高低。将保护化合物1(所述新型杂多钽酸盐)溶解于 40 mL 物质的量浓度为 3.0 × 10−5 mol L−1 的RhB溶液中,并在黑暗条件下搅拌 30 min 以保证催化剂完全溶解。将试管群置于XPA-7 型多试管搅拌仪上搅拌,使试管群在距离 500 W 氙灯大概 4–5 cm 处围绕其周转,打开氙灯开始光催化降解反应并在各个时间节点测试溶液的紫外光谱图。紫外吸收光谱结果显示,在化合物 1 的作用下 RhB 溶液的吸光度 (λ = 553 nm) 随着光照时间的增加而急剧降低,而相同条件下不添加化合物的空白对照实验所对应的 RhB 溶液的吸光度仅略有降低。结果表明,本发明羧酸衍生物具有光催化降解罗丹明B性能。此外,化合物1还能有效降解偶氮荧光桃红和甲基蓝有机染料,说明其是潜在的光催化降解有机染料材料。因此本发明新型杂多钽酸盐可以作为光催化降解有机染料的应用。
和现有技术相比,本发明具有如下优点:1) 本发明提供的新型杂多钽酸盐结构明确,是首例杂多钽酸盐,在光催化降解有机染料领域具有潜在的应用前景;2) 本发明提供的新型杂多钽酸盐稳定性高,在室温下放置2个月仍然保存完好;3) 本发明提供的新型杂多钽酸盐的制备方法属于常见的水溶液制备方法,成本较低,制备工艺安全简单,易于操作,收率高达72%。
附图说明
图1-2为本发明新型杂多钽酸盐的结构图;
图3为本发明实施例1所得新型杂多钽酸盐的红外光谱图;
图4为本发明实施例1所得新型杂多钽酸盐的X-射线粉末衍射谱图;
图5为本发明新型杂多钽酸盐光催化降解罗丹明B图;
图6为本发明新型杂多钽酸盐加入量为10,20,40,60,80 mg时光照不同时间的罗丹明B的浓度变化图;
图7为本发明新型杂多钽酸盐光催化降解偶氮荧光桃红图;
图8为本发明新型杂多钽酸盐光催化降解甲基蓝图。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
实施例1
一种新型杂多钽酸盐的制备方法,包括以下步骤:
(1)按照本领域常规方法合成六钽酸钾盐K8[Ta6O19]·16H2O前驱体(具体参考文献Nelson W H, Tobias R S, Inorg. Chem., 1963, 2 , 985–992);
(2)在搅拌条件下,将1.50 g K8[Ta6O19]·16H2O (0.75 mmol) 溶解在双氧水溶液中(由13.5毫升30 wt%双氧水和165毫升水混合均匀所得),加入6.5毫升3 mol/L磷酸溶液,室温搅拌15分钟后用氢氧化钠溶液调pH至2.5,在90 ℃反应3小时,冷却至室温,加入0.56 g氯化钾 (7.5 mmol) 并在室温下搅拌30 min,过滤除去沉淀后放置8天,得晶体,晶体经后处理(洗涤、干燥)即得,收率为71%。
实施例2
一种新型杂多钽酸盐的制备方法,包括以下步骤:
(1)按照本领域常规方法合成六钽酸钾盐K8[Ta6O19]·16H2O前驱体(具体参考文献Nelson W H, Tobias R S, Inorg. Chem., 1963, 2 , 985–992)。
(2)在搅拌条件下,将1.50 g K8[Ta6O19]·16H2O (0.75 mmol) 溶解在双氧水溶液中(由13.5毫升30 wt%双氧水和165毫升水组成),加入6.2毫升3 mol/L磷酸溶液,室温搅拌15分钟后用氢氧化钠溶液调pH至2.3,在85 ℃反应4小时,冷却至室温,加入0.56 g氯化钾 (7.5 mmol) 并在室温下搅拌30 min,过滤除去沉淀后放置10天,得晶体,晶体经后处理(洗涤、干燥)即得,收率为53%。
实施例3
一种新型杂多钽酸盐的制备方法,包括以下步骤:
(1)按照本领域常规方法合成六钽酸钾盐K8[Ta6O19]·16H2O前驱体(具体参考文献Nelson W H, Tobias R S, Inorg. Chem., 1963, 2 , 985–992);
(2)在搅拌条件下,将1.50 g K8[Ta6O19]·16H2O (0.75 mmol) 溶解在双氧水溶液中(由13.5毫升30 wt%双氧水和165毫升水组成),加入6.5毫升3 mol/L磷酸溶液,室温搅拌15分钟后用氢氧化钠溶液调pH至2.1,在80 ℃反应3小时,冷却至室温,加入0.56 g氯化钾 (7.5 mmol) 并在室温下搅拌30 min,过滤除去沉淀后放置10天,得晶体,晶体经后处理(洗涤、干燥)即得,收率为31%。
对实施例1-3中的产物进行检测,可知产物的化学式均为K3[H3P4(TaO2)6(OH)4O20]·12H2O,本发明新型杂多钽酸盐的结构图如图1-2所示,图1中 a-d: 不同角度1a球棍示意图;图2中a: P2Ta3单元球棍示意图;b:1a多面体示意图;c: 1a热椭图。
利用红外光谱对实施例1中的产品进行检测,结果如图3所示,显示出材料中P-O、Ta-O、O-O及水分子的特征振动吸收带;图4为本实施例1中新型杂多钽酸盐的X-射线粉末衍射谱图,图中实测谱图(experiment)与模拟图谱(simulation)基本一致,说明用于催化性质研究的本发明衍生物是纯净的。
借助XPA-7 型多试管搅拌仪和紫外光谱仪,将实施例1中所得产物溶解在一定量的RhB溶液中,在500 W氙灯的照射下对实施例中所得产物的催化光降解罗丹明B、偶氮荧光桃红和甲基蓝性质进行了测试。结果如图5-8所示,图5a、图5b分别为本发明新型杂多钽酸盐用量分别为0,20 mg时光照不同时间的催化降解罗丹明B紫外吸收光谱图,从图5中可以看出,在不加入新型杂多钽酸盐时,不同时间的罗丹明B紫外光谱图基本没有变化,加入本发明新型杂多钽酸盐后5.5 h后罗丹明B基本上降解完全;图6为本发明新型杂多钽酸盐加入量分别为10,20,40,60,80 mg时光照不同时间的罗丹明B的浓度变化对数图;图7a为本发明新型杂多钽酸盐用量为40 mg时光照不同时间的催化降解偶氮荧光桃红紫外吸收光谱图,图7b 为光照不同时间的偶氮荧光桃红的浓度变化对数图;图8a为本发明新型杂多钽酸盐用量为40 mg时光照不同时间的催化降解甲基蓝紫外吸收光谱图,图8b为光照不同时间的甲基蓝的浓度变化对数图。
结果表明,本发明新型杂多钽酸盐具有光催化降解罗丹明B、偶氮荧光桃红和甲基蓝性能,说明其是潜在的催化降解有机染料材料。
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以作出许多其它的更改和修改。因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些变化和修改。
- 还没有人留言评论。精彩留言会获得点赞!
- 用于与催化剂结构一起使用的密封件的制作方法
- 用于烯烃二聚和/或低聚化的非负载型杂多酸金属盐催化剂的制作方法
- 一种双亲性含钴夹心型杂多酸及其应用
- 基于改性杂多酸催化剂的汽油烷基化脱硫方法及其产品的制作方法
- (S)-1-(2-羟基-1-苯乙基)硫脲修饰的Mn-Anderson型杂多酸催化剂、制备方法及其应用
- 稀土改性杂多酸催化剂的制备方法及生物柴油的制备方法
- 一种磺酸基修饰介孔材料负载杂多酸催化剂的制备方法及其在酯化反应中的应用
- (S)-1-(1-苯乙基)硫脲修饰的Cr-Anderson型杂多酸催化剂、制备方法及其应用
- (R)-1-(1-苯乙基)硫脲修饰的Cr-Anderson型杂多酸催化剂、制备方法及其应用
- 稀土改性杂多酸催化剂、其制备方法及生物柴油的制备方法