复合形式的钙调素样皮肤蛋白CLSP的应用的制作方法
本发明涉及将复合形式的钙调素样皮肤蛋白(calmodulin-like skin protein)(CLSP)、该蛋白的肽片段或其类似物在评价上皮(特别是表皮)的老化状态的标记中的应用。
背景技术:
上皮是细胞彼此接合连接且位于基膜上的组织。它们或者形成外部覆盖层(例如在皮肤的表面,或者表皮),或者在粘膜的表面形成内部覆盖层。它们也可以形成腺。
更具体地,这些上皮是这样一种结构,该结构的动态平衡是通过执行一套细微调节的作用于细胞增殖、迁移和分化以及各种细胞外基质成分合成的所有阶段的细胞内和细胞外信号产生的。这些信号可以特别地由角化细胞产生的因子的作用形成。
特别地,保持上皮的正常生理功能包括上皮细胞末端分化和/或蛋白聚糖合成。
如特别关注的表皮,为上皮,一般分为:由角质形成细胞形成的基底层,所述角质形成细胞特别含有皮肤干细胞并构成表皮的生发层;由位于所述基底层上的多层的多角细胞构成的“棘状”层;含有一至三层的所谓扁平形细胞(含有特殊的细胞质内含物、透明角质颗粒)的“颗粒”层;最后是一组上层细胞,称为角质层(或角化层),由处于分化末期的角质形成细胞构成,称作角化细胞(corneocytes)。
在有机体和环境之间起屏障作用的皮肤的最外部分的角质层,以及构成头发的头部的毛囊的新生部分的毛干都是角质形成细胞分化的结果。表皮分化是来自基底层分化和迁移的角质形成细胞的成熟过程从而导致角化细胞的形成的结果,角化细胞是完全角质化的死亡细胞。这种分化是理想调整现象的结果,使表皮的厚度保持不变,从而保证表皮的动态稳定。
许多皮肤失调或病态状况可能是因为表皮动态稳定的功能障碍导致的。
因此,对于老化的皮肤,这种功能障碍通常表现为出现皱纹(微小的和深的皱纹)、失去弹性、粗糙感和干燥。从组织学的角度看,观察到了真皮-表皮的平坦交界和真皮厚度和表皮厚度的下降。胶原和糖胺聚糖含量下降。皮肤屏障功能受损。长期受阳光照射会加重所有这些现象。
同样地,在妇女的绝经期这种功能障碍会更加恶化。
技术实现要素:
本发明特别地以角质层中的复合形式的钙调素样皮肤蛋白CLSP为特征,还发现该蛋白的表达在上皮的时序老化(chronological ageing)过程中被差异地调整。
CLSP是结合钙的蛋白,属于钙调蛋白族,其前体形式包括146个氨基酸。其分子量约为16kDa,与钙调蛋白的氨基酸序列同源性约为52%。
CLSP的结构包括4个潜在的“EF-hand”钙结合位点、潜在的N-糖基化位点、多个潜在的磷酰化位点和十四烷基化位点。
CLSP与钙的结合引起了其构象的改变,从而使其活化,特别是使其能够与各种目标蛋白相互作用。
已经证明在光诱导老化的过程中编码CLSP的mRNA增加(Urschitz,J.et al.,J.Invest.Dermatol.,2002,119:3-13),即,光诱导老化是由于皮肤反复地暴露于阳光下而引起的,这是与时序老化截然不同的过程,时序老化就是与时间流逝相关的生理性老化。
作为其一部分,文献US 2004/0142335观测到:通过转录组序列分析(transcriptome analysis),与年轻个体相比,老年个体的皮肤中编码CLSP蛋白的mRNA的表达增加。
因此,CLSP可能特别参与了角质形成细胞末端分化过程(B.Mehul et al.,J.Biol.Chem.,2000,Apr.28;275(17):12841-7)、(EP 1204744)。
最近,本发明的发明人意外地发现老年人表皮的角质层中特殊形式的CLSP表达减少。非常明显地,发明人表征的形式对应于与迄今为止研究过的CLSP形式(特别是与上述的不同)不同的蛋白成熟阶段。
如下面所表现的,发明人使用特殊的ELISA测定技术表征了其复合形式,特别是下文中实施例1所描述的复合形式。
因此,根据本发明的一个方面,本发明涉及至少一种复合形式的钙调素样皮肤蛋白(或CLSP)的在作为特别是在体外或离体情况下表征上皮(特别是表皮)时序老化的状态的工具中的应用,所述复合形式至少部分来自于具有以下氨基酸序列的多肽,所述氨基酸序列全部或者部分由SEQ ID NO 1表示的核酸序列或其类似物或片段编码。
“时序老化”在本发明中的含义是将持续暴露于太阳或U.V.下的一种皮肤现象(即光导致的皮肤老化)排除本发明的范围。
就本发明而言,术语“复合形式”包括CLSP蛋白或其衍生物与其它不同于CLSP的蛋白或其片段,或者其它CLSP蛋白或其片段的任何结合物。
就本发明而言,术语“CLSP蛋白的衍生物”表示其片段或下面定义的类似物。
特别地,复合形式可以来自于完整的CLSP蛋白或其片段与其自身或它的一个片段或与目标蛋白,或者甚至与例如角质层中蛋白水解的角化层的蛋白结构的结合。
因此,根据第一种变体,本发明涉及的复合形式可以是CLSP蛋白或这种蛋白的两种相同或不同的肽片段的结合的二聚体形式。
根据另一种变体,这种复合形式可以为由CLSP蛋白或其片段与二级目标蛋白的结合得到的产物。为了说明这些能够与CLSP和/或其片段结合的目标蛋白,可以特别提及的是:14.3.3β多肽、14.3.3σ、膜联蛋白(Annexins)II和V、钙网蛋白(calreticulins)、ERp72、核仁素、转谷氨酰胺酶3、MAGED1(黑素瘤抗原基因D1)、PPP4C(蛋白磷酸酶4)和USF2(上游转录因子2)。这些能够与CLSP和/或其片段结合的目标蛋白还可以为例如YWHAQ基序(14.3.3τ)的肽基序。
出乎意料的是,本发明的发明人发现,将角质层中的这些复合形式量化可以作为确定对应的表皮状态的有效而可靠的方法。如上所述,在时序老化的过程中观察到了这些复合形式表达的减少。
在这方面,根据本发明的复合形式的减少显示出表皮的时序老化的状态。
因此,这些复合形式的表征特别用于建立表皮状态的诊断。
关于这种诊断,可以方便地为个体提供最特别地适合于所述个体的特点的美容处理。很显然,使用者会特别期待和喜欢这种个性化美容处理。本发明满足了这种需求。
根据其另一方面,本发明涉及一种用于表征(特别是在体外或离体)表皮的时序状态的非侵害的(特别是美容用的方法)方法,该方法至少包括定性或定量表征所述表皮的角质层中至少一种本发明的CLSP复合形式的表达。
根据一种不同的实施方式,可以将通过这样的方法得到的数据或值与参考数据或值相比较进行评估,例如,该参考数据或值可以从与待表征的对象不同的状态已知的至少一种上皮,特别是表皮获得。
根据一个方面,本发明涉及一种用于表征上述定义的表皮的时序状态的方法,其中,通过本发明所述的复合形式的减少表示时序老化的状态。
根据另外的方面,本发明还涉及一种用于表征(特别是在体外或离体)美容性的或治疗性的处理的有效性的非侵害性(尤其是美容的)方法,所述处理用于防止和/或治疗与个体的时序老化相联系的皮肤老化的迹象,例如,皱纹或细纹,该方法至少包括定性或定量表征至少一种本发明的CLSP复合形式。
术语“皮肤老化的迹象”是指所有由时序老化引起的皮肤外观的改变,例如,皱纹和细纹、皮肤皱缩、缺乏弹性和/或皮肤紧张、真皮变薄和/或胶原纤维退化,从而导致看上去皮肤松驰和皱缩。
本发明的皮肤老化的迹象是指那些与皮肤时序老化有关的或由皮肤时序老化导致的皮肤老化的迹象。
尤其是,本发明的皮肤老化的迹象不同于那些与光导致的皮肤老化有关的或由光导致的皮肤老化导致皮肤老化的迹象。
本发明的“光导致的老化”特别是由于上皮暴露在U.V(尤其是暴露在U.V.A.)中导致的自由基生成、蛋白质糖基化或一些细胞表面受体的过分激活造成的对组织水平、弹性纤维的厚度的氧化损害。
因此,本发明是针对于预防和/或处理与皮肤时序老化有关的皮肤的表现,而不是针对于预防和/或处理与U.V暴露有关的皮肤的表现。
本发明特别是针对于由于细胞的损失和细胞衰老导致皮肤时序老化的表现。
此外,在上皮细胞水平的时序老化表现为上皮细胞的端粒减少、由于激素(例如,DHEA或生长因子的缺乏)缺乏或者由于细胞受体数量的减少导致的细胞刺激的减少;在组织水平,表现为弹性纤维的消失。
这些现象与U.V暴无关,因此,与光导致的皮肤老化无关。
随后于皮肤时序老化的细胞和组织的缺乏可能导致干燥病、上皮松驰、皱纹和/或细纹、皮肤松驰、脂漏性角化痣(seborrheic keratose)或樱桃状(cherry)血管瘤。
特别地,上述方法可以至少包括如下步骤:
i.提供所述个体的至少一份代表性的第一皮肤表面样品;
ii.特别地通过ELISA测定技术(并且特别是下面的实施例1所描述的方法)定量所述样品中至少一种本发明的复合形式;
iii.在所述个体的代表性的第二皮肤表面样品上重复步骤i和ii;以及
iv.将在结束步骤ii和iii后得到的结果对比,特别地,以从中得出关于处理的至少一种效果的信息,其中,所述第一和第二皮肤表面样品分别对应于不同的处理阶段。
所述参考值,或步骤ii中得到的数据,可以是从上皮获得的数据,特别是从来自这样的个体的表皮的上皮获得的数据,即在进行所述处理之前,或者距离处理开始日期很短的时间内接受处理的受试者。
根据一种优选的实施方式,所述第一样品代表护理前状态,所述第二样品代表护理过程中的状态或护理后的状态。
根据一种不同的实施方式,本发明涉及上述方法中的一种,其中,复合形式的增加表明对皮肤老化迹象的护理是有效的。
根据一种不同的实施方式,上述方法中的一种还可以包括在表征CLSP的复合形式的步骤结束后,进行至少一个附加步骤,目的在于对所述个体施用护理组合物,特别是美容护理组合物,根据由所述复合形式得到的信息确定和选择该组合物。所述附加步骤可以连续于所述特征步骤。
根据一种实施方式,这种组合物还可以选自许多组合物,后者中的每种均特别适于由本发明的方法得到的信息的类型。
因此,本发明的优点是提供一种简单和快速的方法,首先,用于表征上皮的生理状态,特别是皮肤表皮的上皮的生理状态;其次,用于相应地调整适用于皮肤的上皮或表皮的处理。
本发明的方法可以在体外、离体或体内进行。
由如下描述可以看出,本发明的方法特别的优势在于其实施的过程中不需要侵害性的步骤。
这是由于本发明的发明人将用于老化的这些新型生物标记定位于角质层,从而可以通过简单的局部取样定量或定性地表征所述标记的表达。
优选地,该方法可以在待研究的个体的角质层样品上通过简单地剥离进行。例如,取样的方法可以为包括对待研究的上皮(例如,表皮)施用一部分粘性胶带的剥离技术。揭开该粘性胶带,则取得部分上皮(例如,表皮部分)的样品。提取蛋白后,通过本发明所述的ELISA测试方法分析所述样品。
根据另一方面,本发明还涉及本发明的至少一种复合形式的应用,该应用作为筛选能够调节,特别是促进,这些复合形式的增加和/或稳定性和/或生物活性的生物学化合物和化学化合物的工具。
特别地,涉及一种筛选抗老化活性剂的方法,该方法至少包括如下步骤:
a)在适于显示所述复合形式表达的条件下,使至少一种含有至少一种本发明的复合形式的细胞类型与至少一种测试化学化合物或生物化合物接触;以及
b)确定至少一种所述复合形式的含量;
c)将由步骤b)确定的所述含量与不存在测试化学化合物或生物化合物时确定的所述复合形式的含量相比较。
根据一种不同的实施方式,本发明涉及一种上述方法,其中,本发明的复合形式的增加表示活性剂具有抗老化性质。
因此,优选地,在步骤c)之后,还可以进行选择活性剂的步骤,对于所述活性剂观测到本发明的复合形式的含量增加。
根据最后一个方面,本发明涉及有效量的本发明的复合形式的美容用途,该用途是作为用于防止和/或应对皮肤老化迹象的试剂。
根据另一个方面,本发明涉及有效量的本发明的复合形式的美容用途,其中,该用途是防止和/或处理表皮变薄和/或失去紧致(firmness)、弹性、密度和/或表皮紧张和/或起皱纹和细纹。
根据另一个方面,本发明涉及有效量的本发明的复合形式或者至少一种调节所述复合形式形成的试剂的用途,该用途是制备和/或改善复层(pluristratified)细胞模型,特别是重建的皮肤模型。
根据又一个方面,本发明涉及制备分离的重建皮肤的方法,该方法至少包括使本发明的至少一种复合形式与能够生成分离的重建皮肤的细胞(特别是角质形成细胞)接触。
CLSP的“复合形式”的定义
如上所述,本发明的复合形式至少一部分来自于具有以下氨基酸序列的多肽,所述氨基酸序列全部或部分由SEQ ID NO 1或其类似物或片段表示的核酸序列编码。
复合形式的CLSP可以尤其是由至少完整的CLSP蛋白或其片段与它本身或者其片段,或与至少一种靶蛋白、甚至与至少一种例如角质层中的蛋白水解角化层的蛋白结构的结合导致的多聚体。
本发明的CLSP片段是其长度和活性适合用于本发明的复合物形式的片段。
更尤其是,复合形式的CLSP可以二聚体,更尤其是完整的CLSP同型二聚体或其片段。
根据一个特别的实施方式,本发明的二聚体可以包括由完整的CLSP蛋白或其片段表示的第一单体和不同于完整的CLSP蛋白或其片段的结构所表示的第二单体。
适合本发明的不同于完整的CLSP蛋白或其片段的结构所表示的单体的实例可以提及的是上述的能够与完整的CLSP蛋白或其片段形成二聚体的蛋白和其片段。
根据另一个特别的实施方式,适合用于本发明的复合形式可以包括来自于CLSP和不同于完整的CLSP(尤其是不同于氨基酸序列由SEQ ID NO 1表示的核酸序列编码的)的肽。
尤其是,适合于本发明的来自于CLSP的肽可以是CLSP的片段,更尤其是由SEQ ID NO 1表示的核酸序列编码的蛋白片段,所述片段具有适当长度和活性,适合用于本发明的复合形式。
就本发明而言,表达“核酸序列的片段”是指部分地编码本发明的复合形式的核酸序列或其类似物,特别是由SEQ ID NO 1或其类似物表示的核酸序列。
表达“核酸序列的类似物”是指任选地由核酸编码简并得到的,并且编码具有与由所述核酸序列编码的多肽相同或类似的序列的复合形式的至少一部分的任何核酸序列。
所述核酸序列可以来自于任何可能的起源,即,可以是动物,特别是哺乳动物,更特别是人类,或者植物,或者来自于微生物(包括病毒、噬菌体、细菌和其它的事物)或来自于真菌,不用预先判断它们是否天然地存在于所述起源的有机体内。
根据一种不同的实施方式,本发明的复合形式可以是可溶性的。
就本发明而言,术语“可溶性的”是指本发明研究的复合的肽不需要离液剂(chaotropic agent)或离子型洗涤剂的蛋白变性物质能够在水或水性介质中溶解的能力,例如,与天然的CLSP相比,可以仅在这些试剂的存在下提取。
根据另一种实施方式,本发明的复合形式至少一部分来自于其中氨基酸序列完全或部分地由SEQ ID NO 2或其类似物或其片段编码的多肽。
就本发明而言,除非有相反的说明,术语“CLSP”一般是指具有序列(SEQ ID NO 2)的蛋白,该蛋白可以是在25和/或43位置的天冬酰胺残基上经过或不经过翻译后的糖基化型修饰,磷酸化型修饰和/或十四烷基化型修饰,能够改变其表观分子量或其等电点。
此外,已知的是,多肽的一级序列(即其氨基酸的序列)决定被蛋白酶特异性识别的位点,例如胰酶,其中,当这些位点的识别生效时,将通过蛋白水解作用引起多肽的分解。这种蛋白水解导致各种肽,或蛋白水解片段、复合形式的CLSP的生成。
本发明的发明人在角质层中检测到了这种肽的存在。
因此,本发明包括至少具有如下肽序列的CLSP蛋白水解片段的复合形式:SEQ ID NO 3、SEQ ID NO 4、SEQ ID NO 5、SEQ ID NO 6、SEQ ID N07、SEQ ID NO 8、SEQ ID NO 9、SEQ ID NO 10、SEQ ID NO 11、SEQ ID NO 12、SEQ ID NO 13、SEQ ID NO 14、SEQ ID NO 15、SEQ ID NO 16、SEQ ID NO 17、SEQ ID NO 18、SEQ ID NO 19、SEQ ID NO 20、SEQ ID NO 21、SEQ ID NO 22、SEQ ID NO 23、SEQ ID NO 24和SEQ ID NO 25。
因此,根据本发明的一种特殊的实施方式,本发明的复合形式至少来自于氨基酸序列全部或部分地由选自如下的氨基酸序列表示的多肽:SEQ ID NO 3、SEQ ID NO 4、SEQ ID NO 5、SEQ ID NO 6、SEQ ID N07、SEQ ID NO 8、SEQ ID NO 9、SEQ ID NO 10、SEQ ID NO 11、SEQ ID NO 12、SEQ ID NO 13、SEQ ID NO 14、SEQ ID NO 15、SEQ ID NO 16、SEQ ID NO 17、SEQ ID NO 18、SEQ ID NO 19、SEQ ID NO 20、SEQ ID NO 21、SEQ ID NO 22、SEQ ID NO 23、SEQ ID NO 24和SEQ ID NO 25,以及它们的混合物。
术语“多肽的类似物”是指表现出尤其是与所述多肽的特征序列中的一种序列具有同源性,并且具有相同性质的生物活性的任何多肽。
这种类似物可以是仿肽剂(peptidomimetic agent)。
同源性可以至少为85%,例如,至少为90%,例如,至少为95%。可以通过视觉比较或通过本领域常用的任何计算机工具确定同源性,例如,可以在www.ncbi.n1m.nil1.gov获得的BLAST程序,并使用系统设定的参数。
序列同源性可以来自于由本发明肽的序列的突变或改变引起的修饰,可以是来源于本发明的多肽的特征序列中的一个或多个氨基酸的缺失,或是一种或多种氨基酸的插入,或是一种或多种氨基酸的替换。
就本发明而言,术语“片段”是指含有至少4个,至少6个,特别是至少8个,更特别是至少12个CLSP蛋白的连续氨基酸,并具有基本相似的生物活性的任何肽部分。
一般地,该多肽类似物可以包括保守性取代的天然氨基酸序列。
这些修饰中的几种可以结合。
例如,本发明中可以考虑的突变可以提及但不限于:用具有相似水疗指数(hydropathic index)的氨基酸残基替换一个或多个氨基酸残基,而基本上不会影响本发明的复合形式的生物学特性。
所述水疗指数是根据其疏水性和电荷赋予氨基酸的指数(Kyte et al.(1982),J.Mol.Biol.,157:105)。
本发明包括的复合形式还可以来自于经过一种或多种翻译后修饰的上面定义的多肽。
术语“翻译后修饰”包括在肽或蛋白在细胞内合成后能够经历的所有修饰,例如,一次或多次磷酸化、一次或多次硫醇化、一次或多次乙酰化、一次或多次糖基化、一次或多次脂质化,例如,十四烷基化;结构重排,例如,形成二硫桥和/或肽序列内的分解。
此外,所述类似物与天然的多肽具有基本上相同的生物活性。
根据一种实施方式,适于实施本发明的复合形式还可以来自于天然的或合成的多肽,能够通过天然形式的CLSP的酶的或化学的分解适当地得到,或者通过化学的或生物的合成适当地得到,或通过从天然地表达这些复合形式的生物组织(例如,皮肤)中提取适当地得到;适于实施本发明的复合形式还包括它们的各种翻译后形式。
本领域技术人员可以通过基于重组DNA的方法获得本发明的复合形式,例如,在“分子克隆-实验室手册(Molecular Cloning-A Laboratory Manual)”(Sambrook et al.,1989,Vol.1-111,Coldspring Harbor Laboratory,Coldspring Harbor Press,NY,(Sambrook)第二版)的手册中描述的方法。
根据另一种实施方式,适于实施本发明的复合形式还可以和与上述多肽不同的其它多肽、亲水性或疏水性目标试剂、生物转化前体或发光放射性试剂或比色标记性试剂溶合。
在一种非限定性的方式中,可以提及的作为可以与本发明的复合形式结合的化合物的实例是:萤光蛋白,例如,绿色萤光蛋白(Green Fluorescent Protein);萤光化学化合物,例如,罗丹明、荧光素或磷光化合物;放射性元素,例如,3H、14C、35S、121I或125I;或者比色标记性试剂,例如,对半乳糖苷酶、对过氧化物、对氯霉素乙酰基转移酶、对萤光酶或者对碱性磷酸酶敏感的生色物质。
根据可以与本发明的复合形式结合的化合物的性质,所述结合可以通过化学方法进行,特别是通过化学反应性功能团(reactive chemical function)或者通过本领域技术人员公知的分子生物学方法进行。
用于检测多肽的方法可以提及的是:蛋白质印迹法、窄缝式点杂交法(slot blotting)、斑点印迹法、一元或多元型ELISA(酶联免疫吸附测定法)、蛋白质组法或糖组学法、在聚丙烯酰胺凝胶中用银染色剂、考马斯蓝或用SYPRO为多肽染色、荧光免疫检测法、紫外吸收法、常规的免疫组织化学法、电子或共焦显微镜法、FRET(荧光共振能量转换法)、TR-FRET(时间分辨FRET)法、FLIM(荧光寿命成像显微术)法、FSPIM(荧光光谱成像显微术(fluorescence spectral imaging microscopy))法、FRAP(光脱色荧光恢复技术)法、报道基因法、AFM(原子力显微术)法、表面等离子体共振法、微量热法、流式细胞测量法、生物传感器法、放射免疫测定(RIA)法、等电聚焦法和酶法测定,使用肽芯片、糖芯片、抗体芯片的方法,质量光谱测定法、和SELDI-TOF光谱测定法(Ciphergen)。
由下面的描述可以看出,本发明的复合形式的检测特别适于使用ELISA法。
本发明的复合形式的用途,用于判断表皮的状态和/或筛选抗老化活性剂。
如上所述,根据其另一个方面,本发明涉及用于,特别是离体或在体外的方式,表征非病理性的表皮的状态,或者表征美容或治疗处理的有效性的非侵害性方法,其目的在于定性或定量地表征至少一部分为CLSP或其衍生物或片段的复合形式的表达。
这些方法的优势特别在于其实施不需要受外科技术的约束以进行这样的表征。
下面描述的本发明的方法可以在例如来自个体的上皮(特别是表皮)的分离样品上进行。
本发明的方法还可以在上皮样品上进行,特别是来自上皮细胞模型(特别是表皮细胞模型)的表皮的上皮,或者来自重建的分离的皮肤,以确定其状态。
因而可以通过简单的剥离得到表皮的提取物,直接通过下面的实施例1所描述的ELISA法进行分析。
所述剥离技术可以为将粘性表面施加在表皮的表面,例如,来自3M公司的、D'squam(从CuDERM商购的胶粘剂)或氰基丙烯酸酯胶水。通过这种剥离,可以对被粘附的角化细胞及其细胞内的物质进行取样,然后进行提取,从而能够得到蛋白成分。
取得适合于该方法的样品的方法还可以更加直接地通过“清洗”皮肤表面进行,例如,通过将专利FR 2667778中描述的叶式水轮机型或螺旋细胞型配件与循环流体结合,或者简单地通过在皮肤表面滴加/去除缓冲剂。
为了说明能够用于实施本发明的其它取样方式,可以提及的是:通过双刀方式或刮取活组织的方式刮取角质层的表层部分。这种方法可以收集鳞屑,然后直接通过各种方法对其进行分析,从而确定其无机物、氨基酸或脂质含量。
取样之后,通过ELISA法对该样品进行表征。
这种方法特别地基于使用适于检测本发明的复合形式的抗体。可以通过本领域技术人员公知的任何方法获得能够用作评价表皮的状态的工具的抗体,如“抗体:实验室手册(Antibodies:A Labohtory Manual)”(美国冷泉港实验室出版社(Cold Spring Harbor Laboratory Press),纽约冷泉港)中描述的方法。
如下面的实施例1的描述,检测复合形式的CLSP的方法特别地需要使用两种单克隆抗体,由covalAb公司开发,即捕获抗体(克隆DB15C9)和用“sulpho-tag”标记的选择抗体(CLSP克隆DB7g12)。
判断表皮的状态的方法
根据一种实施方式,用于表征上皮(例如,表皮)的状态的方法至少包括如下步骤:
a)测定所述上皮的表皮样品中本发明的至少一种复合形式的含量;以及
b)将步骤a)测得的含量与参考值比较。
优选地,本发明的方法是非侵害性的。
参考值可以例如在取自上皮的表皮样品上测定的复合形式的含量,特别是来自正常皮肤的,即从生理学角度上看是理想的,例如,年轻人的皮肤。
测定参考值可以与测定所述复合形式的所述含量同时进行,也可以随后进行。
将测定的含量与参考值比较可以计算与该值的偏差。
对该偏差(负或正)的大小和/或性质的分析可以作为关于表皮状态的信息。
表皮状态的表征可以表明皮肤障碍的可能性,可以通过使用能够调节本发明的复合形式的表达的化合物而克服该障碍。
因此,本发明的复合形式的减少表明时序老化的状态。
根据一种实施方式,本发明的方法可以在体内、在体外或离体判断上皮(特别是表皮)的生理学状态,特别是评价时序老化的状态,例如,它有关的个体中该复合形式的缺乏和/或改变。
筛选生物化合物或化学化合物
本发明涉及本发明的复合形式在作为筛选用于调节这些复合形式的增加和/或稳定性和/或生物活性的生物化合物或化学化合物的工具中的应用,。
本发明还涉及筛选能够调节本发明的复合形式的量的生物化合物或化学化合物,或者甚至是抗老化活性剂或物理化学要素的方法,该方法至少包括如下步骤:
a)在适于所述复合形式释放的条件下,使含有至少一种本发明的复合形式的细胞类型与至少一种化学化合物或生物化合物接触;
b)测定所述复合形式的含量;以及
c)将由步骤b)确定的所述含量与不存在测试化学化合物或生物化合物时确定的所述复合形式的含量相比较。
步骤c)中进行的比较可以得到关于所述测试化合物调节本发明的复合形式的表达的性质的信息。
如上所述,该方法还可以包括目的在于保留下述活性剂的步骤,对于活性剂观察复合形式的含量增加。
特别地,该方法用于表征防止和/或处理个体的皮肤老化迹象的处理的有效性,该方法至少包括如下步骤:
i.提供所述个体的代表性的至少一份第一皮肤表面样品;
ii.特别地通过ELISA测定技术定量化所述样品中至少一种本发明的复合形式;
iii.在所述个体的代表性的第二皮肤表面样品上重复步骤i和ii;以及
iv.将在步骤ii和iii结束后得到的结果对比,特别地,以从中得出关于处理的至少一种效果的信息,其中,所述第一和第二皮肤表面样品分别对应于不同的处理阶段。
如果在使用所述测试的生物化合物或化学化合物,或者使用测试物理化学因素之前进行参考值的测定,本发明的方法还可以在适当时估计所述化合物的潜在有效性。
该量可以不受所述化合物的存在的影响,或者另一方面,可以被抑制或激活。
如果观测到增加,被测试的化合物则能够用作,例如,抗老化活性剂。
根据一种不同的实施方式,上述方法还可以包括至少一步对个体施用美容护理组合物的步骤,根据步骤iv得到的信息确定或选择该组合物。
通过ELISA法测定本发明的复合形式的含量,特别是下面的实施例1所特别描述的方法。
根据本发明的另一个方面,上述复合形式的CLSP可以用在美容组合物或治疗组合物中。
可以理解的是,本发明的所有美容组合物或治疗组合物均使用生理学上可接受的介质。
就本发明而言,术语“生理学上可接受的介质”是指适用于用在上皮或角蛋白材料上的组合物的介质,例如,在皮肤上,在头皮上,在嘴唇上,在粘膜上和角蛋白纤维上,例如,头发、指甲和体毛,或者适当的时候用于口服或肠胃外给予。
就本发明而言,术语“美容的”是指其用途主要是提供美感和/或舒适感。
就本发明而言,术语“治疗的”是指可以用于预防性的和/或治疗性的处理的组合物,或者用于评价上皮(特别是表皮)的状态的方法。
就本发明而言,术语“预防性的”或“防止”是指降低出现例如病理状况的现象的危险。
根据另一种实施方式,本发明的美容组合物或治疗组合物还可以含有至少一种美容和/或治疗的活性剂。
作为可以用于本发明的活性剂的例子,可以提及的是:化妆油,例如,硅油、甘油三酸酯型植物油、烃类基质油,例如,parleam oil和脂肪酸的酯和脂肪醇的酯。
还可以使用能够改善皮肤状态的其它活性剂,例如,保湿活性剂或者能够增强天然脂质屏障的活性剂,例如,神经酰胺、胆固醇硫酸酯和/或脂肪酸以及它们的混合物。
还可以使用对皮肤具有活性的酶,例如,蛋白酶、脂肪酶、葡萄糖苷酶、酰胺酶、脑苷脂和/或黑素酶(melanases),以及它们的混合物。
一般地,本发明的任何组合物均可以用于皮肤(身体的任何皮肤区域)或者用于粘膜(口腔的、面颊的、齿龈的、生物器的、结膜的,等等)。
在一种已知的方式中,美容组合物还可以含有化妆品领域常规的辅料,例如,亲水性的或亲油性的胶凝剂、亲水性的或亲油性的添加剂、防腐剂、抗氧化剂、溶剂、香料、填料、掩蔽剂(screening agent)、吸味剂和染料。
本发明的组合物的各种成分的含量可以是本领域中常规的值。
本发明的组合物中,本发明的复合形式的含量,也可以称作“有效量”自然取决于该化合物的性质和需要达到的效果,因而可以在很大范围内变化。
为了提供其数量级,组合物可以含有占所述组合物总重量的0.00001%-50重量%的本发明的复合形式,特别地占所述组合物总重量的0.001%-10%,更特别地占所述组合物总重量的0.1%-1%。
本发明的组合物还可以特别地用于减轻和/或处理上皮(特别是表皮)劣化的状况的情况。
这种状态可以是由于时序原因(即,随着时间的流逝,例如,皮肤老化)引起的和/或表现为皮肤障碍,例如与光老化有关的。
因此,本发明的组合物,特别是美容组合物,可以特别地用于防止和/或处理表皮变薄和/或失去紧致、弹性、密度和/或表皮紧张和/或形成皱纹和细纹。
根据另一种实施方式,本发明的组合物,特别是美容组合物,可以,特别地用于防止和/或处理皮肤干燥现象,特别是防止和/或处理表皮脱水。
根据另一种实施方式,本发明的组合物,特别是美容组合物,可以用于防止和/或处理表皮老化的迹象。
根据另一方面,本发明还涉及一种对皮肤老化迹象美容处理的方法,该方法至少包括在皮肤的至少一部分、粘膜和/或角蛋白纤维上施用至少一种本发明的美容组合物的步骤。
根据另一方面,本发明还涉及本发明的CLSP蛋白、该蛋白的肽片段或其类似物,或调节这种多肽的活性、表达和/或稳定性的试剂的复合形式的用途,特别是美容和/或治疗用途,特别是用于防止和/或处理皮肤老化迹象,特别是用于预防和/或处理皮肤老化。
本发明还涉及有效量的本发明的复合形式在制备和/或改善复层(pluristratified)细胞模型,特别是表皮型或粘膜型,特别是重建的皮肤模型中的用途。
就本发明而言,术语“重建的皮肤模型”是指存在各种细胞类型的模型,例如,特别是皮肤的天然组成,例如,角化细胞、成纤维细胞、朗格汉斯细胞(Langerhan cells)和黑色素细胞。
所述成纤维细胞可以是被辐射的或未被辐射的。
这样的模型及其制备为本领域技术人员所公知。
因此,本发明还涉及一种制备分离的重建皮肤的方法,该方法至少包括将至本发明的少一种复合形式与能够生成分离的重建皮肤的细胞接触,特别是角质形成细胞。
下面实施例和附图用于非限定性描述本发明。
附图说明
图1表示前臂和面部皮肤中存在的本发明的复合形式的量与年龄之间的关系;
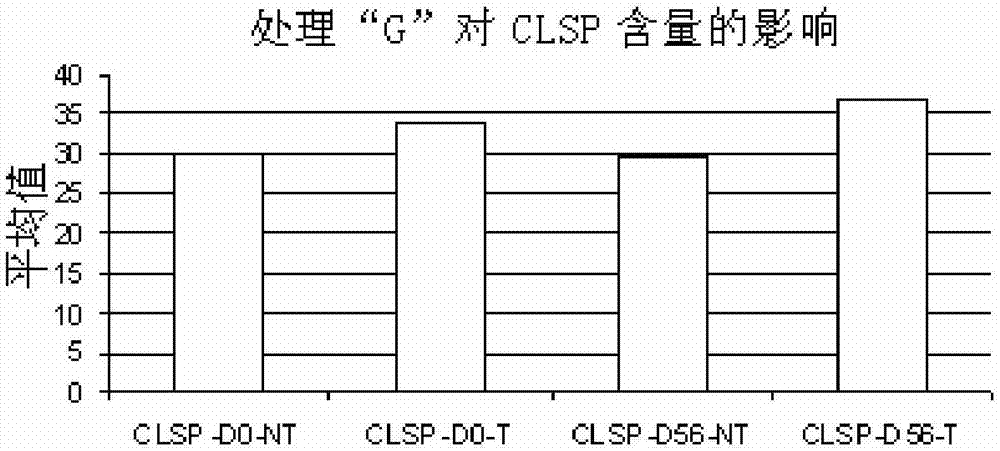
图2表示与使用含有10%bifidiobiotic(CLR复合物)和0.002%植物鞘胺醇-SLC(处理“G”)的美容组合物对前臂和面部皮肤中本发明的复合形式的含量的影响。
具体实施方式
实施例1:
高灵敏ELISA测试分析本发明的复合形式的CLSP的进展:
在本测试中使用通过MesoScale Discovery(MSD)技术定做的CLSP板。针对与GST溶合的重组的“全长”CLSP蛋白的单克隆抗体由CovalAb(Lyon,Prance)(Méhul et al.,2006)公司开发。在“小点”型(MesoScale)标准96孔板上以200μg/ml的浓度使捕获抗体(Clone DBl5C9)沉淀。
使用所述重组的CLSP蛋白确定参照曲线(5-0.078μg/ml)。
在室温下用封闭液(MesoScale)将每个板封闭1小时。将每份25μl样品和25μl标准样品一式三份放置,在室温下搅拌孵育1小时。然后用三羟甲基氨基甲烷(tris)缓冲液(MesoScale)将该板清洗4次。然后在室温下使该板与25μl浓度为1μg/ml的被“sulpho-tag”(CLSP clone DB7g12)标记的检测抗体(Mesoscale)在搅拌下孵育1小时。用三羟甲基氨基甲烷缓冲液(MesoScale)将该板清洗4次,之后加入150μl的1X读出缓冲液(read buffer)T(MesoScale)。在“Sector lmager 6000”仪器上读取该板。按照每μg总蛋白中ng CLSP将该数据标准化。
实施例2:
通过剥离取得的各种样品中的CLSP复合形式的含量的表征
该表征通过实施例1中描述的ELISA分析进行。
进行两项临床研究:用取自前臂和面部的样品进行知识研究(2组20位具有白种人皮肤的女性个体:30-35岁以及60-65岁),在56天(即两个月)后只对来自前臂的样品进行产品研究(1组24位具有白种人皮肤的女性个体,年龄为40-45岁)。
产品是含有10%bifidiobiotic(CLR复合物)和0.002%植物鞘胺醇-SLC(处理“G”)的血清。
该CLR复合物关于一种以INCI名Bifidat ferment Lysate,EINECS名Bifidobacterium longurn,EINECS编号为306-168-4和CAS编号为96507-89-0登记的溶菌产物。
这样的溶菌产物特别地由K.Richter GmbH公司以的商品名出售。
名称植物鞘胺醇-SLC为由Evonik Goldschmidt公司出售的植物鞘胺醇水杨酸酯衍生物。
对于所有研究,D-鳞屑样品取自面部(脸颊)和前臂(面部后部(posterior face))。来自前臂的D-鳞屑角质(corneodiscs)样品用于评价产品的效果。
a)从D-鳞屑角质中提取蛋白
将角质置于2ml的艾本德管(Eppendorf tube)中,粘性表面向内,向每个管中加入550μl“自制(native)+”的提取缓冲液(TBS,1%三硝基甲苯(triton)X-100,1M NaCI),和1个不锈钢包。然后将该管置于MM400振动式研磨机(Retsch)的支架上。通过以30Hz振动研磨2分钟的一个周期进行提取。然后将该介质回收,用0.45μm的Millipore Ultrafree柱滤过,然后在4℃下以5000g离心分离5分钟。将上清液贮存在-20℃下以待分析。
b)统计分析
通过将年龄、区域和年龄*区域相互作用系数作为固定效果、以及受试者因素作为随机效果的偏差分析的混合模型进行年龄(年轻的对年老的)和区域(手臂对面部)效果的生物标记的分析。通过对照方法实现对于一种年龄类型的区域效果和对于一种区域的年龄效果。
通过将时间因素作为固定效果,受试者因素作为随机效果,在成对的活性剂-安慰剂差别的方差分析的混合模型进行处理效果的生物标记的分析。
通过对照测定D0和D56的处理效果。
在需要时,事先将该变量进行log-变型从而使其分布更加高斯化(Gaussian)。
使用第14版的SPSS软件进行描述性分析(平均的曲线图(graph of the means)和柱状图(box plot)),使用SAS Enterprise Guide软件进行干涉部分。
将第一品种α-风险固定为两边接近的5%。
图1和2表示了这两项研究的结果。
如图1所示,数据显示CLSP的复合形式随着年龄增加而减少。
开发的高灵敏ELISA试剂盒确实能够证明复合形式的CLSP的表达随着年龄增加而减少。
图2部分表示了测试产品对复合形式的量的影响。可以清楚地观察到复合形式的量显著增加,从而表明这种产品的活性效果。因此,后者提供了真正的抗老化效果。
- 还没有人留言评论。精彩留言会获得点赞!