一种采用聚集诱导发光型荧光传感分子连续检测Cu2+和焦磷酸根的方法与流程
本发明属于离子检测技术领域,具体涉及一种采用聚集诱导发光型荧光传感分子连续检测Cu2+和焦磷酸根(PPi)的方法。
背景技术:
人体内铜元素绝大多数都以Cu2+表现,同时铜元素又是人体内最丰富的微量元素之一。Cu2+在生理代谢过程中扮演着至关重要的角色,例如可以充当活性氧的解毒物种、神经传递素生物合成和降解。然而,细胞内Cu2+的紊乱将会严重危害人类的健康,特别是会诱发严重的神经退行性疾病,如Alzheimer、Menkes以及Wilson疾病。同样,PPi在生物能量学和代谢过程中起到关键作用,在血清中高浓度的PPi与心血管疾病和急性肾功能衰竭相关,在滑膜液中PPi浓度过高与某些疾病如焦磷酸钙脱水晶体的形成和软骨钙质沉着病有关,鉴别和测定PPi越来越受到人们的重视。因此,检测人体细胞内的Cu2+和PPi有着重要的意义。
荧光检测具有高灵敏度、高选择性、操作简易、快速响应等优势。细胞荧光成像作为生物和药物科学领域里一种高效的探测手段备受关注。
技术实现要素:
本发明所要解决的技术问题在于提供一种采用聚集诱导发光型荧光传感分子高选择性、高灵敏度连续检测Cu2+和PPi的方法。
解决上述技术问题所采用的技术方案由下述步骤组成:
1、将聚集诱导发光型荧光传感分子加入去离子水与二甲基亚砜的体积比为8:2混合溶剂中,配制成10-5mol/L的聚集诱导发光型荧光传感分子溶液。
2、向10-5mol/L的聚集诱导发光型荧光传感分子溶液中加入Cu2+,用荧光光谱仪测量在发射波长为500nm处不同浓度Cu2+对应体系的荧光强度,绘制荧光强度随Cu2+浓度变化的线性曲线。
3、向上述加入Cu2+之后的荧光传感分子中加入聚集诱导发光型荧光传感分子摩尔量的6倍的PPi,用荧光光谱仪测量在发射波长为500nm处不同浓度PPi对应体系的荧光强度,绘制荧光强度随PPi浓度变化的线性曲线。
4、按照步骤2的方法用荧光光谱仪测量待测Cu2+样品的荧光强度,根据待测Cu2+样品的荧光强度,结合步骤2中标准曲线的线性方程即可高选择性识别Cu2+并确定待测样品中Cu2+浓度。
5、根据步骤4确定的待测样品中Cu2+浓度,再向其中补加Cu2+标准样品,使混合体系中Cu2+的摩尔量为聚集诱导发光型荧光传感分子摩尔量的1倍,然后加入待测焦磷酸根样品,用荧光光谱仪测量待测焦磷酸根样品的荧光强度,根据待测样品的荧光强度,结合步骤3中标准曲线的线性方程即可高选择性识别焦磷酸根并确定待测样品中焦磷酸根的浓度。
上述聚集诱导发光型荧光传感分子的结构式如下所示:
其合成路线和具体合成方法如下:
1、在避光和氮气保护下,将4-氨基二苯甲酮(1.0g,5.08mmol)溶于60mL甲醇中,并且加入2-吡啶甲醛(0.48mL,5.08mmol)和乙酸(0.87mL,15.24mmol)常温搅拌12小时后,加入氰基硼氢化钠(319mg,5.08mmol),继续搅拌4小时,然后用50mL饱和氯化铵溶液中和反应液,并用二氯甲烷萃取三次,待萃取完用蒸馏水洗涤有机相,再用无水硫酸钠干燥有机相并旋干溶剂,粗产物用柱层析纯化(洗脱剂为石油醚与乙酸乙酯体积比3:1的混合液),得到白色固体化合物3(1.34g,产率:92%)。
2、在100mL二颈瓶中加入化合物3(500mg,1.74mmol)和2-氯亚甲基吡啶盐酸盐(427mg,2.6mmol)、氢化钠(278.4mg,60%,6.96mmol)、50mL四氢呋喃,在氮气保护下回流反应12小时,待反应结束,用乙醇淬灭反应,并用二氯甲烷萃取有机相,再用无水硫酸钠干燥有机相并旋干溶剂,粗产物用柱层析纯化(洗脱剂为石油醚与乙酸乙酯体积比3:1的混合液),得到白色固体化合物2(501mg,产率:76%)。
3、在氮气保护下,将锌粉(260mg,4.0mmol)加入二颈瓶中,并且加入20mL四氢呋喃,在冰浴条件下加入四氯化钛(0.22mL,2.0mmol),搅拌半小时后缓慢升温回流2小时,然后将化合物2(379mg,1.0mmol)和4-甲基二苯甲酮(196mg,1.0mmol)、10mL四氢呋喃加入到反应液中,回流反应12小时。待反应结束,用质量分数为10%的碳酸钾水溶液淬灭反应,并用乙酸乙酯萃取有机相,然后无水硫酸钠干燥有机相,待在旋转蒸发仪上浓缩有机相之后,粗产物经柱层析纯化(洗脱剂为石油醚与乙酸乙酯体积比6:1的混合液),得到浅黄色化合物1(242mg,产率:45%),即聚集诱导发光型荧光传感分子(以下简称TPE-DPA)。
本发明的荧光传感器分子TPE-DPA结构简单,合成方便,具有聚集诱导发光的特性,即在溶液中不发光、在聚集态下荧光增强的特性,其不但能够单一选择性、高灵敏度的识别Cu2+,还能够在识别Cu2+的基础上连续高灵敏性的识别PPi,而其它阳离子和阴离子对这一检测过程没有干扰。
附图说明
图1是不同浓度的Cu2+存在下TPE-DPA的荧光光谱图。
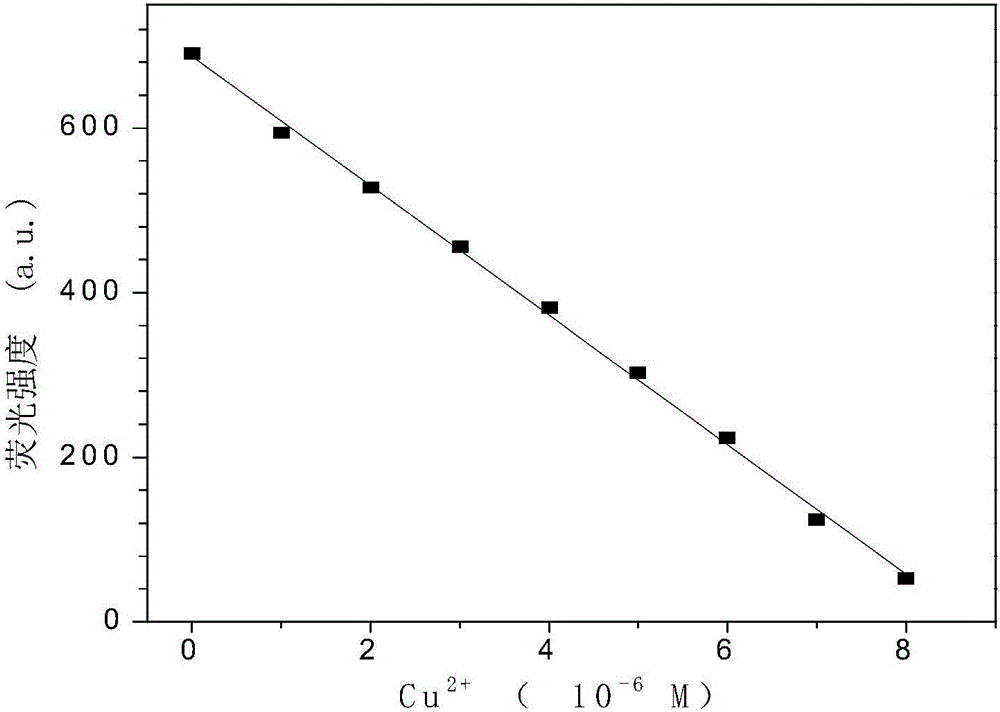
图2是TPE-DPA在500nm处的荧光强度随Cu2+浓度变化的线性关系图。
图3是不同浓度的PPi存在下TPE-DPA-Cu2+的荧光光谱图。
图4是TPE-DPA-Cu2+在500nm处的荧光强度随PPi浓度变化的线性关系图。
图5是TPE-DPA及其加入不同阳离子时的荧光光谱(激发波长360nm,发射波长500nm)。
图6是TPE-DPA对Cu2+识别的抗干扰性能图。
图7是TPE-DPA-Cu2+及加入不同阴离子时的荧光光谱图(激发波长360nm,发射波长500nm)。
图8是TPE-DPA-Cu2+对PPi识别的抗干扰性能图。
具体实施方式
下面结合附图和实施例对本发明进一步详细说明,但本发明的保护范围不仅限于这些实施例。
实施例1
1、将TPE-DPA加入去离子水与二甲基亚砜体积比为8:2的混合液中,配制成10-5mol/L的TPE-DPA溶液。
2、将3mL 10-5mol/L的TPE-DPA溶液加入4mL比色皿中,向其中加入CuCl2·2H2O,分别使所得混合液中Cu2+的浓度为0、1、2、3、4、5、6、7、8、9和10μmol/L,采用荧光光谱仪测量不同浓度Cu2+对应体系的荧光光谱(见图1),并绘制在500nm处不同浓度Cu2+对应体系的荧光强度随Cu2+浓度变化的线性曲线(见图2)。由图1可见,TPE-DPA的荧光强度Cu2+受到浓度的影响,伴随着Cu2+浓度的增加而减弱。说明TPE-DPA在水体系中仍然能单一选择性荧光识别Cu2+。由图2可见,该体系的荧光强度随着体系中Cu2+浓度的增大变化很明显,说明TPE-DPA对Cu2+的检测灵敏度很高。其中Cu2+在浓度为0~8μmol/L时,荧光强度与Cu2+浓度呈线性关系,线性方程为:
y=-78.723x1+687.473
式中y为荧光强度,x1为Cu2+浓度,相关系数R2为0.998。可见荧光强度与Cu2+浓度的线性关系很好。利用最低检出限的公式3σ/k计算检出限,TPE-DPA对Cu2+的检测灵敏度很高,检出限达到了4.29nM。
3、将3mL 10-5mol/L的TPE-DPA溶液加入4mL比色皿中,并加入与TPE-DPA等摩尔量的CuCl2·2H2O,然后其中加入K4P2O7·3H2O,分别使所得混合液中PPi的浓度为0、5、10、15、20、25、30、35、40、45、50、55和60μmol/L,采用荧光光谱仪测量不同浓度PPi对应体系的荧光光谱(见图3),并绘制在500nm处不同浓度PPi对应体系的荧光强度随PPi浓度变化的标准曲线(见图4)。由图3可见,TPE-DPA-Cu2+的荧光强度受到PPi浓度的影响,伴随着PPi浓度的增加而增加,说明TPE-DPA-Cu2+在水体系中仍然能单一选择性荧光识别PPi。由图4可见,该体系的荧光强度随着体系中PPi浓度的增大变化很明显,说明TPE-DPA-Cu2+溶液对PPi的检测灵敏度很高。其中PPi的浓度在5~30μmol/L时,荧光强度与PPi浓度呈线性关系,线性方程为:
y=5.91543x2-1.40333
式中y为荧光强度,x2为PPi浓度,相关系数R2为0.966。可见荧光强度与PPi浓度的线性关系很好。利用最低检测限的公式计算检出限,TPE-DPA-Cu2+溶液对PPi的检测灵敏度很高,检出限达到了56nM。
4、按照步骤2的方法用荧光光谱仪测量待测Cu2+样品的荧光强度,根据待测Cu2+样品的荧光强度,结合步骤2中标准曲线的线性方程即可高选择性识别Cu2+并确定待测样品中Cu2+浓度。
5、根据步骤4确定的待测样品中Cu2+浓度,再向其中补加Cu2+标准样品,使混合体系中Cu2+的摩尔量为聚集诱导发光型荧光传感分子摩尔量的1倍,然后加入待测焦磷酸根样品,用荧光光谱仪测量待测焦磷酸根样品的荧光强度,根据待测样品的荧光强度,结合步骤3中标准曲线的线性方程即可高选择性识别焦磷酸根并确定待测样品中焦磷酸根的浓度。
为了证明本发明的有益效果,发明人进行了大量的实验室研究试验,各种试验情况如下:
1、Cu2+的检测
(1)TPE-DPA对Cu2+检测的选择性测试
分别移取3mL 10-5mol/L的TPE-DPA溶液于4mL比色皿中,采用荧光光谱仪检测,TPE-DPA溶液显绿色荧光,在发射波长500nm处的荧光信号很强。然后向比色皿中分别加入与TPE-DPA等摩尔量的Ag+、Al3+、Ba2+、Ca2+、Cd2+、Co2+、Cr3+、Fe3+、Hg2+、K+、Mg2+、Mn2+、Na+、Ni2+、Pb2+、Sn+、Zn2+和Cu2+的水溶液。采用荧光光谱仪检测,结果发现,只有Cu2+的加入使TPE-DPA溶液荧光淬灭,在500nm处的荧光信号消失。(λex=360nm),而加入其它阳离子,TPE-DPA溶液的荧光颜色及荧光光谱没有明显变化(见图5),说明TPE-DPA对Cu2+表现出很强的专一性,可高选择性、高灵敏度的荧光识别Cu2+。
(2)TPE-DPA对Cu2+检测的抗干扰性能测试
为了测定TPE-DPA溶液对Cu2+的检测效果,发明人将3mL 10-5mol/L的TPE-DPA溶液加入4mL比色皿中,并分别加入与TPE-DPA等摩尔量的阳离子Ag+、Al3+、Ba2+、Ca2+、Cd2+、Co2+、Cr3+、Fe3+、Hg2+、K+、Mg2+、Mn2+、Na+、Ni2+、Pb2+、Sn+、Zn2+和Cu2+的水溶液。常温静置10分钟后,除了之前加入铜离子之外,向其他含有不同阳离子的溶液中各加入与TPE-DPA等摩尔量的Cu2+,混合均匀后再常温静置10分钟,测其荧光发射光谱。结果发现,分别加入Ag+、Al3+、Ba2+、Ca2+、Cd2+、Co2+、Cr3+、Fe3+、Hg2+、K+、Mg2+、Mn2+、Na+、Ni2+、Pb2+、Sn+和Zn2+的水溶液,TPE-DPA溶液在500nm处荧光强度无明显变化,而再加入Cu2+后荧光均被淬灭(见图6)。由此可见,TPE-DPA对Cu2+的检测不受其它阳离子的影响。
2、PPi的检测
(1)TPE-DPA-Cu2+对PPi检测的选择性测试
分别移取3mL 10-5mol/L的TPE-DPA溶液于4mL比色皿中,并加入与TPE-DPA等摩尔量的Cu2+,采用荧光光谱仪检测,所得TPE-DPA-Cu2+溶液无荧光,在发射波长500nm处的荧光信号很弱。然后向比色皿中分别加入阴离子Ac-、Br-、Cl-、ClO4-、CO32-、F-、H2PO4-、HCO3-、HPO42-、I-、IO3-、NO3-、PO43-、S2O32-、SO32-、SO42-、S2-、AMP、ADP、ATP和PPi,其中阴离子的加入量为TPE-DPA摩尔量的6倍,采用荧光光谱仪检测,只有PPi的加入使TPE-DPA-Cu2+溶液在500nm处出现最大荧光发射峰(λex=360nm),而加入其它阴离子,TPE-DPA-Cu2+溶液的荧光颜色及荧光光谱没有明显变化(见图7),说明TPE-DPA-Cu2+溶液对PPi表现出很强的专一选择性,高选择性、高灵敏度。
(2)TPE-DPA-Cu2+对PPi检测的抗干扰性能测试
为了测定TPE-DPA-Cu2+对PPi的检测效果,发明人分别移取3mL 10-5mol/L的TPE-DPA于4mL比色皿中,并加入与TPE-DPA等摩尔量的Cu2+,然后向所得TPE-DPA-Cu2+溶液中分别加入TPE-DPA摩尔量6倍的Ac-、Br-、Cl-、ClO4-、CO32-、F-、H2PO4-、HCO3-、HPO42-、I-、IO3-、NO3-、PO43-、S2O32-、SO32-、SO42-、S2-、AMP、ADP、ATP和PPi,常温静置2分钟,测其荧光发射光谱,并再次向其中各加入TPE-DPA摩尔量6倍的PPi,混合均匀后再常温静置2分钟,测其荧光发射光谱。结果发现,加入Ac-、Br-、Cl-、ClO4-、CO32-、F-、H2PO4-、HCO3-、HPO42-、I-、IO3-、NO3-、PO43-、S2O32-、SO32-、SO42-、S2-、AMP、ADP、ATP的水溶液后,TPE-DPA-Cu2+在500nm处的荧光强度无明显变化,而加入PPi后荧光均被点亮(见图8)。由此可见,TPE-DPA-Cu2+对PPi的检测不受其它阴离子的影响。
- 还没有人留言评论。精彩留言会获得点赞!