一种ASE‑HPLC法测定威灵仙中齐墩果酸含量的方法与流程
本发明属于化学检测领域,尤其是一种ase-hplc法测定威灵仙中齐墩果酸含量的方法。
背景技术:
2015年版药典方法:取本品粉末(过四号筛)约4g,精密称定,置索氏提取器中,加乙酸乙酯适量,加热回流3小时,弃去乙酸乙酯液,药渣挥干溶剂,连同滤纸筒转移至锥形瓶中,精密加入稀乙醇50ml,称定重量,加热回流1小时,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,精密量取续滤液25ml,置水浴上蒸干,残渣加2mol/l盐酸溶液30ml使溶解,加热回流2小时。立即冷却,移入分液漏斗中,用水10ml分次洗涤容器,洗液并入分液漏斗中。加乙酸乙酯振摇提取3次,每次15ml,合并乙酸乙酯液,70℃以下浓缩至近干,加甲醇溶解,转移至10ml量瓶中,加甲醇至刻度,摇匀,即得。
该方法提取时间长,且对技术人员的专业水平要求较高。
技术实现要素:
针对上述不足,本发明旨在提供一种ase-hplc法测定威灵仙中齐墩果酸含量的方法,该方法提取时间短、重复性好,且检测精度高。
为了实现上述技术效果,本发明提供的技术方案是这样的:一种ase-hplc法测定威灵仙中的齐墩果酸含量的方法,依次包括下述步骤:
步骤1:采用ase法萃取威灵仙粉末,并收集甲醇萃取液;
步骤2:采用hplc法测定甲醇萃取液中的齐墩果酸的含量;
其中,步骤1所述的萃取依次包括用乙酸乙酯在80℃下去脂,在120℃下乙醇提取。
优选地,所述的步骤1包括下述子步骤:
步骤s1:将威灵仙粉碎,过三号筛,取1g与1g石英砂混合;
步骤s2:将混合物装于放有滤膜、1g硅藻土的ase萃取池中,加石英砂至与池口平行;
步骤s3:用乙酸乙酯去脂,再用乙醇提取;
步骤s4:蒸干,将沉淀用30ml盐酸溶解,加热回流2h;
步骤s5:冷却,移入分液漏斗中,加45ml乙酸乙酯提取,浓缩;
步骤s6:将步骤s5所得的浓缩物加甲醇溶解,并加甲醇定容至10ml,离心,取上清液。
优选地,步骤s3所述的去脂参数为:压力为1500psi,温度为80℃,萃取时间为3min,循环次数为2次,冲洗体积为100%,吹扫时间为60s。
优选地,步骤s3所述的提取参数为:压力为1500psi,温度为120℃,萃取时间为5min,循环次数为3次,冲洗体积为100%,吹扫时间为60s。
优选地,步骤s4所述的盐酸浓度为2mol/l。
优选地,所述的步骤5具体为:冷却,移入分液漏斗中,提取加乙酸乙酯提取3次,每次15ml,收集3次提取液,浓缩。
优选地,步骤2所述的hplc法的检测参数为:色谱柱为thermoacclaimc30;柱温为20℃;
流速为0.5ml/min;流动相为乙腈-水;检测波长为205nm。
优选地,所述的色谱柱的规格为2.1*150mm,3μm。
优选地,所述的流动相为体积比等于62:38的乙腈-水。
本发明与传统方法相比,具有以下优点:
本发明曾对快速溶剂萃取使用的溶剂进行考察,《中国药典》使用乙酸乙酯除杂,采用稀乙醇提取齐墩果酸结合物再水解成齐墩果酸,杂质较少,故对使用乙酸乙酯、正己烷作为除杂溶剂,甲醇、稀乙醇、乙醇作为提取溶剂进行了溶剂考察,结果显示乙酸乙酯除杂,稀乙醇提取齐墩果酸后采用2mol/l盐酸水解后的含量与2015年版《中国药典》含量一致,且杂质峰基本相同,故采用与药典一致的提取溶剂。期间我们试采用乙酸乙酯除杂,采用5%氨水稀乙醇、3%磷酸稀乙醇作为提取和水解溶液作为仪器的萃取罐内进行水解提取,提取效果不佳,故单独采用药典的2mol/l盐酸溶液杂仪器外进行水解。
在除杂过程中,药典方法加入乙酸乙酯回流3h,时间相对较长,我们采用了多次萃取除杂的方式,发现80℃,提取3min,2次即可达到除去大部分杂质,再多的提取时间和次数已经无明显影响,而相对高的温度会是齐墩果酸结果降低,故最终确定最佳除杂工艺组合为提取温度80℃,提取时间3min,提取次数2次。提取过程中采用120℃。提取5min,提取3次即可达到与药典含量接近,更多的提取时间、温度、次数对结果已经无明显影响。最终确定最佳提取工艺组合为提取温度120℃,提取时间5min,提取次数3次。
附图说明
图1为以齐墩果酸对照品的浓度(μg/ml)-峰面积进行的线性回归图;
图2为齐墩果酸对照品溶液的色谱图;
图3为采用药典方法提取所得的供试品溶液的色谱图;
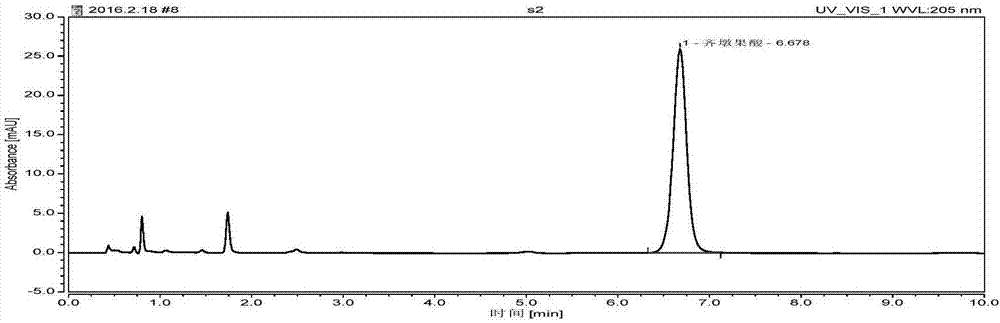
图4为采用ase法提取所得的供试品溶液的色谱图。
具体实施方式
下面结合具体实施方式,对本发明的权利要求做进一步的详细说明,但不构成对本发明的任何限制,任何在本发明权利要求保护范围内所做的有限次修改,仍在本发明的权利要求保护范围内。
实施例1
1、仪器设备及试剂
1.1仪器:
电子分析天平(xa205du)、ase350快速溶剂萃取仪(美国dionex公司)、thermou3000uhplc液相色谱仪
1.2试剂:
水:符合gb/t6682规定的一级水;
甲醇(ch4o):色谱纯;
乙醇(c2h60)、乙酸乙酯(c4h8o2):分析纯;
石英砂:2mm。
2、方法
2.1对照品溶液的制备
取齐墩果酸对照品适量,精密称定,加流动相制成每1ml含1mg的溶液,即得。
2.2供试品溶液的制备
2.2.12015年版药典方法
取本品粉末(过四号筛)约4g,精密称定,置索氏提取器中,加乙酸乙酯适量,加热回流3小时,弃去乙酸乙酯液,药渣挥干溶剂,连同滤纸筒转移至锥形瓶中,精密加入稀乙醇50ml,称定重量,加热回流1小时,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,精密量取续滤液25ml,置水浴上蒸干,残渣加2mol/l盐酸溶液30ml使溶解,加热回流2小时。立即冷却,移入分液漏斗中,用水10ml分次洗涤容器,洗液并入分液漏斗中。加乙酸乙酯振摇提取3次,每次15ml,合并乙酸乙酯液,70℃以下浓缩至近干,加甲醇溶解,转移至10ml量瓶中,加甲醇至刻度,摇匀,即得。
2.2.2快速溶剂萃取法(ase)制备供试品方法
样品经粉碎机粉碎,过三号筛,约1g,精密称定,与适量石英砂混合均匀,待用,在预先放好过滤膜的
2.2.3对照品溶液的制备
取威灵仙对照品适量,精密称定,加流动相制成每1ml含1mg的溶液,即得。
2.3ase萃取条件
去脂参数为:压力为1500psi,温度为80℃,萃取时间为3min,循环次数为2次,冲洗体积为100%,吹扫时间为60s。
提取参数为:压力为1500psi,温度为120℃,萃取时间为5min,循环次数为3次,冲洗体积为100%,吹扫时间为60s。
2.4色谱条件与系统适用性试验
a)仪器:thermo双三元液相(u-3000);
b)色谱柱:thermoacclaimc30,2.1*150mm,3μm
c)柱温:20℃;
d)流速:0.5ml/min;
e)流动相:乙腈-水(62:38);
f)检测波长:205nm;
以十八烷基硅烷键合硅胶为填充剂;理论板数按齐墩果酸峰计算应不低于3000。
2.5测定法
照高效液相色谱法(通则0512)测定;
分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
2.6标准限值要求
本品按干燥品计算,含齐墩果酸(c30h48o3)不得少于0.30%。
2.7计算(外标法)
式中cr—对照品溶液浓度,单位为微克每升(mg/l);
ax—供试品的峰面积;
ar—对照品峰面积。
注意:
使用前萃取池底部应拆卸清理干净,否则容易引起压力不稳;
萃取池底部的滤纸应在密封圈内,否则引起渗漏;
萃取池装样时松紧适中,太松容易导致提取液过多;
开机前检查气瓶气压是否达到1mpa;
使用结束后清理干净,萃取池要及时晾干(容易生锈)。
3、结果
3.1线性关系
取齐墩果酸对照品适量,精密称定,置棕色量瓶中,加甲醇制成每1ml含齐墩果酸1mg的溶液,然后分别精密吸取该溶液0.1μl、0.2μl、0.5μl、0.8μl、1.0μl进入lc测定,并依照上述方法测定,结果详见表1。
以浓度(μg/ml)-峰面积进行线性回归,求得回归方程y=0.00084x+0.03077,r=0.99991。齐墩果酸在108.4~1084μg/ml范围内呈良好的线性关系,详见图1。
表1线性实验结果
3.2重现性实验
取相同批号的样品(批号:150410(z))1.0g,共6份,精密称定,按ase提取方法提取供试品溶液,进样量为1μl,以上述的色谱条件平行试验,测得样品中齐墩果酸的含量见表2,rsd为2.0%,结果表明ase提取方法重复性良好。
表2
3.3精密度和稳定性实验
取齐墩果酸对照品溶液(1.084mg/ml),连续进样6次,记录峰面积,峰面积rsd为0.5%,表明仪器精密度良好。
取同一供试品溶液,室温下放置,分别于0,1,3,6,12h依法测定。结果黄芪甲苷峰面积的rsd为1.5%,表明供试品溶液在12h内稳定。
3.4样品采用药典方法与sae方法含量测定结果(3批)
表3可以看出采用ase仪器1、ase仪器2和药典方法提取后的结果以及ase仪器之间的重复性均良好。
表3
4、讨论:
4.1ase提取溶剂的选择:
试验中,曾对快速溶剂萃取使用的溶剂进行考察,《中国药典》使用乙酸乙酯除杂,采用稀乙醇提取齐墩果酸结合物再水解成齐墩果酸,杂质较少,故对使用乙酸乙酯、正己烷作为除杂溶剂,甲醇、稀乙醇、乙醇作为提取溶剂进行了溶剂考察,结果显示乙酸乙酯除杂,稀乙醇提取齐墩果酸后采用2mol/l盐酸水解后的含量与2015年版《中国药典》含量一致,且杂质峰基本相同,故采用与药典一致的提取溶剂。期间我们试采用乙酸乙酯除杂,采用5%氨水稀乙醇、3%磷酸稀乙醇作为提取和水解溶液作为仪器的萃取罐内进行水解提取,提取效果不佳,故单独采用药典的2mol/l盐酸溶液再仪器外外进行水解。
4.2ase提取条件的优化
在除杂过程中,药典方法加入乙酸乙酯回流3h,时间相对较长,我们采用了多次萃取除杂的方式,发现80℃,提取3min,2次即可达到除去大部分杂质,再多的提取时间和次数已经无明显影响,而相对高的温度会是齐墩果酸结果降低,故最终确定最佳除杂工艺组合为提取温度80℃,提取时间3min,提取次数2次。提取过程中采用120℃。提取5min,提取3次即可达到与药典含量接近,更多的提取时间、温度、次数对结果已经无明显影响。最终确定最佳提取工艺组合为提取温度120℃,提取时间5min,提取次数3次。
以上所述的仅为本发明的较佳实施例,凡在本发明的精神和原则范围内所做的任何修改、等同替换和改进等,均应包含在本发明的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!