允许用于脂质组学研究的全面解决方案的脂质筛选平台的制作方法
相关申请案的交叉参考
本申请案主张2015年2月6日提出申请的序列号为62/113,290的美国临时专利申请案的权益,所述美国临时专利申请案的内容以全文引用的方式并入本文中。
本文中的教示涉及高场非对称波形离子质谱分析(faims)或微分迁移率光谱测定(dms)。更特定来说,本文中的教示涉及用于使用faims或dms装置对脂质进行定量的系统及方法。
背景技术:
脂质为天然有机分子。其一般表征为在水中不溶解且可由有机溶剂溶解。脂质富含于许多不同类型的动物样本或基质(包含但不限于血浆、心脏、肝脏、大脑、肌肉、全血、尿及细胞)中。脂质还富含于其它类型的样本或基质(包含但不限于牛奶、食用油及肉类)中。举例来说,识别且量化动物基质中的脂质在识别且治疗疾病时可为有用的。识别且量化例如食物基质的其它基质中的脂质在检验那些基质的完整性或安全性时可为有用的。不幸地是,当前不存在用于在合理时间量内识别且量化存在于特定基质中的所有脂质的单个系统或方法。
串联质谱为用于对样本基质中的化合物或分子既进行识别又进行量化或定量的方法。在串联质谱仪中,在质量过滤器中选择前体离子,使前体离子碎裂,且在质量分析器中分析产物离子。选择前体离子、使前体离子碎裂且通过质荷比(m/z)分析所得产物离子的整个过程称为串联质谱、质朴分析/质谱分析(ms/ms)或ms/ms扫描。从ms/ms产生的产物离子强度或光谱可用于识别样本中的化合物(前体离子),且一或多个产物离子的强度可用于对存在于样本中的化合物的量进行定量。
信息相依分析(ida)为灵活串联质谱方法,其中用户可规定用于在将样本引入到串联质谱仪中时执行ms/ms的准则。举例来说,在ida方法中,执行前体离子或质谱分析(ms)调查扫描以产生前体离子峰值列表。用户可选择用以针对峰值列表上的前体离子的子集过滤峰值列表的准则。接着对前体离子的子集中的每一前体离子执行ms/ms。针对每一前体离子产生产物离子强度或光谱。在将样本引入到串联质谱仪中时对前体离子子集中的前体离子重复地执行ms/ms。举例来说,通过注入或色谱运行将样本引入到串联质谱仪的离子源。
在ida方法期间执行的一种类型的ms/ms称为多重反应监测(mrm)、选择反应监测(srm)或称为mrm或srm扫描或跃迁。在mrm扫描中,举例来说,选择单个前体离子且使其碎裂,接着从所得产物离子选择单个产物离子,且对选定产物离子进行质量分析。mrm通常用于定量分析。换句话说,mrm通常用于依据产物离子的强度对样本中的前体离子的量进行定量。
例如absciex的
然而不幸的是,甚至使用基于mrm的串联质谱方法,表征特定类型的基质中的所有脂质一直是困难的。完整脂质表征一直是困难的,这是因为许多基质包含混淆识别及准确定量的大量同量异位素及接近同量异位素干扰。一般来说,当样本含有具有或产生具有与分析物类似的m/z的产物离子的另一化合物或所关注化合物时发生同量异位素干扰。在脂质的情形中,许多类别的脂质包含干扰另一类别的脂质的脂质。与复杂样本制备技术及脂质所需要的数据分析有联系的此问题强调对解决这些困难且提供用于分析的简化方法的全面解决方案的需要。
因此,需要用以用合理时间量对存在于特定类型的样本基质中的所有脂质进行识别且定量的系统及方法。
技术实现要素:
提供用于在有针对性的多重反应监测(mrm)获取实验期间使用微分迁移率光谱测定(dms)装置对特定基质的已知脂质分子进行定量的系统及方法的各种实施例。在实验之前,将所述基质的所述已知脂质分子分组成若干脂质类别且将所述脂质类别进一步分组成直通群组及迁移率分离群组。所述直通群组包含具有已知产生对其它脂质分子的同量异位素干扰的脂质分子的脂质类别。所述迁移率分离群组包含具有已知产生同量异位素干扰的脂质分子的脂质类别。
hplc分离系统经由通过低携带率管子进行灌注而引入基质样本。离子源将所述基质样本离子化,从而产生离子束。dms装置针对所述基质样本的第一注入及第二注入从所述离子源接收离子束。对于所述第一注入,所述dms装置被置于被动模式中且不主动地分解脂质分子。对于所述第二注入,所述dms装置用于解决同量异位素干扰。为了解决同量异位素干扰,所述dms装置接收不同补偿电压(cov)值且将不同补偿电压(cov)值施加到所述离子束。所述dms装置接收且施加针对所述迁移率分离群组中的所述脂质类别中的每一者所存储的cov值。
串联质谱仪针对所述第一注入从所述dms装置接收第一离子束。所述串联质谱仪在第一多个循环内针对所述直通群组的每一脂质类别的每一脂质分子的至少一个mrm跃迁执行mrm扫描且存储在所述第一多个循环内的每一mrm扫描的第一强度值集合。
所述串联质谱仪针对所述第二注入接收由所述dms装置根据离子迁移率分离的第二离子束。所述串联质谱仪在第二多个循环内针对所述迁移率分离群组的每一脂质类别的每一脂质分子的至少一个mrm跃迁执行mrm扫描且存储在所述第二多个循环内的每一mrm扫描的第二强度值集合。
与所述质谱仪及所述dms通信的处理器通过将所述第一强度值集合及所述第二强度值集合与所述基质的所述已知脂质分子的已知标准的mrm强度及浓度值进行比较而对所述基质样本中的每一脂质分子进行定量。
附图说明
所属领域的技术人员将理解,下文所描述的图式仅出于图解说明目的。所述图式并非打算以任何方式限制本发明的范围。
图1是图解说明可在其上实施本发明教示的实施例的计算机系统的框图。
图2是示范性微分迁移率光谱测定(dms)装置的示意性图式。
图3是展示根据各种实施例的用于对特定基质中的脂质进行识别且定量的多重反应监测(mrm)方法的初始层次的图式。
图4是展示根据各种实施例的用于对特定基质中的脂质进行识别且定量的mrm方法的在通过同量异位素干扰分组之后的层次的图式。
图5是展示根据各种实施例的用于在有针对性的mrm获取实验期间使用dms装置对基质样本的脂质进行定量的系统的示意性图式。
图6是展示根据各种实施例的用于在有针对性的mrm获取实验期间使用dms装置对基质样本的脂质进行定量的方法的流程图。
在详细描述本发明教示的一或多个实施例之前,所属领域的技术人员将了解,本发明教示在其应用方面并不限于以下详细描述中所陈述或图式中所图解说明的构造细节、组件布置及步骤安排。而且,应理解,本文中所使用的措辞及术语是出于描述目的且不应视为具有限制性。
具体实施方式
图1是图解说明可在其上实施本发明教示的实施例的计算机系统100的框图。计算机系统100包含用于传达信息的总线102或其它通信机构,及与总线102耦合以用于处理信息的处理器104。计算机系统100还包含存储器106,存储器106可为耦合到总线102以用于存储待由处理器104执行的指令的随机存取存储器(ram)或其它动态存储装置。存储器106还可用于在待由处理器104执行的指令的执行期间存储暂时变量或其它中间信息。计算机系统100进一步包含耦合到总线102以用于存储用于处理器104的静态信息及指令的只读存储器(rom)108或其它静态存储装置。提供例如磁盘或光盘等存储装置110且存储装置110耦合到总线102以用于存储信息及指令。
计算机系统100可经由总线102耦合到例如阴极射线管(crt)或液晶显示器(lcd)的显示器112以向计算机用户显示信息。包含字母数字键及其它键的输入装置114耦合到总线102以用于将信息及命令选择传达到处理器104。另一类型的用户输入装置为用于将方向信息及命令选择传达到处理器104且用于控制显示器112上的光标移动的光标控制件116,例如鼠标、轨迹球或光标方向键。此输入装置通常具有在两个轴(第一轴(即,x)及第二轴(即,y))上的两个自由度,这允许所述装置规定在一平面中的位置。
计算机系统100可执行本发明教示。依照本发明教示的某些实施方案,由计算机系统100响应于处理器104执行存储器106中所含有的一或多个指令的一或多个序列而提供结果。可将此类指令从例如存储装置110的另一计算机可读媒体读取到存储器106中。存储器106中所含有的指令序列的执行致使处理器104执行本文中所描述的过程。或者,硬连线电路可取代软件指令或与软件指令组合使用以实施本发明教示。因此,本发明教示的实施方案并不限于硬件电路与软件的任何特定组合。
如本文中所使用的术语“计算机可读媒体”是指参与将指令提供到处理器104以供执行的任何媒体。此媒体可采取许多形式,包含但不限于非易失性媒体、易失性媒体及传输媒体。举例来说,非易失性媒体包含光盘或磁盘,例如存储装置110。易失性媒体包含动态存储器,例如存储器106。传输媒体包含同轴电缆、铜线及光纤,包含包括总线102的导线。
举例来说,常见形式的计算机可读媒体包含软盘、柔性磁盘、硬盘、磁带或任何其它磁性媒体、cd-rom、数字视频光盘(dvd)、蓝光光盘、任何其它光学媒体、拇指驱动器、存储器卡、ram、prom及eprom、快闪eprom、任何其它存储器芯片或盒式磁盘,或者计算机可从其读取的任何其它有形媒体。
在将一或多个指令的一或多个序列载运到处理器104以供执行时可涉及各种形式的计算机可读媒体。举例来说,可最初在远程计算机的磁盘上载运所述指令。所述远程计算机可将指令加载到其动态存储器中并使用调制解调器经由电话线发送指令。在计算机系统100本地的调制解调器可接收电话线上的数据并使用红外发射器将数据转换为红外信号。耦合到总线102的红外检测器可接收在红外信号中载运的数据并将数据置于总线102上。总线102将数据载运到存储器106,处理器104从存储器106检索并执行指令。可任选地在由处理器104执行之前或之后将由存储器106接收的指令存储于存储装置110上。
根据各种实施例,经配置以由处理器执行以执行方法的指令存储于计算机可读媒体上。所述计算机可读媒体可为存储数字信息的装置。举例来说,计算机可读媒体包含此项技术中已知的用于存储软件的光盘只读存储器(cd-rom)。所述计算机可读媒体由适合用于执行经配置以执行的指令的处理器存取。
已出于图解说明及描述的目的而呈现对本发明教示的各种实施方案的以下描述。其并非穷尽性的且不将本发明教示限制于所揭示的精确形式。修改及变化鉴于以上教示而可能存在或可从本发明教示的实践获得。另外,所描述的实施方案包括软件,但本发明教示可实施为硬件与软件的组合或单独以硬件实施。可用面向对象的程序设计系统及非面向对象的程序设计系统两者来实施本发明教示。
脂质筛选平台
如上文所描述,脂质分析中的主要挑战是混淆识别及准确定量的存在于高度复合样本中的许多同量异位素及接近同量异位素干扰。与复杂样本制备技术及数据分析有联系的此问题强调对解决这些困难且提供用于分析的简化方法的全面解决方案的需要。
在各种实施例中,开发包含简化样本制备自动化方法及达成易做到的定量脂质分析的流线数据处理技术的新颖脂质组学平台。微分迁移率光谱测定(dms)已展示为能够解决同量异位素干扰。
对于ida方法,微分迁移率光谱测定(dms)已展示为能够解决同量异位素干扰。具体来说,已利用sciex的selexiontm离子迁移率技术来通过以下操作增强m/z分析的质量:预分离类似m/z的离子,借此移除这些同量异位素干扰。
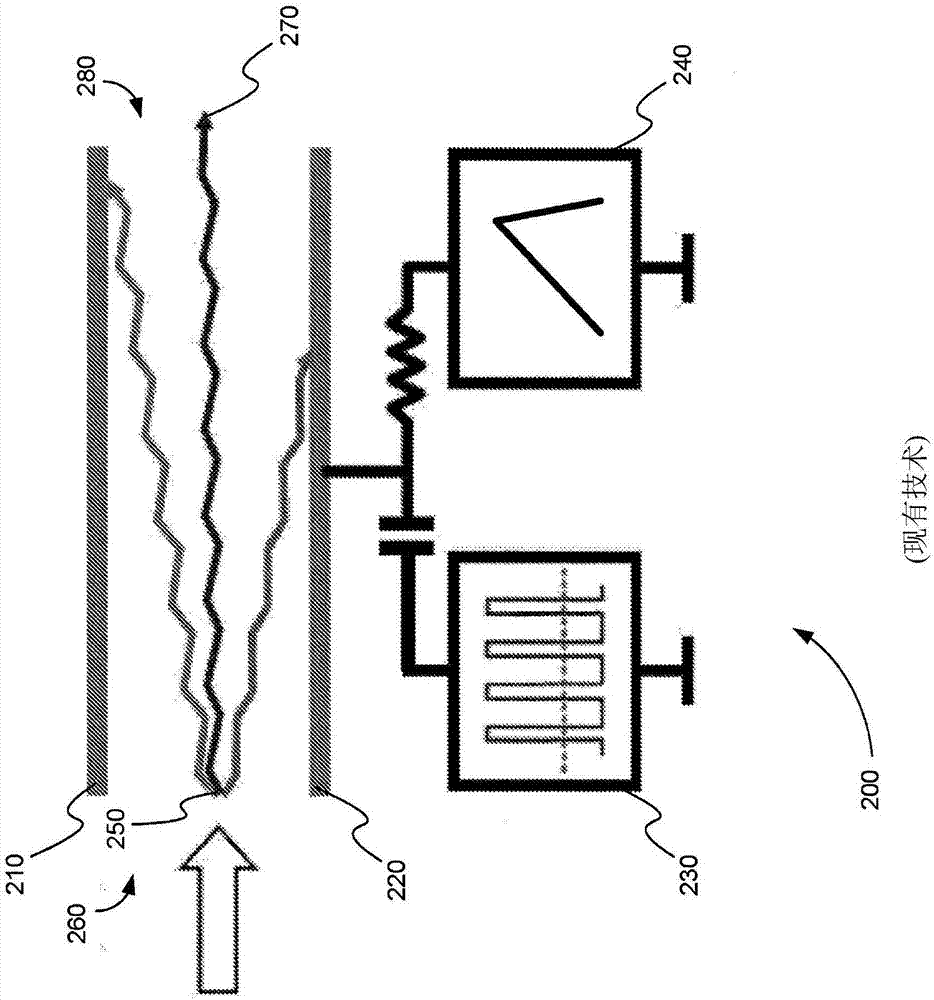
图2是示范性dms装置200的示意图。dms装置200包含两个平行平板,板210及板220。射频(rf)电压源230跨越板210及板220施加rf分离电压(sv),且直流电(dc)电压源240跨越板210及板220施加dc补偿电压(cov)。离子250在开口260处在输送气体中进入dms装置200。dms装置200中的离子250的分离基于其迁移速率在高电场及低电场下的差异。
与传统离子迁移率不同,离子250在其横越装置时不在时间上分离。替代地,离子250基于其迁移率在所施加rf电压源230的高场部分与低场部分之间的差异而在轨道上分离。高场在短时间周期内施加于板210与板220之间,且接着低场在较长时间周期内在相反方向上经施加。所关注化合物的离子的低场与高场迁移率之间的任何差异致使其迁移朝向板中的一者。通过施加称作dc电压源240的cov的第二电压偏移(可用于选择性地滤出所有其它离子的化合物特定参数)使离子朝向装置的中心线往回转向。cov的迅速切换允许用户同时监测许多不同化合物。通过sv与cov的组合选择的离子270通过开口280离开dms装置200到达质谱仪(未展示)的剩余部分。举例来说,dms装置200位于离子源(未展示)与质谱仪的剩余部分之间。
一般而言,dms装置200具有两种操作模式。在第一模式中,dms装置200为接通的,施加sv及cov电压,且将离子分离。举例来说,此为经启用模式。
在第二操作模式中,dms装置200为关断的,将sv设定到零且仅仅将离子250从开口260输送到开口280。举例来说,此为dms装置200的经停用或透明模式。
在经启用模式中,dms装置200可在25毫秒(ms)(举例来说,包含20ms的扫描间暂停时间)内获得用于单个mrm跃迁的数据。在透明模式中,穿过dms装置200的延迟是可忽略的。
在各种实施例中,dms装置用于来自10个不同脂质类别的数百个脂质物种的有针对性的剖析,从而允许综合覆盖。
实验方法
使用唯一内部标准标记协议、新颖选择性工具(dms)及新颖脂质数据分析软件定量地分析血清样本。应用用于简化样本提取及制备的工具包,遵循所提供的协议来使用血清基质。使用
从以下复合脂质类别获得定量脂质类别测量:二酰甘油(dag)、三酰甘油(tag)、磷脂酰胆碱(pc)、磷脂酰乙醇胺(pe)、鞘磷脂(sm)、溶血磷脂酰胆碱(lpc)及溶血磷脂酰乙醇胺(lpe)、自由脂肪酸(ffa)、胆固醇酯(ce)及神经酰胺(cer)。覆盖这些类别需要多次注入方法,但可以短快速梯度收集数据,每注入为5分钟以上的运行时间(针对三次注入)。三次注入类别覆盖tag及sm、ce、cer及dag及ffa、pe/pc及其溶血分量(lpc/lpe)。
用于每一基质的mrm方法制备
为了能够筛选用于脂质的特定基质类型,为所述特定基质建立mrm方法。举例来说,依据实验数据随着时间而建立mrm方法。
图3是展示根据各种实施例的用于对特定基质中的脂质进行识别且定量的mrm方法的初始层次的图式300。通过实验,识别对于基质310可能的所有脂质类别320。举例来说,基质310为血浆。血浆可具有大约1200个不同脂质物种或分子。
基于类似化学结构而将这1200个不同脂质物种分组成若干脂质类别320。血浆的脂质类别可包含但不限于磷脂酰胆碱(pc)、磷脂酰乙醇胺(pe)、溶血磷脂酰胆碱(lpc)、溶血磷脂酰乙醇胺(lpe)、三酰甘油(tag)、二酰甘油(dag)、胆固醇基脂(ce)、自由脂肪酸(ffa)、鞘磷脂(sm)、神经酰胺(cer)、己糖基神经酰胺(hcer)、乳糖基神经酰胺(lcer)及双己糖基神经酰胺(dcer)。
每一脂质类别包含一或多个脂质330。接着使用一或多个mrm跃迁340对每一脂质330进行识别且定量。如上文所描述,每一mrm跃迁为前体离子质荷比(m/z)值及产物离子m/z值。
而且如上文所描述,一些脂质330可包含mrm跃迁340,类似或相同于其它脂质330的那些前体或产物离子m/z值的前体或产物离子m/z值。此产生同量异位素干扰。因此,dms装置用于在分析期间分离前体离子。通过选择前体离子的covdms参数值而将特定前体离子与其它前体离子区分开。由于特定类别的脂质具有类似结构,因此脂质类别的cov值可用于将所述类别的所有前体离子与其它类别中的脂质区分开。换句话说,针对脂质类别以实验方式确定cov值。
然而,并非所有的脂质类别320包含具有对若干类别的脂质330的同量异位素干扰的脂质330。因此,首先确定基质310的哪些脂质330具有同量异位素干扰。接着确定哪些脂质类别320包含具有同量异位素干扰的脂质。最终,针对具有带有同量异位素干扰的脂质的脂质类别确定cov值。换句话说,进一步将脂质类别320分组为干扰或具有cov值的类别,或分组为非干扰类别或不具有cov值的类别。
图4是展示根据各种实施例的用于对特定基质中的脂质进行识别且定量的mrm方法的在通过同量异位素干扰分组之后的层次的图式400。将基质310的脂质类别320进一步分组成两个群组451及452中的一者。群组451包含含有具有同量异位素干扰的脂质的脂质类别,群组452包含不含有具有同量异位素干扰的脂质的脂质类别。进一步地,对于群组451的脂质类别,dmscov参数值460以实验方式被找出且经指派给每一脂质类别。没有dmscov参数值经指派给群组452的脂质类别。
本质上,群组451及452分别允许在接通及不接通dms的情况下执行ms/ms。通过单独分析这些群组,减少使用仪器的总分析时间。换句话说,用充当直通装置的dms分析群组452的脂质类别增加总体分析时间。
在各种实施例中,通过另外根据脂质类别的dmscov参数值460将群组451中的脂质类别排序而进一步减少分析。由于改变dms的cov花费时间且此时间取决于改变量,因此如果根据增加或减小的cov值将脂质类别排序,那么可减少数据获取时间。
用于对脂质进行定量的系统
图5是展示根据各种实施例的用于在有针对性的多重反应监测(mrm)获取实验期间使用微分迁移率光谱测定(dms)装置对基质样本的脂质进行定量的系统的示意图500。图5的系统包含分离装置510、离子源520、dms装置530、串联质谱仪540及处理器550。
分离装置510经配置以顺序地接收基质样本560的第一注入及第二注入。分离装置510也经配置以随着时间将基质的已知脂质分子从第一注入及第二注入分离。举例来说,分离装置510为高性能液相色谱(hplc)装置。在各种替代实施例中,分离装置510可执行包含但不限于气相色谱法(gc)、毛细管电泳(ce)或流动注入分析(fia)的各种分离技术中的一者。
在各种实施例中,分离装置510通过低携带率管子接收第一注入及第二注入。脂质分子为容易粘附到表面的粘性物质。低携带率管子阻止脂质分子粘附到管子表面。一种示范性类型的低携带率管子为peeksiltm。
在实验之前,将基质的已知脂质分子分组成若干脂质类别且将所述脂质类别进一步分组成直通群组及迁移率分离群组。所述直通群组包含具有已知产生对其它脂质分子的同量异位素干扰的脂质分子的脂质类别。所述迁移率分离群组包含具有已知产生同量异位素干扰的脂质分子的脂质类别。
在各种实施例中,根据增加或减小的cov值进一步将迁移率分离群组的脂质类别排序以减少在第二离子束的分析期间改变dms装置的cov值所需要的时间。
离子源520经配置以针对第一注入及第二注入从分离装置510接收经分离脂质分子。离子源520也经配置以针对第一注入及第二注入将经分离脂质分子离子化。
dms装置530经配置以针对第一注入接收经分离脂质分子的第一离子束且在不进行离子迁移率分离的情况下使第一束通过。dms装置530也经配置以针对第二注入接收经分离脂质分子的第二离子束且顺序地对第二束进行迁移率分离。根据针对迁移率分离群组的每一脂质类别以实验方式预定的cov值通过离子迁移率顺序地分离第二离子束。举例来说,dms装置530可为selexiontm装置。
串联质谱仪540经配置以从dms装置接收第一离子束。串联质谱仪540进一步经配置以在第一多个循环内针对直通群组的每一脂质类别的每一脂质分子的至少一个mrm跃迁执行mrm扫描且存储在所述第一多个循环内的每一mrm扫描的第一强度值集合。
串联质谱仪540也经配置以从dms装置接收第二经迁移率分离的离子束。串联质谱仪540进一步经配置以在第二多个循环内针对迁移率分离群组的每一脂质类别的每一脂质分子的至少一个mrm跃迁执行mrm扫描且存储在所述第二多个循环内的每一mrm扫描的第二强度值集合。举例来说,以实验方式预定各个脂质分子的每一mrm跃迁。
在各种实施例中,将第一强度值集合及第二强度值集合存储于存储器或数据存储装置中。所述数据存储装置可为串联质谱仪540的存储装置或单独存储装置。
串联质谱仪540可包含一或多个物理质量滤波器及一或多个物理质量分析器。串联质谱仪540的质量分析器可包含但不限于飞行时间(time-of-flight,tof)、四极、离子陷阱、线性离子陷阱、轨道陷阱、轨陷阱或傅里叶变换质量分析器。
在各种实施例中,串联质谱仪540使用每一脂质类别的预定极性进一步针对基质的已知脂质分子中的每一脂质分子执行每一mrm扫描。
举例来说,处理器550与串联质谱仪540及dms装置530通信。处理器550经配置或编程以接收第一强度值集合及第二强度值集合,接收基质的已知脂质分子的已知标准的mrm强度及浓度值,且对基质样本560中的每一脂质分子进行定量。处理器550通过将第一强度值集合及第二强度值集合与基质的已知脂质分子的已知标准的mrm强度及浓度值进行比较而对基质样本560中的每一脂质分子进行定量。举例来说,在第一多个循环或第二多个循环内针对每一脂质分子的每一mrm计算平均强度值。接着将平均强度值与基质的已知脂质分子的已知标准的mrm强度及浓度值进行比较。
在各种实施例中,处理器550从存储器或数据存储装置接收第一强度值集合、第二强度值集合以及基质的已知脂质分子的已知标准的mrm强度及浓度值。数据存储装置可为串联质谱仪540的存储装置、处理器550的存储装置或单独存储装置。
处理器560可为但不限于图1的系统、计算机、微处理器或能够将控制信息及数据发送到dms装置530及串联质谱仪540以及从dms装置530及串联质谱仪540接收控制信息及数据并处理数据的任何装置。
在各种实施例中,定量经设计以容纳脂质类别的离子化效率的差异以及含有具有不同数目个碳及双键的脂酰链的脂质的微分碎裂效率。每一脂质类别具有在链长度及不饱和程度上变化的多个内部标准,且对目标脂质的mrm具有最少干扰或无干扰。通过关于相应数目个碳及双键使用适当内部标准而正规化目标分子。
在各种实施例中,以实验方式预定其脂质类别的基质可为动物基质。动物基质可包含但不限于血浆、心脏、肝脏、大脑、肌肉、全血、尿或细胞。
在各种实施例中,以实验方式预定其脂质类别的基质可为食物基质。食物基质可包含但不限于牛奶、食用油及肉类。
在各种实施例中,基质的已知脂质分子所分组成的脂质类别包含磷脂酰胆碱(pc)、磷脂酰乙醇胺(pe)、溶血磷脂酰胆碱(lpc)、溶血磷脂酰乙醇胺(lpe)、三酰甘油(tag)、二酰甘油(dag)、胆固醇基脂(ce)、自由脂肪酸(ffa)、鞘磷脂(sm)、神经酰胺(cer)、己糖基神经酰胺(hcer)、乳糖基神经酰胺(lcer)、双己糖基神经酰胺(dcer)、磷脂酰丝胺酸(ps)、磷脂酰甘油(pg)、磷脂酰肌醇(pi)、磷脂酸(pa)、心磷脂(cl)及经氧化脂肪酸代谢物(类花生酸)。
在各种实施例中,基质为血浆。血浆的已知脂质分子所分组成的脂质类别包含磷脂酰胆碱(pc)、磷脂酰乙醇胺(pe)、溶血磷脂酰胆碱(lpc)、溶血磷脂酰乙醇胺(lpe)、三酰甘油(tag)、二酰甘油(dag)、胆固醇基脂(ce)、自由脂肪酸(ffa)、鞘磷脂(sm)、神经酰胺(cer)、己糖基神经酰胺(hcer)、乳糖基神经酰胺(lcer)及双己糖基神经酰胺(dcer)。
用于对脂质进行定量的方法
图6是展示根据各种实施例的用于在mrm获取实验期间使用dms装置对基质样本的脂质进行定量的方法的流程图600。
在图6的方法的步骤610中,使用分离装置顺序地接收基质样本的第一注入及第二注入且随着时间将基质的已知脂质分子从第一注入及第二注入分离。在实验之前,将基质的已知脂质分子分组成若干脂质类别。将所述脂质类别进一步分组成直通群组及迁移率分离群组,所述直通群组包含具有已知产生对其它脂质分子的同量异位素干扰的脂质分子的脂质类别,所述迁移率分离群组包含具有已知产生同量异位素干扰的脂质分子的脂质类别。
在步骤620中,使用离子源针对第一注入及第二注入从分离装置接收经分离脂质分子且针对第一注入及第二注入将经分离脂质分子离子化。
在步骤630中,使用dms装置针对第一注入接收经分离脂质分子的第一离子束且在不进行离子迁移率分离的情况下使第一束通过。
在步骤640中,使用dms装置针对第二注入接收经分离脂质分子的第二离子束且根据针对迁移率分离群组的每一脂质类别以实验方式预定的cov值顺序地对第二束进行迁移率分离。
在步骤650中,使用串联质谱仪在第一多个循环内从dms装置接收第一离子束,针对直通群组的每一脂质类别的每一脂质分子的至少一个mrm跃迁执行mrm扫描,且存储在第一多个循环内的每一mrm扫描的第一强度值集合。
在步骤660中,使用串联质谱仪在第二多个循环内从dms装置接收第二经迁移率分离的离子束,针对迁移率分离群组的每一脂质类别的每一脂质分子的至少一个mrm跃迁执行mrm扫描,且存储在第二多个循环内的每一mrm扫描的第二强度值集合。举例来说,以实验方式预定各个脂质分子的每一mrm跃迁。
在步骤670中,使用处理器接收第一强度值集合及第二强度值集合,接收基质的已知脂质分子的已知标准的mrm强度及浓度值,且对基质样本中的每一脂质分子进行定量。通过将第一强度值集合及第二强度值集合与基质的已知脂质分子的已知标准的mrm强度及浓度值进行比较而对基质样本中的每一脂质分子进行定量。
尽管结合各种实施例描述了本发明教示,但并不打算将本发明教示限制于此类实施例。相反,本发明教示囊括各种替代方案、修改及等效形式,如所属领域的技术人员将了解。
此外,在描述各种实施例时,本说明书可已将方法及/或过程呈现为特定步骤序列。然而,就所述方法或过程不依赖于本文中所陈述的特定步骤序列来说,所述方法或过程不应限制于所描述的特定步骤序列。如所属领域的技术人员将了解,可能有其它步骤序列。因此,说明书中所陈述的步骤的特定次序不应理解为对权利要求书的限制。另外,针对于所述方法及/或过程的权利要求书不应限制于其步骤以所写的次序的执行,且所属领域的技术人员可容易了解,所述序列可变化且仍保持在各种实施例的精神及范围内。
- 还没有人留言评论。精彩留言会获得点赞!