用于婴儿和/或幼儿的包含低聚糖的营养组合物的制作方法
本发明涉及用于婴儿或幼儿的营养组合物及其健康效果。具体地讲,本发明涉及包含用于通过促进和/或减少婴儿或幼儿中特定微生物群落来预防和/或治疗婴儿或幼儿感染的特定低聚糖的营养组合物。
背景技术:
建议所有婴儿采用母乳喂养。然而,在一些情况下,由于某些医学原因,母乳喂养并不足够或不成功,或者母亲不选择母乳喂养。人们已针对这些情况开发出了营养组合物,诸如婴儿配方食品。
用于婴儿和幼儿的营养组合物通常作为用水重构的散剂或在某些情况下作为即饮型或浓缩液体组合物出售。这些组合物旨在覆盖婴儿或幼儿的大部分或所有营养需要。
然而,已经知道人类母乳代表婴儿的营养方面终极的黄金标准。因此,婴儿配方食品制造商已经做出了许多尝试来引起与人类母乳的益处接近或类似的营养健康效果。然而,许多研究表明,婴儿配方食品与人类母乳相比,不会对身体引起同样的效应。例如,喂食婴儿配方食品的婴儿和喂食人类母乳(hbm)的婴儿可表现出不同的肠(肠道)微生物群。
生命的婴儿期,尤其是前几个星期、前3个月、前6个月或前12个月,对于建立平衡的肠道微生物群是至关重要的时期。
已知婴儿期肠道微生物群的调节对于身体的未来健康状况可预期具有重大影响。例如,肠道菌群可对日后的强健的免疫系统的发育、正常的生长具有影响,并且甚至对日后的肥胖的出现具有影响。
类似地,健康的肠内菌群是婴儿健康的指示,肠内微生物群的改变可能是异常健康事件诸如腹泻、营养物质吸收不足、绞痛、睡眠改变和生长发育改变的指示(和/或起因)。
已知分娩方式也可影响婴儿的初始肠道微生物群:通过剖腹产术(剖腹产)分娩的婴儿与阴道分娩的婴儿相比已显示具有不同的肠道微生物群。
然而,在婴儿的发育过程中,肠道微生物群及其进化是许多肠道细菌种群的存在和繁衍(数量)之间的精密平衡。关于肠道细菌对婴儿整体健康的影响,一些肠道细菌被归类为“总体正面的”,而其它肠道细菌是“总体负面的”(或致病性的)。
相比于母乳喂养的婴儿,某些种类的“总体正面的”细菌(诸如双歧杆菌),在喂食常规婴儿配方食品的婴儿中可能不足。类似地,一些细菌种群被认为是致病性的,并且在肠道微生物群中应保持低繁衍。
的确,用婴儿配方食品喂养的婴儿可能不能获益于仅用或主要用人类母乳喂养的婴儿的天然、良好平衡的肠道菌群(肠道微生物群)。在母乳喂养的婴儿中观察到的这样的天然微生物群的确随着时间推移被很好地控制(随着时间推移而进化)并且是复杂的。许多微生物类群共存于肠道/肠内的高度复杂微环境中,每一者以依序限定的比例存在。当限定婴儿或幼儿的微生物群时,应该考虑数量维度和质量维度。此外,肠道微生物群随时间推移的变化增加了复杂性。
合适和健康的肠道微生物群是婴儿的粘膜免疫系统发育的关键因素。虽然许多研究已确定了促进一些阳性细菌在婴儿肠道中的生长和繁衍的方法,但对于诱导可防止感染的特定微生物群特征的方法知之甚少。
需要用于婴儿或幼儿的营养组合物,该营养组合物促进和/或诱导将防止感染的特定微生物群落。
需要为婴儿或幼儿提供使可防止感染的特定微生物群落能够发育的最好营养,所述发育是短期的(即,在营养干预期间)和/或长期的(即,在营养干预之后)。
需要用于婴儿或幼儿的营养组合物,该营养组合物通过营养诱导和/或促进可防止感染的特定微生物群落的发育来诱导最佳的短期或长期健康状态;这种健康状态包括随时间推移的最佳生长,和免疫系统的最佳发育,以及代谢障碍的预防。
需要补偿在非母乳喂养的婴儿或幼儿(例如,常规营养组合物喂养的那些婴儿或幼儿)中观察到的亚常态特定微生物群落。需要重新平衡这样的总体微生物群。
需要以下列方式向这些婴儿或幼儿递送此类健康益处:不引发副作用的方式和/或不仅容易递送,还能获得父母或健康护理人员广泛认可的方式。
技术实现要素:
在一个方面,本发明涉及包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物,其用于通过促进婴儿或幼儿中的群落类型b和/或通过减少群落类型c来预防和/或治疗感染,其中群落类型b被定义为包含至少80%的双歧杆菌(相对丰度%)的微生物群落;
群落类型c被定义为包含50%至80%的双歧杆菌(相对丰度%)并且还包含厚壁菌门(firmicutes)、拟杆菌门(bacteroidetes)和/或变形菌门(proteobacteria)中的一者或多者的微生物群落;并且
其中所述促进或减少是与主要或完全用不包含所述低聚糖的常规营养组合物喂养的婴儿或幼儿的肠道中的微生物群相比而言。
本发明的另一方面涉及通过提供根据本发明的营养组合物来预防和/或治疗婴儿或幼儿感染的方法。
附图说明
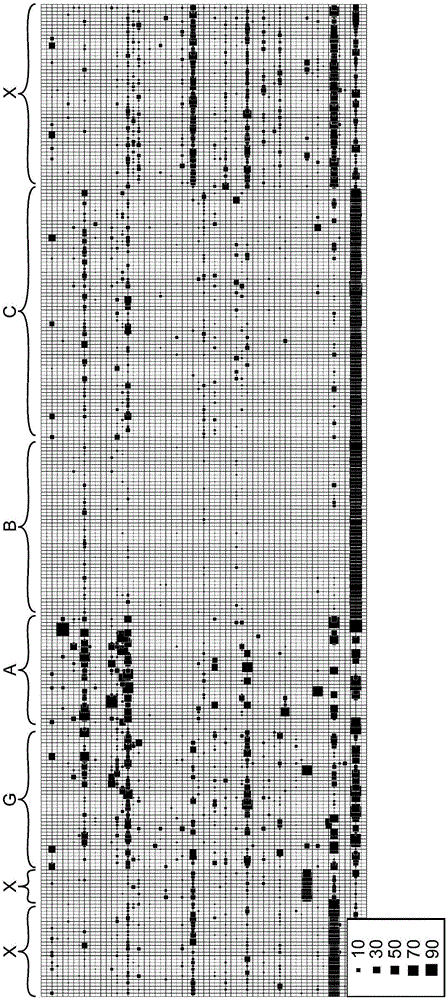
图1示出了将样本中的微生物群分组到群落类型中的概述。样本通过水平线以及垂直线上的分类群示出,其中正方形代表它们在每个样本中的相对量(刻度在右下角)。数字是指群落类型。
图2示出了在我们的研究中定义的七种群落类型的样本中属层级的分类群分布。
图3示出了不同组的个体中微生物群落的分布。
图4示出了具有不同微生物群落的婴儿的抗生素累积使用。另请参见实施例和表4。
图5示出了将来自样本的微生物群特征聚类成群落类型的概述。样本通过水平线以及垂直线上的分类群示出,其中正方形代表它们在每个样本中的相对量(刻度在右下角)。数字是指群落类型。
图6示出了图5的一部分的放大视图,以使得文本清晰易读。
现将在下文中更详细地描述本发明。
具体实施方式
定义
如本文所用,下列术语具有如下含义。
术语“婴儿”是指年龄在12个月以下的儿童。
表述“幼儿”是指年龄介于一岁和三岁之间的儿童,也称为学步儿童。
“剖腹产婴儿或幼儿”是指通过剖腹产术分娩的婴儿或幼儿。这意味着婴儿或幼儿不是经阴道分娩的。
“顺产婴儿或幼儿”是指经阴道分娩而不是通过剖腹产术分娩的婴儿或幼儿。
“早产儿”是指不足月生产的婴儿或幼儿。通常是指在37周妊娠期完成之前出生的婴儿或幼儿。
表述“小于胎龄儿”或“sga”意指个头小于同胎龄出生的正常标准(最常被定义为体重在同胎龄的第10个百分位以下)的婴儿或幼儿。在一些实施方案中,sga可能与宫内生长受限(iugr)相关联,其中iugr是指胎儿无法达到其潜在个头的病症。
表述“低出生体重”应理解为出生时体重不足2500g。
表述“营养组合物”是指供给个体养分的组合物。一般情况下,营养组合物以口服或静脉注射方式摄入,并通常包含脂质或脂肪源、碳水化合物源和蛋白质源。
在一个具体实施方案中,本发明的营养组合物是低变应原营养组合物。表述“低变应原营养组合物”是指不大可能引起变态反应的营养组合物。
在一个具体实施方案中,本发明的营养组合物是“合成营养组合物”。表述“合成营养组合物”是指采用化学和/或生物方法获得的混合物,该混合物的化学性质可能与哺乳动物乳汁中天然存在的混合物相同(即,合成组合物不是母乳)。
如本文所用,表述“婴儿配方食品”是指旨在专用于供给出生后头几个月内的婴儿营养,而且本身满足这类人群的多种营养需求的食料(符合欧盟委员会2006年12月22日颁发的针对婴儿配方食品和较大婴儿配方食品的第91/321/eec2006/141/ec号指令中第2(c)条的规定)。也涉及旨在用于婴儿的营养组合物,如在食品法典委员会(法典stan72-1981)和婴儿特殊品(包括针对特殊医学目的的食品)中所定义的那样。表述“婴儿配方食品”既涵盖“1段婴儿配方食品”,也涵盖“2段婴儿配方食品(follow-upformula)”或“较大婴儿配方食品(follow-onformula)”。在一些实施方案中,婴儿配方食品是早产儿配方食品。
“2段婴儿配方食品”或“较大婴儿配方食品”从第6个月开始给予。婴儿配方食品构成了这类人逐渐多样化饮食中的主要液体元素。
表述“婴孩食物”是指旨在专用于供给不满一岁的婴儿或幼儿营养的食料。
表述“婴儿谷物组合物”是指旨在专用于供给不满一岁的婴儿或幼儿营养的食料,并且包含谷物组分。
术语“强化剂”是指适宜与母乳或婴儿配方食品混合的液态或固态营养组合物。
表述“离乳期”是指在婴儿或幼儿的饮食中逐步用其它食物替代母乳的时期。
表述“x天龄/周龄/月龄/年龄”、“生命的x天/周/月/年”和“出生x天/周/月/年”可互换使用。
“母乳”应理解为母亲的母乳或初乳。hbm是指人类母乳。
表述“只用人类母乳喂养的婴儿/幼儿”、“仅用母乳喂养的婴儿或幼儿”、“完全母乳喂养的婴儿或幼儿”和“母乳喂养的婴儿/幼儿”可互换使用。他们是指用大多数(即,至少90%、或至少95%、或至少99%)或全部(100%)源自人类母乳的营养物质和/或能量喂养的婴儿或幼儿。
表述“只用营养组合物喂养的婴儿或幼儿”是指用大多数(即,至少90%、或至少95%、或至少99%)或全部(100%)源自合成营养组合物(诸如婴儿配方食品、后续乳或成长乳)的营养物质和/或能量喂养的婴儿或幼儿。
表述“主要用营养组合物喂养的婴儿或幼儿”是指用主要源自合成营养组合物(诸如婴儿配方食品、后续乳或成长乳)的营养物质和/或能量的营养源喂养的婴儿或幼儿。“主要”是指那些营养物质和/或能量的至少50%(或至少60%或至少75%),诸如50%至90%、或60%至80%。
表述“常规营养组合物”是指标准合成营养组合物,诸如市场中已经可见的婴儿配方食品、后续乳或成长乳。“不包含所述低聚糖的常规营养组合物”是指不包含“至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖”的标准营养组合物。
本发明的营养组合物可为固体形式(例如,粉末)或液体形式。各种成分(例如低聚糖)的量在组合物为固体形式(例如粉末)时可按照以干重计的g/100g组合物来表示,或者在组合物是指液体形式时表示为g/l组合物的浓度(后者还涵盖可由粉末在液体(诸如乳、水……)中重构之后获得的液体组合物,例如重构的婴儿配方食品或较大/2段婴儿配方食品或婴儿谷物产品或任何其它被设计用于为婴儿提供营养的配制物)。它们也可以g/100kcal表示。
“低聚糖”是含有少量(通常三至二份)普通糖(单糖)的糖类聚合物。
术语“hmo”或“hmos”是指人乳低聚糖。这些碳水化合物高度耐受酶促水解,这表明其表现的重要功能可能不与其热值直接相关。本领域已特别指出,这些碳水化合物在婴儿和幼儿的早期发育(诸如,免疫系统的成熟)过程中发挥关键作用。在人乳中发现了许多不同种类的hmo。每种单独的低聚糖都以葡萄糖、半乳糖、唾液酸(n-乙酰神经氨酸)、岩藻糖和/或n-乙酰基葡糖胺与这些分子间各式各样的键的组合为基础,因此人乳含有大量种类各不相同的低聚糖,迄今已鉴定出逾130种此类结构。几乎所有低聚糖的还原端都有乳糖部分,且非还原端的末端位置都由唾液酸和/或岩藻糖(如果有的话)占据。hmo可以呈酸性(例如,含带电唾液酸的低聚糖),也可以呈中性(例如,岩藻糖基化低聚糖)。
“岩藻糖基化低聚糖”是具有岩藻糖残基的低聚糖。这种低聚糖呈中性。一些示例为2-fl(2'岩藻糖基乳糖)、3-fl(3-岩藻糖基乳糖)、二岩藻糖基乳糖、乳糖-n-岩藻戊糖(例如,乳糖-n-岩藻戊糖i、乳糖-n-岩藻戊糖ii、乳糖-n-岩藻戊糖iii、乳糖-n-岩藻戊糖v)、乳糖-n-岩藻己糖、乳糖-n-二岩藻己糖i、岩藻糖基乳糖-n-己糖、岩藻糖基乳糖-n-新己糖、二岩藻糖基乳糖-n-己糖i、二岩藻糖基乳糖-n-新己糖ii、以及这些物质的任意组合。
表述“包含2'-岩藻糖基表位的岩藻糖基化低聚糖”和“2-岩藻糖基化低聚糖”涵盖了具有一定同源形式的岩藻糖基化低聚糖,这些同源形式的岩藻糖基化低聚糖都包含2’-岩藻糖基表位,因而可推测它们具有一定同源功能。不希望受理论约束,但据信,这些岩藻糖基化低聚糖的2’-岩藻糖基表位特别针对与lrt和/或耳部感染相关的病原体(或病原体所分泌物质)。
表述“n-乙酰化低聚糖”涵盖“n-乙酰氨基乳糖苷”和“含n-乙酰氨基乳糖苷的低聚糖”两者。这种低聚糖是具有n-乙酰氨基乳糖苷残基的中性低聚糖。合适的示例为lnt(乳糖-n-四糖)、对-乳糖-n-新己糖(对-lnnh)、lnnt(乳糖-n-新四糖)以及它们的任意组合。其它示例为乳糖-n-己糖、乳糖-n-新己糖、对-乳糖-n-己糖、对-乳糖-n-新己糖、乳糖-n-八糖、乳糖-n-新八糖、异-乳糖-n-八糖、对-乳糖-n-八糖和乳糖-n-十糖。
表述“至少一种岩藻糖基化低聚糖”和“至少一种n-乙酰化低聚糖”是指“至少一种类型的岩藻糖基化低聚糖”和“至少一种类型的n-乙酰化低聚糖”。
“hmo的前体”是用于制备hmo的关键化合物,诸如唾液酸和/或岩藻糖。
“唾液酸化低聚糖”是含带电唾液酸的低聚糖,即具有唾液酸残基的低聚糖。这种低聚糖呈酸性。一些示例为3-sl(3'-唾液酸乳糖)和6-sl(6'-唾液酸乳糖)。
表述在婴儿或幼儿中“促进和/或诱导”是指所述婴儿或幼儿中特定微生物群落的发育、增加、建立、出现和/或改变。
术语“微生物”、“微生物群落”和“微生物群”可互换使用。
表述“肠道内微生物群”、“肠道的微生物群”“肠道微生物群”和“肠微生物群”可互换使用。
表述“群落类型”是指由狄利克雷多项式混合(dirichletmultinomialmixtures)建模框架(参见参考文献的另外示例)所定义的以分类群比例存在的一组细菌,该建模框架最好地描述了显示类似微生物群组合物的样本聚类(即,群体中不同细菌分类群的比例或相对丰度)。
群落类型b被定义为几乎排他地包含双歧杆菌的微生物群落,诸如至少80%的双歧杆菌(相对丰度%);例如,80%至95%,诸如85%至93%,诸如约90%的双歧杆菌。
群落类型c被定义为由双歧杆菌主导并且还显示较大比例的属于厚壁菌门、拟杆菌门和/或变形菌门的其它分类群组的微生物群落;例如,群落类型c可被定义为包含40%至80%(相对丰度%,诸如50%至80%、诸如60%至80%、例如65%至75%、或约70%的相对丰度)的双歧杆菌以及选自厚壁菌门、拟杆菌门和变形菌门中的一者或多者。
换句话讲,群落类型可被描述为微生物群的亚群,该亚群是通过应用狄利克雷多项式混合建模框架定义的。
相对丰度是指相对于总量的量。因此,80%的相对丰度是指80%的微生物群,无论以何种方式测量总微生物群。总微生物群可例如通过质量、计数等来测量。
微生物群落是指微生物群的亚群。
在本发明的一些实施方案中,群落类型b和群落类型c分别包含如实施例和附图所示的细菌或由其组成。
表述“下调”和“减少”可互换使用。
表述“预防(preventing或prevention)”是指避免身体状况、病症或其后果发生和/或降低其发生率(即减少频率)。
表述“治疗(treating或treatment)”是指减少身体状况、病症或其后果的持续时间和/或降低严重程度。
身体状况、病症或其后果的预防和/或治疗可发生在治疗期间(即,在本发明的组合物的施用期间,要么紧接在施用开始之后或要么在施用开始的一段时间之后,例如在开始后几天或几周)。但是其也可涵盖日后的预防和/或治疗。表述“日后”涵盖干预或治疗结束后的效果。这种“日后的”效果可维持1周至数月,例如,2周至4周、2周至6周、2周至8周、1个月至6个月,或2个月至12个月。
术语“益生元”是指通过选择地刺激健康细菌(诸如人类结肠中的双歧杆菌)的生长和/或其活性而对宿主产生有利影响的非消化性碳水化合物(gibsongr,roberfroidmb.dietarymodulationofthehumancolonicmicrobiota:introducingtheconceptofprebiotics.jnutr.1995;125:1401-12(gibsongr.、roberfroidmb.,“饮食调节人体结肠微生物群:介绍益生菌的概念”,《营养学杂志》,1995年,第125卷,第1401-1412页))。
术语“益生菌”是指对宿主的健康或良好状态具有有益效果的微生物细胞制剂或微生物细胞组分。(salminens,ouwehanda.bennoy.etal.“probiotics:howshouldtheybedefined”trendsfoodsci.technol.1999:10107-10(salminens.、ouwehanda.、bennoy.等人,“如何定义益生菌”,《食品科学与技术趋势》,1999年,第10卷,第107-110页))。微生物细胞一般为细菌或酵母。
术语“cfu”应理解为菌落形成单位。
除非另外指明,否则所有百分比均按重量计。
另外,在本发明的上下文中,术语“包含”或“包括”不排除其它可能的要素。本发明的组合物(包括本文所述的多个实施方案)可包含下列要素、由或基本上由下列要素组成:本文所述的本发明的基本要素和必要限制,以及本文所述的或视需求而定的任何其它或可选成分、组分或限制。
不能将本说明书中对现有技术文献中的任何参考视为承认此类现有技术为众所周知的技术或构成本领域普遍常识的一部分。
现在开始更详细描述本发明。应当注意,本申请描述的多个方面、特征、实施例和实施方案可以相容和/或可以组合在一起。
因此,本发明的第一个目的是包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物,其用于通过促进婴儿或幼儿中的群落类型b和/或通过减少婴儿或幼儿中的群落类型c来预防和/或治疗感染,其中群落类型b被定义为包含至少80%的双歧杆菌(相对丰度%)的微生物群落;
群落类型c被定义为包含40%至80%的双歧杆菌并且还包含厚壁菌门、拟杆菌门和/或变形菌门中的一者或多者的微生物群落;
其中所述促进或减少是与主要或完全用不包含所述低聚糖的常规营养组合物喂养的婴儿或幼儿的肠道中的微生物群相比而言。
另选地,本发明可被描述为涉及包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物,其用于通过促进群落类型b和/或通过减少群落类型c来预防和/或治疗婴儿或幼儿感染,其中与主要或完全用不包含所述低聚糖的常规营养组合物喂养的婴儿或幼儿的肠道中的微生物群相比,所述促进涉及上调双歧杆菌群体并且所述减少涉及下调埃希氏杆菌属和/或消化链球菌科群体,以及预防和/或治疗感染。
岩藻糖基化低聚糖
本发明的营养组合物包含至少一种岩藻糖基化低聚糖。可存在一种或若干种类型的岩藻糖基化低聚糖。岩藻糖基化低聚糖可选自2'-岩藻糖基乳糖、3’-岩藻糖基乳糖、二岩藻糖基乳糖、乳糖-n-岩藻戊糖(诸如乳糖-n-岩藻戊糖i、乳糖-n-岩藻戊糖ii、乳糖-n-岩藻戊糖iii、乳糖-n-岩藻戊糖v)、乳糖-n-岩藻己糖、乳糖-n-二岩藻己糖i、岩藻糖基乳糖-n-己糖、岩藻糖基乳糖-n-新己糖(诸如岩藻糖基乳糖-n-新己糖i、岩藻糖基乳糖-n-新己糖ii)、二岩藻糖基乳糖-n-己糖i、二岩藻基-乳糖-n-新己糖、二岩藻糖基乳糖-n-新己糖i、二岩藻糖基乳糖-n-新己糖ii、岩藻糖基-对-乳糖-n-己糖、三岩藻糖基-对-乳糖-n-己糖i以及它们的任意组合。
在一些具体实施方案中,岩藻糖基化低聚糖包含2'-岩藻糖基表位。岩藻糖基化低聚糖可例如选自包括以下项的列表:2’-岩藻糖基乳糖、二岩藻糖基乳糖、乳糖-n-岩藻戊糖、乳糖-n-岩藻己糖、乳糖-n-二岩藻己糖、岩藻糖基乳糖-n-己糖、岩藻糖基乳糖-n-新己糖、二岩藻糖基乳糖-n-己糖、二岩藻糖基-乳糖-n-新己糖、二岩藻糖基乳糖-n-新己糖、岩藻糖基-对-乳糖-n-己糖以及它们的任意组合。
在一个优选的实施方案中,根据本发明的营养组合物包含2’-岩藻糖基乳糖(或2fl、或2’fl、或2-fl或2’-fl)。在一个具体实施方案中,不存在除2’-岩藻糖基乳糖以外的其它类型的岩藻糖基化低聚糖,即,本发明的营养组合物仅包含2’-岩藻糖基乳糖作为岩藻糖基化低聚糖。
可通过层析技术或过滤技术从天然源诸如动物乳来分离岩藻糖基化低聚糖。或者,也可利用特殊的岩藻糖基转移酶和/或岩藻糖苷酶,通过生物技术手段,通过使用基于酶(重组酶或天然酶)的发酵技术或微生物发酵技术,来制备岩藻糖基化低聚糖。在后一者情况下,微生物可表达其天然酶和底物,或者可被工程改造成产生相应的底物和酶。可使用单一微生物培养物和/或混合培养物。
可以最初具有任意聚合度(dp)的受体底物开始形成岩藻糖基化低聚糖,从dp=1开始。另选地,可以通过由乳糖和游离岩藻糖化学合成来制备岩藻糖基化低聚糖。岩藻糖基化低聚糖也可从例如日本协和发酵工业株式会社(kyowa,hakko,kogyo)购得。
n-乙酰化低聚糖
本发明的营养组合物还包含至少一种n-乙酰化低聚糖。可存在一种或若干种类型的n-乙酰化低聚糖。n-乙酰化低聚糖可以是例如乳糖-n-四糖(lnt)、乳糖-n-新四糖(lnnt)或它们的任意组合。在一些具体实施方案中,n-乙酰化低聚糖为乳糖-n-新四糖(lnnt)、对-乳糖-n-新己糖(对-lnnh)或它们的任意组合。在一些具体实施方案中,n-乙酰化低聚糖为lnnt。在一些具体实施方案中,n-乙酰化低聚糖为lnt。在一些其它具体实施方案中,n-乙酰化低聚糖为lnt与lnnt的混合物。在一些具体实施方案中,组合物包含lnt和lnnt两者,lnt:lnnt的比率为5:1至1:2,或2:1至1:1,或2:1.2至2:1.6。
在一个优选的实施方案中,根据本发明的营养组合物包含乳糖-n-新四糖(lnnt)。在一个具体实施方案中,除了乳糖-n-新四糖(lnnt)之外不包含其它类型的n-乙酰化低聚糖,即本发明的营养组合物只包含乳糖-n-新四糖(lnnt)作为n-乙酰化低聚糖。
n-乙酰化低聚糖可采用酶转移法,即使用糖基转移酶将供体部分的糖单元转移到受体部分来化学合成,如例如美国专利5,288,637和wo96/10086所述。另选地,lnt和lnnt可通过将游离的或与低聚糖(例如,乳果糖)结合的酮-己糖(例如,果糖)化学转化成n-乙酰己糖胺或包含n-乙酰己糖胺的低聚糖来制备,如wrodnigg,t.m.;stutz,a.e.(1999)angew.chem.int.ed.38:827-828中所述。然后可将用这种方式制得的n-乙酰氨基乳糖苷转移到作为受体部分的乳糖。
在本发明的特别有利的实施方案中,该营养组合物包含2'-岩藻糖基乳糖(2fl)和乳糖-n-新四糖(lnnt)。
在另一个具体实施方案中,本发明的营养组合物包含由2’-岩藻糖基乳糖(2-fl)和乳糖-n-新四糖(lnnt)组成的低聚糖混合物。换句话讲,本发明的营养组合物仅包含2’-岩藻糖基乳糖(2-fl)作为岩藻糖基化低聚糖并且仅包含乳糖-n-新四糖(lnnt)作为n-乙酰化低聚糖。
岩藻糖基化低聚糖和n-乙酰化低聚糖的量
在本发明中,岩藻糖基化低聚糖和n-乙酰化低聚糖以一些特定量存在于营养组合物中。除非另有规定,术语“量”是指营养组合物中的这2种组分中的每一者的总量。因此其不是指单个量,除非存在单种类型的这些组分(在这种情况下,总量和单个量相等)。作为例示性示例,如果组合物中存在仅一种(即,仅一种类型)的岩藻糖基化低聚糖(例如2fl),其单个量(因此也是岩藻糖基化低聚糖的总量)将在0.5g/l至2.0g/l的范围内。如果存在几种(即,几种类型)的岩藻糖基化低聚糖,其单个量将降低(例如,如果存在两种不同类型的岩藻糖基化低聚糖,例如2fl+3fl,则单个量可例如各自为0.5g/l),但岩藻糖基化低聚糖的总量将在0.5g/l至2.0g/l的范围内。
一种或多种岩藻糖基化低聚糖可以0.75-1.65g/l组合物的总量存在于根据本发明的营养组合物中。在一些实施方案中,岩藻糖基化低聚糖的总量可为0.8g-1.5g/l组合物,诸如0.85g-1.3g/l组合物、或0.9g-1.25g/l组合物、或0.9g-1.1g/l组合物、或1g-1.25g/l组合物、或1.05g-1.25g/l组合物。在一些实施方案中,岩藻糖基化低聚糖的总量可为0.15g-2g/l组合物,诸如0.2g-1.5g/l组合物。在一个具体实施方案中,岩藻糖基化低聚糖的总量为1g/l组合物。在另一个具体实施方案中,岩藻糖基化低聚糖的总量为1.24g/l组合物。
以干重计,岩藻糖基化低聚糖可以0.52g-1.15g/100g组合物的总量存在于营养组合物中。岩藻糖基化低聚糖的总量可为0.55g-1.05g/100g组合物,诸如0.59g-0.9g/100g组合物、或0.62g-0.87g/100g组合物、或0.62g-0.77g/100g组合物、或0.69g-0.87g/100g组合物、或0.73g-0.87g/100g组合物。岩藻糖基化低聚糖的总量可为0.1g-1.8g/100g组合物,诸如0.15g-0.9g/100g组合物。在一个具体实施方案中,岩藻糖基化低聚糖的总量为0.69g/100g组合物。在另一个具体实施方案中,岩藻糖基化低聚糖的总量为0.86g/100g组合物。
n-乙酰化低聚糖可以0.45g-0.85g/l组合物的总量存在于根据本发明的营养组合物中。
在一些实施方案中,n-乙酰化低聚糖的总量可为0.5g-0.8g/l组合物,诸如0.5g-0.75g/l组合物、或0.5g-0.7g/l组合物。在一些实施方案中,n-乙酰化低聚糖的总量可为0.05g-0.8g/l组合物,诸如0.1g-0.5g/l组合物或0.1g-0.3g/l组合物。在一个具体实施方案中,n-乙酰化低聚糖的总量为0.5g/l或0.1g/l组合物(或至少这些量)。在另一个具体实施方案中,n-乙酰化低聚糖的总量为0.63g/l组合物。
以干重计,n-乙酰化低聚糖可以0.31g-0.59g/100g组合物的总量存在于营养组合物中。n-乙酰化低聚糖的总量可为0.35g-0.56g/100g组合物,诸如0.35g-0.52g/100g组合物或0.35g-0.49g/100g组合物。n-乙酰化低聚糖的总量可为0.04g-0.65g/100g组合物,诸如0.05g-0.5g/100g组合物或0.05g-0.1g/100g组合物。在一个具体实施方案中,n-乙酰化低聚糖的总量为0.35g/100g组合物或0.07g/100g组合物(或至少这些量)。在另一个具体实施方案中,n-乙酰化低聚糖的总量为0.44g/100g组合物。
因此,在本发明的一个实施方案中,营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其中:
-岩藻糖基化低聚糖的总量为0.8g-1.5g/l组合物和/或以干重计总量为0.55g-1.05g/100g组合物;和/或
-n-乙酰化低聚糖的总量为0.5g-0.8g/l组合物和/或以干重计总量为0.35g-0.56g/100g组合物。
在另一个具体实施方案中,本发明的营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其中:
-岩藻糖基化低聚糖的总量为0.85g-1.3g/l组合物和/或以干重计总量为0.59g-0.9g/100g组合物;和/或
-n-乙酰化低聚糖的总量为0.5g-0.75g/l或0.08g-0.6g/l组合物和/或以干重计总量为0.35g-0.52g/100组合物或0.1g-0.5g/100g组合物。
在另一个具体实施方案中,本发明的营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其中:
-岩藻糖基化低聚糖的总量为1g-1.25g/l组合物和/或以干重计总量为0.69g-0.87g/100g组合物;和/或
-n-乙酰化低聚糖的总量为0.5g-0.7g/l组合物和/或以干重计总量为0.35g-0.49g/100g组合物。
在另一个具体实施方案中,本发明的营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其中:
-岩藻糖基化低聚糖的总量为1.05g-1.25g/l组合物和/或以干重计总量为0.73g-0.87g/100g组合物;和/或
-n-乙酰化低聚糖的总量为0.5g-0.7g/l组合物和/或以干重计总量为0.35g-0.49g/100g组合物。
在一个具体实施方案中,根据本发明的营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其中:
-岩藻糖基化低聚糖的总量为1g/l组合物和/或以干重计总量为0.69g/100g组合物;和/或
-n-乙酰化低聚糖的总量为0.5g/l组合物和/或以干重计总量为0.35g/100g组合物。
在另一个具体实施方案中,根据本发明的营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其中:
-岩藻糖基化低聚糖的总量为1.24g/l组合物和/或以干重计总量为0.86g/100g组合物;和/或
-n-乙酰化低聚糖的总量为0.63g/l组合物和/或以干重计总量为0.44g/100g组合物。
根据本发明的营养组合物中所含的岩藻糖基化低聚糖和n-乙酰化低聚糖通常以2:0.54至2:2.26的岩藻糖基化低聚糖:n-乙酰化低聚糖比率存在,诸如2:0.76-2:1.8或2:0.8-2:1.4。在特别有利的实施方案中,该比率为2:1或约2:1。在另一个特别有利的实施方案中,该比率为10:1或介于15:1和2:1之间。
其它低聚糖
根据本发明的营养组合物可还包含至少另外的低聚糖(即,除了必需存在于组合物中的岩藻糖基化低聚糖和n-乙酰化低聚糖以外)和/或至少一种纤维和/或至少一种其前体。另外的的低聚糖和/或纤维和/或其前体可选自包括下列的列表:低聚半乳糖(gos)、低聚果糖(fos)、菊粉、低聚木糖(xos)、聚右旋糖、唾液酸化低聚糖、唾液酸、岩藻糖以及它们的任意组合。它们的量可为组合物的0重量%至10重量%。在一个具体实施方案中,营养组合物还可包含至少一种牛乳低聚糖(bmo)。
除了包含在低聚糖混合物中的低聚糖外,可用以制备根据本发明的营养组合物的合适商用产品包括fos与菊粉的组合,诸如由beneo公司以商标orafti出售的产品,或者由泰莱公司(tate&lyle)以商标
低聚果糖
在一个具体实施方案中,根据本发明的营养组合物可包含每100kcal组合物至少约0.4g或至少0.7g低聚果糖,诸如每100kcal约0.4g至约0.9g、约0.4g至约0.7g、约0.4g至约0.5g、约0.7g至约0.8g、或约0.7g至约0.9g低聚果糖。
在一些实施方案中,低聚果糖具有2至10的聚合度。在一些实施方案中,至少80%、90%、95%、99%或100%的低聚果糖具有2至8(介于2和8之间)的聚合度。
在一个具体实施方案中,根据本发明的营养组合物可包含gos。低聚半乳糖是包含两个或更多个半乳糖分子的低聚糖,其不带电荷,也不具有n-乙酰基残基。还可在根据本发明的营养组合物中添加的合适低聚半乳糖包括:galbeta1,3galbeta1,4glc、gal1,6galbeta1,4glc、galbeta1,3galbeta1,3galbeta1,4glc、galbeta1,6galbeta1,6galbeta1,4glc、galbeta1,3galbeta1,6galbeta1,4glc、galbeta1,6galbeta1,3galbeta1,4glc、galbeta1,6galbeta1,6galbeta1,6glc、galbeta1,3galbeta1,3glc、galbeta1,4galbeta1,4glc和galbeta1,4galbeta1,4galbeta1,4glc,但也可包括它们的任意混合物。合成的低聚半乳糖诸如galbeta1,6galbeta1,4glc、galbeta1,6galbeta1,6galbeta1,6glc、galbeta1,3galbeta1,4glc、galbeta1,6galbeta1,6galbeta1,4glc、galbeta1,6galbeta1,3galbeta1,4glc、galbeta1,3galbeta1,6galbeta1,4glc、galbeta1,4galbeta1,4glc和galbeta1,4galbeta1,4galbeta1,4glc以及它们的混合物可以商标vivinal和elix’or商购获得。低聚糖的其它供应商为dextralaboratories、sigma-aldrichchemiegmbh和kyowahakkokogyoco.,ltd.。另选地,可使用特定的糖基转移酶(诸如半乳糖基转移酶)来产生中性低聚糖。
在一个具体实施方案中,营养组合物可还包含至少一种牛乳低聚糖。可以使用用于对牛乳衍生低聚糖中的牛乳级分进行分级分离和富集的常规技术(这种常规技术包括柱过滤、树脂过滤、纳滤、酶处理(特别是使用β-半乳糖苷酶)、蛋白质沉淀、乳糖的结晶和分离等)。一些富含低聚糖的牛乳级分是可商购获得的,或者已在例如ep2526784a1中有所描述。
唾液酸化低聚糖
在一个具体实施方案中,根据本发明的营养组合物可包含一种或多种唾液酸化低聚糖。可存在一种或若干种唾液酸化低聚糖。
该唾液酸化低聚糖可选自包括下列各项的组:3'-唾液酸乳糖(3-sl)、6'-唾液酸乳糖(6-sl)以及它们的任意组合。在本发明的一些实施方案中,该组合物包含3-sl和6-sl。在一些具体实施方案中,3'-唾液酸乳糖(3-sl)与6'-唾液酸乳糖(6-sl)之间的比率可在5:1至1:10、或3:1至1:1、或1:1至1:10的范围内。
在一些具体实施方案中,该组合物中的唾液酸化低聚糖为6'-唾液酸乳糖(6-sl)。
可通过层析技术或过滤技术从天然源(诸如,动物乳)分离唾液酸化低聚糖。或者,也可使用特殊的唾液酸转移酶或唾液酸酶、唾液酸苷酶,通过生物技术手段,通过基于酶(重组酶或天然酶)的发酵技术、通过化学合成或通过微生物发酵技术,来制备唾液酸化低聚糖。在后一种情况下,微生物可表达其天然酶和底物,或者可经工程化以产生相应的底物和酶。可使用单一微生物培养物或混合培养物。可以最初具有任意聚合度(dp)的受体底物开始形成唾液酸化低聚糖,从dp=1开始。另选地,可通过由乳糖和游离n'-乙酰神经氨酸(唾液酸)的化学合成来产生唾液酸乳糖。唾液酸乳糖也可从例如日本的kyowahakkokogyo商购获得。
在具体示例中,该组合物可包含0.05g/l至5g/l的唾液酸化低聚糖,或0.1g/l至4g/l、或0.3g/l至2g/l、或0.4g/l至1.5g/l、或0.4g/l至1g/l,例如0.5g/l或0.9g/l的唾液酸化低聚糖。在一些具体实施方案中,该组合物可包含0.8g/l至1.7g/l的唾液酸化低聚糖。
根据本发明的组合物以干重计每100g组合物可包含0.03g至3.88g的唾液酸化低聚糖,例如以干重计每100g组合物0.08g至3.10g、或0.23g至1.55g、或0.31g至1.16g、或0.31g至0.77g、或0.39g至0.7g、或0.62g至1.32g的唾液酸化低聚糖。
在本发明的一些具体实施方案中,以干重计,营养组合物以低于0.1g/100g组合物的量包含唾液酸化低聚糖。
在本发明的一些具体实施方案中,营养组合物不含任何唾液酸化低聚糖。
在一个具体实施方案中,营养组合物可还另外包含低聚糖混合物(“bmos”),该低聚糖混合物包含0.1重量%至4.0重量%的n-乙酰化低聚糖,92.0重量%至98.5重量%的低聚半乳糖以及0.3重量%至4.0重量%的唾液酸化低聚糖。
前体
根据本发明的组合物可任选地还包含至少一种低聚糖前体。可存在一种或若干种低聚糖前体。例如,人乳低聚糖的前体为唾液酸、岩藻糖或者它们的混合物。在一些具体实施方案中,该组合物包含唾液酸。
在具体示例中,该组合物包含0g/l至3g/l的低聚糖前体,或0g/l至2g/l、或0g/l至1g/l、或0g/l至0.7g/l、或0g/l至0.5g/l、或0g/l至0.3g/l、或0g/l至0.2g/l的低聚糖前体。
以干重计,根据本发明的组合物可包含0g至2.1g的低聚糖前体/100g组合物,例如以干重计,0g至1.5g、或0g至0.8g、或0g至0.15g的低聚糖前体/100g组合物。
益生菌
本发明的营养组合物可还包含至少一种益生菌(或益生菌菌株),诸如益生细菌菌株。
最常用的益生微生物主要是以下属的细菌和酵母:乳酸杆菌属菌种(lactobacillusspp.)、链球菌属菌种(streptococcusspp.)、肠球菌属菌种(enterococcusspp.)、双歧杆菌属菌种(bifidobacteriumspp.)和酵母属菌种(saccharomycesspp.)。
在一些具体实施方案中,益生菌为益生细菌菌株。在一些具体实施方案中,其具体为双歧杆菌和/或乳酸杆菌。
合适的益生细菌菌株包括得自芬兰瓦利奥公司(valiooy,finland)的商标为lgg的鼠李糖乳杆菌(lactobacillusrhamnosus)atcc53103;鼠李糖乳杆菌(lactobacillusrhamnosus)cgmcc1.3724、类干酪乳杆菌(lactobacillusparacasei)cncmi-2116、约氏乳杆菌(lactobacillusjohnsonii)cncmi-1225、新西兰blis科技有限公司(blistechnologieslimited,newzealand)以商品名ki2销售的唾液链球菌(streptococcussalivarius)dsm13084、丹麦科汉森公司(christianhansencompany,denmark)以商标bb12特别销售的乳酸双歧杆菌(bifidobacteriumlactis)cncm1-3446、日本森永乳业株式会社(morinagamilkindustryco.ltd.,japan)以商标bb536销售的长双歧杆菌(bifidobacteriumlongum)atccbaa-999、丹尼斯克公司(danisco)以商标bb-03销售的短双岐杆菌(bifidobacteriumbreve)、森永(morinaga)以商标m-16v销售的短双岐杆菌(bifidobacteriumbreve)、宝洁公司(procter&gambieco.)以商标bifantis销售的婴儿双歧杆菌(bifidobacteriuminfantis),以及加拿大rosell生物研究所(institutrosell-lallemand)以商标r0070销售的短双岐杆菌(bifidobacteriumbreve)。
在一个具体实施方案中,益生菌是乳酸双歧杆菌(bifidobacteriumlactis),诸如乳酸双歧杆菌cncm1-3446。
以干重计,根据本发明的营养组合物可包含每g组合物10e3至10e12cfu的益生菌菌株,更优选地10e7至10e12cfu(诸如,10e8至10e10cfu)的益生菌菌株。
在一个实施方案中,益生菌是活的。在另一个实施方案中,益生菌是非复制的或失活的。在一些其它实施方案中,可同时存在活的益生菌和失活的益生菌。
本发明的营养组合物可还包含至少一种噬菌体(细菌噬菌体)或噬菌体的混合物,这些噬菌体优选地针对病原性链球菌、嗜血杆菌(haemophilus)、莫拉氏菌(moraxella)和葡萄球菌(staphylococci)。
根据本发明的营养组合物可为例如婴儿配方食品、1段婴儿配方食品、较大或2段婴儿配方食品、早产儿配方食品、婴孩食物、婴儿谷物组合物、强化剂(诸如,人乳强化剂)或补充剂。在一些具体实施方案中,本发明的组合物为旨在用于4月龄或6月龄婴儿的婴儿配方食品、强化剂或补充剂。在一个优选的实施方案中,本发明的营养组合物是婴儿配方食品。
在一些其它实施方案中,本发明的营养组合物是强化剂。强化剂可为母乳强化剂(例如,人乳强化剂)或配方食品强化剂(诸如婴儿配方食品强化剂或较大/2段婴儿配方食品强化剂)。
当营养组合物是补充剂时,其可以单位剂量的形式提供。
本发明的营养组合物可为固体(例如粉末)、液体或凝胶形式。
蛋白质
根据本发明的营养组合物通常含有蛋白质源。蛋白质的量可为1.6g至3g/100kcal。在一些实施方案中,特别是当组合物旨在用于早产儿时,蛋白质的量可为2.4g/100kcal至4g/100kcal或高于3.6g/100kcal。在一些其它实施方案中,蛋白质的量可低于2.1g/100kcal,例如1.8g/100kcal至2.1g/100kcal、或1.8g/100kcal至2g/100kcal、或1.9g/100kcal至2.1g/100kcal之间,或者量低于1.8g/100kcal,诸如1.4g/100kcal-1.8g/100kcal或1.5g/100kcal-1.7g/100kcal。
只要满足必需氨基酸含量的最低要求并确保令人满意的生长,蛋白质的类型被认为对本发明无关紧要。因此,可使用基于乳清、酪蛋白以及它们的混合物的蛋白质源,也可使用基于大豆的蛋白质源。就所关注的乳清蛋白而言,蛋白质源可基于酸乳清或甜乳清或它们的混合物,并且可包含任何所需比例的α-乳白蛋白和β-乳球蛋白。
“α-乳白蛋白”是指高质量、易消化的乳清蛋白,其占总人类母乳(hbm)蛋白质的20%-25%并且是hbm中存在的主要蛋白质。α-乳白蛋白的结构由123个氨基酸和4个二硫键组成,并且该蛋白质具有14.2k道尔顿的分子量。由于α-乳白蛋白具有高含量的必需氨基酸(具体地色氨酸),所以它是低蛋白婴儿配方食品的理想选择。在一个实施方案中,本发明的营养组合物以约0.2g/100kcal至约0.4g/100kcal的营养组合物的量,或以至少1.7g/l、或至少2.0g/l、或至少2.3g/l、或至少2.6g/l的营养组合物的量包含α-乳白蛋白。
在一些有利的实施方案中,蛋白质源以乳清为主(即多于50%的蛋白质来自乳清蛋白,诸如60%或70%)。
该蛋白质可为完整的或水解的,或为完整蛋白质和水解蛋白质的混合物。所谓的术语“完整的”是指蛋白质的主要部分是完整的,即分子结构未发生改变,例如至少80%的蛋白质未发生改变,诸如至少85%的蛋白质未发生改变,优选地,至少90%的蛋白质未发生改变,甚至更优选地,至少95%的蛋白质未发生改变,诸如至少98%的蛋白质未发生改变。在一个具体实施方案中,100%的蛋白质未发生改变。
术语“水解的”是指在本发明的上下文中,蛋白质已被水解或分解成其组成氨基酸。该蛋白质可以是完全(即,广泛)水解或部分水解的。例如,对于被认为处于发生牛乳变应性风险的婴儿或幼儿而言,提供部分水解的蛋白质(水解程度为2%至20%)可能是可取的。如果需要水解的蛋白质,则可根据需要并且如本领域已知的那样进行水解过程。例如,可通过在一个或多个步骤中对乳清级分进行酶法水解来制备乳清蛋白水解产物。如果用作原料的乳清级分基本上不含乳糖,则发现该蛋白质在水解过程期间经受少得多的赖氨酸封闭(lysineblockage)。这使得能够将赖氨酸封闭的程度从约15重量%的总赖氨酸降低至小于约10重量%的赖氨酸;例如约7重量%的赖氨酸,这大大地改善蛋白质源的营养质量。
在本发明的一个实施方案中,至少70%的蛋白质被水解,优选地,至少80%的蛋白质被水解,诸如至少85%的蛋白质被水解,甚至更优选地,至少90%的蛋白质被水解,诸如至少95%的蛋白质被水解,特别地至少98%的蛋白质被水解。在一个具体实施方案中,100%的蛋白质被水解。
在一个具体实施方案中,营养组合物的蛋白质是水解的、完全水解的或部分水解的。蛋白质的水解程度(dh)可为8至40、或20至60、或20至80,或大于10、20、40、60、80或90。
在一个具体实施方案中,根据本发明的营养组合物是低变应原性的组合物。在另一个具体实施方案中,根据本发明的组合物是低变应原性的营养组合物。
根据本发明的营养组合物通常含有碳水化合物源。这在本发明的营养组合物为婴儿配方食品的情况下是特别优选的。在这种情况下,可使用通常存在于婴儿配方食品中的任何碳水化合物源,诸如乳糖、蔗糖(sucrose)、糖精(saccharose)、麦芽糖糊精、淀粉以及它们的混合物,但是优选的碳水化合物源之一是乳糖。
脂质
根据本发明的营养组合物通常包含脂质源。这在本发明的营养组合物为婴儿配方食品的情况下是特别相关的。在这种情况下,脂质源可以是适合用于婴儿配方食品中的任何脂质或脂肪。一些合适的脂肪源包括棕榈油、高油酸葵花油和高油酸红花油。也可加入必需脂肪酸亚油酸和α-亚麻酸,以及少量包含大量预先形成的花生四烯酸和二十二碳六烯酸的油,诸如鱼油或微生物油。脂肪源中n-6脂肪酸与n-3脂肪酸的比率可为约5:1至约15:1,例如约8:1至约10:1。
在一个实施方案中,本发明的营养组合物包含具有高sn-2棕榈酸酯的甘油三酯,优选地为在sn-2位具有超过33%的棕榈酸的甘油三酯。
在一个实施方案中,本发明的营养组合物包含约5g/100kcal或6g/100kcal的脂肪,并且例如至少约7.5重量%的该脂肪,例如约7.5%-12.0%的由sn-2位中的棕榈酸组成。
在本发明的一个实施方案中,该组合物包含至少7.5%、优选地8%、更优选地至少9.6%的脂肪,该脂肪是sn-2棕榈酸酯,例如约7.8%至11.8%、约8.0重量%至11.5重量%、约8.5至11.0%或约9.0至10.0重量%的脂肪在甘油三酯的sn-2位为棕榈酸。
在一些实施方案中,按重量计,棕榈酸占配方食品的总脂肪酸含量的约15%至约25%,诸如约15%至约20%,并且至少约30%、例如约35%至约43%的总棕榈酸含量处于sn-2位。
由脂类营养公司(lipidnutrition)出售的可商购获得的组合物是betapoltmb-55,其为来源于植物油的甘油三酯混合物,其中至少54%的棕榈酸处于甘油分子的sn-2位。在一个实施方案中,本发明的营养组合物包含的脂肪含量按重量计为约40%至50%的betapoltmb-55,例如约43重量%至约45重量%。本领域技术人员将会理解,在不脱离本发明的实质和范围的情况下,配方食品中所使用的高sn-2脂肪的百分比以及sn-2棕榈酸酯的总量可以有所变化,并且可使用不同的高sn-2棕榈酸酯油。
维生素和矿物质
本发明的营养组合物可还包含被认为是日常饮食所必需的所有维生素和矿物质,这些维生素和矿物质以营养显著量存在于营养组合物中。已确定某些维生素和矿物质的最低需求量。矿物质、维生素和任选地存在于本发明组合物中的其它营养物质的示例包括维生素a、维生素b1、维生素b2、维生素b6、维生素b12、维生素e、维生素k、维生素c、维生素d、叶酸、肌醇、烟酸、生物素、泛酸、胆碱、钙、磷、碘、铁、镁、铜、锌、锰、氯、钾、钠、硒、铬、钼、牛磺酸和左旋肉碱。矿物质通常以盐的形式添加。特定矿物质和其它维生素的存在和量将根据适用人群而有所不同。
如有必要,本发明的营养组合物可包含乳化剂和稳定剂,诸如大豆、卵磷脂、柠檬酸甘油单酯和柠檬酸甘油二酯等。
本发明的营养组合物可还包含可能具有有益效果的其它物质,诸如乳铁蛋白、核苷酸、核苷等。
本发明的营养组合物可还包含类胡萝卜素。在本发明的一些具体实施方案中,本发明的营养组合物不包含任何类胡萝卜素。
根据本发明的营养组合物可通过任何合适的方式制备。现将以举例的方式描述组合物。
例如,可通过将蛋白质源、碳水化合物源和脂肪源以适当的比例共混在一起来制备配方食品诸如婴儿配方食品。如果使用乳化剂,则可在此时加入。可在此时加入维生素和矿物质,但其通常在稍后加入以避免热降解。在共混之前,可先将任何亲脂性维生素、乳化剂等溶解于脂肪源中。然后可混入水(优选地经受反渗透的水),以形成液体混合物。合适的水温便利地在约50℃至约80℃的范围内以有助于分散成分。可使用可商购获得的液化剂来形成液体混合物。
尤其是如果最终产物是液体形式,则可在此阶段加入岩藻糖基化低聚糖和n-乙酰化低聚糖。如果最终产物为粉末,可根据需要同样在此阶段加入这些成分。
然后,例如以两个阶段对液体混合物进行均质化。
然后,可对液体混合物进行热处理以减少细菌载量,例如通过将液体混合物快速加热到约80℃至约150℃范围内的温度并且持续约5秒至约5分钟的持续时间。这可通过蒸汽注入、高压灭菌器或热交换器(例如,板式热交换器)来进行。
然后,例如通过急速冷却将液体混合物冷却到约60℃至约85℃。然后再次例如以两个阶段对液体混合物进行均质化,其中第一阶段的压力为约10mpa至约30mpa,第二阶段的压力为约2mpa至约10mpa。然后可将均质化的混合物进一步冷却,以便添加任何热敏组分,诸如维生素和矿物质。此时便利地调节均质化的混合物的ph和固体含量。
如果最终产物将为粉末,则将该均质化的混合物转移至合适的干燥装置,诸如喷雾干燥器或冷冻干燥器,然后将其转化为粉末。该粉末的含水量应小于约5重量%。还可以或作为替代在此阶段加入岩藻糖基化低聚糖和n-乙酰化低聚糖,方法是通过将其与益生菌菌株(如果使用)干混,或通过以晶体的糖浆形式与益生菌菌株共混,然后对混合物进行喷雾干燥或冷冻干燥。
如果优选液体组合物,可对该均质化的混合物进行杀菌,然后在无菌条件下将其装入合适的容器中,也可以先将其装入容器中,再进行灭菌。
在另一个实施方案中,本发明的组合物可为补充剂。
补充剂可以是例如片剂、胶囊、锭剂或液体的形式。补充剂可还含有保护性亲水胶体(诸如胶类、蛋白质、改性淀粉)、粘结剂、成膜剂、包囊剂/材料、壁/壳材料、基质化合物、包衣、乳化剂、表面活性剂、增溶剂(油类、脂肪类、蜡类、卵磷脂类等)、吸附剂、载体、填充剂、共化合物、分散剂、润湿剂、加工助剂(溶剂)、流动剂、掩味剂、增重剂、胶凝剂和凝胶形成剂。补充剂可还含有常规的药物添加剂和佐剂、赋形剂和稀释剂,包括但不限于:水、任何来源的明胶、植物胶、木素磺酸盐、滑石、糖类、淀粉、阿拉伯树胶、植物油、聚亚烷基二醇、风味剂、防腐剂、稳定剂、乳化剂、缓冲剂、润滑剂、着色剂、润湿剂、填充剂等。
另外,补充剂可包含适用于口服或非肠道施用的有机或无机载体材料,以及维生素、矿物质微量元素和根据政府机构(诸如usrda)推荐的其它微量营养素。
婴儿或幼儿
根据本发明的营养组合物用于婴儿或幼儿。该营养组合物特别适于6月龄以下的婴儿。
婴儿或幼儿可为足月儿或早产儿。在一个具体实施方案中,本发明的营养组合物用于早产婴儿或幼儿。在一个具体实施方案中,本发明的营养组合物用于早产婴儿。
在一个实施方案中,本发明的营养组合物可还用于小于胎龄出生或出生体重低的婴儿或幼儿。
低出生体重的婴儿或幼儿可能是或可能不是早产儿,类似地,小于胎龄的婴儿或幼儿可能是或可能不是早产儿。
本发明的营养组合物可还用于剖腹产或经阴道分娩的婴儿或幼儿。
所有婴儿和幼儿都可从本发明受益,因为他们全都或可能在某个年龄时易受感染的影响。
在本发明的一些有利的实施方案中,营养组合物用于具有脆弱免疫系统的婴儿或幼儿,诸如早产婴儿、剖腹产出生的婴儿、小于胎龄出生或具有低出生体重的婴儿、住院的婴儿/幼儿、和/或接受或曾接受抗生素治疗的婴儿/幼儿、和/或患有或曾患有肠道感染和/或肠道炎症的婴儿/幼儿。的确可以预见的是,本发明的组合物对于出生时具有可能受损的免疫系统的婴儿或虚弱的婴儿/幼儿(诸如过早出生的婴儿和/或剖腹产出生的婴儿)可能甚至更有益。另外可以预见的是,本发明的组合物对于特别是在出生后,例如在出生后前4周期间表现出肠道疾病(诸如腹泻、感染或绞痛)的婴儿/幼儿可能甚至更有益。
在本发明的实施方案中,本发明的组合物针对的是过早出生、或剖腹产出生、或小于胎龄出生或具有低出生体重、或患有或曾患有肠道感染和/或肠道炎症的婴儿,特别是当婴儿为0至6月龄时。不受理论约束,据信年幼的婴儿从本发明的组合物中受益甚至更多,特别是当婴儿具有虚弱的健康状况时(或存在相关风险时)(如上文引用的状况所例示)。
在一些实施方案中,根据本发明的组合物可用于离乳期前和/或离乳期过程中。
在一个实施方案中,婴儿或幼儿是0至36月龄,诸如0至12月龄或0至6月龄。可以预见的是,本发明的组合物对于刚出生(0至4周或0至8周)的婴儿可能甚至更有利,因为它们的免疫系统可能更脆弱。
营养组合物的施用(提供或喂养)年龄和持续时间可根据需要而确定。本发明的营养组合物可用于以下预防或治疗目的:
-通过促进群落类型b和/或减少群落类型c来减少婴儿或幼儿发烧;
-减少对婴儿或幼儿使用抗生素(在施用组合物期间和/或在施用期之后);
-减少对婴儿或幼儿使用退热剂;和/或
-预防和/或治疗婴儿或幼儿的与发烧和/或抗生素的施用或退热剂的施用相关的疾病/病症;
-促进群落类型b和/或减少群落类型c,从而预防和/或治疗感染。
在一些具体实施方案中,营养组合物可以是婴儿配方食品,并且可以特别用于主要用婴儿配方食品喂养的0至12月龄的婴儿。在一些实施方案中,营养组合物用于预防目的。营养组合物可例如在婴儿出生后立即提供。本发明的组合物可还在婴儿出生后头1周期间、或在出生后头2周期间、或在出生后头3周期间、或在出生后头1个月期间、或在出生后头2个月期间、或在出生后头3个月期间、或在出生后头4个月期间、或在出生后头6个月期间、或出生后头8个月期间、或在出生后头10个月期间、或在出生后头1年期间、或在出生后头2年期间、或甚至更长时间内给予。在本发明的一些特别有利的实施方案中,营养组合物在婴儿出生后前4个月或6个月提供(或施用)给所述婴儿。
在一些其它实施方案中,本发明的营养组合物在出生后几天(例如,1天、2天、3天、5天、10天、15天、20天……)、或几周(例如,1周、2周、3周、4周、5周、6周、7周、8周、9周、10周……)或几个月(例如,1个月、2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月……)给予。这可以尤其指婴儿是早产儿的情况,但这并不是必需的。
本发明的营养组合物可根据需要给予数天(1天、2天、3天、4天、5天、6天……)、或数周(1周、2周、3周、4周、5周、6周、7周、8周或甚至更多周)、或数月(1个月、2个月、3个月、4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月或甚至更多个月)。
在一个实施方案中,将本发明的组合物作为母乳的补充组合物提供给婴儿或幼儿。在一些实施方案中,婴儿或幼儿在至少前2周、或前1、2、4或6个月接受母乳喂养。在一个实施方案中,本发明的营养组合物在用母乳提供营养的这段时间之后提供给婴儿或幼儿,或者在用母乳提供营养的这段时间内与母乳一起提供给婴儿或幼儿。在另一个实施方案中,在至少一段时间内(例如,在生命的前1、2、或4个月后),在至少1、2、4或6个月期间,将该组合物作为唯一或主要的营养组合物提供给婴儿或幼儿。
在一个实施方案中,本发明的营养组合物是完全营养组合物(满足个体全部或大部分营养需求)。在另一个实施方案中,营养组合物是旨在用于例如补充人乳或者补充婴儿配方食品或较大/2段婴儿配方食品的补充剂或强化剂。
在一些其它实施方案中,提供根据本发明的营养组合物用于治疗目的。用于治疗感染或促进群落类型b和/或减少群落c的情况将更多。
在这些情况下,可根据需要提供营养组合物数天(1、2、3、4、5、6天……)、或数周(1、2、3、4、5、6、7、8周或甚至更多周)、或数月(1、2、3、4、5、6、7、8、9、10、11个月或甚至更多个月)。一旦症状出现或一旦诊断出这些健康疾病/病症,即可提供该组合物。可在所治疗疾病/病症的症状消失后,或在所述消失之后若干天/周/月,停止提供该组合物。
本发明人也已发现,根据本发明的具体营养组合物能特别有效地在婴儿或幼儿中减轻发烧以及减少抗生素的使用和退热剂的使用(即,施用)。
根据本发明的营养组合物因此也可用于在婴儿或幼儿中减轻发烧和/或促进群落类型b和/或减少群落类型c,从而减少抗生素的使用和退热剂的使用。
在一个具体方面,本发明还涉及包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物,其用于在婴儿或幼儿的肠道中促进或增加群落类型b和/或减少群落类型c,从而减轻婴儿或幼儿的发烧和/或减少抗生素的使用和/或减少退热剂的使用,其中
-岩藻糖基化低聚糖的总量为0.75g-1.65g/l组合物和/或以干重计总量为0.52g-1.15g/100g组合物;以及
-n-乙酰化低聚糖的总量为0.45g-0.85g/l组合物和/或以干重计总量为0.31g-0.59g/100g组合物。
此前提及的实施方案和实施例(例如,涉及低聚糖的类型和量、营养组合物、施用、目标人群……)也适用于该方面。
在另一个具体方面,本发明还涉及包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物,其用于在婴儿或幼儿的肠道中促进或增加群落类型a和/或减少群落类型b,从而预防和/或治疗与婴儿或幼儿的发烧和/或抗生素的施用或退热剂的施用相关的疾病/病症(例如,感染、炎症……),其中
-岩藻糖基化低聚糖的总量为0.75g-1.65g/l组合物和/或以干重计总量为0.52g-1.15g/100g组合物;以及
-n-乙酰化低聚糖的总量为0.45g-0.85g/l组合物和/或以干重计总量为0.31g-0.59g/100g组合物。
此前提及的实施方案和实施例(例如,涉及低聚糖的类型和量、营养组合物、施用、目标人群……)也适用于该方面。
健康有益效果讨论
本发明的营养组合物对婴儿或幼儿具有保护和/或预防效果:与主要或完全用不包含所述低聚糖(即,不包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖)的常规营养组合物喂养的婴儿或幼儿的肠道中的相应群落相比,该营养组合物在用本发明的营养组合物喂养的婴儿或幼儿的肠道中促进和/或诱导群落类型b并且减少群落类型c。
本发明的营养组合物的主要和令人惊讶的健康有益效果是它降低了针对婴儿和幼儿的抗生素处方量。这是由于微生物群的特定分类群发生变化。
在一个具体方面,本发明还涉及用于预防和/或治疗婴儿或幼儿感染的营养组合物。
感染是指病理感染,即通常不是指细菌的肠道定殖,而是婴儿或幼儿由于感染而生病的情况。通常,这将导致婴儿或幼儿发烧和/或腹泻、咳嗽或其它症状。对于病理感染,医生可开抗生素处方。
由本发明的组合物提供的有益健康益处可以是短期和/或长期效果。
该效果可在施用本发明的组合物后立即出现,或者日后出现,即在组合物的施用之后,例如所述施用后1周至数月,例如2周至4周、2至6周、2至8周、1个月至6个月,或2个月至12个月。
其它目的:
本发明的另一个目的是至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖在制备营养组合物方面的用途,与主要或完全用不包含所述低聚糖的常规营养组合物喂养的婴儿或幼儿的肠道中的那些群落相比,其用于在婴儿或幼儿中促进群落类型b和/或减少群落类型c。
本发明的另一个目的是根据本发明的营养组合物的用途,其用于在婴儿或幼儿中促进群落类型b和/或减少群落类型c,从而防止和/或治疗婴儿或幼儿感染。
本发明的另一个具体目的涉及包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物,其用于在婴儿或幼儿中促进群落类型b和/或减少群落类型c,从而预防和/或治疗与婴儿或幼儿发烧和/或抗生素的施用或退热剂的施用相关的疾病/病症(例如,感染、炎症……),其中
-岩藻糖基化低聚糖的总量为0.75g-1.65g/l组合物和/或以干重计总量为0.52g-1.15g/100g组合物;以及
-n-乙酰化低聚糖的总量为0.45g-0.85g/l组合物和/或以干重计总量为0.31g-0.59g/100g组合物。
此前提及的实施方案和实施例(例如,涉及低聚糖的类型和量、营养组合物、施用、目标人群等)也适用于该方面。
本发明的另一个目的是包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的药物组合物,与主要或完全用不包含所述低聚糖的常规营养组合物喂养的婴儿或幼儿的肠道中的那些群落相比,该组合物用于在婴儿或幼儿中促进群落类型b和/或减少群落类型c。
该药物组合物可用于预防和/或治疗婴儿或幼儿的感染。
本发明的另一个目的是与主要或完全用不包含所述低聚糖的常规营养组合物喂养的婴儿或幼儿的肠道中的整体群落相比,用于在婴儿或幼儿的肠道内促进群落类型b和/或减少群落类型c的方法,所述方法包括向所述婴儿或幼儿施用包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物。
本发明的另一个目的是用于预防和/或治疗婴儿或幼儿感染的方法,所述方法包括向所述婴儿或幼儿施用包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物。
此前提及的实施方案和示例(例如,涉及低聚糖的类型和量、营养组合物、施用、目标群体……)也适用于这些各种目的(即,用途、药物组合物、方法……)。
应当注意,在本发明的其中一个方面的上下文中描述的实施方案和特征也适用于本发明的其它方面。
本申请所引用的所有专利和非专利参考文献均据此全文以引用方式并入。
现将在下面的非限制性实施例中进一步详细描述本发明。
实施方案
本发明可在以下实施方案中进行描述;这些实施方案中的每一个可与上述实施方案组合:
1.营养组合物,所述营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其用于通过在婴儿或幼儿中促进群落类型b和/或减少群落类型c来预防和/或治疗感染,其中与主要或完全用不包含所述低聚糖的常规营养组合物喂养的婴儿或幼儿的肠道中的微生物群相比,所述促进包括上调双歧杆菌群体并且所述减少包括下调埃希氏杆菌属和/或消化链球菌科群体。
2.根据实施方案1所述的营养组合物,其中所述用途是预防和/或治疗日后的感染。
3.根据前述实施方案中任一项所述使用的营养组合物,其中所述岩藻糖基化低聚糖选自这样的岩藻糖基化低聚糖,该岩藻糖基化低聚糖选自由以下项组成的列表:2'-岩藻糖基乳糖、3'-岩藻糖基乳糖、二岩藻糖基乳糖、乳糖-n-岩藻戊糖i、乳糖-n-岩藻戊糖ii、乳糖-n-岩藻戊糖iii、乳糖-n-岩藻戊糖v、乳糖-n-岩藻己糖、乳糖-n-二岩藻己糖i、岩藻糖基乳糖-n-己糖、岩藻糖基乳糖-n-新己糖i、岩藻糖基乳糖-n-新己糖ii、二岩藻糖基乳糖-n-己糖i、二岩藻糖基乳糖-n-新己糖i、二岩藻糖基乳糖-n-新己糖ii、岩藻糖基-对-乳糖-n-己糖以及它们的任意组合。
4.根据实施方案1所述的营养组合物,其中所述用途是预防和/或治疗日后的感染。
5.根据前述实施方案中任一项所述使用的营养组合物,其中所述岩藻糖基化低聚糖的总量为0.2g-2.2g/l组合物和/或以干重计总量为0.15g-1.75g/100g组合物;并且所述n-乙酰化低聚糖的总量为0.05g-0.85g/l组合物和/或以干重计总量为0.04g-0.59g/100g组合物。
6.根据前述实施方案中任一项所述的营养组合物,其中所述岩藻糖基化低聚糖包含2’-岩藻糖基表位。
7.根据前述实施方案中任一项所述的营养组合物,其中所述岩藻糖基化低聚糖为2’-岩藻糖基乳糖(2’fl)。
8.根据前述实施方案中任一项所述的营养组合物,其中所述n-乙酰化低聚糖为乳糖-n-四糖(lnt)、乳糖-n-新四糖(lnnt)或它们的任意组合。
9.根据前述实施方案中任一项所述的营养组合物,其中所述n-乙酰化低聚糖为乳糖-n-新四糖(lnnt)、对-乳糖-n-新己糖(对-lnnh)或它们的任意组合,优选地其中所述n-乙酰化低聚糖为乳糖-n-新四糖(lnnt)。
10.根据前述实施方案中任一项所述的营养组合物,其包含2'-岩藻糖基乳糖和乳糖-n-新四糖(lnnt),或者包含由2'-岩藻糖基乳糖(2’fl)和乳糖-n-新四糖(lnnt)组成的低聚糖混合物。
11.根据前述实施方案中任一项所述的营养组合物,其中所述岩藻糖基化低聚糖的总量为0.8g-1.5g/l组合物和/或以干重计总量为0.62g-1.16g/100g组合物;和/或所述n-乙酰化低聚糖的总量为0.5g-0.8g/l组合物和/或以干重计总量为0.39g-0.62g/100g组合物。
12.根据前述实施方案中任一项所述的营养组合物,其包含选自包括以下项的列表的至少一种另外的低聚糖和/或纤维和/或其前体:低聚半乳糖(gos)、低聚果糖(fos)、低聚木糖(xos)、菊粉、聚葡萄糖、唾液酸化低聚糖、唾液酸、岩藻糖以及它们的任意组合。
13.根据前述实施方案中任一项所述的营养组合物,所述组合物还包含至少一种益生菌,所述益生菌的量为103cfu至1012cfu/g所述组合物(干重)。
14.根据前述实施方案中任一项所述的营养组合物,其中所述营养组合物为婴儿配方食品、1段婴儿配方食品、较大或2段婴儿配方食品、早产儿配方食品、婴孩食物、婴儿谷物组合物、强化剂或补充剂。
15.根据前述实施方案中任一项所述的营养组合物,其用于6月龄以下婴儿。
16.根据前述实施方案中任一项所述的营养组合物,其中所述婴儿或幼儿选自早产婴儿、剖腹产出生的婴儿、小于胎龄出生或具有低出生体重的婴儿、住院的婴儿/幼儿、接受或曾接受抗生素治疗的婴儿/幼儿和/或患有或曾患有肠道感染和/或肠道炎症的婴儿/幼儿。
17.根据前述实施方案中任一项所述的营养组合物,其用于在婴儿或幼儿中减轻发烧和/或减少抗生素的使用和/或减少退热剂的使用。
18.营养组合物,所述营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其用于在婴儿或幼儿中减轻发烧和/或减少退热剂的施用,其中岩藻糖基化低聚糖的总量为0.2g-2.2g/l组合物和/或以干重计总量为0.15g-1.75g/100g组合物;并且n-乙酰化低聚糖的总量为0.05g-0.85g/l组合物和/或以干重计总量为0.04g-0.59g/100g组合物。
19.营养组合物,所述营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其用于减少婴儿或幼儿中的抗生素的施用,其中岩藻糖基化低聚糖的总量为0.2g-2.2g/l组合物和/或以干重计总量为0.15g-1.75g/100g组合物;并且n-乙酰化低聚糖的总量为0.05g-0.85g/l组合物和/或以干重计总量为0.04g-0.59g/100g组合物。
20.营养组合物,所述营养组合物包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖,其用于预防和/或治疗与婴儿或幼儿的发烧和/或抗生素的施用和/或退热剂的施用相关的疾病/病症,其中岩藻糖基化低聚糖的总量为0.2g-2.2g/l组合物和/或以干重计总量为0.15g-1.75g/100g组合物;并且n-乙酰化低聚糖的总量为0.05g-0.85g/l组合物和/或以干重计总量为0.04g-0.59g/100g组合物。
21.包含至少一种岩藻糖基化低聚糖和至少一种n-乙酰化低聚糖的营养组合物在婴儿或幼儿中用于减轻发烧和/或用于减少抗生素的施用和/或退热剂的施用的用途,其中岩藻糖基化低聚糖的总量为0.2g-2.2g/l组合物和/或以干重计总量为0.15g-1.75g/100g组合物;并且n-乙酰化低聚糖的总量为0.05g-0.85g/l组合物和/或以干重计总量为0.04g-0.59g/100g组合物。
22.通过提供根据前述实施方案1至20中任一项所述的营养组合物来预防和/或治疗婴儿或幼儿感染的方法。
实施例
背景和目的:hmo可通过形成肠道微生物群的发育来部分地向婴儿提供健康有益效果。我们探讨了粪便微生物群与用补充有2种hmo的配方食品喂养的婴儿的报告发病率和药物使用的关系。
实施例1
下表1给出了根据本发明的营养组合物(例如,婴儿配方食品)的组成的示例。该组成仅以举例的方式给出。
表1:营养组合物(例如,婴儿配方食品)的组成的示例
实施例2
临床研究说明
在意大利巴勒莫的aoup“paologiaccone”的母婴科、新生儿科和新生儿重症监护室(dipartimentomaternoinfantile,unitàoperativacomplessadineonatologiaeterapiaintensivaneonatale)以及比利时哈瑟尔特的幼儿科(kinderartsenpraktijk)进行了安全性试验。
该研究是2个并行配方食品喂养组的随机、对照、双中心介入临床试验。配方食品喂养组的研究人群包括健康的足月的男性和女性婴儿,入选时只有0到14天,这些婴儿在入选时只用配方食品喂养。符合条件的婴儿被随机分配到两种研究配方食品(对照或测试)中的一个,使用分娩方法(顺产或剖腹产)和性别作为分层因素。对于第1阶段,随机的婴儿从入选至4月龄以适合于其体重、年龄和食欲的量接受测试或对照配方食品的排他性喂养。父母/护理人员、调查人员、研究支持人员和临床项目经理对研究配方食品的种类不知情。
用于研究中的婴儿配方食品如下:
·将对照配方食品给予对照组:其为含有lc-pufa且不含益生菌的标准乳清为主的1段婴儿配方食品(66.9kcal/100ml重构配方食品、乳清:酪蛋白比率为71.6%:28.4%的1.889g蛋白/100kcal粉末,详细组成参见表2)。
·将测试配方食品给予测试组:其为对照配方食品,不同之处在于一部分乳糖已以下面的量替换为2种hmo(2fl和lnnt):每升重构配方食品0.5g-0.6glnnt和1.0g-1.2g2’fl(详细组成参见表2)。
作为参照组(母乳喂养组=bf组),招募至少3个月完全母乳喂养的婴儿以便在3月龄时进行粪便取样。
表2:对照配方食品和测试配方食品的组成
在3月龄时使用不同技术来对每个组的粪便微生物群进行评估,参见表3。
表3:样本概览
表3给出了样本的概述。意向治疗组(itt)、符合方案组(pp)的婴儿数量和可从符合方案组或母乳喂养参照组获得的粪便样本数量,用于通过整体16srdna测序进行微生物群分析。
材料和方法
粪便收集
所有个体的父母在为期3个月的访视前48小时内在家收集粪便样本。为此,向父母提供了试剂盒(隔离袋、冰袋、刮刀罐、可密封的塑料袋、说明书)。要求父母收集2个样本,将样本储存在家中-20℃的冰箱内,并且将包含冷冻冰袋的隔离袋内的粪便样本运送到访视地点,在此将样本在-80℃下冷冻保存。然后将样本置于干冰上运输到瑞士的雀巢研究中心(nestleresearchcenter,switzerland),并冷冻保存在-80℃下直到分析。
排泄物dna提取
遵循制造商的说明书使用qiaampdna粪便小提试剂盒(凯杰公司(qiagen))来提取总dna,不同之处在于增加了使用fastprep装置和lysingmatrixb管(mp生化公司(mpbiochemicals))进行的一系列机械破碎步骤(11×45s)(junick和blaut,2012年,quantificationofhumanfecalbifidobacteriumspeciesbyuseofquantitativereal-timepcranalysistargetingthegroelgene.applenvironmicrobiol78:2613-2622(通过使用靶向groel基因的定量实时pcr分析来定量人粪便双歧杆菌物种,《应用环境微生物学》,第78卷,第2613-2622页))。
16s基因的扩增以及测序
然后,使用通用引物对16s可变区v3至v4进行pcr扩增(klindworth等人,2013年,evaluationofgeneral16sribosomalrnagenepcrprimersforclassicalandnext-generationsequencing-baseddiversitystudies.nucleicacidsres41:e1(用于基于传统和下一代测序的多样性研究的通用16s核糖体rna基因pcr引物的评估,《核酸研究》,第41卷,第e1页)),并且用此前所述的illuminamiseq技术来进行测序(caporaso等人,2012年,ultra-high-throughputmicrobialcommunityanalysisontheilluminahiseqandmiseqplatforms.ismej6:1621-1624(在illuminahiseq和miseq平台上的超高通量微生物群落分析,《国际微生物生态学会会刊》,第6卷,第1621-1624页))。
16s数据分析
在质量过滤之后,6’710’039个序列描述了符合方案(pp)组的154个样本的微生物群(参见表3),平均覆盖率为每个样本有42’739个序列归入173个otu中。从16srdna分析中排除了具有少于10’000个序列的三个样本。
综合使用mothur(schloss等人,2009年,introducingmothur:open-source,platform-independent,community-supportedsoftwarefordescribingandcomparingmicrobialcommunities.applenvironmicrobiol75:7537-7541(mothur介绍:用于描述和比较微生物群落的开源、独立于平台、群落支持的软件,《应用环境微生物学》,第75卷,第7537-7541页))和qiime(caporaso等人,2010年,qiimeallowsanalysisofhigh-throughputcommunitysequencingdata.natmethods7:335-336(qiime允许分析高通量群落测序数据,《自然方法》,第7卷,第335-336页))软件包来分析原始序列数据。按照所述的方式对末端配对的序列进行去多重化和连接(kozich等人,2013年,developmentofadual-indexsequencingstrategyandcurationpipelineforanalyzingampliconsequencedataonthemiseqilluminasequencingplatform.applenvironmicrobiol79:5112-5120(开发用于在miseqillumina测序平台上分析扩增序列数据的双指数测序策略和管理管道,《应用环境微生物学》,第79卷,第5112-5120页))。然后,使用mothur命令[deunique.seqs()、degap.seqs()和split.groups()]对于每个样本将序列分割为单独的fasta文件。在qiime中使用add_qiime_labels.py执行向qiime格式的转换并执行后续的分析步骤。使用uchime通过pick_open_reference.py以97%同一性执行嵌合体检查和otu拾取(edgar等人,2011年,uchimeimprovessensitivityandspeedofchimeradetection.bioinformatics27:2194-2200(uchime提高嵌合体检测的灵敏度和速度,《生物信息学》,第27卷,第2194-2200页))。使用rdp分类器以0.6的置信度阈值对代表性序列进行分类学分配(wang等人,2007年,naivebayesianclassifierforrapidassignmentofrrnasequencesintothenewbacterialtaxonomy.applenvironmicrobiol73:5261-5267(用于将rrna序列快速分配到新细菌分类的朴素贝叶斯分类器),《应用环境微生物学》,第73卷,第5261-5267页))。使用pynast方法(caporaso等人,2010年,pynast:aflexibletoolforaligningsequencestoatemplatealignment.bioinformatics26:266-267(pynast:用于将序列与模板比对进行比对的灵活工具,《生物信息学》,第26卷,第266-267页))和uclust作为成对比对方法来比对otu代表性序列。然后过滤所得的多重比对并且用于以fasttree方法构建系统发生树(price等人,2009年,fasttree:computinglargeminimumevolutiontreeswithprofilesinsteadofadistancematrix.molbiolevol26:1641-1650(fasttree:用配置文件代替距离矩阵来计算较大的最小进化树,《分子生物与进化》,第26卷,第1641-1650页))。在质量过滤(bokulich等人,2013年,quality-filteringvastlyimprovesdiversityestimatesfromilluminaampliconsequencing.natmethods10:57-59(质量过滤极大改善了illumina扩增测序的多样性估计,《自然方法》,第10卷,第57-59页))之后,在qiime、mother中执行多样性分析,并且采用网站calypso(http://bioinfo.qimr.edu.au/calypso)上的属水平。
结果
对小于14天的足月健康婴儿随机分配婴儿配方食品(对照组)或包含1.0g/l2'岩藻糖基乳糖和0.5g/l乳糖-n-新四糖的相同配方食品(测试组),从加入实验开始至6月龄期间食用;所有婴儿从6月龄至12月龄接受不含hmo的相同2段配方食品。母乳喂养婴儿(bf)用作参考组。在3个月和12个月时,通过16srdna测序分析每个婴儿的粪便微生物群。群落类型的定义基于使用狄利克雷多项式混合(dmm)建模框架的这些微生物组合物特征(参见holmesi、harrisk、quincec(2012年),dirichletmultinomialmixtures:generativemodelsformicrobialmetagenomics.plosone7(2):e30126.doi:10.1371/journal.pone.0030126(狄利克雷多项式混合:微生物宏基因组的生成模型,《公共科学图书馆-综合》,第7卷第2期:e30126.doi:10.1371/journal.pone.0030126))。通过此概率建模方法,每个样本在属层级上关联到一个粪便群落类型(群落类型)。它是无监督方法,不考虑样本的起源(在这种情况下,即不考虑是哪个治疗组)。最佳数量的群落类型及其分类组合物取决于微生物群组合物特征的完整数据集并且由dmm定义。
在聚类成群落类型后,比较所述类型在治疗组之间的分布。
在3月龄婴儿样本中仅观察到群落a、b和c,而在12月龄婴儿的样本中仅实质上观察到群落d、e、f和g。
在3个月时,就微生物群落类型(a、b或c)的分布而言,测试组(n=58,用hmo组合物喂养)中的微生物群组合物看起来比对照组(用常规婴儿配方食品组合物喂养,n=62)更接近母乳喂养组(bf,n=35)。hmo补充剂减少了具有群落c的婴儿数量,该群落特定于配方食品喂养的婴儿。同时,hmo补充剂增加了具有群落b的婴儿数量,该群落是母乳喂养婴儿中最常见的。
它们与配方食品补充剂以及报告的发病率的关联确定了先验,12个月内的药物使用情况使用χ2检验进行分析。
数据使我们得出结论,含有hmo的婴儿配方食品将微生物群带向母乳喂养婴儿。据信通过hmo降低药物使用的可能性与肠道微生物群落类型相关。
图1中示出将微生物群分组成群落类型。
表2:粪便群落类型在治疗组中的分布
还可参见图2。
群落类型b和c的分布在各组中显著不同。
表3:在3个月时按喂养组列出的群落类型的频率和列百分比
bf=母乳喂养组;ctrl=对照组(不含hmo补充剂的婴儿配方食品);test=测试组(补充有hmo的婴儿配方食品)。
表3示出了12个月内的累积报告抗生素使用可能性的结果。其在携带群落c的婴儿中增加,并且在具有群落b的婴儿中减少。
表4a:4个月时的抗生素使用情况
表4a中的数据也示于图3a中。
表4b:6个月时的抗生素使用情况
表4b中的数据也示于图4b中。
表4c:
表4c中的数据也示于图4c中。
具有微生物群落类型b的婴儿在生命的第一年(12个月)中具有较低的需要抗生素的风险。具有微生物群落类型c的婴儿具有增大的需要抗生素的风险。
对于使用抗生素至4个月和6个月,没有统计学显著性证据。然而,基于数量,人们可在相同方向上看出趋势。具有微生物群类型b的婴儿具有较低的风险。
12个月内的累积报告抗生素使用情况的可能性在携带群落c的婴儿中增大,而在具有群落b的婴儿中减小。
因此,本发明促进群落b并减少群落c。
- 还没有人留言评论。精彩留言会获得点赞!