一种具有荧光基团的苯甲酰胺类化合物的应用的制作方法与工艺
本发明涉及已知化合物的新用途,具体地说,涉及一种具有荧光基团的苯甲酰胺类化合物的应用。
背景技术:
肝癌是我国的重大肿瘤疾病之一,发病率高,死亡率高,研制新的防治药物极为重要。目前,已发现烟酰胺磷酸核糖转移酶(Nampt)可调控哺乳动物细胞内必需能量物质NAD的水平。而肝癌细胞具有很高的NAD消耗和代谢速率,对于Nampt抑制剂较为敏感。因而NAD合成途径的限速酶Nampt成为癌症治疗的新靶标,其酶抑制剂FK866(HasmannM,etal.,CancerResearch2003;63:7436-7442.)和CHS-828(HjarnaaPJV,etal.,CancerResearch1999;59:5751-5757.)目前已进入癌症治疗的临床研究。化合物4-(3-氧代-4-丙基-3,4-二氢喹喔啉-2-基)-N-(吡啶-3-基甲基)苯甲酰胺是一种苯甲酰胺类化合物,其英文名为4-(3-oxo-4-propyl-3,4-dihydroquinoxalin-2-yl)-N-(pyridin-3-ylmethyl)benzamide,结构式如式I所示,目前关于该化合物在预防和/或治疗肝癌方面的应用还未见报道。。
技术实现要素:
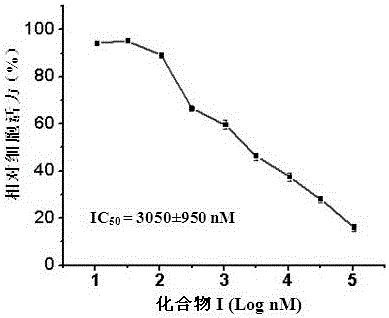
本发明的目的是针对现有技术中的不足,提供如式I所示的具有荧光基团的苯甲酰胺类化合物的新用途,。为实现上述目的,本发明采取的技术方案是:在本发明的第一方面,如式I所示的具有荧光基团的苯甲酰胺类化合物用于制备预防和/或治疗肝癌的药物。在本发明的第二方面,如式I所示的具有荧光基团的苯甲酰胺类化合物用于制备试剂,所述的试剂用于抑制人肝癌细胞株HepG2的增殖。在本发明的第三方面,如式I所示的具有荧光基团的苯甲酰胺类化合物用于制备试剂,所述的试剂用于抑制烟酰胺磷酸核糖转移酶的活性。在本发明的第四方面,如式I所示的具有荧光基团的苯甲酰胺类化合物用于制备试剂,所述的试剂用于肝癌的影像学诊断。所述的“药物”可为任何适用的常规剂型,其中所含如式I所示的化合物的用量为治疗有效量以上,可根据具体情况选择,一般为0.01~100mg/kg/天。所述的药物可以仅以如式I所示的化合物作为唯一活性成分,也可还含有除如式I所示的化合物以外的其它活性成分。所述的其它活性成分为对如式I所示的化合物的抑制烟酰胺磷酸核糖转移酶的活性没有不良影响可联合使用的其它活性成分,如其它通过抑制烟酰胺磷酸核糖转移酶来防治的药物的活性成分。所述的“试剂”是指生物化学试剂或试药,其概念包含诊断试剂、预防或治疗疾病的药物等。本发明优点在于:本发明发现了一种具有荧光基团的苯甲酰胺类化合物的全新用途,该化合物对于烟酰胺磷酸核糖转移酶表现出较好的抑制活性,可用于制备通过抑制烟酰胺磷酸核糖转移酶来预防和/或治疗的疾病的药物,可用于防治肝癌;同时该化合物还具有荧光基团,因此也可用于诊断肝癌。附图说明图1为实施例1中,化合物I对烟酰胺磷酸核糖转移酶的抑制曲线图。图2为实施例2中,化合物I对人肝癌细胞HepG2增殖能力抑制的量效曲线图。图3为实施例3中,化合物I在人肝癌细胞HepG2中的荧光成像图。具体实施方式下面结合附图对本发明提供的具体实施方式作详细说明。下列实施例中未注明具体条件的实验方法,按照常规方法和条件,或按照商品说明书选择。实施例1化合物I抑制烟酰胺磷酸核糖转移酶的活性以下的酶是指烟酰胺磷酸核糖转移酶,可购自康肽生物科技有限公司(003-82)或美国ChemDiv公司(M049-0244),也可自行制备。1、酶的制备:将转化有重组质粒(Nampt-pET28a+)的BL21(DE3)plysS细胞接种于2×YT培养基(37μg/ml氯霉素和75μg/ml卡那霉素)中,37℃振摇过夜,收集菌体后用20倍于原体积的新鲜培养基重悬,37℃培养至OD600约0.6,在0.5mMIPTG、28℃条件下诱导5小时。离心收集菌体,并重悬于lysisbuffer(20mMTris-HCl,300mMNaCl,pH=7.5)中,200W超声裂解细胞,超声1秒间歇9秒,共进行30分钟。将裂解液于12500rpm、4℃离心50分钟后吸取上清液。该上清液与Ni-NTA柱(购自QIAGEN公司)在冰上振摇孵育2小时,再依次用bindingbuffer(5mMimidazole,0.5MNaCl,20mMTris-HCl,pH=7.5)、washbuffer1(20mMimidazole,0.5MNaCl,20mMTris-HCl,pH=7.5)、washbuffer2(40mMimidazole,0.5MNaCl,20mMTris-HCl,pH=7.5)、washbuffer3(60mMimidazole,0.5MNaCl,20mMTris-HCl,pH=7.5)依次洗去杂蛋白,最后用Elutionbuffer(200mMimidazole,0.5MNaCl,20mMTris-HCl,pH=7.5)洗脱收集目的蛋白,并进行SDS-PAGE检测。将收集的目的蛋白与无菌甘油以1:1比例混合,用Bradford方法测定蛋白浓度后保存于-20℃备用。2、酶反应体系为25μl,其中各种组分的浓度为:50mMTris-HCl(pH=7.5)、0.02%BSA、12mMMgCl2、2mMATP、0.4mMPRPP、2mMDTT、2μg/mlNampt、0.2μMNAM、2%DMSO和倍比稀释的化合物I。先将0.5μl不同浓度的化合物I加于96孔板,再加入20μl酶反应混合溶液(除底物之外的酶反应组分),室温孵育5分钟后,加入4.5μl底物NAM溶液以启动反应,37℃反应15分钟后于95℃加热1分钟终止酶反应。3、待酶反应液在冰上冷却后,依次加入10μl20%苯乙酮和10μl2MKOH,涡旋混合仪上混匀后于冰水中作用2分钟,加入45μl88%甲酸,37℃加热10分钟,冰上冷却。4、使用酶标仪测定激发波长382nm、发射波长445nm处的荧光值。5、根据公式:E=R/(1+(C/IC50)S)+B(其中E为酶活性,C为化合物浓度,R、IC50、S、B为待拟合的参数),在origin7.0软件中将酶相对活性对化合物I浓度的曲线进行拟合(见图1),求出化合物I的IC50,结果见表1:表1实施例2化合物I抑制人肝癌细胞的体外增殖我们考察了化合物I对人肝癌细胞体外增殖能力的抑制作用。用梯度浓度的化合物I作用于对数生长期的细胞株2天,利用细胞活力法进行检测:1、将对数生长期的HepG2细胞消化后,吹打成单细胞悬液,接种于96孔培养板,1×104细胞/孔,每孔培养基100μl,37℃、5%CO2培养箱中培养过夜。2、待细胞贴壁后,加入梯度浓度的受试化合物I在培养箱中再培养2天。3、细胞活力测定:取细胞活力试剂(CCK-8试剂)10μl依次加到96孔细胞培养板中,混合均匀后于37℃反应30分钟,酶标仪检测各孔OD值(检测波长:450nm),记录结果,按下列公式计算抑制率:抑制率(%)=(OD对照-OD给药)/OD对照×100%。结果显示(见图2),化合物I对人肝癌细胞株HepG2的增殖表现出不同程度的抑制作用,化合物I对细胞活力抑制的IC50值为3050±950nM。实施例3化合物I在人肝癌细胞中的荧光成像我们通过激光共聚焦显微镜观测了化合物I在人肝癌细胞HepG2中的荧光成像。具体方法为:1、将对数生长期的细胞消化后,吹打成单细胞悬液,接种于培养皿中,37℃、5%CO2培养箱中培养过夜。2、待细胞贴壁后,加入终浓度为3µM的化合物I,溶剂对照则加入同等体积的溶剂DMSO,即二甲基亚砜。3、30分钟后,在激光共聚焦显微镜下观测化合物荧光。4、观测完毕后,迅速去除含有化合物的培养液,并用磷酸盐缓冲液清洗3次后再次在激光共聚焦显微镜下观测细胞中的荧光。5、观测完毕后,立刻换为无化合物培养液继续孵育4小时。6、4小时后,取出培养皿再次观测细胞中的荧光。化合物I在人肝癌细胞HepG2中的荧光成像图见图3,在体外培养条件下,发现其可富集于肝癌细胞中,因此可用于肝癌的影像诊断。以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明方法的前提下,还可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1