一种术后防粘连高分子薄膜及其制备方法与流程
本发明涉及医疗用品技术领域,尤其涉及一种术后防粘连高分子薄膜及其制备方法。
背景技术:
术后腹腔黏连是一种常见的临床症状,国外资料报道,术后腹腔黏连的发生率高达80%。腹腔黏连是术后腹膜进行修复的必然过程。没有粘连就没有修复,但当其修复无序或纤维降解不全以致成为点状、成角、索条状纤维带时,就会带来严重的并发症,如肠梗阻、不孕不育、术后疼痛等,这使得病人不得不二次进院进行手术,不仅给病人带来痛苦也增加了经济负担。
近年来,在术后容易发生粘连的部位植入隔离材料即防粘连材料,已成为国际上防止术后粘连的通用做法。目前临床常用透明质酸钠预防术后粘连,但是效果不尽如人意,尤其是其纯度不高、无消炎作用,因此临床应用范围较窄。国外通常使用具有一定强度和形状的可吸收聚乳酸类固体材料来达到隔离创面并预防和减少粘连的目的,但由于较高的强度和刚度,较差的柔韧性和抗冲击性,其防粘连效果也并不理想。公开号为cn1241442a的中国专利将聚乙醇酸和聚乳酸的共聚物制成薄膜,用于术后防粘连;但上述材料不仅柔韧性有限,其降解可控性也较差,不利于应用。国际专利wo2006/100895和中国专利cn101052425a公开了以丙交酯和己内酯共聚物为组成的医用膜,其具有很好的柔性和强度,但是材料本身的表面性能差(表面多孔),体内粘连蛋白和细胞容易粘附在材料表面引起粘连,而且材料的降解速率慢,完全吸收需要6个月。中国专利cn1436801a公开了一种溶液聚合法,其以甲苯、二甲苯为溶剂制备聚(d,l-乳酸)-乙醇酸共聚物;由于其制备过程中使用的溶剂具有毒性,可能对环境和操作人员有一定影响,从而限制了其在临床医用领域的应用。公开号为cn1532216a中国专利申请公开了将聚酯与聚醚共混制备医用膜。然而可溶性的聚醚在体内会溶解到体液中从而从膜内流失,起不到抑制成纤维细胞在膜表面增殖的作用。此外,以上医用膜与组织的亲附性都难以达到令人满意的效果,这给粘连的防治带来了新的难题。
静电纺丝技术主要具有以下两方面的优点:首先,设备简单,价格低廉,易实现规模化生产,其主要装置包括高压电源、喷头及收集装置,易搭建可灵活设计;其次,通过简单的调控纺丝参数,如溶剂体系的选择、溶液浓度的确定、改变电压、溶液喷出速度等,即可得到微观形貌及宏观性能可控的无纺布纤维材料。由于其自身的灵活性和易操作性,静电纺丝技术已被广泛应用于组织工程领域,尤其是制备多孔纤维薄膜应用于术后防粘连。
技术实现要素:
本发明解决的技术问题在于提供一种术后防粘连高分子薄膜及其制备方法,本申请提供的术后防粘连高分子薄膜具有优异的柔韧性、高度的组织亲和性,能够有效地防止创面粘连并减少细胞在膜表面的贴附、增生和穿透。
有鉴于此,本申请提供了一种术后防粘连高分子薄膜的制备方法,包括以下步骤:
a),将可生物降解高分子材料、乳化剂与有机溶剂混合,得到高分子溶液;将葡聚糖与水混合,得到水相溶液;
b),将所述水相溶液加入至高分子溶液中,混合乳化后,得到均质乳液;
c),将所述均质乳液进行静电纺丝,得到静电纺丝纤维膜;
d),将所述静电纺丝纤维膜干燥后进行紫外臭氧处理,得到术后防粘连高分子薄膜。
优选的,步骤a)中,在制备高分子溶液的过程中,所述混合的原料还包括抗纤维化药物药物;在制备水相溶液的过程中,所述混合的原料还包括抗炎药物。
优选的,所述高分子溶液中的抗纤维化药物为十羟基喜树碱、塞来昔布或多烯紫杉醇;所述水相溶液中的抗炎药物为双氯芬酸钠、茶多酚或阿司匹林。
优选的,所述混合乳化在高速剪切机中进行,所述高速剪切机的转数为3000~6000转/分。
优选的,所述静电纺丝的过程中,环境温度为20~40℃;注射器的针尖与接地板的距离为10~15cm;高压电源的电压为20~25kv,注射器的给料速度为0.1mm/min。
优选的,所述可生物降解高分子材料为生物医用级聚酯,所述葡聚糖的数均分子量为100000。
优选的,所述紫外臭氧处理的时间大于0且小于等于60s。
优选的,所述静电纺丝纤维膜的厚度为0.02~0.4mm。
本申请还提供了一种术后防粘连高分子薄膜,由静电纺丝纤维膜经紫外臭氧处理得到,所述静电纺丝纤维膜由含有可生物降解高分子材料、乳化剂与有机溶剂的高分子溶液与含有葡聚糖与水的水相溶液经静电纺丝得到。
优选的,所述术后防粘连高分子薄膜中的电纺丝为核壳结构。
本申请提供了一种术后防粘连高分子薄膜的制备方法,具体为:首先将含有可生物降解高分子材料、乳化剂与有机溶剂的高分子溶液与含有葡聚糖与水的水相溶液混合乳化,得到均一、稳定的乳液,然后将得到的乳液进行静电纺丝,得到静电纺丝纤维膜,最后将静电纺丝纤维膜进行紫外臭氧处理,得到术后防粘连高分子薄膜。在上述过程中,静电纺丝纤维膜经过紫外臭氧处理,改变了纤维膜的亲水性,使其具有较好的组织亲和性,增加了其与组织的贴附能力,增加了其作为物理屏障而防止粘连的效果;进一步的,在静电纺丝过程中,高分子溶液与水相溶液分离,内层水相溶液依靠外层高分子油相溶液的拖拽作用形成喷射流,得到的术后防粘连高分子薄膜的电纺丝具有核壳结构,从而使不同的药物可搭载于核壳结构中,通过药物的程序性控制释放,利于药物的协同作用,达到更好的粘连防治作用。
附图说明
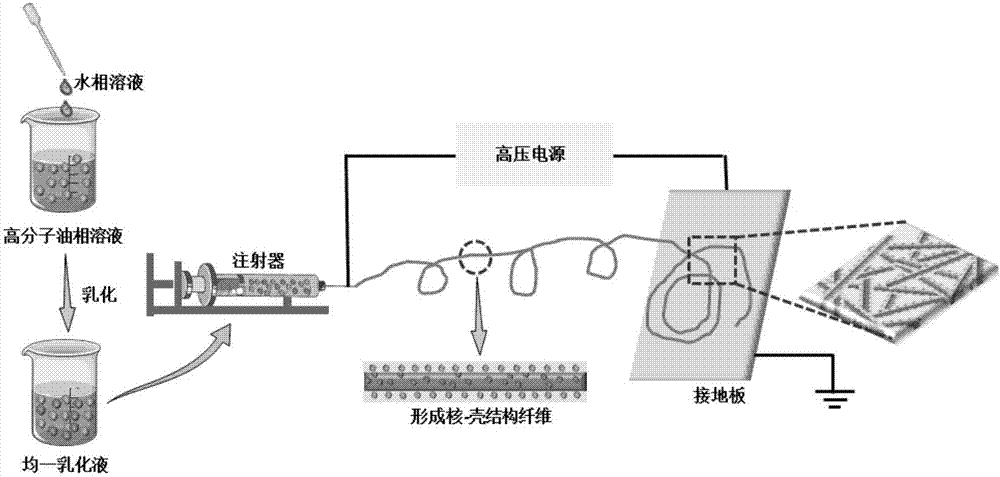
图1为本发明术后防粘连高分子薄膜的制备流程示意图;
图2为本发明实施例1与2制备的术后防粘连高分子薄膜的扫描电子显微镜照片;
图3为本发明实施例3与4制备的术后防粘连高分子薄膜的扫描电子显微镜照片;
图4为本发明实施例9与10制备的术后防粘连高分子薄膜的扫描电子显微镜照片;
图5为本发明实施例15与16制备的术后防粘连高分子薄膜扫描电子显微镜照片;
图6为本发明实施例17制备的术后防粘连高分子薄膜中的电纺丝纤维的透射电镜照片;
图7为本发明实施例17制备的静电纺丝纤维膜经过紫外臭氧处理前后的拉伸曲线图;
图8为本发明实施例2、实施例4、实施例10与实施例16制备的搭载不同药物的术后防粘连高分子薄膜的防粘连效果图。
具体实施方式
为了进一步理解本发明,下面结合实施例对本发明优选实施方案进行描述,但是应当理解,这些描述只是为进一步说明本发明的特征和优点,而不是对本发明权利要求的限制。
本发明实施例公开了一种术后防粘连高分子薄膜的制备方法,包括以下步骤:
a),将可生物降解高分子材料、乳化剂与有机溶剂混合,得到高分子溶液;将葡聚糖与水混合,得到水相溶液;
b),将所述水相溶液加入至高分子溶液中,混合乳化后,得到均质乳液;
c),将所述均质乳液进行静电纺丝,得到静电纺丝纤维膜;
d),将所述静电纺丝纤维膜干燥后进行紫外臭氧处理,得到术后防粘连高分子薄膜。
本发明利用工艺简单、生产过程无污染且节能高效的静电纺丝技术,制备了一种生物可降解的医用手术防粘连膜,该防粘连膜具有优异的柔韧性,高效的组织亲和性,能够有效的防止创面粘连并减少细胞在膜表面的贴附、增生和穿透。由此,本申请提供的术后防粘连高分子薄膜的制备过程具体为:
首先,分别配置术后防粘连高分子薄膜需要的油相溶液与水相溶液;油相溶液即高分子溶液,其是将可生物降解高分子材料、乳化剂与有机溶剂混合,得到高分子溶液,所述高分子溶液中还包括抗纤维化药物或抗炎药物;其中,可生物降解高分子材料为生物医用级聚酯,在实施例中,所述可生物降解高分子材料为聚乙二醇/聚(乳酸-羟基乙酸),其粘均分子量为10万,所述可生物降解高分子材料在所述高分子溶液中的含量为3wt%~6wt%;所述乳化剂优选为苄基三乙基氯化铵,所述乳化剂的含量为所述可生物降解高分子材料的3wt%~8wt%,在实施例中,所述乳化剂的含量为所述可生物降解高分子材料的5wt%;所述有机溶剂优选为氯仿;在实施例中,所述抗纤维化药物为十羟基喜树碱、塞来昔布或多烯紫杉醇,所述抗纤维化药物的含量为所述可降解高分子材料的含量为3wt%~6wt%;所述高分子溶液获得的方式通过磁力搅拌混合得到,所述磁力搅拌的时间优选为5~10h。
所述水相溶液通过葡聚糖与水混合得到。为了避免引入额外的杂质,所述水优选为二次水。所述水相溶液中葡聚糖的含量为3~8wt%,在具体实施例中,所述葡聚糖的含量为5wt%,所述葡聚糖的分子量为100000;所述水相溶液中还包括抗炎药物,所述抗炎药物优选为双氯芬酸钠、茶多酚或阿司匹林;其含量为所述葡聚糖的3~6wt%。本申请所述油相溶液与所述水相溶液中的抗纤维化药物或抗炎药物根据可以同时都存在,也可以不都存在,对此本申请没有特别的限制。所述水相溶液的获得是通过涡旋振荡的混合方式实现的,所述涡旋振荡的时间为3~5min。
在得到油相溶液与水相溶液后,本申请则将所述水相溶液加入至油相溶液中,混合乳化,得到均质乳液。在所述混合乳化的过程中,采用高速剪切机进行混合乳化,所述高速剪切机的转数为3000~6000转/分,在实施例中,所述高速剪切机的转数优选为4000~5000转/分;所述混合乳化的转数可影响所得乳液的均一性,太小不能得到均一的乳液,太大易产生热量,使油相溶液快速挥发。
按照本发明,得到均质乳液后则将其进行静电纺丝,得到静电纺丝纤维膜。所述静电纺丝的过程为本领域技术人员熟知的技术手段,本申请对其技术手段没有特别的限制。如图1所示,图1为本发明制备术后防粘连高分子薄膜的流程示意图,其中在静电纺丝的过程中,包括注射器、高压电源与接地板。在静电纺丝的过程中,环境温度优选为20~40℃,在具体实施例中,所述环境温度优选为25~30℃;温度过高,有机溶剂过快挥发,纤维直径变小;温度过低,有机溶剂挥发慢,油相和水相不能很好分离,不易形成具有核-壳结构的纤维丝。静电纺丝过程中所述注射器的针尖与接地板的距离为10~15cm,针尖与接地板之间的距离主要是保证有效成丝后,最大限度的接收在接地板上,得到纤维膜;距离太近,接收到的不是有效的纤维丝,距离太远,细小的纤维丝可能断裂。静电纺丝的电压为20~25kv,电压过高,纤维丝在强电场作用下会断裂,电压过低不易成丝;注射器的给料速度为0.1mm/min,给料速度决定了整个纺丝过程的连续性,配合电场强度和温度,合适的给料速度能保证电纺丝的流畅进行。本申请中油相溶液和水相溶液不互溶,通过乳化,可得到均一、稳定的乳液,然后将得到的乳液进行电纺,电纺过程中,油相和水相分离,内层液体(水相)依靠外层液体(油相)的拖拽作用形成喷射流,即可形成具有核-壳结构的乳液电纺丝。在形成的核-壳结构的乳液电纺丝中,可根据实际需要,在核层与壳层分别搭载两种不同的抗纤维化药物或抗炎药物;搭载的药物在上述制备油相溶液与水相溶液中进行添加。
本申请最后将静电纺丝纤维膜干燥后进行紫外臭氧处理,所述干燥的温度优选为25~50℃,时间优选为4~12h,所述干燥直到有机溶剂含量小于0.01wt%。所述紫外臭氧处理优选在紫外臭氧仪中处理,所述紫外臭氧处理按照本领域技术人员熟知的方式进行即可,对此本申请对其技术手段没有特别的限制。所述紫外臭氧处理的时间优选大于0且小于等于60s,所述紫外臭氧处理的时间改变纤维膜的亲水性,时间太短,不足以增加纤维膜的亲水效果,时间太长,会明显改变纤维膜的机械特性。实验结果表明,静电纺丝纤维膜经过紫外臭氧处理不同时间(具体依次为10s、20s、30s、40s、50s、60s)后,电纺丝纤维膜具有不同的组织亲附性,其接触角分别为110°、100°、95°、90°、80°、70°。
本发明在制备术后防粘连高分子薄膜的过程中,乳液电纺丝纤维膜能有效搭载两种不同药物于核-壳结构中,通过药物的程序性控制释放,利于药物的协同作用,达到更好的粘连防治作用;通过紫外臭氧处理技术,改变电纺纤维膜表面的亲水性,增加其与组织的贴附能力,增加其作为物理屏障而防治粘连的效果。较同类产品而言,本发明提供的高亲附性医用手术防粘连膜柔韧性良好,与组织贴合能力强,不需要其他措施,如缝合,将其固定于手术部位,因此利于应用于各种外科手术中;实验结果表明,本发明制备的防粘连膜孔径较小,孔隙率大,纤维丝直径较小,增大与组织的贴合面积,能很好地贴附组织而使膜在组织或器官表面不易滑动,利于营养物质交换,避免积血与积液现象;采用本发明的制备方法,其设备要求及工艺流程简单,成本低,易实现规模化生产,经济高效,便于推广应用,最终产品完全能够满足各种临床需求。
综上所述,本发明结合乳液静电纺丝技术和紫外臭氧处理技术,制备了搭载不同药物的经紫外臭氧处理的高分子纤维膜,并从扫描电镜形貌、热性能、力学性能、降解行为、亲水性、细胞毒性及防粘连效果等多方面进行比较,力图获得综合性能优异的医用术后防粘连膜。本申请制备的术后防粘连高分子薄膜具有优良的柔韧性、可生物降解性、良好的组织相容性、药物控制释放及优异的防粘连能力;采用本发明的制备方法,工艺简单,制备手段易操作,成本低,容易实现规模化,所述的最终产品性能优异,完全能够满足各种临床需求,可广泛用做体内防粘连材料,如术后腹腔内肠粘连、十二指肠粘连、食道粘连、蛛网膜下腔粘连、胸膜粘连、卵巢子宫粘连等,从而有效地避免术后并发症,减轻患者的痛苦,提高生活质量。
为了进一步理解本发明,下面结合实施例对本发明提供的术后防粘连高分子薄膜的制备方法进行详细说明,本发明的保护范围不受以下实施例的限制。
实施例1
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,磁力搅拌5小时以获得均匀的有机相溶液;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质w/o乳液;
(4)静电纺丝:将上述均质w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例2
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,磁力搅拌5小时以获得均匀的有机相溶液;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液静电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例3
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例4
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例5
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%的乳化剂(以质量分数计)苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例6
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%的(以质量分数计)乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例7
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例8
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例9
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例10
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例11
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例12
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例13
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的苄基三乙基氯化铵于上述体系中,作为乳化剂,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例14
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例15
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例16
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的苄基三乙基氯化铵于上述体系中,作为乳化剂,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例17
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例18
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例19
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%乳化剂(以质量分数计)的苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例20
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的十羟基喜树碱,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例21
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例22
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例23
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例24
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例25
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%乳化剂(以质量分数计)的苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例26
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的塞来昔布,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例27
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例28
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的双氯芬酸钠,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例29
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例30
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的茶多酚,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
实施例31
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理0秒,得到术后防粘连高分子薄膜。
实施例32
(1)有机相溶液的配制:将聚乙二醇/聚(乳酸-羟基乙酸)(粘均分子量10万)溶于氯仿中,配制成浓度为6%(以质量分数计)的高分子溶液,加入占聚乙二醇/聚(乳酸-羟基乙酸)5%(以质量分数计)的乳化剂苄基三乙基氯化铵于上述体系中,并加入占聚乙二醇/聚(乳酸-羟基乙酸)3%(以质量分数计)的多烯紫杉醇,磁力搅拌5小时以获得均匀的有机相溶液体系;
(2)水相溶液的配置:将10万分子量的葡聚糖溶于二次水中,配置成浓度为5%(以质量分数计)的高分子溶液,并加入占葡聚糖3%(以质量分数计)的阿司匹林,涡旋振荡3分钟以获得均匀的水相溶液体系;
(3)乳化液配置:将水相溶液逐滴滴入有机相溶液中,设置高速剪切机的转数为4000转/分,进行混合、乳化,得到均质的w/o乳液;
(4)静电纺丝:将上述均质的w/o乳液置于静电纺丝设备的给料注射器内,调节注射器针尖与静止接地板之间的距离为15cm;纺丝的环境温度为25℃;开启高压电源以及给料注射器泵,调节电压至25kv,溶液的给料速度为0.1mm/min,在静止接地板上得到乳液电纺丝纤维薄膜(膜厚度为0.2mm);
(5)将静电纺丝纤维薄膜置于真空烘箱中蒸发脱除有机溶剂,烘箱温度设置为45℃,干燥时间为12小时,直到有机溶剂重量含量小于0.01%;
(6)将上述电纺丝纤维膜用紫外臭氧处理50秒,得到术后防粘连高分子薄膜。
如图2~图5所示,图2为本发明实施例1与实施例2制备的高分子薄膜的扫描电子显微镜照片,其中图a为实施例1的扫描电子显微镜照片,图b为实施例2的扫描电子显微镜照片;图3为本发明实施例3与实施例4制备的高分子薄膜的扫描电子显微镜照片,其中图a为实施例3的扫描电子显微镜照片,图b为实施例4的扫描电子显微镜照片;图4为本发明实施例9与实施例10制备的高分子薄膜的扫描电子显微镜照片,其中图a为实施例9的扫描电子显微镜照片,图b为实施例10的扫描电子显微镜照片;图5为本发明实施例15与实施例16制备的高分子薄膜的扫描电子显微镜照片,其中图a为实施例15的扫描电子显微镜照片,图b为实施例16的扫描电子显微镜照片。
图2~图5均为不同实施例制备的高分子薄膜的未经紫外臭氧处理和经过紫外臭氧处理后的表面结构以及水接触角,可以说明纺制的纤维丝表面光滑,几乎没有节点,纤维丝均一,直径较小,孔径均匀;且经过紫外臭氧处理后,纤维膜的水接触角明显减小。
对于经紫外臭氧处理的防粘连膜产品,紫外臭氧能明显减少纤维膜的水接触角,增加纤维膜的亲水性和组织贴附能力;随着紫外臭氧处理的时间增加,防粘连膜的亲水性逐渐增强,但当处理时间超过50秒后,纤维膜的表面形态发生较大变化,纤维丝变软、变粗,彼此交联增多。经紫外臭氧处理50秒的纤维膜,相对于未处理的而言,纤维分布、纤维直径、纤维孔径、力学性能等均没有明显的差异。
对于搭载双药的乳液电纺丝体系,两种药物可被程序性的控制释放,随着纤维丝的溶解,外层药物优先释放,内层药物随后释放,且两种药物的突释现象都被明显缓解,药物释放可持续约20天。体外降解实验表明,紫外臭氧处理对纤维膜的降解没有影响,且纤维膜在体内至少可存在4周,意味着本产品能作为物理屏障有效抑制术后粘连的发生。对于双重药物共载的纤维膜,相比于不搭载药物或搭载单种药物的纤维膜,其炎症抑制作用及抗纤维化作用更好,腹腔粘连的防治作用更显著。
采用紫外线照射对静电纺丝纤维薄膜消毒灭菌的方法,将材料置于24孔培养板中,接种5×104个/孔成纤细胞(l929cells),培养1,3,5,7天后进行cck-8测试及免疫荧光染色法判断静电纺丝纤维薄膜的生物活性,结果表明,我们的防粘连膜产品具有较好的生物相容性。
图6为本发明实施例17制备的术后防粘连高分子薄膜中的电纺丝纤维的透射电镜照片,由图6可以清楚看出薄膜中的电纺丝纤维具有明显的核-壳结构;图7为本发明实施例17制备的静电纺丝纤维膜经过紫外臭氧处理前后的拉伸曲线图;由图7可知,经过紫外臭氧处理的纤维膜的抗拉能力更好,柔韧性更强。
对实施例中制备的防粘连高分子薄膜,经灭菌后进行动物实验,实验动物模型采用小鼠的腹壁-盲肠损伤模型。将麻醉后的小鼠沿中心线切开腹腔,在右侧腹腔内壁距离切口1厘米位置处,切去一块1厘米×1厘米见方的腹壁肌肉,创面深度约0.5毫米,然后将对应位置的盲肠用手术刷摩擦,使粘膜破坏至渗血。将所述防粘连膜缝合于腹壁磨损部位,并将磨损的盲肠与邻近组织隔离开,而对照组动物的创面不加处理,手术完成后缝合腹腔肌肉和皮肤。将动物正常饲养两周后处死,打开腹腔检查粘连情况。如图8所示,图8本发明实施例2、实施例4、实施例10与实施例16制备的搭载不同药物的乳液静电纺丝纤维薄膜的防粘连效果图,图a为实施例2,无药物搭载、经过紫外臭氧处理的纤维膜;图b为实施例4,搭载十羟基喜树碱、经过紫外臭氧处理的纤维膜;图c为实施例10,搭载双氯芬酸钠、经过紫外臭氧处理的纤维膜;图d为搭载十羟基喜树碱和双氯芬酸钠两种药物的、经过紫外臭氧处理的纤维膜。
实验结果显示,未载药的空白纤维膜,在纤维膜的边缘仍有明显纤维粘连带形成,搭载一种药物的纤维膜仅有较少的纤维粘连生成,而搭载两种药物的纤维膜,几乎没有粘连形成,防粘连效果较好,由此表明,本发明制备的防粘连膜能够有效抑制术后粘连的发生,且生物相容性良好,不影响创面的生长愈合。此外,本发明提供的防粘连膜具有较好的柔韧性和降解可控性,综合性质优异,能满足临床上的多种需求。
以上实施例的说明只是用于帮助理解本发明的方法及其核心思想。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也落入本发明权利要求的保护范围内。
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
- 还没有人留言评论。精彩留言会获得点赞!