紫花牡荆素在制备抗溃疡性结肠炎药物中的应用的制作方法
本发明涉及紫花牡荆素在制备防治溃疡性结肠炎药物中的应用,以及紫花牡荆素在制备抗炎药物中的应用,紫花牡荆素在制备抗氧化药物中的应用。
背景技术:
蔓荆子为马鞭草科牡荆属多年生草本植物单叶蔓荆vitextrifolial.var.simplicifoliacham.或蔓荆vitextrifolial.的干燥成熟果实,在我国有悠久的药用历史,始载于《本草经集注》,其性辛、苦,微寒,具有疏散风热,清利头目的功效,在传统中医里被广泛用于治疗风热感冒头痛,齿龈肿痛,目赤多泪,目暗不明,头晕目眩等。
紫花牡荆素(casticin)又名蔓荆子黄素(vitexicarpin),是从蔓荆子中提取出来的多甲基黄酮类成分。其分子式为c19h18o8,分子量为374.35,白色粉末状化合物,可溶于水、甲醇、乙醇,易溶于热水,不溶氯仿及苯。据研究显示紫花牡荆素具有抗肿瘤、抗高催乳素血症、抗氧化、镇痛等广泛药理活性,用于治疗肿瘤、高催乳素血症、疼痛。
溃疡性结肠炎是一种慢性反复发作性、非特异性、全球流行性炎症性肠道疾病,与克罗恩病(crohn’sdiseasecd)统称为炎症性肠病(inflammatoryboweldisease,ibd)。其发病机制不明,主要表现为炎症细胞在结肠组织中的浸润,产生的炎症因子扩大炎症反应,同时破坏其抗氧化能力,造成过氧化损伤。
与溃疡性结肠炎发生相关的促炎症因子主要有il-1β、il-6、tnf-α。溃疡性结肠炎的的组织中,相关促炎症因子的表达显著上升,发挥了扩大炎症反应,诱导了炎症细胞的聚集、趋化、加重组织损伤的作用。
在溃疡性结肠炎组织中,各种炎性细胞浸润使得活性氧(ros)的水平上升,对结肠组织造成氧化损伤,加重了结肠上皮组织的损伤。
技术实现要素:
本发明的目的是提供紫花牡荆素的新用途,所述的紫花牡荆素的化学结构如下式所示:
本发明具体涉及紫花牡荆素在制备抗溃疡性结肠炎药物制剂的应用。
所述药物制剂含有治疗有效量的紫花牡荆素、其药学上可接受的盐或它们的溶剂合物。
所述药物制剂含有治疗有效量的紫花牡荆素、其药学上可接受的盐或它们的溶剂合物外,还包含药用辅料或其它可配伍的药物。
所述药用辅料是指常规的药用赋形剂,如溶剂、崩解剂、矫味剂、防腐剂、着色剂和粘合剂中的一种或两种组合。
所述其它可配伍的药物,指的是以有效剂量的紫花牡荆素为药物原料,再配伍其它天然药物或化学药品。
所述的抗溃疡性结肠炎药物制剂均包括多种临床药物剂型,如胶囊剂、颗粒剂、片剂、注射剂、脂质体纳米粒、缓释剂、控释剂或分散片等。
本发明相对于现有技术具有如下的优点及技术效果:
(1)本发明的紫花牡荆素具有良好的抗溃疡性结肠炎的活性,具有良好的药用前景。
(2)本发明的紫花牡荆素在治疗剂量下未观察到明显的毒副作用,尤其是对肝脏、肺和肾脏的毒副作用。
附图说明
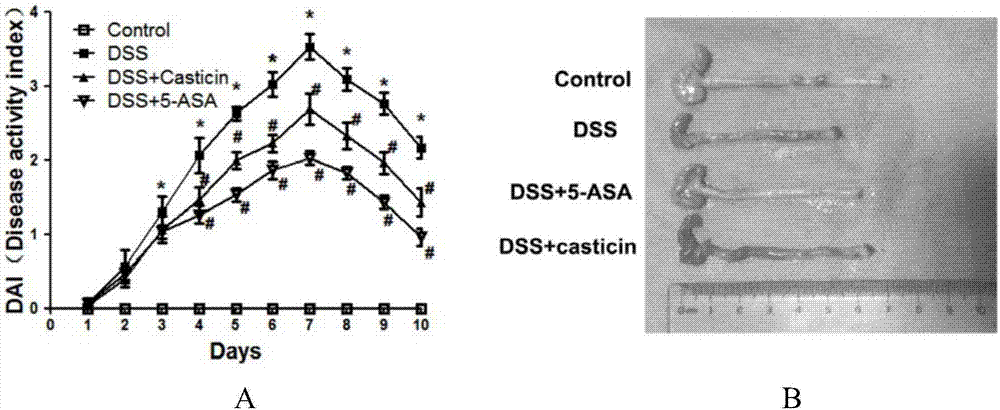
图1紫花牡荆素改善葡聚糖硫酸钠诱导的小鼠溃疡性结肠炎(a:疾病活动度dai,b:结肠长度),
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
*p<0.05,同对照组相比,#p<0.05,同dss组相比;
图2紫花牡荆素抑制了dss诱导的溃疡性结肠炎小鼠的结肠中炎症细胞的浸润和聚集。(a:he染色,b:cd4免疫荧光染色),
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
he:苏木素-伊红染色if:免疫荧光染色标尺=200μm下图为上图方框区放大;
图3.1紫花牡荆素抑制葡聚糖硫酸钠诱导的溃疡性结肠炎小鼠的血清中促炎症因子il-1β、il-6、tnf-α的产生,
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
*p<0.05,同对照组相比,#p<0.05,同dss组相比;
图3.2紫花牡荆素抑制葡聚糖硫酸钠诱导的溃疡性结肠炎小鼠的结肠组织中促炎症因子il-1β、il-6、tnf-α的产生,
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
*p<0.05,同对照组相比,#p<0.05,同dss组相比;
图3.3紫花牡荆素抑制lps诱导的raw264.7细胞中促炎症因子il-1β、il-6、tnf-α的产生,
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
*p<0.05,同对照组相比,#p<0.05,同dss组相比;
图4紫花牡荆素抑制dss诱导的溃疡性结肠炎小鼠结肠组织中活性氧ros、脂质过氧化产物mda的升高,
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
*p<0.05,同对照组相比,#p<0.05,同dss组相比;
图5紫花牡荆素能够升高结肠组织中的总抗氧化能力(tac)以及升高抗氧化物质gsh以及抗氧化酶sod的表达,
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
tac:总抗氧化能力gsh:谷胱甘肽sod:超氧化物歧化酶;
*p<0.05,同对照组相比,#p<0.05,同dss组相比;
图6紫花牡荆素升高溃疡性结肠炎小鼠结肠组织中抗过氧化酶prdx3、mnsod的表达,
control:对照组dss:dss诱导组dss+5-asa:5-asa药物对照组dss+casticin:紫花牡荆素处理组;
图7紫花牡荆素能够升高氧化应激下结肠上皮细胞系caco-2中的prdx3、mnsod水平,
control:对照组h2o2:h2o2诱导组casticin:紫花牡荆素处理组。
具体实施方式
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
本发明实施例用到的紫花牡荆素均购自于成都普瑞法公司,纯度经hplc-dad峰面积归一化法测得均在99%以上。
动物实验方法:利用5%葡聚糖酸钠自由饮水模型造模,将48只小鼠平均分为4组,每组12只小鼠,分别为对照组(con组)、dss诱导组(dss组)、5-asa处理组(dss+5-asa组)、紫花牡荆素处理组(dss+casticin组)给予dss组、5-asa处理组以及紫花牡荆素处理组以5%dss自由饮水7天,后给予3天普通自来水饮水。空白对照组以及阳性药物对照5-asa治疗组,在实验的10天内全程给予普通自来水饮水。紫花牡荆素处理组(dss+casticin组)每日给予紫花牡荆素灌胃,剂量20mg/kg/d,5-asa处理组每日给予5-asa灌胃,剂量为50mg/kg/d。每日称取小鼠体重,测量相关数据,在实验的第10天处死小鼠,取材行相关实验。
实施例1:紫花牡荆素改善葡聚糖硫酸钠诱导的小鼠溃疡性结肠炎。
实验方法:
在动物实验的每天,称取各组小鼠的体重,绘制体重变化曲线;每日计算小鼠的疾病活动指数(dai);以及在实验结束取材后测量每组小鼠结肠长度。
实验结果:
紫花牡荆素处理组的小鼠体重下降最少,紫花牡荆素能够抑制dss诱导的溃疡性结肠炎引起的体重减轻。紫花牡荆素处理组的小鼠疾病活动指数(dai)最小,说明紫花牡荆素能抑制dss诱导的溃疡性结肠炎的疾病活动。紫花牡荆素处理组的小鼠结肠长度长于dss诱导的溃疡性结肠炎组小鼠,说明紫花牡荆素抑制了dss诱导导致的溃疡性结肠炎导致的结肠短缩。正常小鼠、dss诱导小鼠以及紫花牡荆素处理小鼠的各组间效应差别具有统计学意义(图1)。
实施例2:紫花牡荆素抑制了dss诱导的溃疡性结肠炎小鼠的结肠中炎症细胞的浸润和聚集。实验方法:
在动物实验结束后取结肠组织,行脱水后石蜡包埋,切3μm片,行he染色。拍照后分析结肠组织结构。利用石蜡切片,脱蜡水化后利用抗cd4抗体行免疫荧光染色,使用含dapi的封片剂封片,利用荧光显微镜拍摄后分析。
实验结果:
he染色分析显示,紫花牡荆素治疗组中炎症细胞浸润少,结肠组织结构保存较好,有着更多的正常的结肠上皮组织。说明紫花牡荆素能够抑制dss诱导的炎症细胞的浸润,抑制结肠上皮细胞的脱落,从而抑制溃疡性结肠炎的发生、发展。cd4的免疫荧光显示,紫花牡荆素治疗组中cd4阳性的细胞明显少于dss诱导组,说明紫花牡荆素能够抑制淋巴细胞在dss诱导的溃疡性结肠炎上皮组织中的集聚(图2)。
实施例3:紫花牡荆素抑制葡聚糖硫酸钠诱导的溃疡性结肠炎小鼠的炎症因子的产生。
3.1紫花牡荆素抑制葡聚糖硫酸钠诱导的溃疡性结肠炎小鼠的血清中促炎症影子il-1β、il-6、tnf-α的产生
实验方法:
在动物实验结束时利用心脏取血置于1.5mlep管中,静止30min后,1500rpm离心15min,取上清。利用elisa试剂盒(碧云天),测定血清中il-1β、tnf-α、il-6的含量。
实验结果:
elisa实验结果显示,紫花牡荆素处理的dss诱导小鼠,其血清中的il-1β、tnf-α、il-6含量较dss诱导小鼠低,各组间差异存在统计学差异。
实验显示紫花牡荆素能够有效的抑制dss诱导导致的il-1β、tnf-α、il-6升高,说明紫花牡荆素能够抑制溃疡性结肠炎过程中炎症因子的上升(图3.1)。
3.2紫花牡荆素抑制葡聚糖硫酸钠诱导的溃疡性结肠炎小鼠的结肠组织中促炎症因子il-1β、il-6、tnf-α的产生
实验方法:
实验结束时取各组小鼠结肠组织,以1:2比例加入pbs,将组织磨碎,置于4℃4小时,后以3000rpm/分离心30min取上清。利用elisa试剂盒(碧云天)测定各组间结肠组织中il-1β、tnf-α、il-6的含量。
实验结果:
紫花牡荆素组小鼠结肠中il-1β、tnf-α、il-6的含量较dss诱导小鼠低,各组间差异存在统计学意义。实验显示紫花牡荆素能够抑制溃疡性结肠炎小鼠中结肠组织中的il-1β、tnf-α、il-6升高,说明紫花牡荆素能够抑制溃疡性结肠炎过程中炎症因子的上升(图3.2)。
3.3紫花牡荆素抑制lps诱导的raw264.7细胞中促炎症影子il-1β、il-6、tnf-α的产生实验方法:
取对数生长期raw264.7细胞,接种于6孔培养板,每孔100μl,设空白组、对照组和不同浓度的样品组,每组设3个平行孔。置37℃、5%(v/v)co2的培养箱中培养,培养24h后,加入脂多糖lps(1μg/ml)后,加入不同浓度紫花牡荆素(1μm、2.5μm、10μm),继续培养24h。采用qpcr法检测培养细胞中的il-1β,il-6和tnf-α。
实验结果:
紫花牡荆素对lps所致的raw264.7细胞的促炎因子il-1β、il-6、tnf-α的生成有明显的抑制作用,且这种抑制作用存在浓度依赖性。实验显示紫花牡荆素对lps所致raw264.7细胞炎症,及促炎症因子的升高具有显著的抑制作用(图3.3)。
本发明通过以下相关实验证明紫花牡荆素能通过提高抗氧化能力,抑制ros的生成以及过氧化损伤的产生,从而抑制溃疡性结肠炎的发生。
实验例4紫花牡荆素能够抑制dss引起的小鼠结肠组织中脂质过氧化产物mda的升高。
实验方法:在动物实验结束时取各组小鼠结肠组织,以1:2比例加入pbs,将组织磨碎,置于4℃4小时,后以3000rpm/分离心30min取上清。利用ros试剂盒测定各组间结肠组织中ros的含量,利用elisa试剂盒(碧云天)测定结肠组织中mda的含量。
实验结果:结果显示紫花牡荆素组小鼠结肠组织中mda的含量较dss处理组显著下降,且各组间差异存在统计学意义。实验显示:紫花牡荆素能够抑制溃疡性结肠炎小鼠中结肠组织的过氧化,表现在ros以及mda水平的下降(图4)。
实施例5紫花牡荆素能够升高结肠组织中的总抗氧化能力(tac)以及升高抗氧化物质gsh以及抗氧化酶sod的表达。
实验方法:在动物实验结束时取各组小鼠结肠组织,以1:2比例加入pbs,将组织磨碎,置于4℃4小时,后以3000rpm/分离心30min取上清。利用tac试剂盒测定各组间结肠组织中tac的含量,利用elisa试剂盒测定结肠组织中gsh、sod的含量。
实验结果:结果显示紫花牡荆素组小鼠结肠组织中tac较dss处理组显著上升,且各组间差异存在统计学意义。紫花牡荆素组小鼠结肠组织中gsh以及抗氧化酶sod含量较dss处理组上升,且各组间差异存在统计学意义。实验显示:紫花牡荆素能够升高溃疡性结肠炎小鼠中结肠组织的抗氧化能力,表现在升高tac以及gsh、sod的表达(图5)。
实施例6紫花牡荆素能够升高溃疡性结肠炎小鼠结肠组织中抗过氧化酶prdx3、mnsod的表达。
实验方法:在动物实验结束时取各组小鼠结肠组织,常规固定、脱水、石蜡包埋后,切3微米切片,利用抗mnsod抗体、prdx3抗体行免疫组化分析结肠组织中prdx3、mnsod的表达情况。
实验结果:紫花牡荆素升高了抗过氧化酶prdx3、mnsod的表达。实验结果显示,紫花牡荆素通过升高结肠组织中抗过氧化酶prdx3、mnsod的表达,抑制结肠组织中的过氧化(图6)。
实施例7紫花牡荆素能够升高氧化应激下结肠上皮细胞系caco-2中的prdx3、mnsod水平。
实验方法:将对数生长期caco-2细胞,接种于12孔培养板,设空白组、对照组和不同浓度的样品组,每组设6个平行孔。置37℃、5%(v/v)co2的培养箱中培养,培养24h后,加入过氧化氢(0.3%)预处理24h后,加入紫花牡荆素(10μm),继续培养24h。采用westernblot法检测细胞培养上清中的prdx3、mnsod水平。
实验结果:紫花牡荆素处理组中prdx3、mnsod表达量较dss处理组增高。实验显示:紫花牡荆素能够通过促进抗过氧化酶prdx3、mnsod的表达抑制溃疡性结肠炎小鼠结肠组织中的氧化应激损伤(图7)。
实施例8胶囊剂的制备
紫花牡荆素2g,乳糖20g,羟甲基淀粉钠0.1g,淀粉浆适量,硬脂酸镁0.1g混合,过筛制粒,干燥后混匀装入胶囊,每个胶囊含紫花牡荆素0.02g,每日口服1-2粒,每日两次。
实施例9片剂的制备
紫花牡荆素5g,乳糖200g,淀粉浆适量,硬脂酸镁1g,混合,过筛,干燥后压片。每片含紫花牡荆素0.02g。每日口服1-2片,每日两次。
实施例11注射液的制备
紫花牡荆素2g,丙二醇50g,研磨,再加少量注射用水稀释,混匀,然后加入氯化钠适量,溶解后再加入注射用水至1000ml,调ph值5.5-6.5,滤过,灌封,灭菌,即得1000支注射用针剂。
实施例12脂质体纳米粒的制备
紫花牡荆素1g,大豆卵磷脂500mg,溶于25ml乙醇中,另取硬脂酸200mg和大豆卵灵脂500mg溶于25ml环己烷中,混合搅拌均匀。于37℃恒温水浴中减压旋转蒸发除去有机溶剂,使药物及辅料在烧瓶壁形成均匀脂质薄膜,于真空干燥器中放置过夜,除尽有机溶剂;另取聚乙二醇单硬脂酸酯3750mg,搅拌溶解在175ml水中,加入上述薄膜中,超声10min,定容至250ml,得淡黄色透明溶液。将此溶液冷冻干燥可得冻干粉。用球磨机研磨24小时,制得粒径均匀的纳米粒,混匀并分装。每袋含紫花牡荆素0.005g。口服,一次一袋,每日两次。
实施例13缓释剂的制备
将紫花牡荆素50g,羟丙基甲基纤维素30g,乳糖10g,加适量粘合剂制备软材,过20目筛制粒。干燥,整粒,加入硬脂酸镁0.3g,混合均匀,压片。每片含紫花牡荆素0.005g。每日口服1-2片,每日一次。
实施例14控释剂的制备
紫花牡荆素1g,乳糖40g和淀粉浆适量直接装到旋转制粒机/包衣器制备颗粒,将稀释到15%固体的塑化乙基纤维素包衣剂悬浮液喷雾到紫花牡荆素颗粒的旋转床上。在喷雾期间,用泊洛沙姆188制成的分散体载体膜包衣紫花牡荆素颗粒,形成平均颗粒度大约为450μm的持续释放的颗粒。混匀装入胶囊,每个胶囊含紫花牡荆素0.005g,每日口服1-2粒,每日两次。
实施例15分散片的制备
取紫花牡荆素50g,羟乙酸淀粉钠50g,预凝胶淀粉340g,低取代羧丙基纤维素25g,糖精钠3g,薄荷香精3g,混合均匀制粒,并控制粒度在35-80μm范围内,直接压片。每片含紫花牡荆素0.005g。每日口服1-2片,每日两次。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!