一种复合纳米纤维神经支架的制备方法与流程
本发明属于生物医用材料和神经组织工程领域,涉及一种适于周围神经再生的复合纳米纤维神经支架的制备方法。
背景技术:
周围神经损伤在临床上十分常见,尤其长段距离的神经缺损修复一直是医学界难以攻克的难题。迄今为止,经历了神经吻合、自体神经移植、同种异体神经移植、自体非神经组织移植和生物材料替代等几个过程,但几种治疗方式各有利弊,神经缺损修复的问题未得到根本性的解决。
面对长距离的神经损伤,目前研究的重点是将生物材料加工成管状结构的神经支架来使神经再生。这种支架不仅可以防止损伤神经末端分泌的神经生长因子逸散,为其提供扩散的通道,也可有效地促进近端神经末端的轴突生长,减少瘢痕组织的侵入,从而扩大外源性蛋白的浓度,为管腔与周围再生环境间大分子的选择性扩散提供良好的屏障。因此,神经支架保证了神经再生所需的“微环境”,是最有潜力替代自体神经移植法的修复方法。但是当遇到长距离、粗大神经的缺损时,这类单纯由生物材料组成的支架往往由于缺乏生物活性物质等营养物质的支持,取得的修复效果十分有限。因此,为了进一步提高神经支架的修复能力,为神经再生创造良好的微环境,近十几年快速发展的组织工程为神经修复提供了新的思路。如大多数组织工程材料一样,用于神经组织工程的材料应具备以下条件:(1)能负载生长因子和活体细胞,从而保证神经修复所需的营养供应;(2)具有良好的生物相容性、生物可降解吸收性,对材料进行加工,能够提高支架材料的力学性,利用支架里面定向分布的纤维结构,引导神经纤维定向生长;(3)有利于代谢产物的交换和营养物质的输送,并保证良好的血液供应;(4)比表面积及孔隙率较高,更能促进细胞的點附、增殖和分化及电刺激作用。
依据人体本身具有生物电这一事实,以及电刺激能促进细胞的粘附、增殖和dna合成等研究结果,学者们提出一种新设想,即希望研究出一种新型的生物材料,它既具有与人体组织的生物相容性,同时又具有相似于人体的生物电性能。将它植入人体时,不需要外加电源,仅靠自身的电效应不断地产生合适的电刺激。最早出现的这类材料为驻极体材料如聚偏二氟乙烯、聚四氟乙烯等,这类材料具有表面电荷,能促进周围神经的再生。然而,这些材料的表面电荷主要是由于俘获电荷载流子或微小机械形变而产生,因此电荷很不稳定,电刺激的强度和持续的时间难以控制。氧化石墨烯(grapheneoxide,go)是石墨烯经过化学修饰后高度氧化得到,大多含氧官能团(羟基、环氧基和羧基)被连接于氧化石墨烯的单层碳原子的表面或者边缘处,其分散性比石墨烯更好,有利于生物材料方面的运用。研究表明go作为纳米增强成分微量掺杂到聚合物基体中,可以使聚合物的机械性能得到有效提升,此外,其具备细胞毒性低和生物相容性好等优势而备受大量科研工作者的青睐。其对神经干细胞分化能力有积极影响。中药中蕴含着大量治疗周围神经的药物资源,在促进受损周围神经组织恢复和再生方面具有相当广阔的前景。
技术实现要素:
本发明所要解决的技术问题是提供一种复合纳米纤维神经支架的制备方法,其所得神经支架具有电刺激作用和中药提取物(traditionalchinesemedicineextraction,tcme)促进神经损伤修复作用,可以作为复合多功能神经损伤修复支架材料。
本发明解决上述技术问题所采用的技术方案是:一种复合纳米纤维神经支架的制备方法,以具有生物相容性的生物医用高分子/导电材料为壳层预电纺液,细胞外基质成分或类细胞外基质成分/中药提取物为芯层预电纺液,通过静电纺丝技术,制得具有导电性能和中药促进再生功能的复合纳米纤维支架。
按上述方案,所述导电材料为无机导电材料或高分子导电材料。
按上述方案,所述无机导电材料包括有氧化石墨烯、碳纳米管和金属离子中的任意一种或它们的混合,所述的高分子导电材料包括有聚吡咯、聚苯胺以及它们的混合。
按上述方案,所述的细胞外基质成分包括有透明质酸、硫酸软骨素、胶原以及它们的混合,所述的类细胞外基质成分为壳聚糖,所述的具有生物相容性的生物医用高分子包括有聚乳酸、聚己内脂、聚乙烯醇、聚乙醇酸以及它们的混合。
按上述方案,所述的细胞外基质成分或类细胞外基质成分与中药提取物的质量比例为0.25~50:1,所述的具有生物相容性的生物医用高分子与导电材料的质量比例为25~50:1。
按上述方案,所述的中药提取物为太子参、人参、西洋参、黄芪、银杏、丹参和川芎中的任意一种或它们的复合采用常规工艺的提取物。
按上述方案,所述导电材料与中药提取物的用量比例为1:1-1:1000(g/g)。
按上述方案,所述的静电纺丝技术为同轴静电纺丝法或共混电纺法。
按上述方案,所述的静电纺丝技术或共混电纺法的控制参数:电压:10kv~30kv,推进速度:0.1~2ml/h,喷丝头与接收装置的接收距离:10~25cm;环境参数:温度:25~30℃,湿度:50~80%。
按上述方案,所述复合纳米纤维神经支架为孔隙率在72%以上直径均匀的连续纤维丝,其直径大小为1-1000nm。
本发明所述的合成生物医用高分子不仅包括上述所述的,还包括有:聚酰胺、环氧树脂、聚乙烯、聚甲醛、聚甲基丙烯酸甲酯、聚四氟乙烯、聚醋酸乙烯酯、硅橡胶和硅凝胶;以及天然生物医用高分子:甲壳类、昆虫类动物体中提取的甲壳质壳聚糖纤维,从海藻植物中提取的海藻酸盐,从桑蚕体。
本发明采用静电纺丝技术,不仅可以制备具有高孔隙率、高比表面积的纳米纤维,其工艺调节能使纤维支架强度、孔隙率和孔径能有效控制,还可改善和优化材料性能,将力学性能差的材料或不易电纺的材料如透明质酸和壳聚糖等作为芯材,将力学性能好的材料如聚乳酸作为壳材,通过降解速度的控制,使得核壳结构发挥功能。中药提取物包覆在芯材中,可实现药物的有效释放,所得到的仿生纳米纤维支架能够起到支撑细胞生长、引导组织再生、控制组织结构等作用,从而达到神经组织修复的作用。
本发明的有益效果在于:
(1)导电材料如氧化石墨烯与其他导电材料相比,易制备、物理化学和生物学性能好,可以发挥电刺激作用,更好地诱导神经再生,为探索电刺激调控干细胞促进周围神经再生的作用机制和改进周围神经修复用材料提供新思路,所述的中药提取物具有促进周围神经损伤后神经生长因子蛋白表达、雪旺细胞增殖、保护受损神经元和促进神经再生及结构重建的作用。因此中药在周围神经损伤方面具有广阔的应用前景;
(2)本发明制备的具有电刺激和中药复合纳米纤维支架可以控制各类药物的有效释放,生物相容性好,性能稳定易于保存,在周围神经损伤修复等生物医学领域中具有良好的应用前景。
(3)本发明采取的方法操作简单,工艺省时,原材料价格适中易获得,反应条件温和,绿色友好,经济性好,适于工行业生产。
附图说明
图1为pla/go/ha/tcme纳米纤维支架的制备示意图;
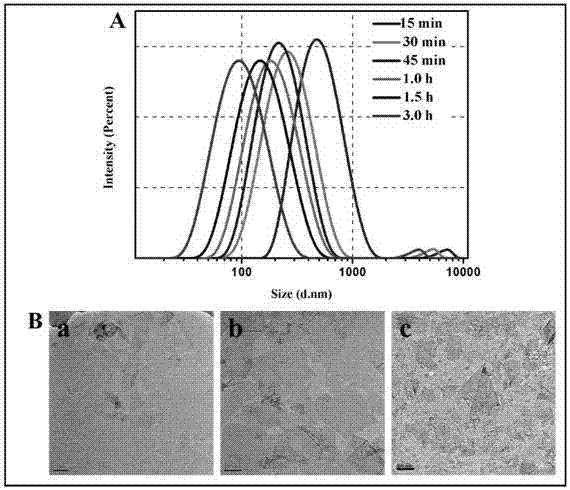
图2中的图2(a)不同超声时间go的粒径图;图2(b)是不同超声功率go的透射电镜图;
图3为制备得到的pla/go/ha/tcme纳米纤维支架的sem图;
图4为pla/go/ha/tcme纳米纤维支架与bmmsc细胞共培养7天的荧光图。
具体实施方式
为了更好地理解本发明,下面结合实施例进一步阐明本发明的内容,但本发明的内容不仅仅局限于下面的实施例。
下述实施例1-4为go的制备方法
实施例1:取1.0g天然石墨粉,0.5g硝酸钠于三口烧瓶中,在冰浴条件下缓慢加入23ml浓硫酸,持续搅拌15min。再缓慢加入5g高锰酸钾并保持系统温度不超过20℃,继续搅拌2h。移除冰浴将系统加热到35℃,持续搅拌1.5h。缓慢加入46ml去离子水,维持体系温度98℃,剧烈搅拌30min。然后在空气中冷却,加入140ml去离子水和10ml双氧水去终止反应,悬浮液变亮黄色。离心10min洗涤,用5%hc1和去离子水充分洗涤至ph接近中性,冷冻干燥得到棕色固体氧化石墨。将得到固体分散到去离子水中(1mg/ml),以50w功率超声剥离10min,得到氧化石墨烯纳米片,离心10min(10000r/pm)除去未剥离氧化石墨,最后获得棕色go悬浮液,冷冻干燥得到go固体。氧化石墨烯的片层厚度约为1.0nm左右,表明可能是多层氧化石墨烯,也可能是单层氧石墨烯。其平均片层宽度在200-500nm之间。
实施例2:取1.0g天然石墨粉,0.5g硝酸钠于三口烧瓶中,在冰浴条件下缓慢加入23ml浓硫酸,持续搅拌15min。再缓慢加入5g高锰酸钾并保持系统温度不超过20℃,继续搅拌2h。移除冰浴将系统加热到35℃,持续搅拌1.5h。缓慢加入46ml去离子水,维持体系温度98℃,剧烈搅拌30min。然后在空气中冷却,加入140ml去离子水和10ml双氧水去终止反应,悬浮液变亮黄色。离心20min洗涤,用5%hc1和去离子水充分洗涤至ph接近中性,冷冻干燥得到棕色固体氧化石墨。将得到固体分散到去离子水中(1mg/ml),以100w功率超声剥离20min,得到氧化石墨烯纳米片,离心20min(10000r/pm)除去未剥离氧化石墨,最后获得棕色go悬浮液,冷冻干燥得到go固体。
实施例3:取1.0g天然石墨粉,0.5g硝酸钠于三口烧瓶中,在冰浴条件下缓慢加入23ml浓硫酸,持续搅拌15min。再缓慢加入5g高锰酸钾并保持系统温度不超过20℃,继续搅拌2h。移除冰浴将系统加热到35℃,持续搅拌1.5h。缓慢加入46ml去离子水,维持体系温度98℃,剧烈搅拌30min。然后在空气中冷却,加入140ml去离子水和10ml双氧水去终止反应,悬浮液变亮黄色。离心洗涤,用5%hc1和去离子水充分洗涤至ph接近中性,冷冻干燥得到棕色固体氧化石墨。将得到固体分散到去离子水中(1mg/ml),以180w功率超声剥离90min,得到氧化石墨烯纳米片,离心30min(10000r/pm)除去未剥离氧化石墨,最后获得棕色go悬浮液,冷冻干燥得到go固体。
实施例4:取1.0g天然石墨粉,0.5g硝酸钠于三口烧瓶中,在冰浴条件下缓慢加入23ml浓硫酸,持续搅拌15min。再缓慢加入5g高锰酸钾并保持系统温度不超过20℃,继续搅拌2h。移除冰浴将系统加热到35℃,持续搅拌1.5h。缓慢加入46ml去离子水,维持体系温度98℃,剧烈搅拌30min。然后在空气中冷却,加入140ml去离子水和10ml双氧水去终止反应,悬浮液变亮黄色。离心60min洗涤,用5%hc1和去离子水充分洗涤至ph接近中性,冷冻干燥得到棕色固体氧化石墨。将得到固体分散到去离子水中(1mg/ml),以1000w功率超声剥离600min,得到氧化石墨烯纳米片,离心60min(10000r/pm)除去未剥离氧化石墨,最后获得棕色go悬浮液,冷冻干燥得到go固体。
对不同条件下制备的go进行粒径分析,分别将其配制成一定浓度的去离子水分散液,常温下分别采用马尔文激光粒度仪进行粒径测量、透射电镜(tem)进行形貌分析。从图2a中可以看出当超声功率一定时,氧化石墨烯片层尺寸随超声时间增长而减小,当超声时间为3h时,go的片层尺寸逐渐减小至90nm左右,但从图中可以看出超声太长go粒径反而分布不均匀,说明有部分片层结构遭到破坏。另外从图2b的gotem图可以看出,超声时间固定1.5h,不同的超声功率对go的片层结构影响很大。当超声功率为100w时(图2b-a),go大部分片尺寸较大,片层间并未完全剥离分散开;当超声功率为180w时(图2b-b),go片结构完整、尺寸均一、大小合适,有利于后期的功能化改性;当超声功率为500w时(图2b-c),go大部分被超散成碎片,尺寸大小很不均一,且部分片层中出现很多孔洞,片层结构的完整性严重遭到破坏。说明超声超声功率小或太大,都不利于go的剥离。综合数据结果最终选择超声功率180w,超声时间1.5h的条件剥离go。
实施例5-9为本发明复合纳米纤维神经支架的制备方法
实施例5:
(1)二氯甲烷(dcm)和n-n-二甲基甲酰胺(dmf)体积比7:3的复合溶剂作为纺丝溶剂,制取聚乙烯醇质量(1g)百分比为10%,将上述实施例3制备的go0.02g加入到pla溶液,搅拌使之均匀分散,制备得到壳层预电纺液;
(2)称取质量为1g的ha,溶于水溶液(体积比1:40)中,得到质量百分比为2%的ha水溶液。取银杏提取物0.02g加入其中,磁力搅拌6h后使药物分散均匀,脱泡处理后,后处理备用,作为芯层预电纺液。
(3)将以上制备的两种预电纺液分别装在内径不同的注射器嵌入注射泵中,采取同轴静电纺丝法,调节电压至10kv,流速为0.3ml/h,温度为22℃,接收距离为15cm,用细质铜网(10cm×10cm)作为接收装置,从接收辊上取下纤维膜,真空干燥去除溶剂,得到复合纤维膜。如图3所示,该复合纤维膜由直径均匀的直径1-1000nm,孔隙率为90%的连续纤维丝组成。
实施例6:
(1)二氯甲烷(dcm)和n-n-二甲基甲酰胺(dmf)体积比3:1的复合溶剂作为纺丝溶剂,制取聚乙醇酸质量(1g)百分比为10%,将上述实施例3制备的中go0.02g加入到pla溶液,搅拌使之均匀分散,制备壳层预电纺液。
(2)称取1g的ha,溶于水溶液(体积比1:40)中,得到质量百分比为2%的ha水溶液。取人参提取物0.2g加入其中,磁力搅拌6h后使药物分散均匀,脱泡处理后,后处理备用,作为芯层预电纺液。
(3)将以上制备的两种预电纺液分别装在内径不同的注射器嵌入注射泵中,调节电压至15kv,流速为0.2ml/h,温度为22℃,接收距离为15cm,用细质铜网(10cm×10cm)作为接收装置,从接收辊上取下纤维膜,真空干燥去除溶剂,得到复合纤维膜。
实施例7:
(1)二氯甲烷(dcm)和丙酮体积比3:1的复合溶剂作为纺丝溶剂,制取聚己内脂质量(1g)百分比为15%,将上述实施例3制备的中go0.02g加入到pla溶液,搅拌使之均匀分散,制备壳层预电纺液。
(2)称取1g的胶原,溶于水溶液(体积比1:40)中,得到质量百分比为2%的ha水溶液。取当归提取物0.4g加入其中,磁力搅拌6h后使药物分散均匀,脱泡处理后,后处理备用,作为芯层预电纺液。。
(3)将以上制备的两种预电纺液分别装在内径不同的注射器嵌入注射泵中,调节电压至20kv,流速为0.1ml/h,温度为25℃,接收距离为20cm,用细质铜网(10cm×10cm)作为接收装置接受,从接收辊上取下纤维膜,真空干燥去除溶剂,得到复合纤维膜。
实施例8:
(1)氯仿1ml作为纺丝溶剂,制取pla质量(1g)百分比为20%,将上述实施例3制备的中go0.04g加入到pla溶液,搅拌使之均匀分散,制备壳层预电纺液。
(2)称取1g的硫酸软骨素,溶于水溶液(体积比1:40)中,得到质量百分比为2%的ha水溶液。取太子参提取物2.0g加入其中,磁力搅拌6h后使药物分散均匀,脱泡处理后,后处理备用,作为芯层预电纺液。
(3)共混电纺法,向步骤(2)制备的预电纺液中加入适量乳化剂,搅拌均匀后,将步骤(1)制备的预电纺液缓慢滴加其中使成均匀,两相间的混溶性好,两相相互渗透溶解。调节电压至23kv,流速为2ml/h,温度为22℃,接收距离为20cm,用细质铜网(10cm×10cm)作为接收装置,从接收辊上取下纤维膜,真空干燥去除溶剂,得到复合纤维膜。
实施例9:
(1)六氟异丙醇1ml的复合溶剂作为纺丝溶剂,制取pla(1g)质量百分比为20%,将上述实施例3制备的中go0.04g加入到pla溶液,搅拌使之均匀分散,制备壳层预电纺液。
(2)称取1g的ha,溶于水溶液(体积比1:40)中,得到质量百分比为2%的ha水溶液。取川芎提取物4.0g加入其中,磁力搅拌6h后使药物分散均匀,脱泡处理后,后处理备用,作为芯层预电纺液。
(3)将以上制备的两种预电纺液分别装在内径不同的注射器嵌入注射泵中,调节电压至10kv,流速为1ml/h,温度为22℃,接收距离为15cm,用细质铜网(10cm×10cm)作为接收装置,从接收辊上取下纤维膜,真空干燥去除溶剂,得到复合纤维膜,工艺如图1所示。
实施例10:
从培养箱中将骨髓间充质干细胞(bmmscs)与材料共培养7天后的培养板取出,吸去培养液,用pbs清洗表面残留细胞,3min/次,再用4%的多聚甲醛固定30min,弃去多聚甲醛,再用pbs清洗残余多聚甲醛3次5min/次,接着加0.1%的tritonx-100来增加膜的通透性,15min/次接着用pbs清洗3次,5min/次。取浓度为5-10μm的dil母液稀释到100ml的pbs中,然后加入到一个孔的比例进行加样,在室温下避光静置20min,之后对多余的染料进行清洗。最后向每个孔中加入200μl的dapi染色液,在室温下避光放置30min,用pbs清洗多余的染色液,加入适量抗荧光淬灭剂然后将培养板于倒置荧光显微镜下观察dii和dapi的染色具体情况,进行拍照。结果如图4所示,bmmscs呈长梭形,形态正常。可以成片的粘附在材料表面,说明细胞的铺展程度较好。
- 还没有人留言评论。精彩留言会获得点赞!