抗滥用药物组合物的制作方法
许多药物活性成分除了在其适当的应用中具有优异的活性外,还具有滥用的可能性,即它们可被滥用者用于产生除预期的医学效果之外的效果。例如,处方阿片类药物产品是现代疼痛管理的重要组成部分。然而,滥用和误用这些产品已造成越来越多的严重公共卫生问题。实现创造更安全阿片类镇痛药目标的一个可能重要的步骤是开发能阻止滥用的配方的阿片类药物。这些产品的开发被例如美国fda视作公共卫生重要优先事项(参见“抗滥用阿片类药物-评估和标签”;2015年4月fda产业指南,fda;“fda指南”)。
由于阿片类药物产品常常通过改变给药途径或者破坏延长释放(er)特性而被操作以实现滥用目的,因此迄今为止开发的大多数抗滥用技术都旨在使操作更加困难或者使得对被操作的产品的滥用更不具有吸引力或更不具有回报。值得注意的是,这些技术尚未被证明能成功地阻止最常见的滥用形式-吞下许多完整的胶囊或片剂以达到欣快的感觉。此外,一个产品具有抗滥用特性并不意味着没有滥用的风险。而是,它意味着滥用的风险低于不具有这些特性的产品。因为阿片类药物产品最终必须能够将阿片类药物送达患者,所以可能总会有对这些产品的滥用。
在fda指南中,抗滥用特性被定义为,即使不能完全防止滥用、也是显示有意义地阻止滥用的那些属性。术语滥用(abuse)被定义为,药物产品或物质的有意的、非治疗的使用,哪怕是使用一次,以实现预期的心理或生理效果。滥用与误用(misuse)不同,误用是指以不恰当的方式对药品进行有意的治疗性使用,这里特别排除了滥用的定义。fda指南使用术语“抗滥用(abuse-deterrent)”而不是“防篡改(tamper-resistant)”,因为后一术语是指或是用于某些类别的药物、装置和化妆品的包装要求。
抗滥用科学相对较新,配制技术以及用于评估这些技术的分析、临床和统计方法都在迅速发展。fda指南确定了七类抗滥用配制剂:
1.物理/化学屏障-物理屏障可以防止剂型的咀嚼、压碎、切割、磨损或研磨。化学屏障,例如胶凝剂,可以抵抗常见溶剂如水、模拟生物介质、酒精或其他有机溶剂对阿片类药物的提取。物理和化学屏障可以限制机械操作后的药物释放,或改变药物的物理形式,使其不易被滥用。
2.激动剂/拮抗剂组合-可以添加阿片类拮抗剂来干扰,减少或消除与滥用相关的欣快感。拮抗剂可以是隔离的,仅仅在操作该产品时被释放。例如,可以将药物产品配制为,当吞咽该产品(即以预期方式和完整的方式施用)时,作为拮抗剂的物质不具有临床活性,但如果该产品被压碎并被注射或鼻吸则变得有活性。
3.厌恶剂-可以在产品中添加一些物质,使得以高于指导的剂量操作或使用该剂型时,产生令人不快的效果。例如,制剂可包括研磨和鼻吸后刺激鼻粘膜的物质。
4.输送系统(包括使用储库可注射制剂和植入物)-某些药物释放设计或药物输送方法可以提供抗滥用性。例如,持续释放储库可注射制剂或皮下植入物可能难以操作。
5.新分子实体和前药-新分子实体(nme)或前药的特性可能包括需要酶活化,不同受体结合谱,更慢渗透到中枢神经系统,或其他新的效果。具有抗滥用特性的前药可能为母体阿片类药物的体外转化提供化学屏障,这可能会阻止母体阿片类药物的滥用。为了“管制药品法”(controlledsubstancesact,csa)的目的,对新分子实体和前药进行滥用可能性的评估。
6.组合-可以组合两种或更多种上述方法以阻止滥用。
7.新方法-此类别包含以前类别中未收录的新方法或技术。
尽管基于上面的类别1至5已经已有多个提议,但在提供这些方法的有效组合以及尤其提供新方法方面,仍然存在未满足的需求。
rodriguez-delgado等人的文章。(trendsanal.chem.74(2015):第21-45页)公开了基于漆酶的生物传感器,用于检测食品工业中的苯酚化合物以及用于环境和医学应用,例如,具有固定化漆酶的克拉克(clark)氧电极(bauer等,freseniusj.anal.chem.364(1999);179-183)。
wo98/18909a1公开了用酶转化的转基因生物,其能够在吡啶核苷辅因子之间转移还原当量。
ep0032286a2,us3852157a和us4391904a公开了使用测试表面来分析成对免疫成员(例如,吗啡:辣根过氧化物酶偶联物和羧基甲基-吗啡:乙二酸还原酶)的方法,以检测样品中的抗体。
wo2012/122422a2和us2011/623535a1公开了具有杂环接头的活性剂前药,一旦前药在口服摄入后进入胃肠道,其可以被胃肠酶酶促切割。为了从前药提供药物,需要酶的作用来切割前药以便可控地释放药物。这种前药的供给也用于阻止实际药物的滥用。
us2014/330021a1公开了与氢吗啡酮化学缀合的芳基羧酸,作为阻止滥用的策略。
us2005/176644a1和us2012/178773a1公开了具有与氧可酮(oxycodone)偶联的化学部分的氧可酮衍生物,以阻止滥用或显着降低氧可酮的药理活性。
au2012/201450a1和wo2006/058249a2涉及抗滥用口服剂量制剂,其包含形成凝胶的聚合物,鼻粘膜刺激性表面活性剂和潮红剂以及具有滥用可能性的药物。
所有这些文件都涉及常见和已知的策略用于阻止这些具有滥用潜力的药物如氧可酮的滥用。
不相关领域的现有技术公开了各种组合物,其中酶与试剂或组合物组合用于各种用途:
wo00/27204a1涉及一种抗微生物组合物,其包含氧化还原酶和n-羟基苯胺型增强剂。wo00/27204a1的组合物旨在作为洗涤剂或清洁组合物,但也用作消毒剂或用于油漆、食品、饮料等的保存。
wo01/98518a2涉及通过漆酶和锰过氧化物酶转化生物活性成分(例如抗生素)的方法。根据wo01/98518a2,已知的活性成分应通过漆酶/锰过氧化物酶转化以引入另外的官能团以获得具有改性性质的新活性物质(例如克服对某些抗生素的抗性)。
ep0919628a1公开了一种通过具有多酚氧化活性的酶如漆酶的作用使苯酚化合物或芳香胺化合物“高分子化”的方法。因此,ep0919628a1也公开了酶促方法将某些物质(包括抗微生物剂或病毒感染抑制剂)转化为具有较高分子量的物质,这些物质随后可用作增稠剂、稳定剂以及抗微生物剂或病毒感染抑制剂。还有人建议废水通过高分子化处理来消除苯酚化合物或芳香胺化合物。ep0919628a1提出漆酶,儿茶酚氧化酶,多酚氧化酶,抗坏血酸氧化酶或胆红素氧化酶作为可以(在工业上)用于所公开的方法的酶。
wo97/41215a1涉及工业酶技术及与储存/输送这类酶有关的问题。这些酶或者以干燥形式(其中粉尘形成据说是不利的)或液体制剂(其具有两个缺点:酶不能稳定储存和以其活性状态即与底物反应的状态存在)递送。为防止这种与底物的过早作用,wo97/41215a1提出了在基本上不含水的液体组合物中提供酶和底物,该液体组合物将在含水条件下反应但在无水液体组合物中不反应。
de102006048833a1公开了一种用于治疗骨质疏松症的药物制剂,其包含除胶原和含钙物质(作为主要活性物质)之外的交联剂,其包含交联剂(例如多羟基芳族化合物)和能使交联剂交联的交联反应催化剂(例如,像漆酶这样的酶)。de102006048833a1的目的是建立用于骨支撑的三维基质(“液体骨”)。
wo97/27841a1涉及稳定化的酶制剂,其可以通过双组分分配系统(“分配器”)储存和容易地获得。该文献因此总体上涉及在例如清洁液、洗发剂或维生素制剂中提供酶,例如氧化还原酶或蛋白酶。
wo2005/063037涉及可含有酶的口香糖。酶因其对降解的催化作用而被掺入口香糖中。几乎所有可能的酶都列在此文中,而未用其他底物注解(“配对”)。wo2005/063037的口香糖可以进一步含有药学活性、美容活性或生物活性物质,选自一长串与所述酶无任何相关性的物质。
wo2007/143989a1也涉及一种口香糖,其包含可生物降解的聚合物和作为疏水酶制剂而包含在口香糖中的酶。同样,这种酶是用于降解口香糖(中的可生物降解的聚合物)。因此,在疏水性酶制剂中提供此酶用于防止过早降解。
wo2012/003367a2涉及药物递送方法,其中具有多个长丝的非织造纤维网含有活性剂,其中活性剂从长丝中的释放可以由酶触发。这种非织造长丝不适合口服。
wo00/02464a1涉及通过用酚氧化酶氧化烟草中的酚化合物来处理烟草的方法。
因此,本发明的目的是提供一种用于抗滥用药物制剂的新方法和技术。
因此,本发明提供了一种抗滥用药物组合物,其包含具有滥用潜力的药物,以及能够与酶反应官能团反应的酶(以下称为“药物加工酶”),其中具有酶反应官能团的药物以储存时能够稳定的、具有酶反应性的状态,在没有酶活性作用于该药物的条件下,包含在药物组合物中。
本发明提供了一种新的抗滥用策略(“新方法”),它为存在或不得不假设有滥用风险的几乎所有药物组合物提供了实用的工具箱。这样的原则在现有技术中尚未有人提出或建议。因此,现有技术的组合物(例如上面提到的那些)无一提出或建议包含具有滥用潜力的药物和酶的组合物,其中具有滥用可能性的药物与能够与该药物的酶反应官能团反应的酶一起,以储存时能够稳定的、具有酶反应性的状态,在没有酶活性作用于该药物的条件下,包含在药物组合物中。
抗滥用原则对于每一种药物而言是相同的:将有滥用风险的药物与一或多种酶(可选还有必需的辅因子/共同底物/介体(mediators))一起混合在药用制剂中,处于储存稳定状态(通常是干的状态),其中的酶是可活化的(即,使所述酶处于酶反应性状态);但其中药物制剂中的酶包含在不允许酶活性作用于药物的条件下。因此,药物组合物中可以有例如空间隔离或反应性的隔离。因此,该原则也特别适用于滥用风险高的药物,如阿片类药物,以及镇静剂(tranquilizers)(特别是苯二氮卓类药物(benzodiazepins)),兴奋剂和麻醉剂(narcotics)。
如果药物按预期给药-例如通过食入片剂-则酶被灭活(在口服给药组合物的情况下,优选通过胃中的酸性环境和/或胃肠道中存在的蛋白水解酶来灭活)。如果想从这样的药物组合物中提取活性物质来滥用药物,则酶变为活性并作用于药物,将药物加工成另一种化合物,它要么完全无法再使用,要么具有-至少-较低的滥用潜力,并且因此降低了滥用的积极性(即,使根据本发明的药物组合物具有抗滥用性)。
因此,本发明提供了具有滥用可能性的药物(下文中称为“药物”或“目标药物”)和药物加工酶的组合,一旦有人想用滥用措施对本发明的药物组合物进行加工,以便从本药物组合物中提取该药物,则该药物加工酶被活化。尽管本发明的组合物通常是口服给药,但以滥用方式提取药物常常是为了提供可(静脉内)注射的组合物。药物加工酶原则上是已知的;几乎所有加工特定药物的酶,无论是否含有额外的辅因子/辅底物/介体,如果它们可以适当地制造并且可以在组合物中提供以合适方式(在溶于水溶液时)处理药物的活性,都适用于本发明的组合物。已知酶催化超过5,000种生化反应类型。根据本发明的酶可能需要额外的组分,以便它们可以作用于根据本发明的目标药物。例如,根据本发明的酶可能需要辅助因子,辅底物和/或介体。介体通常是一种电子传递物质但起催化剂的作用(或以与催化剂类似的方式起作用)。辅底物(cosubstrate)(以化学计量的方式)参与到(与目标药物)的反应中。辅因子是在生物化学转化中与药物反应时对酶进行辅助的“辅助分子”。因此,本发明适用于这样的反应,其中,酶催化介体化合物的氧化或还原,而介体化合物再去使目标药物氧化或还原;其中酶催化辅底物与药物的结合;以及第二种酶(或其他酶)催化活化药物的转化。
优选的药物加工酶是特异于药物的各种官能团的,即c3位的甲氧基(下文举例的原子是按氧可酮分子来说的;对于其他类似结构的药物(就像多种阿片类目标药物一样)本领域技术人员可以立即找到相应的官能团),c4和c5之间的环氧基,c6位的氧代基,以及17位的n原子上的甲基。因此,这些优选的酶包括氧化还原酶(特别是单加氧酶),转移酶(如乙酰基酶,磺基转移酶和葡萄糖醛酸基转移酶)和水解酶,尤其环氧化物水解酶。因此,优选的酶是催化药物的o-脱甲基化(尤其是o-脱甲基或o-脱乙基),n-脱烷基化(尤其是n-脱甲基或n-脱乙基),酮还原(keto-reduction),n-氧化,将酮重排成酯(baeyer-villiger反应;用单加氧酶将酮转化为酯(例如环酮至内酯)),环氧-羟基化,酯化,脱酰胺化,过氧化,或脱卤,或给药物添加分子(例如葡萄糖醛酸化,硫酸化和乙酰化)的酶。o-脱甲基化主要导致甲氧基转化为羟基,然后可以通过添加其他分子(包括二聚或聚合)或进一步氧化而发生进一步反应。进一步的反应也可以由第二种酶催化。n-脱甲基化主要产生仲胺基,然后可以通过添加其他分子(包括二聚或聚合)或进一步氧化而进一步反应。同样,该进一步的反应可以由第二种酶催化。酮还原导致酮基转化为羟基,然后通过加入其他分子(包括二聚或聚合)或进一步氧化而进一步反应。同样,该进一步反应也可由第二种酶催化。n-氧化产生n-氧化物化合物,其可直接导致药物失活或随后通过添加其他分子(包括二聚或聚合)而进一步反应。环氧-羟化产生二羟基二醇(通常:反式-二羟基二醇),然后可以通过添加其他分子(包括二聚或聚合)或进一步氧化来进一步反应。分子的添加(例如硫酸化,葡萄糖醛酸化和乙酰化,但也包括二聚或聚合)导致通常不可溶的产物或因加速排泄潜力而被剥夺其滥用潜力的产物。在这些反应中,可加入合成底物(例如在葡萄糖醛酸化中)以增强药物的失活。酯化通过酯酶(对于oh-基团)或反式酯酶(例如对于杜冷丁)进行。脱酰胺化可以通过酰胺酶(ec3.5.1.4)作用于例如芬太尼而进行;过氧化酶(例如ec1.11.2.1)可以在多种p450反应中反应,脱卤素酶(如ec3.8.1)可以对含卤素的目标药物如西博帕多反应。
通过使用这种酶,目标药物被加工成无活性形式或-至少-比目标药物活性低的药剂,因此对那些打算滥用药学目标药物组合物的人的吸引力较小。
已知药物加工酶的实例是nad(p)(h)依赖性氧化还原酶,例如来自醛酮还原酶(akr)超家族的药物还原酶,尤其akr1c1(20alpha-羟基类固醇脱氢酶)(ec1.1.1.149)),akr1c2和akr1c4。特别优选的氧可酮加工酶是3-α-羟基类固醇3-脱氢酶(ec1.1.1.213)。nad(p)(h)依赖性氧化还原酶在nad(p)h存在下将目标药物转化为其还原型降解产物。另一组优选的药物加工酶是酮-类固醇还原酶,如3-,6-和17-酮类固醇还原酶。
根据优选的实施方案,药物加工酶是单加氧酶。单加氧酶能够将一个氧原子插入各种有机底物中。分子氧需要激活才能进行这种类型的反应,并且为此,电子从有机/无机辅因子转移到分子氧。有广泛多种氧化反应被单加氧酶催化,如脂族和芳香族化合物的羟化,烯烃的环氧化,baeyer-villiger氧化,硫氧化,胺氧化,硒化物氧化,卤化,亚磷酸酯氧化和有机硼氧化。
单加氧酶分为以下几个家族:细胞色素p450单加氧酶或血红素-依赖性单加氧酶(ec1.14.13,ec1.14.14,ec1.14.15)是最知名且最大的单加氧酶家族,主要存在于真核生物(哺乳动物,植物,真菌)以及细菌基因组中,能够将非活化的碳原子羟化。血红素铁非依赖性单加氧酶(ec1.14.16)催化羟化和环氧化反应,并利用两个铁原子作为辅因子。属于该家族的酶包括烯烃单加氧酶,酚羟化酶,膜结合型烷烃羟化酶以及芳香单加氧酶。铜依赖性单加氧酶(ec1.14.17和ec1.14.18)代表一个很小的酶家族,需要铜离子进行底物的羟基化。黄素(flavin)依赖性单加氧酶(ec1.13.12和ec1.14.13)主要存在于原核基因组中,并且已知催化环氧化,baeyer-villiger氧化和卤化。另外,发现了几种新型单加氧酶不依赖辅因子就能催化羟基化(辅因子非依赖性单加氧酶),但只接受有限范围的底物。另一方面,解偶联反应可以逆转;这种机制存在于某些单加氧酶的催化循环中,利用过氧化氢产生氧化酶中间体。更普遍和完善的方法涉及nad(p)h的再生。基于化学的再生和基于酶的再生目前都在使用。化学再生可以使用铑配合物催化剂并以甲酸盐作为底物,其被氧化成二氧化碳。由此,电子被转移nad(p)+还原辅酶。同样地,nad(p)h的酶促再生已是成熟的,其是基于广泛多种nad(p)+依赖性脱氢酶如甲酸脱氢酶或葡萄糖-6-磷酸脱氢酶。
优选的酚氧化酶是漆酶(laccase)(ec1.10.3.2),儿茶酚氧化酶(ec1.10.3.1),单酚单加氧酶(ec1.14.18.1),抗坏血酸氧化酶(ec1.10.3.3);过氧化物酶例如辣根过氧化物酶(hrp;ec1.11.1.7)。
根据进一步优选的实施方案,药物加工酶是过加氧酶(peroxygenase)(ec1.11.1和1.11.2)。真菌非特异性过氧化酶(ec1.11.2.1)能够通过将过氧化物携带的氧转移到不同的底物来使各种化合物氧化。这类催化反应类似于由细胞色素p450单加氧酶催化的反应,包括脂族化合物的羟化,直链、支链和环状烯烃的环氧化,脱烷基化,芳香族化合物和杂环化合物的氧化,以及有机杂原子和无机卤化物的氧化。
苯酚产物是芳香过氧化的产物,由于这些酶的过氧化活性,这些苯酚随后可以通过其相应的苯氧基自由基进行偶联和聚合反应。这些酶最常见于担子菌和子囊菌(例如柱状田头菇(agrocybeaegerita),弧形鬼伞(coprinellusradians),轮冠小皮伞(marasmiusrotula))中,也见于毛霉(mucoromycotina),壶菌(chytridiomycota),球囊菌(glomeromycota)以及卵菌(oomycota),但未见于植物、动物或原核生物中。所需的过氧化氢可以通过各种氧化酶原位产生,如葡萄糖氧化酶(ec1.1.3.4),纤维二糖脱氢酶(ec1.1.99.18)或乳酸氧化酶(ec1.1.3.2),通过氧化诸如葡萄糖、寡糖、多糖、乳酸等底物而产生h2o2的酶,以及其他多种可见于配方中者。
酚氧化酶是本发明药物组合物中的优选酶。在本发明的上下文中,酚氧化酶可以是具有过氧化酶活性的酶或漆酶或漆酶相关酶。具有过氧化酶活性的化合物可以是含有酶分类(ec1.11.1.7)中任何过氧化酶、或其表现出过氧化酶活性的任何衍生片段的酶。优选地,根据本发明的过氧化物酶可由植物产生(例如辣根过氧化物酶或大豆过氧化物酶)或由诸如真菌或细菌等微生物产生。一些优选的真菌包括属于半知菌亚门(deuteromycotina)、丝孢菌纲(hyphomycetes)的菌株,例如,鐮孢菌属(fusarium),腐质霉属(humicola),木霉属(tricoderma),漆斑菌属(myrothecium),轮枝菌属(verticillum),arthromyces,卡尔霉属(caldariomyces),细基格孢属(ulocladium),埃里格孢属(embellisia),枝孢属(cladosporium)或凹脐蠕孢属(dreschlera),特别是尖孢镰孢(fusariumoxysporum)(dsm2672),特异腐质霉(humicolainsolens),里氏木霉(trichodermaresii),疣孢漆斑菌(myrotheciumverrucaria)(ifo6113),黄萎轮枝菌(verticillumalboatrum),大丽轮枝菌(verticillumdahlia),arthromycesramosus(fermp-7754),烟霉卡尔霉菌(caldariomycesfumago),纸细基格孢(ulocladiumchartarum),阿利埃里格孢(embellisiaalli)或dreschlerahalodes。其他优选的真菌包括属于担子菌亚门(basidiomycotina)、担子菌纲(basidiomycetes)的菌株,例如,鬼伞属(coprinus),毛平格菌属(phanerochaete),革盖菌属(coriolus)或栓菌属(trametes),特别是灰盖鬼伞(croprinuscinereusf.microsporus)(ifo8371),长根鬼伞(coprinusmacrorhizus),黄孢原毛平革菌(phanerochaetechrysosporium)(例如na-12)或栓菌属(以前称为多孔菌(polyporus)),例如,变色栓菌(trametesversicolor)(例如pr428-a)。进一步优选的真菌包括属于接合菌亚门(zygomycotina)、mycoraceae纲,例如,根霉属(rhizopus)或毛霉属(mucor),特别是冻土毛霉(mucorhiemalis)。一些优选的细菌包括放线菌目(actinomycetales)的菌株,例如类球形链霉菌(streptomycesspheroides)(attc23965)、热紫链霉菌(streptomycesthermoviolaceus)(ifo12382)或轮枝链霉菌轮枝亚种(streptoverticillumverticilliumssp.verticillium)。其他优选的细菌包括球形红细菌(rhodobactersphaeroides),沼泽红胞藻(rhodomonaspalustri),乳链球菌(streptococcuslactis),pseudomonaspurrocinia(atcc15958),荧光假单胞菌(pseudomonasfluorescens)(nrrlb-11)和芽孢杆菌菌株,例如,短小芽孢杆菌(bacilluspumilus)(atcc12905)和嗜热脂肪芽孢杆菌(bacillusstearothermophilus)。进一步优选的细菌包括属于粘球菌属(myxococcus)的菌株,例如变绿粘球菌(m.virescens)。过氧化物酶还可以是,经以下方法能够生成的酶,所述方法包括将重组dna载体转化的宿主细胞在培养基中允许所述过氧化物酶表达的条件下的培养,并从培养中回收所述过氧化物酶,其中所述载体携有编码所述过氧化物酶的dna序列、以及编码允许其表达的功能的dna序列。特别是,重组产生的过氧化酶酶是衍生自鬼伞菌(coprinussp.),特别是长根鬼伞(c.macrorhizus)或灰盖鬼伞(c.cinereus)的过氧化物酶,见wo92/16634a。在本发明的上下文中,具有过氧化物酶活性的化合物包括过氧化物酶和衍生自细胞色素、血红蛋白或过氧化物酶的过氧化物酶活性片段。
过氧化物酶活性(poxu)可以例如通过以下方式测定:一个过氧化物酶单位(poxu)是在下列条件下每分钟催化1μmole过氧化氢转化的酶量:0.1m磷酸盐缓冲液ph7.0,0.88mm过氧化氢,1.67mm2,2'-联氨-双(3-乙基苯并噻唑啉-6-磺酸)(abts)30℃。该反应随后(是在混合15秒后)通过在418nm处吸光度的变化(其应在0.15至0.30的范围内)进行60秒。为了计算活性,氧化型abts的吸收系数为36mm-1cm-1,每2摩尔氧化型abts转化1微摩尔h2o2的化学计量。
优选的酶还包括儿茶酚氧化酶(ec1.10.3.1),胆红素氧化酶(ec1.3.3.5)单酚单加氧酶(ec1.14.18.1),锰过氧化物酶(ec1.11.1.13),单酚单氧化酶(ec1.14.99.1),酪氨酸酶(ec1.14.18.1)和抗坏血酸氧化酶(ec1.10.3.3)。
用作根据本发明的药物加工酶的特别优选的其他酶包括以下酶:
o-脱甲基化(c3):细胞色素p450(ec1.14;+血红素+h-供体,如nad(p)h),尤其cyp2c亚家族;cyp2d6;非特异性单加氧酶(ec1.14.14.1;+nad(p)h),可待因(codeine)3-o-脱甲基酶(codm;ec1.14.11.32;+2-氧化戊二酸(+o2));二甲基吗啡(thebaine)6-o-脱甲基酶(t6odm;ec1.14.11.31;+2-氧化戊二酸(+o2));过氧化物酶(ec1.11.1和ec1.11.2;+h2o2),尤其辣根过氧化物酶(hrp,ec1.11.1.7;+h2o2)和真菌非特异性过加氧酶(ec1.11.2.1)。
优选地,o-脱甲基化与进一步的加工步骤组合,因为羟吗啡酮、α-和β-氧吗啡酚或其它羟吗啡酮样产物可能导致目标药物的这类o-脱甲基化,例如在氧可酮的例子中。由于羟吗啡酮可具有与目标药物相似的滥用可能性,因此可提供另外的步骤(即用另外的羟吗啡酮加工酶处理),例如葡萄糖醛酸化步骤。
n-脱甲基化(n17):cyp1-3(全部:ec1.14.14.1;+血红素+h-供体,如nad(p)h,fad,fmn,铁氧还蛋白等),优选cyp3a,cyp1a,cyp2b,cyp2c和cyp2d,尤其cyp3a4,cyp3a5,cyp3a7,cyp1a2,cyp2b6,cyp2c9,cyp2c19和cyp2d6,尤其cyp3a4和cyp3a5。过氧化物酶(ec1.11.1和ec1.11.2;+h2o2),辣根过氧化物酶(hrp,ec1.11.1.7;+h2o2)。n-脱甲基化可能导致产品如去甲氧可酮(如果例如氧可酮被转化),或者去甲羟吗啡酮,α-和β-noroxycodol,或无滥用潜力或具有低滥用潜力的类似产品(尽管具有某种(但非常低的)阿片类激动剂活性,但远低于氧可酮(也是由于它们很难被摄入大脑))。
酮还原(c6):羰基还原酶(nadph)(ec1.1.1.184;+nad(p)h),如二羟基吗啡酮酮还原酶(dmkr;i至v型)和二羟基可待因酮(codeinone)酮还原酶(dckr,i型和ii型);另外,脱氢酶,如吗啡6-脱氢酶(ec1.1.1.218;+nad(p)h)。酮还原可能导致多种产品,如α-和β-oxycodol,或去甲-6-oxycodol,它们没有(或只有弱的)滥用潜力。
n-氧化(n):含黄素的单加氧酶(ec1.14.13.8;+nad(p),fad)。
环氧-羟基化:微粒体环氧化物水解酶(ec3.3.2.9),环氧化物水合酶(ec3.3.2.3和4.2.1.63),可溶性环氧化物水解酶(ec3.3.2.10)。
葡萄糖醛酸化:udp-葡萄糖醛酸基转移酶(ec2.4.1.17;+udp-葡萄糖醛酸酯),尤其ugt1和ugt2酶,如ugt1.1,ugt2b7,胆红素-葡萄醛酸苷葡萄糖醛酸基转移酶(ec2.4.1.95;+udp-葡萄糖醛酸酯)。在所有情况下,可以用合成的官能化辅底物例如代替udp-葡糖醛酸,以更好地促进目标药物的灭活。
乙酰化:酰基(乙酰基)转移酶(ec2.3)和coa-转移酶(ec2.8.3),尤其n-乙酰基转移酶(nat,ec2.3.1;通常+乙酰基-辅酶a(ac-coa))和o-乙酰基转移酶(oat;ec2.3.1;通常为+ac-coa)。
硫酸化:磺基转移酶(ec2.8.2),尤其人的sult转移酶。
合适的药物加工酶的另一个选择是,从酶数据库选择已知对给定反应类型(例如o-脱甲基化,n-脱甲基化,酮还原,环氧-羟基化,n-氧化,或分子添加(例如葡萄糖醛酸化和乙酰化))有效且特异性的酶,所述数据库例如brenda(braunschweigenzymedatabase)酶入口(http://www.brenda-enzymes.org)。brenda是功能性生化和分子酶数据大信息系统,可以访问七个互连的数据库。
brenda包含270万个关于酶发生,功能,动力学和分子特性的手动注释数据。每个条目都连接到参考生物和来源生物。酶配体与它们的结构一起存储,并且可以通过它们的名称,同义词或通过结构搜索来访问。
frenda(fullreferenceenzymedata)和amenda(automaticminingofenzymedata)基于文本挖掘方法,代表pubmed摘要的完整调查,其中包含不同生物,组织或细胞器中酶的信息。补充数据库drenda在自动搜索和酶病相关信息分类的超过51万个参考文献中提供了超过910000个新的ec编号-疾病联系。kenda(kineticenzymedata),一项新修改,从pubmed摘要中提取并显示动力学值。
enzymedetector的整合提供了原核基因组酶功能注释的自动比较,评估和预测。生化反应数据库bkm-react包含非冗余的酶催化自发反应,并且被开发以促进和加速生化模型的构建。
药物加工酶通常需要辅因子,例如h和/或电子供体和受体,例如nad(p)h,fmn,fad,铁氧还蛋白,2-氧代戊二酸,血红素(cyp超家族);或者用于将基团添加到目标药物的供体(乙酰基(如ac-coa),葡萄糖酸(如udp-葡糖醛酸)等)。这些辅因子也提供在根据本发明的组合物中,除非这些因素已经以任何方式存在于潜在滥用情况中(例如,如果组合物溶于水溶液中,则上述某些氧化反应需要的o2,或环氧-羟基化所需的h2o,可在这种滥用条件下获得;有时甚至需要离子,只要它们包含在提取溶剂中)。在本说明书中,有时明确提及与目标药物进行特异性酶促反应所需的辅因子(并且在本发明组合物中提供,例如作为与酶直接连接的辅基);然而,本领域技术人员充分了解所需的辅因子和适于获得本发明组合物的条件,其中酶活性通常优化为滥用情况,例如,当组合物溶于水或水性缓冲液中时。
在一些实施方案中,可优选在根据本发明的制备中提供酶(及其各自的辅因子)的组合。例如,可以优选添加另外的加工酶,例如葡糖醛酸糖苷酶和/或乙酰转移酶,以进一步加工o-脱甲基化,n-脱甲基化,酮还原环氧-羟基化或n-氧化中出现的目标药物产品,例如通过在新产生的羟基上提供葡糖醛酸化/乙酰化衍生物来加工。如果药物加工本身的结果代表滥用的潜在目的(例如对于羟吗啡酮而言),也可以应用这样的组合。
如果药物加工酶是膜依赖性酶,则此酶可以以脂质体形式提供,优选以干脂质体的形式提供(在这种情况下,可以优选添加辅助物质,例如蔗糖或海藻糖;参见例如sun等,biophys.70(1996):1769-1776)。
根据一个具体实施方案,本发明的药物组合物包含另外的酶,优选另外的药物加工酶或对已加工的药物形式进行进一步加工的酶,尤其漆酶(ec1.10.3.2)。
因此,本发明的一个具体实施方案在本发明组合物中另外提供漆酶。漆酶可以使经过药物处理的分子二聚化或多聚化(或引发或以其他方式促进其多聚化)。虽然漆酶本身可能不直接构成药物加工酶(因为它不处理目标药物本身),但漆酶可与上文公开的药物加工酶一起使用,以进一步增强本发明组合物的抗滥用特性。漆酶也可以与电子介体一起使用以直接氧化目标药物,或与具有某些功能的辅底物(苯酚,芳香胺,双键)一起使用以形成防止滥用的寡聚物或聚合物。漆酶也适合于创制水凝胶,特别是当与形成水凝胶的组分一起使用时,所述组分例如壳聚糖和/或儿茶酚或羧基甲基壳聚糖和/或香草醛(vanillin)。漆酶(ec1.10.3.2;cas登记号80498-15-3)经常被描述和分析为在许多植物、真菌和微生物中发现的含铜氧化酶(riva,trendsinbiotechnology24(2006),219-226)。漆酶作用于苯酚和类似分子,进行单-电子氧化。根据brenda数据库,漆酶的系统名称是苯二酚:氧氧化还原酶。漆酶被定义为一组具有低特异性的多铜蛋白,作用于邻喹啉和对喹啉,并且通常也作用于氨基酚和苯二胺。半醌可以进一步反应,以酶促或非酶促方式。
另外,一些非-漆酶底物可以利用介体进行反应来氧化。当这些得到确认的漆酶介体被漆酶氧化时,它们产生强氧化性反应性物质(自由基,自由基醌和醌),其可进一步与非-漆酶底物反应。如果经漆酶氧化的介体被还原成其原始化合物,则它再次被漆酶再氧化以产生反应性物质,其可再次氧化另一分子。这种漆酶介体能够氧化那些不能被漆酶直接氧化的分子。在漆酶制剂中使用的介体有许多类型,包括以芳香族为中心的介体(aroh;例如阿魏酸,丁香醛)和以氮为中心的介体(rnoh;例如紫尿酸,1-羟基苯并三唑)。
合适的介体在本领域中广泛可用。例如,在wo95/01426a1,wo96/10079a1或wo2012/085016a1中公开了能够增强氧化还原酶(尤其酚-氧化酶,例如漆酶)活性的介体。
另一种策略涉及将辅底物与漆酶一起使用。辅底物被加入到反应中,并被漆酶氧化,随后与非漆酶底物反应并形成共价键,导致产生寡聚物或聚合物。通常,多种漆酶底物可以作为辅底物结合到非漆酶的底物,例如酚(儿茶酚),芳香胺,烯烃等上。
漆酶通过促进单木质醇(一种天然存在的酚类)的氧化偶联而在木质素的形成中发挥作用。漆酶可以是聚合的,而且酶活性形式可以是二聚体或三聚体。其他漆酶,例如由真菌糙皮侧耳菌(pleurotusostreatus)产生的漆酶,在木质素的降解中起作用,因此可以包括在木质素修饰酶的广泛类别中。因为漆酶属于氧化酶家族,它需要氧作为酶促作用的第二底物。分光光度法可用于检测漆酶,使用底物abts(2,2'-联氮-双-(3-乙基苯并噻唑啉-6-磺酸),丁香醛连氮,2,6-二甲氧酚,和二甲基邻苯二胺。活性还可以用氧气传感器监测,因为底物的氧化与氧还原成水的反应是成对的。
本组合物中使用的漆酶可以容易地选出,并在可用性、与所选药物的反应性、有计划的储存以及给药条件方面进行优化。漆酶可从各种来源获得,例如来自真菌,细菌或植物。大多数常见的漆酶也可以重组生产。如果需要一致和连续的量并且在天然来源有问题(例如可能有杂质)的情况下,重组生产是优选的。多种漆酶是工业用的,并因此是能够以大规模生产所需的量获得的。例如真菌漆酶可得自金钱菌(collybia),fomus,香菇(lentinus),侧耳菌(pleurotus),曲霉(aspergillus),链孢霉(neurospora),柄孢壳菌(podospora),射脉菌(phlebia)(齿射脉菌(p.radiate)),革盖菌(毛革盖菌(c.hirsitus)),葡萄孢菌(botrytis),多孔菌(截短多孔菌(p.pinsitus)或变色多孔菌(p.versicolor),立枯丝核菌(rhizoctoniasolani),柱顶孢霉(scytalidium)(嗜热柱顶孢霉(s.thermophilium)),梨孢菌(pyricularia)(米梨孢菌(p.oryzae),鬼伞菌(灰盖鬼伞),栓菌(毛栓菌(t.hirsute),长绒毛栓菌(t.villosa)和变色栓菌),革孔菌(coriolopsis)(粗毛革孔菌(c.gallica)),黄孢原毛平革菌,多年异担子菌(heterobasidionannosum),spinigermeineckellus和嗜热毁丝霉(myceliophthorathermophila);细菌漆酶可获自芽孢杆菌,假单胞菌,链霉菌和固氮螺菌(azospirillum)。特别优选来自长绒毛栓菌(trametesvillosa),嗜热毁丝霉,以及糙皮侧耳菌的漆酶。
优选的漆酶是已经在工业上应用的那些,例如,在rodriguez-delgado等人综述的基于漆酶的生物传感器中使用的那些(trendsanal.chem.74(2015),21-45,尤其该文献的项目2下和表2至5中)。漆酶的其它合适和优选的实例公开在wo00/27204a1中,例如来自真菌的漆酶,包括衍生自曲霉,链孢霉等的漆酶,例如,粗糙链孢霉(n.crassa),柄孢壳菌,葡萄孢菌,金钱菌,层孔菌(fomes),香菇,侧耳菌,栓菌例如长绒毛栓菌和变色栓菌,丝核菌例如立枯丝核菌,鬼伞菌例如灰盖鬼伞、毛头鬼伞(c.comatus)、费奈斯鬼伞(c.friesii)和褶纹鬼伞(c.plicatilis),小脆柄菇属(psathyrella)例如黄盖小脆柄菇(p.condelleana),斑褶菇属(panaeolus)例如蝶形斑褶菇(p.papilionaceus),毁丝霉(myceliophthora)例如嗜热毁丝霉,schytalidium例如s.thermophilum,多孔菌例如截短多孔菌,密孔菌例如朱红密孔菌(p.cinnabarinus),射脉菌例如齿射脉菌(wo92/01046a),或革盖菌例如毛革盖菌(jp2-238885);衍生自细菌的实例包括衍生自芽孢杆菌菌株的漆酶;衍生自鬼伞,毁丝霉,多孔菌,密孔菌,scytalidium或丝核菌的漆酶;衍生自灰盖鬼伞,嗜热毁丝霉,截短多孔菌,朱红密孔菌,scytalidiumthermophilum或立枯丝核菌的漆酶。
测定漆酶活性(lacu)的方法是测定有氧条件下丁香醛连氮氧化反应中的漆酶活性。所产生的紫色在530nm通过分光光度法测量。分析条件是19mm丁香醛连氮,23mm乙酸缓冲液,ph5.5,30℃,1分钟。反应时间。1个漆酶单位(lacu)是在这些条件下每分钟催化1.0μmole丁香醛连氮转化的酶量(wo00/27204a1)。
本发明提供了目标药物与药物加工酶的组合作为抗滥用药物制剂的新方法。本发明所基于的新策略是使用药物加工酶(或酶系统)将药物转化为非活性形式(例如转化为沉淀的或灭活的或活性较低的产物),使其成为不可用的(例如通过将其转化为无活性(或至少:活性较低)形式或通过使该药物不可能用注射器注射)。另一方面,如果目标药物按照预见的方式给药(例如口服),来自身体的蛋白酶(或胃和小肠的总环境)使药物加工酶变得不活跃,目标药物可以在不被伴随的酶灭活的情况下展开其效果。为了改善蛋白酶可降解性,可以通过引入(额外的)蛋白酶切割位点来修饰药物加工酶,以便增加这些酶暴露于这类蛋白酶后的降解速率。
根据本发明的抗滥用策略的先决条件是,在储存期间和使用前,含有目标药物和药物加工酶的组合的本发明组合物保持在药物加工酶不(尚未)与目标药物反应的环境中。这可以是例如通过在药物加工酶失活的条件下保持(储存)两种组分或通过两种组分的空间分隔来确保。例如,如果组合物保持干燥形式,则药物加工酶不能与目标药物反应,因为这种反应需要水性条件。一旦将本发明的干燥组合物溶于水中(例如,为了提取阿片类药物进行滥用),药物加工酶可以与目标药物反应并将目标药物酶促转化为因其降解或聚合而不再能被使用(滥用)的分子。防止药物加工酶对目标药物起反应的另一个例子是,将目标药物加工酶与目标药物进行空间分隔,以便-同样地-只有在组合物与水或类似溶剂接触后,药物-加工酶才可以对目标药物起反应。这种空间分离可以例如通过在药物制剂的不同区室中提供药物加工酶和目标药物,通过提供特定的包衣,通过分开制粒等来建立。.
另一方面,本发明组合物中的药物加工酶必须是反应性的,例如,一旦暴露于水环境或其他与预期给药途径或给药活动不一致的情况(即如果很可能滥用),它必须与伴随的目标药物反应,以防止或至少阻止滥用该药物。
本发明的抗滥用新策略原则上适用于任何具有滥用风险的目标药物。对于每种这样的药物,可以根据本说明书中给出的基本原理找到合适的酶(或酶系统)。
本发明的优选目标药物是那些具有最高滥用潜力的药物,尤其阿片类,替代型安非他明,巴比妥类,苯二氮卓类药物(特别是氟硝西平,奥沙西平(oxazepam),阿普唑仑,劳拉西平,地西平和氯硝西平),可卡因,甲喹酮(methaqualone),大麻(cannabis)。适用本发明抗滥用策略的阿片类药物选自吗啡(morphine),他喷他多,氧可酮(oxycodone),丁丙诺啡,西博帕多(cebranopadol),二乙酰吗啡(=海洛因),二羟基可待因,乙基吗啡,氢可酮(hydrocodone),氢吗啡酮,美沙酮(methadone)和左美沙酮,羟吗啡酮,喷他佐辛(pentazocine),杜冷丁(pethidine),芬太尼(fentanyl),左啡诺(levorphanol)和左美沙芬(左美沙芬e)以及可药用的盐,酯,前药,还有它们的混合物。
其它优选的目标药物可以是选自阿片(opiates),阿片类物质(opioids),镇静剂(tranquillizers),优选苯二氮平类药物(benzodiazepines),兴奋剂和其它麻醉剂(narcotics)。本发明的药物剂型特别适用于防止选自下组的阿片,阿片类物质,镇静剂,和其他麻醉剂的滥用:n-{1-[2-(4-乙基-5-氧-2-四唑-1-基)乙基]-4-甲氧基甲基-4-哌啶基}丙酰苯胺(阿芬太尼),5,5-二烯丙基巴比妥酸(allobarbital),烯丙普鲁汀(allylprodine),阿法普鲁汀(alphaprodine),8-氯-1-甲基-6-苯基-4h-[1,2,4]三唑[4,3-a][1,4]-苯二氮平(阿普唑仑),2-二乙基氨苯丙酮(安非拉酮),(±)-[alpha]-甲基苯乙基胺(安非他明),2-([alpha]-甲基苯乙基氨)-2-苯乙腈(安非他尼),5-乙基-5-异戊基巴比妥酸(amobarbital)阿尼利定,阿朴可待因(apocodeine),5,5-二乙基巴比妥酸(barbital),苄基吗啡,贝齐米特(bezitramide),7-溴-5-(2-吡啶基)-1h-1,4-苯二氮平-2(3h)-酮(溴西平),2-溴-4-(2-氯苯基)-9-甲基-6h-噻吩并[3,2-f][1,2,4]三唑[4,3-a][1,4]二氮平(溴替唑仑),17-环丙基甲基-4,5[alpha]-环氧-7[alpha][(s)-1-羟基-1,2,2-三甲基-丙基]-6-甲氧基-6,14-内-吗啡乙-3-醇(丁丙诺啡),5-丁基-5-乙基巴比妥酸(butobarbital),布托菲诺(butorphanol),(7-氯-1,3-二羟基-1-甲基-2-氧-5-苯基-2h-1,4-苯二氮平-3-基)二甲基氨基甲酸盐(卡马西平),(1s,2s)-2-氨-1-苯基-1-丙醇(去甲伪麻黄碱(cathine)/d-正伪麻黄碱),7-氯-n-甲基-5-苯基-3h-1,4-苯二氮平-2-基氨基4-氧化物(氯二氮平氧化物),7-氯-1-甲基-5-苯基-1h-1,5-苯二氮平-2,4(3h,5h)-二酮(氯巴占(clobazam)),5-(2-氯苯基)-7-硝基-1h-1,4-苯二氮平-2(3h)-酮(氯硝西平),氯尼他秦(clonitazene),7-氯-2,3-二羟基-2-氧-5-苯基-1h-1,4-苯二氮平-3-羧酸(氯拉卓酸),5-(2-氯苯基)-7-乙基-1-甲基-1h-噻吩并[2,3-e][1,4]二氮平-2(3h)-酮(氯噻西平),10-氯-11b-(2-氯苯基)-2,3,7,11b-四氢恶唑[3,2-d][1,4]苯二氮平-6(5h)-酮(氯恶唑仑),(-)-甲基-[3[beta]-苯甲酰氧-2[beta](1[alpha]h,5[alpha]h)-羧酸托品酯](可卡因),4,5[alpha]-环氧-3-甲氧基-17-甲基-7-吗啡-6[alpha]-醇(可待因),5-(1-环己烯基)-5-乙基巴比妥酸(环巴比妥),环啡烷(cyclorphan),环丙诺菲(cyprenorphine),7-氯-5-(2-氯苯基)-1h-1,4-苯二氮平-2(3h)-酮(地落西平),二氢脱氧吗啡(desomorphine),右吗拉胺(dextromoramide),(+)-(1-苄基-3-二甲基氨-2-甲基-1-苯基丙基)丙酸盐(右丙氧芬(dextro丙氧酚)),地佐辛(dezocine),地恩丙胺(diampromide),diamorphone,7-氯-1-甲基-5-苯基-1h-1,4-苯二氮平-2(3h)-酮(地西平(diazepam)),4,5[alpha]-环氧-3-甲氧基-17-甲基-6[alpha]-吗啡烷醇(二羟基可待因),4,5[alpha]-环氧-17-甲基-3,6[alpha]-吗啡烷二醇(二羟基吗啡),地美沙朵(dimenoxadol),dimephetamol,二甲基噻吩丁烯胺(thiambutene),丁酸二异辛酯,地匹哌酮(dipipanone),(6ar,10ar)-6,6,9-三甲基-3-戊基-6a,7,8,10a-四氢-6h-苯并[c]chromen-1-醇(屈大麻酚),依他佐辛(eptazocine),8-氯-6-苯基-4h-[1,2,4]三唑[4,3-a][1,4]苯二氮平(艾司唑仑),依索庚嗪(ethoheptazine),乙基甲基噻吩丁烯胺,乙基[7-氯-5-(2-氟苯基)-2,3-二羟基-2-氧-1h-1,4-苯二氮平-3-羧酸盐](氯氟乙酯),4,5a-环氧-3-乙氧基-17-甲基-7-吗啡-6a-醇(乙基吗啡),依托尼秦(etonitazene),4,5[alpha]-环氧-7[alpha]-(1-羟基-1-甲基丁基)-6-甲氧基-17-甲基-6,14-内-吗啡乙-3-醇(埃托啡),n-乙基-3-苯基-8,9,10-三降冰片-2-基胺(fencamfamine),7-[2-([alpha]-甲基苯乙基氨)乙基]-茶碱)(芬乙茶碱),3-([alpha]-甲基苯乙基氨)丙腈(芬普雷斯),n-(1-苯乙基-4-哌啶基)丙酰苯胺(芬太尼),7-氯-5-(2-氟苯基)-1-甲基-1h-1,4-苯二氮平-2(3h)-酮(氟地西平),5-(2-氟苯基)-1-甲基-7-硝基-1h-1,4-苯二氮平-2(3h)-酮(氟硝西平),7-氯-1-(2-二乙基氨乙基)-5-(2-氟苯基)-1h-1,4-苯二氮平-2(3h)-酮(氟西平),7-氯-5-苯基-1-(2,2,2-三氟乙基)-1h-1,4-苯二氮平-2(3h)-酮(哈拉西平),10-溴-11b-(2-氟苯基)-2,3,7,11b-四氢[1,3]恶唑[3,2-d][1,4]苯二氮平-6(5h)-酮(卤恶唑仑),海洛因,4,5[alpha]-环氧-3-甲氧基-17-甲基-6-吗啡烷酮(氢可酮),4,5[alpha]-环氧-3-羟基-17-甲基-6-吗啡烷酮(氢吗啡酮),羟基杜冷丁,异美沙酮,羟基甲基吗啡烷,11-氯-8,12b-二羟基-2,8-二甲基-12b-苯基-4h-[1,3]氧联氮[3,2-d][1,4]苯二氮平-4,7(6h)-二酮(凯他唑仑),1-[4-(3-羟基苯基)-1-甲基-4-哌啶基]-1-丙酮(凯托米酮(ketobemidone)),(3s,6s)-6-二甲基氨-4,4-二苯基庚-3-基乙酸酯(左乙酰美沙醇(levacetylmethadol,laam)),(-)-6-二甲基氨-4,4-二苯酚-3-庚酮(左美沙酮),(-)-17-甲基-3-吗啡烷醇(左啡诺),左苯甲酰甲基吗啡,洛芬太尼(lofentanil),6-(2-氯苯基)-2-(4-甲基-1-哌嗪基亚甲基)-8-硝基-2h-咪唑并[1,2-a][1,4]-苯二氮平-1(4h)-酮(氯普唑仑),7-氯-5-(2-氯苯基)-3-羟基-1h-1,4-苯二氮平-2(3h)-酮(劳拉西平),7-氯-5-(2-氯苯基)-3-羟基-1-甲基-1h-1,4-苯二氮平-2(3h)-酮(氯甲西平),5-(4-氯苯基)-2,5-二羟基-3h-咪唑并[2,1-a]异吲哚-5-醇(马吲哚),7-氯-2,3-二羟基-1-甲基-5-苯基-1h-1,4-苯二氮平(咪达唑仑),n-(3-氯丙基)-[alpha]-甲基苯乙基胺(美分雷司),杜冷丁(meperidine),2-甲基-2-丙基三亚甲基二氨基甲酸盐(meprobamate),美普他酚(meptazinol),美他佐辛(metazocine),甲基吗啡,n,[alpha]-二甲基苯乙基胺(甲基安非他明(metamphetamine)),(±)-6-二甲基氨-4,4-二苯酚-3-庚酮(美沙酮),2-甲基-3-o-甲苯基-4(3h)-喹唑啉酮(甲喹酮),甲基[2-苯基-2-(2-哌啶基)乙酸](哌甲酯(methylphenidate)),5-乙基-1-甲基-5-苯基巴比妥酸(甲基苯巴比妥),3,3-二乙基-5-甲基-2,4-哌啶二酮(甲普龙(methyprylon)),麦托朋(metopon),8-氯-6-(2-氟苯基)-1-甲基-4h-咪唑并[1,5-a][1,4]苯二氮平(咪达唑仑(midazolam)),2-(二苯甲基亚磺酰基)乙酰胺(modafinil),4,5[alpha]-环氧-17-甲基-7-吗啡n-3,6[alpha]-二醇(吗啡),密罗啡因(myrophine),(±)-反式-3-(1,1-二甲基庚基)-7,8,10,10[alpha]-四氢-1-羟基-6,6-二甲基-6h-二苯并-[b,d]吡喃-9(6[alpha]h)-酮(nabilone),纳布啡(nalbuphine),纳洛芬(nalorphine),那碎因(narceine),尼可吗啡(nicomorphine),1-甲基-7-硝基-5-苯基-1h-1,4-苯二氮平-2(3h)-酮(硝甲西平(nimetazepam)),7-硝基-5-苯基-1h-1,4-苯二氮平-2(3h)-酮(硝西平(nitrazepam)),7-氯-5-苯基-1h-1,4-苯二氮平-2(3h)-酮(去甲西平(nordazepam)),去甲左啡诺(norlevorphanol),6-二甲基氨-4,4-二苯基-3-己酮(去甲美沙酮(normethadone)),去甲吗啡(normorphine),诺匹哌酮(norpipanone),罂粟(papaversomniferum)植物提取物(阿片(opium)),7-氯-3-羟基-5-苯基-1h-1,4-苯二氮平-2(3h)-酮(奥沙西平),(顺-反)-10-氯-2,3,7,11b-四氢-2-甲基-11b-苯基恶唑[3,2-d][1,4]苯二氮平-6-(5h)-酮(奥沙唑仑(oxazolam)),4,5[alpha]-环氧-14-羟基-3-甲氧基-17-甲基-6-吗啡烷酮(氧可酮),羟吗啡酮,罂粟(包括亚种)植株或其一部分,阿片全碱(papaveretum),2-亚氨基-5-苯基-4-恶唑烷酮(pernoline),1,2,3,4,5,6-六氢-6,11-二甲基-3-(3-甲基-2-丁烯基)-2,6-methano-3-benzazocin-8-醇(喷他佐辛),5-乙基-5-(1-甲基丁基)-巴比妥酸(戊巴比妥),乙基(1-甲基-4-苯基-4-哌啶羧酸)(杜冷丁),苯吗庚酮(phenadoxone),非诺啡烷(phenomorphane),非那佐辛(phenazocine),苯哌利定(phenoperidine),匹米诺定(piminodine),酚可待因,3-甲基-2-苯基吗啉(苯甲吗啉(phenmetrazine)),5-乙基-5-苯基巴比妥酸(苯巴比妥),[alpha],[alpha]-二甲基苯乙基胺(芬特明(phentermine)),7-氯-5-苯基-1-(2-丙炔基)-1h-1,4-苯二氮平-2(3h)-酮(匹那西平(pinazepam)),[alpha]-(2-哌啶基)二苯甲基醇(哌苯甲醇(pipradrol)),1'-(3-氰基-3,3-二苯基丙基)[1,4'-二哌啶]-4'-羧酰胺(哌腈米特(piritramide)),7-氯-1-(环丙基甲基)-5-苯基-1h-1,4-苯二氮平-2(3h)-酮(普拉西平(prazepam)),profadol,普罗庚嗪(proheptazine),promedol,丙哌利定(properidine),丙氧酚(propoxyphene),n-(1-甲基-2-哌啶基乙基)-n-(2-吡啶基)丙酰胺,甲基{3-[4-甲氧基羰基-4-(n-苯基propanamido)哌啶基]丙酸酯}(瑞芬太尼(remifentanil)),5-仲-丁基-5-乙基巴比妥酸(仲丁巴比妥(secbutabarbital)),5-烯丙基-5-(1-甲基丁基)-巴比妥酸(司可巴比妥(secobarbital)),n-{4-甲氧基甲基-1-[2-(2-噻吩基)乙基]-4-哌啶基}丙酰苯胺(舒芬太尼(sufentanil)),7-氯-2-羟基-甲基-5-苯基-1h-1,4-苯二氮平-2(3h)-酮(替马西平(temazepam)),7-氯-5-(1-环己烯基)-1-甲基-1h-1,4-苯二氮平-2(3h)-酮(四氢西平(tetrazepam)),乙基(2-二甲基氨-1-苯基-3-环己烯-1-羧酸)(痛立定(tilidine),顺式和反式)),曲马多(tramadol),8-氯-6-(2-氯苯基)-1-甲基-4h-[1,2,4]三唑[4,3-a][1,4]苯二氮平(三唑仑(triazolam)),5-(1-甲基丁基)-5-乙烯基巴比妥酸(乙烯比妥(vinylbital)),(1r*,2r*)-3-(3-二甲基氨-1-乙基-2-甲基-丙基)-苯酚,(1r,2r,4s)-2-(二甲基氨)甲基-4-(p-氟苄基氧)-1-(m-甲氧基苯基)环己醇,在每种情况下,任选地为相应的立体异构化合物和相应的衍生物的形式,特别是酯或醚,以及各自相应的生理学上可接受的化合物,特别是盐和溶剂化物。
特别优选的阿片类物质(opioids)可以选自含有酚羟基的阿片类物质,诸如吗啡(morphine),他喷他多(tapentadol),氢吗啡酮(hydromorphone),埃托啡(etorphine),二氢脱氧吗啡(desomorphine),羟吗啡酮(oxymorphone),丁丙诺啡(buprenorphine),包含苯丙氨酸残基的阿片肽,诸如adrenorphin,amidorphin,酪啡肽(casomorphin),dadle([d-ala2,d-leu5]-脑啡肽(enkephalin)),damgo([d-ala2,n-mephe4,gly-醇]-脑啡肽),皮啡肽(dermorphin),内吗啡肽(endomorphin),吗啡感受素(morphiceptin),以及trimu5(l-酪氨酰-n-{[(3-甲基丁基)氨]乙酰基}-d-丙氨酰胺(alaninamide));东罂粟碱(oripavine),6-mddm(6-亚甲基二羟基脱氧吗啡),氯纳曲胺(chlornaltrexamine),二羟基吗啡,氢吗啡醇(hydromorphinol),甲基desorphine,n-苯乙基正吗啡,ram-378(7,8-二羟基-14-羟基-n-苯乙基正吗啡),异可待因(heterocodeine),7-螺环茚满基(spiroindanyl)羟吗啡酮,morphinone,戊吗啡酮(pentamorphone),司吗啡酮(semorphone),氯吗啡(chloromorphide),纳布啡,oxymorphazone,1-碘代吗啡,吗啡-6-葡糖苷酸(glucuronide),6-单乙酰基吗啡,去甲吗啡,吗啡-n-氧化物,环啡烷,dextrallorphan,左啡诺,左芬啡烷(levophenacylmorphan),去甲左啡诺,奥昔啡烷(oxilorphan),非诺啡烷(phenomorphan),毛乙基去甲左啡诺(furethylnorlevorphanol),佐尔啡诺(xorphanol),布托菲诺,6,14-内亚乙烯四氢东罂粟碱,bu-48(n-环丙基甲基-[7α,8α,2',3']-环己醇'[s]-羟基-6,14-内-亚乙烯四氢去甲东罂粟碱),丁丙诺啡,环丙诺菲,二羟基埃托啡,埃托啡,去甲丁丙诺啡,5'-胍基纳曲吲哚(guanidinonaltrindole),二丙诺啡(diprenorphine),左洛啡烷(levallorphan),甲基纳曲酮(methylnaltrexone),纳呋拉啡(nalfurafine),纳美芬(nalmefene),纳洛刹腙(naloxazone),纳洛酮(naloxone),纳洛芬,纳曲酮,纳曲本(naltriben),纳曲吲哚,6β-纳曲醇(naltrexol)-d4,伪吗啡(pseudomorphine),纳洛肼(naloxonazine),norbinaltorphimine,阿拉佐辛(alazocine),布瑞玛佐辛(bremazocine),地佐辛,可他佐辛(ketazocine),美他佐辛,喷他佐辛,非那佐辛,环佐辛(cyclazocine),羟基杜冷丁(bemidone),凯托米酮,优选吗啡,他喷他多,丁丙诺啡,尤其吗啡。具有酚氨基的阿片类药物的一个例子是阿尼利定。上述这些阿片类药物可以例如被漆酶作为药物加工酶来加工。
本发明特别优选的药物组合物是其中具有滥用潜力的药物选自下组的那些组合物:吗啡,氧可酮,他喷他多,二乙酰基吗啡,氢吗啡酮,美沙酮,羟吗啡酮,和二羟基可待因。
优选地,吗啡在c3位发生酚-氧化,起作用的是漆酶(ec1.10.3.2)和相关酶,例如,儿茶酚氧化酶(ec1.10.3.1),单酚单加氧酶(ec1.14.18.1),抗坏血酸氧化酶(ec1.10.3.3),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);发生n-脱烷基化,起作用的是混合氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);在c6位发生酮还原/oh氧化,起作用的是吗啡脱氢酶(ec1.1.1.218),仲醇氧化酶(ec1.1.3.18);在n17发生n-氧化,起作用的是过氧化物酶/过加氧酶(ec1.11),fad-单加氧酶(ec1.14.13.8);在c4/5位被环氧化物水解酶(ec3.3.2.9)催化而环氧羟化;被其他加氧酶活性作用并额外引入氧,被酚2-单加氧酶(ec1.14.13.7)催化而酚羟基化;在c3/c6位添加额外的分子,起作用的是葡萄糖醛酸基转移酶,n-乙酰基转移酶,磺基转移酶,o-甲基转移酶(ec2.1.1)。
优选地,他喷他多在c1位酚-氧化,起作用的是漆酶(ec1.10.3.2)和相关酶:例如儿茶酚氧化酶(ec1.10.3.1),单酚单加氧酶(ec1.14.18.1),抗坏血酸氧化酶(ec1.10.3.3),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);n-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);n-氧化,起作用的是过氧化物酶/过加氧酶(ec1.11),fad-单加氧酶(ec1.14.13.8);被其他加氧酶活性作用,被cyp2d6催化而羟化;在c1位添加额外的分子,起作用的是葡萄糖醛酸基转移酶和n-乙酰基转移酶。
优选地,氧可酮发生o-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp2d6);单加氧酶(ec1.14);过氧化物酶,例如辣根过氧化物酶(ec1.11.1.7);n-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);酮还原/oh氧化,起作用的是3alpha-羟基类固醇3-脱氢酶(ec1.1.1.213);nadph脱氢酶(oye);20alpha-羟基类固醇脱氢酶(ec1.1.1.149);在n17位发生n-氧化,起作用的是过氧化物酶/过加氧酶(ec1.11),fad-单加氧酶ec1.14.13.8);在c4/5位发生环氧-羟化,起作用的是环氧化物水解酶(ec3.3.2.9);被非特异性单加氧酶(ec1.14.14.1)催化,被其他加氧酶活性作用并额外引入氧,被单加氧酶(ec1.14.13.7)催化而发生baeyer-villiger反应;被醛缩酶(ec4.1.2)催化发生醇醛缩合(二聚化)。
优选地,二乙酰基吗啡发生n-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);在n17位发生n-氧化,起作用的是过氧化物酶/过加氧酶(ec1.11),fad-单加氧酶(ec1.14.13.8);在c4/5位发生环氧-羟化,起作用的是环氧化物水解酶(ec3.3.2.9);被其他加氧酶活性作用并额外引入氧;脱乙酰化而除去一些分子,作用酶是水解酶例如酯酶,角质化酶(cutinases);羧基酯酶(ec3.1.1.1),乙酰基酯酶(ec3.1.1.6);胆碱酯酶(ec3.1.1.8).
优选地,氢吗啡酮在c3发生酚-氧化,起作用的是漆酶(ec1.10.3.2)和相关酶:例如儿茶酚氧化酶(ec1.10.3.1),单酚单加氧酶(ec1.14.18.1),抗坏血酸氧化酶(ec1.10.3.3),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);n-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14);在c6发生酮还原/oh氧化,起作用的是3alpha-羟基类固醇3-脱氢酶(ec1.1.1.213),nadph脱氢酶(oye);在n17位发生n-氧化,起作用的是过氧化物酶/过加氧酶(ec1.11),fad-单加氧酶(ec1.14.13.8);在c4/5位发生环氧-羟化,起作用的是环氧化物水解酶(ec3.3.2.9);被其他加氧酶活性作用,被环加氧酶(ec1.14.99.1)作用,被非特异性单加氧酶(ec1.14.14.1)作用,二羟基吗啡的形成,baeyer-villiger反应,被酚2-单加氧酶(ec1.14.13.7)催化而酚羟基化;在c3添加分子,作用酶是葡萄糖醛酸基转移酶,n-乙酰基转移酶,磺基转移酶;被醛缩酶(ec4.1.2)催化发生醇醛缩合(二聚化)。
优选地,美沙酮发生n-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);在c5发生酮还原/oh氧化生成美沙醇,起作用的是nadph脱氢酶(ove);被其他加氧酶活性作用,被单加氧酶(ec1.14.13)催化,额外引入氧并形成酚基,是通过baeyer-villiger反应。
优选地,羟吗啡酮在c3发生酚-氧化,起作用的是漆酶(ec1.10.3.2)和相关酶,例如儿茶酚氧化酶(ec1.10.3.1),单酚单加氧酶(ec1.14.18.1),抗坏血酸氧化酶(ec1.10.3.3),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);n-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);酮还原/oh氧化,起作用的是3alpha-羟基类固醇3-脱氢酶(ec1.1.1.213),nadph脱氢酶(oye);在n17位发生n-氧化,起作用的是过氧化物酶/过加氧酶(ec1.11),fad-单加氧酶(ec1.14.13.8);在c4/5位发生环氧-羟化,起作用的是环氧化物水解酶(ec3.3.2.9);被其他加氧酶活性作用并额外引入氧,被酚2-单加氧酶(ec1.14.13.7)催化而酚羟基化;在c3添加分子,起作用的是葡萄糖醛酸基转移酶,n-乙酰基转移酶,磺基转移酶;被醛缩酶(ec4.1.2)催化发生醇醛缩合(二聚化)。
优选地,二羟基可待因发生o-脱烷基化和n-脱烷基化,起作用的是混合功能氧化酶cyt.p450(cyp3a4;cyp2c8),单加氧酶(ec1.14),过氧化物酶例如辣根过氧化物酶(ec1.11.1.7);在c6发生酮还原/oh氧化,起作用的是吗啡脱氢酶(ec1.1.1.218),仲醇氧化酶(ec1.1.3.18),可待因酮还原酶(ec1.1.1.247);在n17位发生n-氧化,起作用的是过氧化物酶/过加氧酶(ec1.11),fad-单加氧酶(ec1.14.13.8);在c4/5位发生环氧-羟化,起作用的是环氧化物水解酶(ec3.3.2.9);被其他加氧酶活性作用并额外引入氧;在c3/c6位添加分子,起作用的是葡萄糖醛酸基转移酶,n-乙酰基转移酶,磺基转移酶.
本发明特别优选的药物组合物因此包含吗啡,氧可酮,他喷他多,二乙酰基吗啡,氢吗啡酮,美沙酮,羟吗啡酮,或二羟基可待因(作为有滥用潜力的药物),并包含上述的酶(作为药物加工酶)。
本发明优选的药物组合物包含选自下组的作为药物/药物加工酶形式的组合:吗啡/漆酶,他喷他多/漆酶,羟吗啡酮/漆酶,氢吗啡酮/漆酶,喷他佐辛/漆酶,丁丙诺啡/漆酶,二乙酰基吗啡/水解酶/漆酶,左啡诺/漆酶,和氧可酮/漆酶/氧可酮-加工酶。
本药物组合物可以按预期的(非抗滥用)给药途径进行配制,必要时,适应于本发明(例如当药物加工酶和目标药物在空间上隔开时)。优选地,本发明药物组合物以剂量单位形式提供。因此,优选本组合物是片剂,例如迷你片剂(即直径为3mm或以下的小片剂),包衣-核心片剂(包衣片剂),双层片剂,多层片剂,胶囊,泡腾(effervescent)片剂,可溶性片剂,可分散的片剂,球团剂(pellet),mups(多单元球团系统),粒剂(granulate),粉剂(powder),尤其它们的包衣、糖衣和/或功能性包衣(例如肠衣)形式。肠衣特别有利于预防药物加工酶过早失活,即在生理蛋白酶对药物加工酶起作用之前预防。肠衣通常定义为在口服用药情形中保护药物免受胃酸损害的聚合物屏障。因此肠衣通常在胃中强酸性ph下是稳定的,但在肠道(即离开胃后)的较弱酸性(相对更碱性;ph值7-9)ph下迅速分解。用于这类肠衣的典型物质/材料是虫胶(shellac),纤维素乙酸酯邻苯二甲酸酯(cap),聚乙烯乙酸邻苯二甲酸酯(pvap),羟丙基甲基纤维素邻苯二甲酸酯,和甲基丙烯酸酯共聚物,或玉米醇溶蛋白,例如,以及疏水或亲水聚合物,和这些物质的混合物,如果适当的话。疏水聚合物包衣包括丙烯酸聚合物,丙烯酸共聚物,甲基丙烯酸聚合物或甲基丙烯酸共聚物,其中包括
优选的肠衣材料是甲基丙烯酸酯-甲基丙烯酸共聚物,纤维素乙酸琥珀酸酯,羟丙基甲基纤维素邻苯二甲酸酯,羟丙基甲基纤维素乙酸琥珀酸酯,聚乙烯乙酸邻苯二甲酸酯(pvap),甲基丙烯酸甲酯-甲基丙烯酸共聚物,虫胶,纤维素乙酸偏苯三酸酯,海藻酸钠和玉米醇溶蛋白。
本发明药物组合物的另一实施方案是包衣组合物,其中所述包衣包含药物加工酶。当包衣组合物溶于水性液体(用于提取药物(阿片类))时,药物加工酶作用于目标药物,而在(按处方指示的(口服)给药途径)摄入胃或肠后,药物加工酶立即被破坏或灭活。
由于本发明药物制剂是打算给需要其中的药物的人类患者施用,故这些制剂都依据gmp(优选依据欧洲药典标准)来制造并完成为药物制剂。这意味着,本发明的药物制剂是以适当无菌的、洁净的、并且是适当包裹的形式在市场上销售,符合药品监管部门对上市销售的药品的要求,尤其符合ema对阿片类药物如吗啡或氧可酮的要求。
特别优选的实施方案是这样一种组合物,其中所述药物加工酶有包衣,只要是按事先计划的给药途径用药,就能保持药物加工酶对目标药物无活性,即,在有包衣的情形下,例如直至(仍有包衣)的药物加工酶被患者排泄,都能保持药物加工酶的活性不作用于目标药物,而滥用活动则破坏包衣,使得药物加工酶立即作用于目标药物。例如,药物加工酶可以由上述一或多种用于肠衣的物质/材料,例如
所述药物组合物优选包含不抗滥用的原始组合物中设想的量的目标药物。因此,目标药物优选含量为每剂量单位0.1至5000mg(即0.1mg至5克),优选0.5至1000毫克,特别是1到500毫克。目前市售的药学目标药物制剂含有2.5,5,7.5,10,15,20,30,40,80,120或160毫克的药物,尤其氧可酮,例如为盐的形式,如盐酸盐。因此,这样的单个剂量单位中目标药物的优选量可以是0.5至500毫克,尤其1至200mg。根据制剂和正常施用期间药物加工酶的预期活性,目标药物的量也可以增加(与不抗滥用的原始组合物相比,即与无抗滥用特征的目标药物的药学制剂相比)例如以补偿药物活性的可能损失(如果活性的这类轻微损失是很可能的或是不能完全排除的)。
在本药物组合物中药物加工酶的量可以主要基于目标药物的量和制剂的细节来调整。确定优选的药物加工酶的说明性例子已知实施例章节列出。
更具体地,本药物组合物中药物加工酶的量可主要基于药量、酶反应性和制剂细节来调整。例如,药物加工酶在组合物中的添加量可以是0.1至10,000个单位(即0.1u至10ku)。根据一优选实施方案(例如,漆酶用作药物加工酶),漆酶含量为1至1000个单位(即1u至1ku),优选为10至100个单位。有几种方法来确定漆酶活性。对于本发明,在25℃、100mm磷酸钠缓冲液100(ph7)中,通过分光光度法监测420nm处(ε=11.4mlμmol-1cm-1)的abts氧化,以此来测定活性。酶活性以单位来表示,一个单位(u)定义为,每分钟催化1μmoleabts转化的酶量(1u=μmolmin-1)(下文称“本发明的漆酶测试”)。
本发明优选的药物组合物是干的组合物,通常具有(远)低于10%的含水量,优选含水量低于5%,尤其低于2%。
含水量优选用本领域已接受的方法来确定,例如,欧洲药典的指定方法。一个测定水含量的特别优选方法是karlfischer滴定法(欧洲药典8.5(2015),2.5.12,水的半定量),其中也包括结晶物的水。
尽管本发明提供了抗滥用药物的一个全新策略,本新方法也可组合于其他抗滥用策略,例如已在fda指导2015中、或在schaeffer,j.med.toxicol.8(2012),400-407被鉴定的那些。因此,本发明的药物组合物优选包含另外的抗滥用特征,例如选自:物理或化学屏障,尤其增加片剂硬度,(药物加工酶不敏感型)药物拮抗剂,厌恶组分,抗滥用递送系统和前药。特别优选提供物理屏障,尤其增加片剂硬度,或厌恶组分,尤其胶凝剂和/或非交凝增粘剂(例如λ角叉菜胶)或,例如催吐剂或鼻刺激剂。例如,本组合物可以是电阻大于400n,尤其大于500n的制剂,参见欧洲药典(ph.eur.8(2014)2.9.8)。可与本发明组合的抗滥用特征的其他例子是提供,离散的机械增强颗粒(wo2012/061779a1),亲水且疏水的材料(wo2012/112952a1),酸可溶性成分(阳离子聚合物)带缓冲成分(us9,101,636b2),通过加热方法制备的整体化固体口服剂型(us2008/0075771a1),催吐药或鼻刺激物(us2008/075771a1),阿片样物质(us2015/016835a1)的排出制剂(us2015/0057304a1)或其无定形或其聚合有机酸盐(us2015/0057304a1),等。
根据一优选实施方案,药物组合物包含基体,该基体含有1~80%(重量)的一或多种疏水或亲水聚合物,优选该基体包含琼脂,alamicacid,海藻酸,羧甲醚纤维素(carmellose),羧甲基纤维素钠,卡波姆(如
根据本发明一优选实施方案,药物组合物包含形成水凝胶的组分和/或合适的交联剂,一旦药物加工酶因滥用步骤而激活,该交联剂允许药物生成可溶性交联水凝胶(任选地,上文公开的漆酶也可能对这类交联有贡献)。优选的形成水凝胶的组分是壳聚糖和羧甲基壳聚糖;优选的交联剂是酚交联剂,尤其儿茶酚和香草醛。这种水凝胶/交联剂组合物的优选实例的是,包含壳聚糖和儿茶酚的组合物或包含羧基甲基壳聚糖和香草醛的组合物。
本发明药物组合物优选是储存稳定的组合物,在25℃干燥条件下储存6个月后,优选包含小于5%、尤其小于1%的被药物加工酶加工过的目标药物降解产物。
一般地,药物加工酶应该是酸不稳定的,只要与施用了该组合物的患者的胃液和/或肠环境一接触,药物加工酶在本发明组合物中的活性就被立即灭活。
本药物组合物可以是改良释放组合物,尤其缓释组合物。术语“改良形式”是指包括加速释放,受控释放,和持续释放形式。某些释放形式可以用它们的溶出曲线来表征。“溶出曲线(dissolutionprofile)”是指活性成分释放量相对于时间的函数作图(ph.eur.8(2014)2.9.3)。该溶出曲线可以用美国药典的药物释放试验<724>来测量,该试验结合了标准试验usp26(试验<711>)。曲线的特征取决于所选的试验条件。故,可以在预选的仪器、轴速度(shaftspeed)、温度、体积、和溶出介质ph值来产生溶解曲线。第一溶出曲线可在接近胃ph的水平来测量。第二溶出曲线可在接近一个肠ph值的水平或几个肠ph值的水平测量。强酸性ph可模拟胃,弱酸性至碱性ph可以模拟肠。术语“强酸性ph”是指约ph1~4。“弱酸性至碱性ph”是指约ph4~7.5,优选约6~7.5。约ph1.2可模拟胃的ph。约ph6.0~7.5,优选约ph7.5可模拟肠的ph。
与改良释放相反,“立即释放”是常规的或者非改良的释放形式,其中大于或等于约50%,或更优选约75%的本发明药物在施用后例如2小时内被释放,优选施用后1小时内,尤其施用后30分钟内。“控释”剂型是指,在一段时间内控制或改良药物释放。控制可能意味着,例如,加速,持续,延迟或在特定时间脉冲式释放。可替代地,控制释放可意味着药物释放比立即释放剂型的时间更加延长,即,延长至少数小时。
“延迟释放(delayedrelease)”表示在实现药物的显著血浆水平之前有时间上的延迟。本发明的一个延迟释放制剂避免了药物的初始突释,或者可以配制为避免药物在胃中释放。“脉冲释放(pulsedrelease)”制剂可以在同一剂型中包含立即释放,持续释放,和/或延迟释放制剂的组合。“半延迟释放”制剂是一个“脉冲释放制剂,其中给药后立即提供中等剂量、数小时后提供较大剂量。
术语“持续释放”或“延长释放”是指包括这样的药物释放速率,其使得在给药后达到稳态时,有至少约8小时该药物的血液(例如血浆)水平维持在治疗范围内、但低于毒性水平,优选至少约12小时,尤其至少24小时(特别优选用于每天1次的剂量方案)。术语“稳态”是指,给定药物的血浆水平已实现,且随后多次给药都能将血浆水平维持在等于或高于该药物的最低有效治疗水平、且低于该药物的最小毒性血浆水平或过量血浆水平。上述大部分的聚合物基体和非聚合物基体形成物具有在本发明制剂中提供给定药物的延长释放或持续释放的能力。
根据一个优选实施方案,本发明的药物组合物只包含目标药物(作为唯一的有效成分),或包含目标药物与其它药学活性成分的组合,优选与非阿片类止痛剂(analgesic)的组合,尤其与布洛芬(ibuprofen)、双氯芬酸(diclofenac)、萘普生(naproxen)、对乙酰氨基酚和乙酰水杨酸的组合。
在一个优选实施方案中,当药物组合物以预期方式和完整形式施用(即吞食完整无损的药物)时,该组合物中的酶基本上不会在体内对药物(或药物组合物的任何其它成分)产生作用。
优选地,当本发明药物组合物以预定方式给药并且完整(即完整吞咽)时,该组合物中的酶以基本上不可释放的形式存在于组合物中。
本发明的一个优选实施方案中,本药物组合物的酶在体内是失效的。
根据另一方面,本发明还涉及制备本发明药物组合物的方法,包括将目标药物或其可接受的盐、水合物、溶剂化物、酯或前药与药物加工酶混合,并将混合物制成为(finish)药物组合物的步骤。或者,制造本发明药物组合物的方法包括以下步骤:以分隔开的形式提供目标药物或其药学上可接受的盐、水合物、溶剂化物、酯或前药,和药物加工酶,并将这些分开的组分完成为药物组合物。
根据另一方面,本发明提供了一种组合物,其包含目标药物和形成水凝胶的组分和/或交联剂。一旦药物组合物在滥用步骤的过程中与含水混合物混合,就形成水凝胶的组分和/或交联剂允许产生可溶性交联分子,尤其是水凝胶。优选的形成水凝胶的组分是壳聚糖和羧甲基壳聚糖;优选的交联剂是酚交联剂,尤其儿茶酚和香草醛。这种水凝胶/交联剂组合物的优选实例是包含壳聚糖和儿茶酚的组合物或包含羧基甲基壳聚糖和香草醛的组合物。
优选地,根据本发明的组合物以水凝胶形式提供。这涉及包括另一种抗滥用方法,即产生改变反应溶液的流变性质的系统,即形成水凝胶。水凝胶非常粘稠,因此不可能用针抽出来。
本发明还涉及-根据其性质-给有需要的患者施用本发明抗滥用药物组合物(即包含具有与酶反应的官能团的药物,其中该药物具有滥用潜力,和能够与该酶反应官能团反应的酶(药物加工酶),其中所述具有酶反应官能团的药物以储存稳定的酶反应性状态、在对该药物没有酶活性的条件下包含在药物组合物中)的方法,其中根据本发明的药物组合物以有效量口服给予该患者,并且其中药物加工酶在该口服给药过程中(被存在于该患者胃肠道(口腔,食道,胃,和(小)肠))中的组分,例如被患者的唾液、胃液和肠液以及以及其中含有的酶)自动失活,如此一来,药物加工酶不会作用于药物,因此药物可以在患者体内发挥其预定的作用。
另外,本发明通过以下实施例和附图进一步说明,但不受其限制。
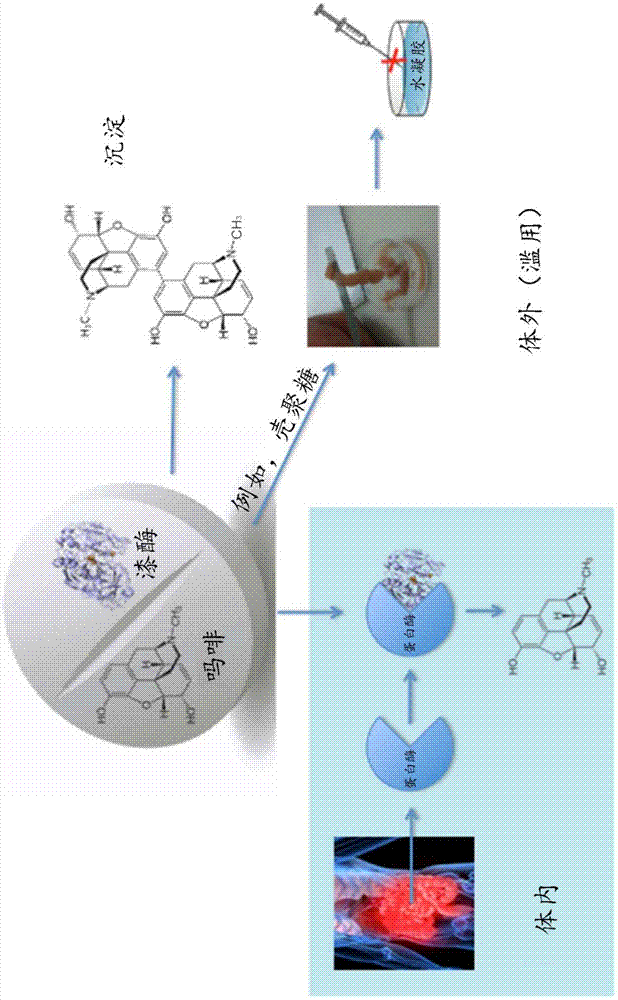
图1显示了本发明的策略,以吗啡作为药物的例子来举例。根据本发明的抗滥用吗啡/漆酶系统或者将吗啡转化为沉淀产物或者与添加剂组合产生水凝胶,不再能用注射器注射该药物。如果药物是按预期施用的,则来自身体的蛋白酶使漆酶失活,而药物则能展开其效果。
图2示出了在实施例中所研究的阿片类药物(吗啡(左),他喷他多(中间)和氧可酮(左))。
图3显示嗜热毁丝霉(mtl)(紫)和长绒毛栓菌(tvl)(绿)对吗啡的漆酶氧化。
图4显示mtl(紫)和tvl(绿)对他喷他多的漆酶氧化。
图5显示mtl(绿)和tvl(紫)对氧可酮的漆酶氧化。
图6显示与吗啡作为参照(第一泳道)相比,吗啡在不同时间点酶促转化后的tlc。
图7显示与他喷他多作为参照(第一泳道)相比,他喷他多在不同时间点酶促转化后的tlc。
图8显示吗啡沉淀物的ftir(红线:吗啡参考,蓝线:沉淀的吗啡聚合物)。
图9显示酶促氧化的吗啡的hplc测量。
图10显示吗啡酶促转化后的gc-ms谱。
图11显示来自gc-ms数据库的吗啡的gc-ms谱图;将测量的光谱与数据库光谱进行比较。
图12显示吗啡被漆酶转化,是gc-ms测定结果。
图13显示壳聚糖-儿茶酚-吗啡水凝胶。
图14显示羧甲基壳聚糖-吗啡水凝胶。
图15显示本发明的策略。根据本发明的抗滥用氧可酮/氧可酮加工酶系统或者将氧可酮转化为无或低滥用潜力的加工后氧可酮衍生物,或者与添加剂组合产生水凝胶,不再能用注射器注射该药物。如果氧可酮是按预期施用的,则来自身体的蛋白酶(以及胃中和小肠中的条件)使氧可酮加工酶失活,而氧可酮则能展开其效果。
图16显示了氧可酮酶促转化为部分沉淀的产物。
图17显示了用各种阿片类药物和漆酶进行的氧浓度测量。
图18显示漆酶介体系统的氧浓度测量。
图19显示漆酶介体系统的氧浓度测量,氧可酮配合介体香草醛、乙基香草醛、没食子酸(gallicacid)和丁香酸(syringicacid)。
图20显示各种漆酶介体系统(lms)的氧可酮百分比浓度,实验用氧可酮和各自的对照进行。
图21显示对分子式为c17h19no4,就是羟吗啡酮的ms-tof分析所发现的峰面积[pa]。
图22显示漆酶介体系统的氧浓度测量,美沙酮配合的介体是abts。
图23显示二乙酰基吗啡经酯酶的酶促脱乙酰化而生成吗啡的反应路线图。然后,吗啡被漆酶氧化。
图24显示经hplc/ri测量的不同酶和不同温度随时间的乙酸产量。
图25显示了在有不同酶和温度的测定中dam和吗啡的浓度。
图26显示了人体内酶的失活。
图27的sds-page凝胶显示不同酶的蛋白水解降解,即嗜热毁丝霉漆酶mtl,特异腐质霉角质化酶hic和辣根过氧化物酶hrp。
图28显示使用abts作为底物的mtl的ph活性谱。
图29显示了mtl在不同ph水平下随时间的稳定性曲线。
图30显示用10u/ml漆酶消除各种浓度的吗啡。
图31显示漆酶浓度的增加与吗啡浓度的降低是线性相关的(→多10倍的漆酶导致降解快~10倍)。
图32显示结果用60000mg/l吗啡(几乎是吗啡的溶解度极限)得到的结果。
实施例:
i.:用于抗滥用阿片类药物配方的漆酶
阿片类药物是现代疼痛管理的重要组成部分,尽管滥用和/或误用这些药物已经造成了日益严重的公共卫生问题。为了解决这个问题,人们强烈要求采用新技术来防止滥用阿片类药物。因此,本项目试图以一种基于使用酶的独特方式来解决这个问题。
本文研究了酶聚合阿片类药物从而防止滥用的潜力。当阿片类药物正确使用时,这些酶不会起作用。本项目彻底调查了这些可能性。
在本实施例中,显示了从溶液中消除阿片类物质的合适酶系统的开发。此外,提供了用于有效转化阿片类药物溶液、防止通过注射给药的优化的反应条件。最后,通过按预期用药时显示的破坏阿片类药物的酶的蛋白水解失活,来验证该系统的功能。
1.材料
所研究的阿片类药物是吗啡,他喷他多和氧可酮,如图2所示。
用两种不同的漆酶来消除阿片类药物-其中一种来自长绒毛囊菌(tvl),另一种来自嗜热毁丝霉(mtl)。
2.氧测量
为确定漆酶是否作用于任一种给定的阿片类物质(吗啡,他喷他多,氧可酮),使用光学氧传感器。漆酶使用氧作为电子受体,因此氧浓度在底物氧化时降低。
以下反应的条件如表1所示:
表1:阿片类药物的漆酶催化氧化的氧测量条件
在图3中,显示了吗啡由两种不同的漆酶氧化,即嗜热毁丝霉的漆酶(mtl)和长绒毛囊菌的漆酶(tvl)。蓝色和红色线代表两个空白,蓝色用蒸馏水和酶,红色用蒸馏水和吗啡。紫色和绿色线表示两个与酶的反应(紫:mtl,绿:tvl)。大约过了5分钟,溶液中的氧浓度明显降低,这意味着漆酶将吗啡转化为反应产物。另外,两种溶液变浑浊,这意味着反应产物沉淀。两种酶之间没有显着差异。
在图4中,显示了他喷他多由mtl(紫色)和tvl(绿色)氧化。与用tvl的氧降低相比,mtl的氧降低要慢得多。这可能是因为tvl具有比mtl高得多的氧化还原电位。不同的曲线也表明两种酶的特异性在他喷他多上是非常不同的。tvl更好地转换他喷他多,证据是曲线的斜率以及tvl曲线降到几乎0%氧的事实。
在图5中,显示了氧可酮的氧化。所有曲线看起来都相似,表明所用的两个酶不能转化氧可酮。其原因是氧可酮中缺失的酚-oh基团(如图2所示),这是漆酶所需要的。
3.薄层层析
吗啡和他喷他多的反应还通过薄层色谱法分析,并显示在图6和7中。图6显示了吗啡的转化。第一泳道代表吗啡作为参考,而其他泳道显示在不同时间点(2,10,30,60,120分钟)拍摄的样品。仅2分钟后,在tlc板上出现2个新点,表明吗啡酶促反应形成了新产物。吗啡参考点在30分钟后消失,这表明所有吗啡都被转换。对于他喷他多,图7中显示了相同的过程。他喷他多的转换速度要慢得多,但是2分钟后也出现了一个新的点,120分钟后他喷他多点就消失了。
4.对沉淀产物的分析
如上所述,吗啡的反应产物沉淀,因此下一部分是分析该沉淀物。以下条件用于该反应(表2)。
表2:对mtl酶促反应形成的吗啡沉淀进行分析的条件
24小时后,将反应混合物在16.100rcf(相对离心力)下离心15分钟。弃去上清液,将剩余的沉淀物冻干过夜。第二天,通过ftir分析干沉淀物,如图8所示。红线表示吗啡,蓝线表示沉淀的反应产物。可以看出,由于吗啡的聚合反应,出现新的峰和其他峰减少。
为了进一步分析,进行沉淀物的溶解度测试。如表3所示,溶解度试验的结果是矛盾的。在所用的多种溶剂中,沉淀物都不可溶,很可能意味着在酶促反应时形成高分子量产物。这对于项目的主要目标是可取的,但是为了进一步分析,可溶性化合物是必需的。
表3:因漆酶催化的吗啡氧化形成的沉淀物的溶解度测试
5.对沉淀产物的分析
为了解决第二个任务-改变反应混合物的流变性质(rheologicalproperties)-加入不同的添加剂以增加溶液的粘度。所测试的添加剂显示在表4中,并如所述混合到反应中。大多数所选添加剂已经用于制药应用。仅在使用羟丙基甲基纤维素(hpmc)时才实现所需的粘度增加。
表4:用于增加粘度的酶促吗啡反应的添加剂
6.用hplc和gc测量酶促转化
利用hplc和gc分析吗啡的酶促转化动力学。
在反应过程中的不同时间点(0,2,5,10,15,30分钟)取样。起始溶液是蒸馏水中的0.2mg/ml吗啡。为了开始反应,加入mtl至终浓度为78.3u/ml。取100μl样品并置于900μl甲醇(meoh)中以沉淀该酶。将溶液离心,上清液经0.2μm滤器转移至hplc小瓶中。然后该溶液用以下表5所示的hplc条件测量。
表5:用于确定酶促氧化的吗啡的反应速率的hplc测量条件
hplc测量结果见图9。可清楚地看到吗啡被漆酶转化。15分钟后,不再测量到吗啡信号。这意味着大约在15分钟,100%的吗啡被转化为部分沉淀的产物。必须进一步分析确切的反应机理和反应产物。
除hplc方法外,建立gc-ms方法,使用下表6中所列条件分析样品。
柱agilenttechnologiesdb17ms
温度程序120℃-320℃
运行时间11.5min
表6:用于确定酶促氧化的吗啡的反应速率的gc-ms条件
图10中的ms谱图显示了反应后吗啡的gc-ms测量结果。右边的尖峰代表吗啡,由图11所示的ms光谱库证实。这是检测到吗啡的证据。
图12中显示了吗啡的反应转化率,还显示了嗜热毁丝霉漆酶。对于该反应,使用蒸馏水中的2mg/ml吗啡。为了开始反应,加入mtl至终浓度为78.3u/ml。取100μl样品并置于900μl甲醇(meoh)中以沉淀该酶。将溶液离心,上清液经0.2μm滤器转移至hplc小瓶中。此小瓶中有naso4结合所述酶的剩余水,这些水可能在gc色谱中引起一些问题。
与上述hplc测量条件相比,转化率要慢得多。30分钟后,约60%的吗啡被转换。其原因很可能是酶/底物比例的不同。为进行hplc测量,与gc测量所制样品相比,使用了更多的酶。这表明可以用酶与底物的比例来影响转化率。
7.水凝胶
根据优选的实施方案,本发明组合物以水凝胶形式提供。这涉及包括另一种抗滥用方法,即产生改变反应溶液的流变性质的系统,即水凝胶的形成。水凝胶是非常粘稠的,因此不可能用针吸取。为此目的,尝试了不同的配方,如表7所示。将这些物质混合在一起直至形成凝胶。
用壳聚糖进行的第一次试验在约15分钟后形成水凝胶。其想法是,儿茶酚使壳聚糖分子交联,而吗啡经michael式反应而共价嵌入。该试验成功证明,儿茶酚需要用其他已用作药物添加剂的分子代替。
用羧甲基壳聚糖进行的第二次试验在约24小时后与吗啡形成水凝胶。24小时。该系统无害,反应时间可以优化。
物质粘度增加
壳聚糖2%(w/v)+500μm儿茶酚+(15min后)
+吗啡10mg/ml+2u/mlmtl
羧甲基壳聚糖2%(w/v)+吗啡10mg/ml+2umtl+(24h后)
表7:酶促交联水凝胶的条件
图13显示了壳聚糖-儿茶酚-吗啡水凝胶。图14显示了羧基甲基壳聚糖-吗啡水凝胶。两种水凝胶都不能再次注射,也不能再用于给药。
讨论:
该研究证实了一种用于开发抗滥用阿片类药物的全新酶促方法。他喷他多和吗啡被漆酶成功转化,这通过耗氧量测量,tlc,hplc-ms,ftir和gc-ms分析证实。
由于吗啡的酶促转化非常直接,因此选择该反应作为进一步分析的模型。嗜热毁丝霉漆酶作用于吗啡的反应速率通过hplc和gc测量来分析。大约过了15分钟,100%的吗啡被转化为沉淀产物。通过ftir分析该沉淀的反应产物,并进行溶解度测试。该沉淀物在任一种所用的溶剂中都几乎不可溶,这是防止滥用所需的。
总之,成功开发了基于酶聚合的所需防滥用系统。根据所呈现的结果,本系统原则上可扩展至所有药物,尤其是具有漆酶反应性官能团的所有阿片类药物,这是合理的。
ii.用过氧化物酶/漆酶组成的酶系统灭活氧可酮
阿片类药物是现代疼痛管理的重要组成部分,尽管滥用和/或误用这些药物已经造成了日益严重的公共卫生问题。为了解决这个问题,人们强烈要求采用新技术来防止滥用阿片类药物。因此,本项目试图以一种基于使用酶的独特方式来解决这个问题。
本项目调查了酶聚合阿片类药物从而防止滥用的潜力。当阿片类药物正确使用时,这些酶不会起作用。这些可能性都在本项目中进行了彻底调查。
在本实施例中,可以显示开发适当的酶系统以从溶液中消除阿片类物质。过氧化物酶用于在氧可酮中产生羟基,而这种“活化的”分子被漆酶进一步转化。此外,提供了优化的反应条件,用于有效转化阿片类溶液,防止通过注射给药。最后,通过显示按预期施用药物时阿片破坏酶进行的蛋白水解灭活,验证了该系统的功能。
材料
所研究的阿片类药物是氧可酮。
为了实现氧可酮的消除,使用以下酶:辣根过氧化物酶和源自嗜热毁丝霉(mtl)的漆酶。葡萄糖氧化酶(god,来自黑曲霉(aspergillusniger))用于产生过氧化物酶反应所需的h2o2。
氧测量
为了确定漆酶是否作用于活化的氧可酮,使用光学氧传感器。漆酶使用氧作为电子受体,因此氧浓度在底物氧化时降低。
以下反应的条件如表1所示:
用hplc测量酶促转化
吗啡的酶促转化动力学通过hplc-ms来分析。
在反应过程中的不同时间点(0,2,5,10,15,30分钟)取样。取出500μl样品并放入500μl甲醇(meoh)中以沉淀该酶。溶液用vivaspin500离心并转移至hplc小瓶中。然后该溶液用下表2所示的hplc条件测量:
表2:确定酶促氧化的氧可酮的反应速率的hplc-ms测量条件
结果可以通过hplc-ms测量来评估。从这些数据可清楚看出,氧可酮被酶促转化为部分沉淀的产物。用以下方法进一步分析确切的反应机理和反应产物:gpc和nmr。
水凝胶
根据优选的实施方案,本发明的组合物以水凝胶形式提供。这涉及纳入另一种抗滥用方法,即产生改变反应溶液的流变性质的系统,即水凝胶的形成。水凝胶是非常粘稠的,因此不可能用针吸取。
讨论
该研究证实了一种用于开发抗滥用阿片类药物的全新酶促方法。氧可酮通过hrp酶和漆酶(加上葡萄糖氧化酶产生的辅因子)成功转化,这通过氧消耗测量和hplc-ms分析证实。
这些酶作用于氧可酮的反应速率通过hplc-ms测量来分析。氧可酮转化为沉淀的产物。
总之,成功开发了基于酶聚合的所需防滥用系统。从目前的结果可以看出,本系统原则上可延伸至所有药物,尤其是具有漆酶反应性官能团的所有阿片类药物。
iii.用于所选和优选氧可酮加工酶的酶测定是众所周知的,并且可用于本文列出的大多数优选的酶。作为例子,下文以一套已知用于2-氧化戊二酸依赖性o-脱甲基化的系统进行举例:
o-脱甲基化(2-氧化戊二酸-依赖性)
对2-氧化戊二酸依赖性双加氧酶活性的直接酶测定可以用反应混合物进行以下:100mmtris-hcl(ph7.4),10%(v/v)甘油,14mm2-巯基乙醇,1mm生物碱,10mm2-氧化戊二酸,10mm抗坏血酸钠,0.5mmfeso4,和至多100μg纯化的重组酶。测定在30℃进行1或4小时,通过将反应管浸入沸水中5分钟来停止,并进行lc-ms/ms分析。2-氧化戊二酸依赖性双加氧酶活性还用基于[1-14c]2-氧化戊二酸的o-脱甲基化-偶联脱羧反应进行间接测定。简而言之,标准测定法含有10μm经90%摩尔/摩尔(n/n)未标记型2-氧化戊二酸稀释的10%n/n[1-14c]2-氧化戊二酸溶液(比活性55mci/mmol),10μm未标记的生物碱底物,10mm抗坏血酸钠,0.5mm硫酸铁,和5μg纯化的酶,溶于500μl缓冲液(100mmtris-hcl,10%[v/v]甘油,14mm2-巯基乙醇,ph7.4)反应。测定通过添加酶开始,在30℃保温45分钟,并通过从反应小瓶中移除14co2-捕获性玻璃纤维滤器(whatmangf/d级,用ncs-ii组织增溶剂预处理,amershambiosciences)来停止测定。为进行酶动力学分析,使用经99%(n/n)未标记型2-氧化戊二酸稀释的10μm1%(n/n)[1-14c]2-氧化戊二酸溶液(比活性55mci/mmol)。将缺乏生物碱底物时的测定结果从含有多种生物碱底物的相应测定中扣除,以解释2-氧化戊二酸的未偶联消耗。当2-氧化戊二醇浓度恒定在500μm时,使反应中的底物浓度在1和500μm之间变化,可以获得例如t6odm的动力学数据。相反,当底物浓度恒定在30μm时,2-氧化戊二酸浓度可在1和500μm之间变化,这产生最大反应速度。当可待因浓度恒定在50μm时,使2-氧化戊二酸浓度在1和500μm之间变化,可获得例如codm的动力学数据。饱和曲线和动力学常数可以用figpv.2.98(biosoft,cambridge,uk;http://www.biosoft.com)基于michaelis-menten动力学计算。生物碱进行o-脱甲基化时的甲醛释放可以用nash测定的基于荧光的改良测定来监测。nash试剂通过将0.3ml冰醋酸和0.2ml乙酰丙酮加入100ml2m乙酸铵中来制备。酶测定可以如上述进行,不同在于使用未标记的2-氧化戊二酸,并且通过添加2倍体积的nash试剂来淬灭所述反应,然后在60℃保温10分钟,使甲醛转化为二乙酰二羟基二甲基吡啶(ddl)。ddl荧光可用caryeclipse荧光分光光度计(varian;www.varianinc.com)在λex=412nm和λem=505nm处记录。酰基环己烷二酮,调环酸钙(prohexadionecalcium)或抗倒酯(trinexapac)-乙基可以作为可能的酶抑制剂,以高达500μm的浓度,在标准测定中用100μm2-二氢化戊二酸进行测试。
iv.其他实验
1.另外的漆酶o2测量
进行氧浓度测量以确认在先前多个实验中收集的结果。测试了以下另外的阿片类药物:美沙酮,二羟基可待因,二乙酰基吗啡和氢吗啡酮。
最终反应混合物:1000mgl-1阿片样药物,10单位/ml漆酶溶于napi缓冲液ph750mm。
测量结果可见图17。这些反应证实了先前对氧可酮,他喷他多和吗啡的测量结果,其中氧浓度下降和因此的漆酶活性只在有酚基团的情况下能见证。对于这些新测试的阿片类药物,只有氢吗啡酮显示出漆酶活性,而对于所有其他阿片类药物,浓度保持稳定。
2.漆酶介体系统(lms):阿片类药物的消除
介体可以用作电子穿梭机,以促进复杂底物的氧化,否则它们本身不会被漆酶氧化。含有苯酚基团的阿片类药物容易作为漆酶的底物,而其他阿片类药物如氧可酮,美沙酮或二羟基不那么容易被氧化。漆酶的底物范围可以通过介体增加:这些常见小分子在第一步中被漆酶氧化,然后在其氧化态与广泛多种目标底物反应。
在反应中,氧作为电子受体起作用,被漆酶还原成水而介体被氧化。氧浓度如上述测量。氧气的消耗直到介体完全氧化为止。选一个开放的实验系统;因此,氧浓度可以恢复到其起始值。反应的第二步通过加入目标底物来引发,该底物随后被介体氧化。现在减少的介体可以再次被漆酶靶定,这导致氧浓度再次下降(见图18)。
在这些实验中,最终反应混合物含有0.2~6mm介体,1~10单位/ml漆酶和100~3000mgl-1阿片样物质。
2.1.lms和氧可酮
图19显示了漆酶介体体系中氧可酮的氧浓度水平。使用浓度为2mm的的不同介体和10单位/ml漆酶和1000mg/l氧可酮。氧浓度的第一次下降代表相应介体被漆酶氧化,第二次下降-在加入阿片样物质后马上发生-是由于随后阿片样物质的氧化。
加入氧可酮后,介体香草醛,乙基香草醛和丁香酸都显示氧浓度下降,如图19所示。这表明了氧可酮的氧化。
为了进一步证实氧可酮的氧化和消除,进行hplc-ms/tof测量。
浓度用agilent的液相色谱-电喷雾电离-飞行时间(hplc-esi-tof)质谱仪(a1260系列,agilentus)测定。这些样品中包含的物质通过zorbaxhilicplus,2.1x100mm,3.5μm(agilent,us)柱分离。梯度设定为在40℃流速为0.4mlmin-1的100%流动相a(65mm甲酸铵ph3.2),并在15分钟内以注射体积1μl变为100%流动相b(乙腈)。以每秒两个光谱的扫描速率,在100至3000m/z范围内获得光谱。每种阿片样物质的标准曲线用0.001至50mgl-1的相应标准物确定。
除图18所示反应外,介体香草醛以更高的浓度(6mm)使用。结果可见图20和图21。氧可酮浓度的降低得到确认。氧可酮的一种主要降解产物,羟吗啡酮,在所有样品中都发现了。羟吗啡酮是氧可酮的杂质,因此即使在未使用漆酶或介体的对照物中也存在。然而,羟吗啡酮随时间而出现的峰面积增加仅可见于氧可酮与漆酶介体体系组合的情况中。唯一对氧可酮无明显影响的介体是没食子酸,这一观察得到氧浓度测量和ms-tof分析两者的支持。
2.2.lms和美沙酮
对于美沙酮,进行氧测量,但配以更宽泛的介体组合:除了上述介体外,还测试了丁香酸,tempo,丁香酚和abts。用abts观察到最佳效果,如图22所示。同样,氧浓度的下降表明目标物质的氧化。
3.二乙酰基吗啡(dam)酯酶api酶配对
作为api-酶配对的两步反应的实例,研究了二乙酰基吗啡。在第一反应中,使用酯酶将二乙酰基吗啡脱乙酰化为单乙酰基吗啡,再生成吗啡。总反应方案可见图23。然后吗啡可如前所述被漆酶氧化。
除了hplcms-tof定量之外,dam脱乙酰化导致的乙酸盐增加通过hplc/ri测量。
3.1.酯酶活性测定
酯酶活性用光度法测定,是以对硝基苯酚乙酸酯(pnpa)为底物,在50mm磷酸钠缓冲液(ph7)中测定。所用方法如hugginsetal.,j.biol.chem.170(1947)467-482所述,有一些修改(herreroacero等,macromolecules44(2011),4632-4640)。酯酶可以将pnpa水解成乙酸和对硝基苯酚。此外,对硝基苯酚的吸光度的增加也可以测量。
8.3mmpnpa储液在dmso中制备,并在磷酸钠缓冲液中稀释。最终的反应混合物含有200μlpnpa溶液和20μl适当稀释的酶溶液。释放的对硝基苯酚的吸光度在30℃、405nm(ph=7时,ε=90.32mlμmol-1cm-1)使用多模式酶标仪测量。一个酯酶活性单位定义为,在实验条件下每分钟释放1μmol对硝基苯酚的酶量。对于空白,反应混合物以相同的方式制备,不同仅在于酶溶液被水取代。用20μl缓冲液代替样品来测量空白。以体积计的酶活性使用lambertbeer定律(hugheset等,anal.chem.24(1952),1349-1354)的适应版本来计算。
3.2.二乙酰基吗啡酶促转化为吗啡
特异腐质霉的角质酶(hic)购自novozymes(丹麦),解纤维高温双歧菌(thermobifidacellulosilytica)的角质酶1(thc)按herreroacero等,2011所述生产并纯化。这些酶过去已显示能够水解多种复杂结构(perzetal.,nat.biotechnol.33,(2016),295-304)。这两种酶的活性都通过pnpa活性试验来确定。
使用两种不同的酶,hic和thc,将二乙酰基吗啡酶促转化为吗啡。水解反应是将50mm磷酸钠缓冲液(ph7)中的15mg二乙酰基吗啡与10uml-1的其中一种酶在室温和50℃一起温育5天。反应混合物的最终体积为10ml,并在整个实验过程中都以400rpm摇动。由于乙酸是挥发性的,因此反应必须在气密密封的玻璃管中进行。取出每个时间点的1ml样品,通过注射器和孔径为0.45μm的滤器过滤,随后用carrez沉淀法沉淀以除去酶。向1ml样品中加入20μlcarrez试剂1(10.6%w/v六氰基高铁酸钾(ii)-三水合物)并涡旋。1分钟后,加入20μlc2(28.8%w/v七水合硫酸锌),涡旋并再温育5分钟,然后13000rpm离心30分钟。将上清液用于进一步分析。
经高效液相色谱(参数如下所述)分离后,所得乙酸的量用ri-检测器检测。所得乙酸的量通过hplc-ri分析来测定。为了定量,在超纯水中制备1gl-1至0.01gl-1的乙酸标准品。在hplc分析之前,须通过添加10-20μl1mhcl将每个样品的ph调至4-6。所有实验一式两份。作为阳性对照,二乙酰基吗啡在0.1mnaoh中化学水解,如nakamura等人所述(nakamuraetal.,j.chromatogr.110(1975),81–89)。
3.3.通过hplc定量脱乙酰化
所得产物通过agilent的高效液相色谱(hplc)分离(a1100系列,agilentus)。这是由transgenomic(us)提供的icsepion300,7.8x300mm,7μm柱完成的。在45℃使用流动相0.01nh2so4,流速为0.325mlmin-1。在60分钟的运行时间内,注射40μl样品。乙酸的量通过所述设备的ri-检测器测定。该方法用10mgl-1至1000mgl-1的乙酸标准品校准。
3.4.结果
随时间的乙酸总产量可见于图24。在50℃,两种酶都能水解超过50%的二乙酰基吗啡,表明吗啡完全脱乙酰化。
阿片样物质浓度的直接测量证实了这一假设,见图25:虽然所有样品中的dam浓度下降,但吗啡浓度仅在50℃温育的样品中增加。在较低的温度,似乎只产生单乙酰基吗啡。
4.酶的灭活–sgf和蛋白酶
当药物按预期施用时酶的灭活是本发明的组成部分。通过酸性变性和蛋白水解降解可以实现灭活(图26)。
为了评估灭活方法的可行性,在各种ph水平进行蛋白酶消化实验以及酶稳定性试验。
4.1.胃蛋白酶消化试验
用于证明mtl的胃蛋白酶消化的方法由thomas等人描述(thomas等,regul.toxicol.pharmacol.39(2004),87–98),是使用模拟胃液(sgf)进行的标准化方案。根据美国药典(1995),sgf每反应混合物含有0.084mhcl,0.035mnacl,4000u胃蛋白酶,ph值为1.2。在整个测定中使用10000单位胃蛋白酶活性比对1mg测试蛋白的比率,这是基于对美国药典(第24版,2000)中推荐的胃蛋白酶平均活性的评估,并进行了一些修改。胃蛋白酶(目录号#p7000)购自sigma-aldrich(us)。将所有使用的蛋白质以5mgml-1的浓度溶于50mmtris-hcl(ph9.5)中。反应混合物含有1.52mlsgf,预热至37℃后加入0.08ml蛋白溶液(thomas等,2004)。将混合物置于热混合器中37℃、以400rpm振荡。为进行变性sds-聚丙烯酰胺凝胶电泳分析(sds-page),在开始后0分钟,0.5分钟和15分钟时取出160μl样品。
4.2sds-page分析
进行sds-page以分析并目视检查多个染色的蛋白条带,看每个蛋白条带在消化实验后是仍然完整或是已成片段。含有4-15%聚丙烯酰胺的预制precasttris-glycin凝胶(目录号#456-1086),10xtris-甘氨酸-sds(tgs)缓冲液(目录号1610772)和4xlaemmli样品缓冲液(目录号#1610747),都购自bio-radlaboratories(hercules,usa)。在使用前,将4xlaemmli缓冲液用2-巯基乙醇以10:1稀释。以下样品制备方法由thomas等人(thomas等人,2004)描述。
每个160μl消化样品通过添加56μl200mmnahco3作为中和步骤和56μl4xlaemmli(laemmli1970)缓冲液来猝灭,以备电泳。将样品立即加热至99℃维持10分钟并直接分析,或在-20℃储存。用于胃蛋白酶和测试蛋白稳定性的对照样品(不含胃蛋白酶但含有测试蛋白的sgf)以与上述相同的方式处理。零时间点消化样品的制备方式不同,因为胃蛋白酶一旦进入溶液就会立即开始消化和自我消化。在添加测试蛋白之前,胃蛋白酶已在猝灭溶液中变性、并加热至99℃持续5分钟。然后将样品再次加热5分钟以确保测试蛋白的正确变性。将15μl每种样品和5μl预先染色的蛋白标记物iv(目录号#27-2110,peqlab)加载到凝胶上,随后在tris-glycin运行缓冲液中以200v运行30~45分钟。为了进行观察,将这些凝胶与考马斯蓝染色溶液(0.1%wv-1考马斯r250,10%vv-1乙酸,45%vv-1甲醇)孵育30分钟,然后进行10~30分钟脱色(10%vv-1乙酸,40%vv-1甲醇)。
蛋白水解酶降解的结果可参见图27。mtl和hrp对蛋白水解降解非常敏感,因为它们各自的蛋白条带在30秒内消失。hic显示出浓缩时温和降低。
4.3漆酶稳定性试验
为了建立mtl的ph曲线,使用abts作为底物,在酸性至中性(ph2.5~ph7)的不同ph水平测量酶活性。对于每种ph水平,将mtl在各自的缓冲液中以1:100稀释,并在室温温育1小时。酶活性在不同的时间点测量。活性通过abts试验(如上所述)测量和计算,用到了每种ph水平的消光系数,它们各不相同(ph7:ε=11.38mlμmol-1cm-1,ph6:ε=23.34mlμmol-1cm-1,ph5:ε=32.03mlμmol-1cm-1,ph4:ε=35.49mlμmol-1cm-1,ph3,2:ε=36.00mlμmol-1cm-1;硕士论文(“laccasessaseffectivesiccativesinalkydresins”),scholz,2015.。
mtl的ph曲线可参见图28,而不同ph水平随时间的稳定性曲线如图29所示。mtl具有两个活性最大值,一个在ph7,第二个在ph3,并且在sgf培养基条件下无活性。稳定性曲线表明,mtl在ph4至7时仍保持其大部分活性,但在较低ph下相当快地失去活性。
5.额外的漆酶–吗啡试验(高浓度)
使用各种浓度的吗啡和漆酶进行了几个额外的实验。以下实施例和附图中呈现的结果支持有关降解速率与漆酶量以及阿片样物质浓度直接相关的观点。这些实施例也基于更可靠和改进的分析。
5.1.用嗜热毁丝霉的漆酶进行吗啡聚合
吗啡聚合以不同的方法进行,吗啡浓度范围为1mgl-1至60000mgl-1。这些反应在50mm磷酸钠缓冲液ph7中进行。因加入漆酶mtl至最终活性为10u至100u,开始了氧化过程。图30中显示了各种浓度的吗啡。
图31显示,漆酶浓度的增加与吗啡浓度的降低成线性关系(即,10倍以上的漆酶导致降解快~10倍)。图32显示了60000mg/l吗啡的转化率,这几乎是吗啡的溶解度极限。
因此,这些结果完全符合上述i.6。.
优选的实施方案:
本发明因此涉及以下优选实施方案:
1.抗滥用药物组合物,包含具有与酶反应的官能团的药物,其中所述药物具有滥用潜力,和能够与该酶反应官能团反应的酶(药物加工酶),其中所述具有与所述酶反应的官能团的药物以储存稳定的能与酶反应的状态、并处在无酶促活性作用于该药物的条件下包含在药物组合物中。
2.实施方案1的药物组合物,其中酶选自还原酶和/或转移酶和/或水解酶,尤其是单加氧酶。
3.实施方案1或2的药物组合物,其中的酶反应官能团是酚羟基或酚氨基,优选酚羟基。
4.实施方案1~3任一的药物组合物,其中的酶催化所述药物的o-脱烷基化优选o-脱甲基化,n-脱烷基化优选n-脱甲基化,酮还原,n-氧化,环氧-羟基化,酯化,脱酰胺化,过加氧化(peroxigenation),或脱卤,或者催化给所述药物添加分子,尤其葡萄糖醛酸化,硫酸化和乙酰化。
5.实施方案1~4任一的药物组合物,其中的酶选自3-alpha-羟基类固醇3-脱氢酶(ec1.1.1.213),细胞色素p450(ec1.14),尤其非血红素铁依赖性单加氧酶(ec1.14.16),铜依赖性单加氧酶(ec1.14.17和ec1.14.18),cyp2c亚家族;cyp2d6;非特异性单加氧酶(ec1.14.14.1),可待因3-o-脱甲基酶(codm;ec1.14.11.32),cyp1-3(ec1.14.14.1),优选cyp3a,cyp1a,cyp2b,cyp2c和cyp2d,尤其cyp3a4,cyp3a5,cyp3a7,cyp1a2,cyp2b6,cyp2c9,cyp2c19,和cyp2d6;过氧化物酶(ec1.11.1和ec1.11.2),优选辣根过氧化物酶(ec1.11.1.7)和真菌非特异性过加氧酶(ec1.11.2.1);羰基还原酶(nadph)(ec1.1.1.184),优选二羟基morphinine酮还原酶(dmkr;i~v型),二羟基可待因酮酮还原酶(dckr,i型和ii型)或吗啡6-脱氢酶(ec1.1.1.218);黄素依赖性单加氧酶(ec1.13.12和ec1.14.13),尤其含黄素的单加氧酶(ec1.14.13.8);微粒体环氧化物水解酶(ec3.3.2.9),辅因子非依赖性单加氧酶;环氧化物水合酶(ec3.3.2.3和4.2.1.63),和可溶性环氧化物水解酶(ec3.3.2.10);udp-葡萄糖醛酸基转移酶(ec2.4.1.17),优选ugt1和ugt2酶,尤其ugt1.1和ugt2b7;胆红素-葡糖醛酸苷葡萄糖醛酸基转移酶(ec2.4.1.95);酰基(乙酰基)转移酶(ec2.3),磺基转移酶(ec2.8.2),coa-转移酶(ec2.8.3),尤其n-乙酰基转移酶(nat,ec2.3.1)和o-乙酰基转移酶(oat;ec2.3.1);儿茶酚(catechol)氧化酶(ec1.10.3.1),胆红素氧化酶(ec1.3.3.5),单酚单加氧酶(ec1.14.18.1),锰过氧化物酶(ec1.11.1.13),单酚monooxigenases(ec1.14.99.1),酪氨酸酶(ec1.14.18.1)和抗坏血酸氧化酶(ec1.10.3.3)。
6.实施方案1~5任一的药物组合物,其中的药物是具有酶反应官能团的阿片类药物,优选选自吗啡,他喷他多,氧可酮,丁丙诺啡,西博帕多,二乙酰吗啡(=海洛因),二羟基可待因,乙基吗啡,氢可酮,氢吗啡酮,美沙酮和左美沙酮,羟吗啡酮,喷他佐辛,杜冷丁,芬太尼,左啡诺和左美沙芬,以及它们的可药用的盐,酯,前药和混合物,尤其氧可酮或吗啡。
7.实施方案1~6任一的药物组合物,其中的组合物包含选自下组的药物/酶组合:吗啡/漆酶,他喷他多/漆酶,羟吗啡酮/漆酶,氢吗啡酮/漆酶,喷他佐辛/漆酶,丁丙诺啡/漆酶,二乙酰基吗啡/水解酶/漆酶,左啡诺/漆酶,氧可酮/漆酶/氧可酮-加工酶。
8.实施方案1~7任一的药物组合物,其中的药物组合物选自片剂,迷你片剂,包衣-核心片剂(包衣片剂),双层片剂,多层片剂,泡腾片剂,可溶性片剂,可分散的片剂,胶囊,球团剂,mups(多单元球团系统),粒剂,粉剂,尤其它们的包衣剂,糖衣剂/或功能性包衣剂(例如肠衣)形式。
9.实施方案1~8任一的药物组合物,其中所述药物的含量为每剂量单位中0.1~5000mg,优选0.5~1000mg,尤其1~500mg。
10.实施方案1~9任一的药物组合物,其中的酶含量是1~1000个单位,优选10~100个单位。
11.实施方案1~10任一的药物组合物,其中的组合物包含另外的抗滥用特征,优选选自物理或化学屏障,尤其增加的片剂硬度,药物拮抗剂,厌恶组分,抗滥用递送系统和前药,尤其是物理屏障或厌恶成分,尤其是胶凝剂和/或非胶凝增粘剂。
12.实施方案1~11任一的药物组合物,其中的该组合物包含酶的辅因子,优选h和/或电子供体和受体,尤其nad(p)h,fmn,fad,铁氧还蛋白,2-氧化戊二酸和/或血红素;或者用于给药物添加基团的供体,尤其乙酰辅酶a(ac-coa)或udp-葡萄糖醛酸酯。
13.实施方案1~12任一的药物组合物,其中的组合物包含基体,该基体含有1~80%重量的一或多种疏水或亲水聚合物,优选该基体包含琼脂,alamicacid,海藻酸,羧甲醚纤维素(carmellose),羧甲基纤维素钠,卡波姆,角叉菜胶,壳聚糖,尤其羧甲基壳聚糖,儿茶酚,共聚维酮(copovidone),糊精,明胶,羟乙基纤维素,羟丙基纤维素,羟丙基甲基纤维素,甲基丙烯酸共聚物,甲基纤维素衍生物,微晶纤维素,聚丙烯酸,聚亚烷基氧化物,尤其聚乙二醇,聚乙烯醇,聚乙烯乙酸酯,聚维酮,丙二醇藻酸酯,聚乙烯己内酰胺-聚乙烯乙酸-聚乙二醇接枝共聚物,普鲁兰糖(pullulan),二氧化硅,藻酸钠,淀粉,乙烯基吡咯烷酮-乙烯乙酸共聚物,或非聚合物基体形成物,优选微晶蜡,脂肪醇和脂肪酸,尤其硬脂醇,十六烷基硬脂醇,硬脂酸,棕榈酸,或它们的盐和混合物,链长16~22个碳原子的饱和脂肪酸的单-、二-、和三-甘油酯,以及这类单-、二-、和三-甘油酯的混合物。
14.实施方案1~13任一的药物组合物,其中的组合物是储存稳定的,优选在干燥条件下25℃储存6个月后包含不到5%,尤其不到1%的被酶加工的药物。
15.实施方案1~14任一的药物组合物,其中的酶是酸-不稳定的。
16.实施方案1~15任一的药物组合物,还包含形成水凝胶的组分和/或交联剂,优选壳聚糖和/或儿茶酚或羧甲基壳聚糖和/或香草醛。
17.实施方案1~16任一的药物组合物,其中的组合物是改良释放的组合物,尤其延长释放的组合物。
18.实施方案1~17任一的药物组合物,其包含另一种酶,优选另一种药物加工酶或对已加工的药物形式进行另外加工的酶,尤其漆酶(ec1.10.3.2)。
19.实施方案1~18任一的药物组合物,其中的药物是具有漆酶反应性官能团的阿片类药物,优选选自吗啡,他喷他多,氢吗啡酮,二氢脱氧吗啡,羟吗啡酮,丁丙诺啡,含苯丙氨酸残基的阿片肽如adrenorphin,amidorphin,酪啡肽,dadle([d-ala2,d-leu5]-脑啡肽),damgo([d-ala2,n-mephe4,gly-醇]-脑啡肽),皮啡肽,内吗啡肽,吗啡感受素,和trimu5(l-酪氨酰-n-{[(3-甲基丁基)氨]乙酰基}-d-丙氨酰胺);东罂粟碱,6-mddm(6-亚甲基二羟基脱氧吗啡),氯纳曲胺,二羟基吗啡,氢吗啡醇,甲基desorphine,n-苯乙基正吗啡,ram-378(7,8-二羟基-14-羟基-n-苯乙基正吗啡),异可待因,二羟基异可待因,7-螺环茚满基羟吗啡酮,morphinone,戊吗啡酮,司吗啡酮,氯吗啡,纳布啡,oxymorphazone,1-碘代吗啡,吗啡-6-葡糖苷酸,6-单乙酰基吗啡,去甲吗啡,吗啡-n-氧化物,环啡烷,dextrallorphan,左啡诺,左芬啡烷,去甲左啡诺,奥昔啡烷,非诺啡烷,毛乙基去甲左啡诺,佐尔啡诺,布托菲诺,6,14-内亚乙烯四氢东罂粟碱,bu-48(n-环丙基甲基-[7α,8α,2',3']-环己醇'[s]-羟基-6,14-内-亚乙烯四氢nor东罂粟碱),,环丙诺菲,二羟基埃托啡,埃托啡,去甲丁丙诺啡,5'-胍基纳曲吲哚,二丙诺啡,左洛啡烷,美普他酚,甲基纳曲酮,纳呋拉啡,纳美芬,纳洛刹腙,纳洛酮,纳洛芬,纳曲酮,纳曲本,纳曲吲哚,6β-纳曲醇-d4,伪吗啡,纳洛肼,norbinaltorphimine,阿拉佐辛,布瑞玛佐辛,地佐辛,可他佐辛,美他佐辛,喷他佐辛,非那佐辛,环佐辛,羟基杜冷丁(bemidone),凯托米酮,甲基凯托米酮,丙基凯托米酮,阿维莫泮(alvimopan),哌西那多(picenadol)和它们的可药用盐,酯,前药和混合物,更优选吗啡,他喷他多,丁丙诺啡,尤其吗啡。
20.实施方案1~19任一的药物组合物,其中的药物是选自下组的阿片类药物:吗啡,他喷他多,氢吗啡酮,二氢脱氧吗啡,羟吗啡酮,丁丙诺啡,含苯丙氨酸残基的阿片肽如adrenorphin,amidorphin,酪啡肽,dadle([d-ala2,d-leu5]-脑啡肽),damgo([d-ala2,n-mephe4,gly-醇]-脑啡肽),皮啡肽,内吗啡肽,吗啡感受素,和trimu5(l-酪氨酰-n-{[(3-甲基丁基)氨]乙酰基}-d-丙氨酰胺);东罂粟碱,6-mddm(6-亚甲基二羟基脱氧吗啡),氯纳曲胺,二羟基吗啡,氢吗啡醇,甲基desorphine,n-苯乙基正吗啡,ram-378(7,8-二羟基-14-羟基-n-苯乙基正吗啡),异可待因,二羟基异可待因,7-螺环茚满基羟吗啡酮,morphinone,戊吗啡酮,司吗啡酮,氯吗啡,纳布啡,oxymorphazone,1-碘代吗啡,吗啡-6-葡糖苷酸,6-单乙酰基吗啡,去甲吗啡,吗啡-n-氧化物,环啡烷,dextrallorphan,左啡诺,左芬啡烷,去甲左啡诺,奥昔啡烷,非诺啡烷,毛乙基去甲左啡诺,佐尔啡诺,布托菲诺,6,14-内亚乙烯四氢东罂粟碱,bu-48(n-环丙基甲基-[7α,8α,2',3']-环己醇'[s]-羟基-6,14-内-亚乙烯四氢去甲东罂粟碱),环丙诺菲,二羟基埃托啡,埃托啡,去甲丁丙诺啡,5'-胍基纳曲吲哚,二丙诺啡,左洛啡烷,美普他酚,甲基纳曲酮,纳呋拉啡,纳美芬,纳洛刹腙,纳洛酮,纳洛芬,纳曲酮,纳曲本,纳曲吲哚,6β-纳曲醇-d4,伪吗啡,纳洛肼,norbinaltorphimine,阿拉佐辛,布瑞玛佐辛,地佐辛,可他佐辛,美他佐辛,喷他佐辛,非那佐辛,环佐辛,羟基杜冷丁(bemidone),凯托米酮,甲基凯托米酮,丙基凯托米酮,哌西那多,可待因,二甲基吗啡,二乙酰基吗啡(吗啡二乙酸;海洛因)尼可吗啡(吗啡二烟酸),二丙酰基(dipropanoyl)吗啡(吗啡二丙酸),二乙酰基二羟基吗啡,乙酰基丙酰基(propionyl)吗啡,二苯甲酰吗啡,二羟基可待因,乙基吗啡,氢可酮,氧可酮,芬太尼,α-甲基芬太尼,阿芬太尼,舒芬太尼,瑞芬太尼,卡芬太尼(carfentanyl),羟甲基芬太尼(ohmefentanyl),杜冷丁(pethidine)(美吡利啶meperidine),mppp,烯丙普鲁汀,阿法罗定(α-prodine),pepap,丙氧酚,右丙氧芬,右吗拉胺,贝齐米特,哌腈米特,美沙酮,左美沙酮,杜冷丁,地匹哌酮,左乙酰美沙酮(levomethadylacetate,laam),地芬诺辛(difenoxin),地芬诺酯(diphenoxylate),左美沙芬(levomethorphan),右美沙芬(dextromethorphan),利非他明(lefetamine),帽柱木碱(mitragynine),痛立定,曲马多,伊卢多啉(eluxadoline),2,4-二硝基苯吗啡,二羟基海洛因,6-mac,苄基吗啡,可待因甲基溴化物,福尔可定(pholcodine),密罗啡因,8-cac,4-氟杜冷丁,烯丙基去甲杜冷丁,阿尼利定,苄替啶(benzethidine),卡哌利定(carperidine),依托利定(etoxeridine),呋替啶(furethidine),吗啡利定(morpheridine),羟芬利定(oxpheneridine),苯乙利定(pheneridine),苯哌利定,匹米诺定,丙哌利定,沙美利定(sameridine),阿法美罗定(α-meprodine),prosidol,三甲利定(trimeperidine),乙酰氧凯托米酮,droxypropine,地匹哌酮,去甲美沙酮,苯吗庚酮,地美庚醇(dimepheptanol),左乙酰美沙醇,右吗拉胺,左吗拉胺(levomoramide),消旋吗拉胺(racemoramide),二乙基噻吩丁烯胺,二甲基噻吩丁烯胺,乙基甲基噻吩丁烯胺,哌啶基噻吩丁烯胺,吡咯烷基噻吩丁烯胺,噻吩丁烯胺,替培啶(tipepidine),地美沙朵,右丙氧芬,左丙氧酚,去甲丙氧酚,吗苯丁酯(dioxaphetylbutyrate),地恩丙胺,非那丙胺(phenampromide),丙吡兰(propiram),methiodone,异米尼尔(isoaminile),利非他明,r-4066,3-烯丙基芬太尼,3-甲基芬太尼,4-苯基芬太尼,阿芬太尼,α-甲基乙酰基芬太尼,β-羟基芬太尼,β-羟基硫代芬太尼,β-甲基芬太尼,布芬太尼(brifentanil),洛芬太尼,米芬太尼(mirfentanil),奥芬太尼(ocfentanil),对氟芬太尼,酚那利定(phenaridine),硫代芬太尼,曲芬太尼(trefentanil),依索庚嗪,美庚嗪(metheptazine),美索庚嗪(metethoheptazine),普罗庚嗪,贝齐米特,哌腈米特,氯尼他秦,依托尼秦,18-mc,7-羟基帽柱木碱,akuammine,毒扁豆酚碱(eseroline),浩京素(hodgkinsine),帽柱木碱,pericine,bw373u86,dpi-221,dpi-287,dpi-3290,snc-80,ad-1211,ah-7921,阿扎普罗辛(azaprocin),bromadol,brl-52537,溴朵啉(bromadoline),c-8813,西拉马多(ciramadol),多匹可明(doxpicomine),伊那朵啉(enadoline),faxeladol,gr-89696,herkinorin,ici-199441,ici-204448,j-113397,jtc-801,lpk-26,甲氧夫啉(methopholine),mt-45,以及它们的可药用盐,水合物,溶剂化物,酯,前药和混合物,更优选吗啡,氧可酮,他喷他多,丁丙诺啡,西博帕多,二乙酰吗啡(=海洛因),二羟基可待因,乙基吗啡,氢可酮,氢吗啡酮,美沙酮和左美沙酮,羟吗啡酮,喷他佐辛,杜冷丁,芬太尼,左啡诺和左美沙芬,尤其氧可酮和吗啡。
21.实施方案1~20任一的药物组合物,其中的组合物能立即释放、改良释放、或是其组合。
22.实施方案1~21任一的药物组合物,其中的该组合物包含单独的阿片类止痛剂或与非阿片类止痛剂组合,尤其与布洛芬,双氯芬酸,萘普生,对乙酰氨基酚和乙酰水杨酸组合。
23.制备实施方案1~22任一的药物组合物的方法,其中包括将药物与酶混合并将混合物制成为药物组合物的步骤。
24.制备实施方案1~22任一的药物组合物的方法,包括提供分开的药物和酶,以及使分开的药物和酶制成为药物组合物的步骤。
25.实施方案1~22任一的药物组合物,是用于治疗药物成瘾的。
26.实施方案1~22任一的药物组合物,是用于治疗疼痛的。
27.实施方案1~22任一的药物组合物,其中当组合物以预定方式给药并且完整时,药物加工酶基本上不作用于体内药物。
28.实施方案1~22任一的药物组合物,其中当组合物以预定的方式给药并且完整时,药物加工酶以基本上不可释放的形式存在于制剂中。
29.实施方案1~22任一的药物组合物,其中的药物加工酶在体内失活。
30.实施方案1~29任一的药物组合物,含水量低于10%,优选含水量低于5%,尤其含水量低于2%。
31.给有需要的患者施用实施方案1~30任一的抗滥用药物组合物的方法,其中的药物组合物以有效量口服给予该患者,并且其中药物加工酶在该口服给药过程中自动失活。
- 还没有人留言评论。精彩留言会获得点赞!