包含杨树芽提取物的组合物及其用途的制作方法
本发明涉及包含杨树芽提取物的组合物,其用于在治疗口咽腔病变、泌尿器病变、消化/排泄器官病变、皮肤病变及细菌感染中使用。
背景技术:
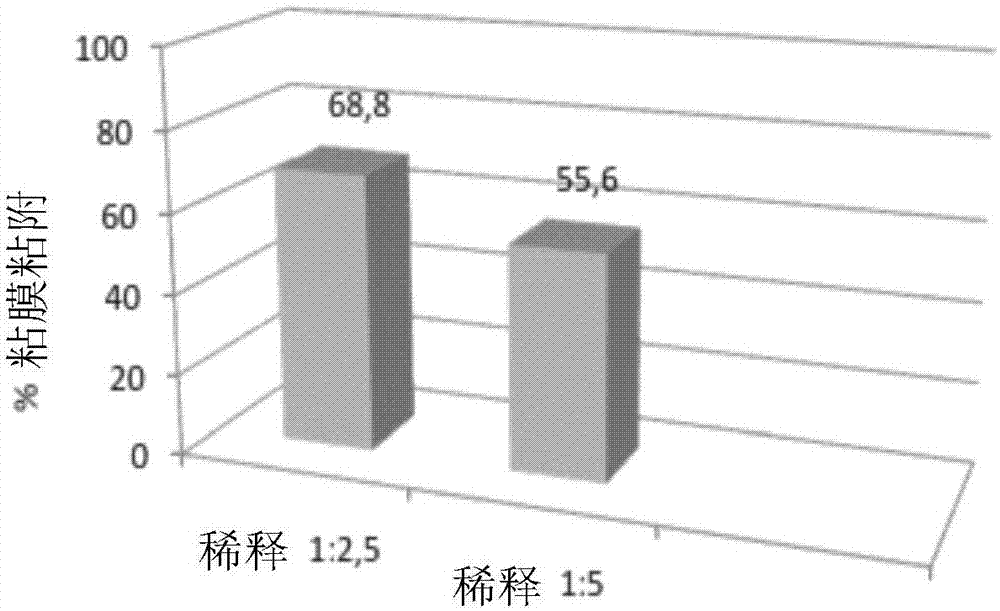
:由文献已经知晓黑杨(populusnigra)的树脂状渗出物是欧洲蜂胶(且通常为温带地区的蜂产蜂胶)的基本元素。蜂胶以其多种药理活性而闻名,其是由蜜蜂在收集树脂状渗出物(主要是黑杨的树脂状渗出物)后产生的物质。平均而言,其包含25-35%的蜂蜡、5%的花粉、5%的蜂腿上存在的各种物质以及约50%的植物树脂。由文献也已经知晓基于杨树芽的药物的各种用途。鉴于对于采用天然来源的物质治疗各种病变的兴趣持续上升,且鉴于目前显示蜜蜂具有显著的灭绝危害,寻找以可比较的方式或以甚为更有效的方式来可比较地替代蜂产物质的天然来源的产品是重要的。技术实现要素:本发明的作者已经分析了杨树芽提取物,以验证其作为完全来源于植物的蜂胶替代物,可以用于治疗目的的用途。杨树芽提取物与蜂胶不同,其还具有不含来源于动物的物质和如花粉的过敏物质的优点。本发明的作者已经出乎意料地证实,与欧洲蜂胶相比,杨树芽提取物表现出可比较的或甚至更强的粘膜粘附性能。本发明的作者还首次证明了杨树芽提取物的有效抗菌活性,特别是针对酿脓链球菌(streptococcuspyogenes)、绿脓杆菌(pseudomonasaeruginosa)和金黄色葡萄球菌(staphylococcusaureus),任选地将其冻干,任选地将其与天然树胶共同冻干(用树胶负载)。因此,本发明的目的是组合物,其包含:重量百分比为0.1至70%的杨树芽提取物,以及一种或多种用于治疗口咽腔病变、泌尿器病变、消化/排泄器官病变、皮肤病变及细菌感染的药学上可接受的载体、辅料、香料、防腐剂,将其用于在治疗口咽腔病变、泌尿器病变、消化/排泄器官病变、皮肤病变及细菌感染中使用。此外,本发明的目的是对于口咽腔病变、泌尿器病变、消化/排泄器官病变、皮肤病变及细菌感染的治疗,其是通过向受所述疾病影响的受试者给予本发明的混合物或组合物来进行的。附图说明图1,按照实施例1描述而进行各种配方的粘膜粘附测定。图1a:组合物-稀释(1:2.5和1:5)的实例固体组合物4对人类口颊细胞的粘膜粘附性百分比;图1b:组合物-稀释(1:2.5和1:5)的实例固体组合物3对人类口颊细胞的粘膜粘附性百分比;图1c:组合物-非稀释的或稀释(1:2和1:5)的实例液体组合物4对人类口颊细胞的粘膜粘附性百分比;图1d:组合物-非稀释的或稀释(1:2和1:5)的实例液体组合物3对人类口颊细胞的粘膜粘附性百分比。图2-粘膜粘附层(用多种稀释度和不同时间下的不同的本发明配方获得的)在不同时间对模拟的唾液溶液(0.9%nacl生理溶液)的抗性。图2a:组合物-(1:2.5稀释的)实例固体组合物4在不同时间(0小时、0.5小时、1小时和2小时)对模拟的唾液溶液(0.9%nacl生理溶液);图2b:组合物-(1:2.5稀释的)实例固体组合物3在不同时间(时间:0小时、0.5小时、1小时和2小时)对模拟的唾液溶液(0.9%nacl生理溶液);图2c:组合物-(1:2稀释的)实例液体组合物4在不同时间(时间:0小时、0.5小时、1小时和2小时)对人工唾液溶液。图3:阻隔测定法中产生的il6;图表示出了本发明组合物对细胞发挥的保护作用,并且以与对照c-相比的倍数(f.o.)表示数据相对于c-的倍数=[il-6测定值]/[c-il-6]图3a:组合物-实例固体组合物4,图3b:组合物-实例固体组合物3,图3c:组合物-实例液体组合物4,图3d:组合物-实例液体组合物3。图4图示了对所描述的多个本发明实施方式计算的阻隔效应,以il6释放抑制的百分比表示。图4a:组合物-实例固体组合物4,图4b:组合物-实例固体组合物3,图4c:组合物-实例液体组合物4,图4d:组合物-实例液体组合物3。图5图示了以相对于内部对照中c-的倍数表示的细胞产生的il-6值。图5a:组合物-实例固体组合物4,图5b:组合物-实例固体组合物3,图5c:组合物-实例液体组合物4,图5d:组合物-实例液体组合物3。图6:根据本发明的杨树芽提取物与抗坏血酸相比的抗氧化活性。图7:根据本发明的杨树芽提取物对细菌生物膜的抑制活性。具体实施方式因此,本发明的目的是组合物,其包含:重量百分比为0.1至70%的杨树芽提取物,以及一种或多种用于治疗口咽腔病变、泌尿器病变、消化/排泄器官病变、皮肤病变及细菌感染的药学上可接受的载体、辅料、香料、防腐剂,将其用于在治疗口咽腔病变、泌尿器病变、消化/排泄器官病变、皮肤病变及细菌感染中使用。根据一个实施方式,该组合物可以包含以下或由以下组成:重量百分比为0.1至70%的杨树芽提取物,重量百分比为1至80%的辅料,重量百分比为0至80%的溶剂,重量百分比为0至50%的天然或冻干的果汁,重量百分比为0.05%至2%的天然或人工的香料,重量百分比为0.01至1%的精油。根据另一个实施方式,本发明的组合物可以包含以下或由以下组成:重量百分比为0.5至10%的冻干的干燥杨树芽提取物,重量百分比为10-97%的辅料,重量百分比为0.5至3%的天然或人工的香料,重量百分比为0.05至1%的精油,重量百分比为0.5至15%的粉状或冻干的果汁和/或天然提取物,重量百分比为1至10%的甜味剂。出于本发明的目的,“杨树芽提取物”是指由叶芽,或主要是黑杨(populusnigra)的叶芽制备的提取物。具体地,根据本发明的提取物是指未展开状态叶芽的提取物。处于未展开状态的芽主要存在于春季,在欧洲通常是从3月到5月。根据本发明的一个实施方式,组合物的唯一活性成分是杨树芽提取物。根据上述任一实施方式,组合物中的杨树芽提取物可以与天然树胶结合,提取物:树胶比被包含在1:2至1-20的范围内。如上文定义且如下文实施例中进一步举例说明的,可以如本文提及的将该组合物用于治疗口咽腔病变。这种病变可以选自例如咽喉痛、咽炎、口疮、口腔炎症或感染。在将该组合物用于治疗消化/排泄器官病变的实施方式中,这些病变可以选自胃炎、反流、炎性肠病、肠应激综合征、痔疮、感染。此外,本发明的组合物可以用于治疗泌尿道病变,例如膀胱炎。在一个优选的实施方式中,可以将本发明的组合物用于治疗细菌感染,在其中特别优选酿脓链球菌、绿脓杆菌、金黄色葡萄球菌中的至少一种的感染。在酿脓链球菌感染的治疗中,可以将根据本发明的组合物例如用于治疗咽炎、猩红热、脓皮病或脓疱病、丹毒、蜂窝组织炎、坏死性筋膜炎、链球菌中毒性休克综合征、菌血症、急性风湿热、急性肾小球肾炎、结节性红斑、p.a.n.d.a.s(与链球菌感染相关的小儿自身免疫性神经精神疾病)、慢性疲劳综合征(cfs)和纤维肌痛、良性肌束颤综合征(bfs)。为了实施本发明的组合物,可以优选采用杨树芽的水醇提取物,其中浓度为30至70醇度。在特别优选的实施方式中,可以将该提取物冻干。任选地,可以将提取物与天然树胶共同冻干,以增加提取物在水中的溶解度,并使干燥的提取物更易于加工。然而,所获得且可以在实验部分看到的数据表明,与天然树胶共同冻干(负载)提高了提取物的粘膜粘附性能和保护性能,使得包含由树胶负载的提取物的本发明组合物特别有效。具体地,杨树芽提取物可以是通过包括以下步骤的方法能够获得的提取物:a.通过用85°乙醇提取来制备杨树芽的水醇提取物,b.通过用13°乙醇提取来制备杨树芽的水醇提取物,c.通过将在a.和b.中制备的提取物混合以获得多级分醇提取物,d.倾析和/或离心并过滤所述醇提取物(c.),收集上清液,e.将在d.中获得的经过过滤的上清液进行浓缩和冻干,并且任选地,f.向d.中获得的经过过滤的上清液加入天然树胶(选自在以下说明书中指出的多种树胶或其组合,特别是加入阿拉伯胶),然后进行浓缩和冻干。具体地,可以通过以下两个步骤来制备a.和b.中的提取物:通过利用单一提取溶剂的流动而渗滤消化来进行提取,以及利用装配有叶片搅拌器的提取器并将溶剂和芽二者移动来进行提取。可以在包括在35和55℃之间的温度下(例如,在包括在40℃-50℃范围(包括端点值)的温度下,特别是在约40℃或50℃的温度下)进行提取。可以将提取进行4至12个小时的时间长度,例如进行约8个小时。在步骤c.中将在步骤a.和b.中制备的提取物混合,优选以50:50的比率混合,但也可以以35:65、40:60、45:55、55:45、60:40、65:35的比率混合。通过将13°醇提取物逐渐加入至85°醇提取物中(添加速率:15至20l/min)来进行混合,但也可以进行逆向添加。在20°±5℃的温度下进行混合。通过在装配有锥形底部的容器中倾析至少72个小时以将在步骤c.中制备的多级分提取物澄清。一旦达到所述时间,使该提取物溢出,并在纤维素过滤器上进行过滤。可以以单一步骤或者以多次连续步骤在例如截留值为0.5至50微米(包括端点值)的板式过滤器上进行这种过滤,例如,0.5微米、15微米或30微米或甚至更高的截留值。在过滤结束时,控制醇浓度,并将其调节至50°±15°的醇度。作为倾析的替代方案,可以通过在立式离心机上离心以分离提取物,所述离心机以5至20升/分钟的流速进料。可以将在步骤d.中澄清的提取物以其原样作为多级分醇提取物。将在步骤d.中澄清的提取物如步骤e.那样进行浓缩和冻干工艺,以提供可以用于作为固体制剂的冻干提取物。将如在步骤d.中澄清的提取物(添加有阿拉伯胶或天然树胶)如步骤f.那样进行浓缩和冻干,以提供由阿拉伯胶负载的冻干提取物,可以将其用于作为固体制剂。可以以例如产生10-20%百分比固体的量采用阿拉伯胶或一种或多种天然树胶。图1:杨树芽的多级分醇提取物的方框图图2:杨树芽的冻干多级分提取物的方框图图3:杨树芽的由阿拉伯胶(或如下所示的一种或多种天然树胶)负载的冻干的多级分提取物的方框图根据上述方法获得的提取物表征为以下组分:根据上述报道的方法,以不同提取物的分析平均值得到这些值。根据一个实施方式,以上定义的以任何形式的杨树芽提取物可以具有0.3至45wt%的重量百分比。例如,根据以下的实施例可以是以液体形式的组合物:液体组合物实例1组分wt%杨树芽提取物0.70黄原胶1.00水55.40桃香料0.40柠檬香料0.10澄清的柠檬汁1.40食用植物甘油,以千克计15.00橙汁26.00总计100.00液体组合物实例2组分wt%杨树芽提取物1.00瓜尔胶1.00水55.10桃香料0.40柠檬香料0.10澄清的柠檬汁1.40食用植物甘油,以千克计15.00橙汁26.00总计100.00液体组合物实例3(强效喷雾剂)组分wt%62.7°杨树芽醇提取物39.76去离子水3.92植物甘油55.70柠檬稀精油0.01甜橙稀精油0.01天然的柑橘香料0.60总计100.00液体组合物实例4(无醇喷雾剂)固体组合物实例1组分wt%冻干的杨树芽提取物5.00甘露醇46.14他拉胶6.56菊粉38.60冻干的树莓汁0.40冻干的桃汁2.50天然的柠檬香料0.80天然的樱桃香料1冻干的锦葵提取物0.8总计100.00固体组合物实例2固体组合物实例3(成人片剂)组分wt%冻干的杨树芽提取物1.08红糖71.5阿拉伯胶10.82蜂蜜3青柠(树)提取物1.5冻干的橙汁10.5橙香料1.5柠檬精油0.1总计100固体组合物实例4(儿童片剂)组分wt%冻干的杨树芽提取物1.14红糖83.5阿拉伯胶6.56菊粉1.6冻干的草莓汁2.4冻干的接骨木汁2天然的草莓香料1天然的樱桃香料1冻干的青柠(树)提取物0.8总计100.00本发明的组合物可以是例如以粉剂、片剂、胶囊剂、硬明胶或软明胶、糖浆剂、喷雾剂、混悬剂的形式。因此,可以采用本领域技术人员已知的药学上可接受的载体、辅料、香料、防腐剂中的一种或多种。从广义上讲,当将组合物制备成液体形式时,该组合物将包含作为活性成分的本文所述的任意实施方式中的杨树芽提取物和本领域技术人员已知的辅料、溶剂、香料、防腐剂等中的一种或多种。作为非限制性的实例,可以采用以下中的一种或多种作为辅料:天然树胶,例如阿拉伯胶、黄原胶、瓜尔胶、他拉胶或其混合物;天然和合成的多元醇,例如蔗糖、甘露醇、山梨糖醇、木糖醇或其混合物;纤维素和纤维素衍生物,例如羟乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素或其混合物;合成聚合物,例如聚乙烯吡咯烷酮、聚甲基丙烯酸酯或其混合物;麦芽糖糊精、菊粉和/或环糊精。通常作为非限制性的实例,可以采用乙醇、异丙醇、甘油、丙二醇或其混合物作为溶剂。也可以采用天然或冻干的果汁,例如苹果汁、梨汁、橙汁、柠檬汁、树莓汁、蓝莓汁或其混合物;天然或人工的香料,例如草莓香料、柠檬香料、橙香料、树莓香料、桃香料、樱桃香料、复合莓果香料、橘子香料或其混合物;精油(e.o.),例如柠檬精油、橙精油、薄荷精油、桉树精油或其混合物。从广义上讲,当将组合物制备成固体形式时,该组合物将包含作为活性成分的本文所述的任意实施方式中的杨树芽提取物和本领域技术人员已知的辅料、溶剂、香料、防腐剂等中的一种或多种。作为非限制性的实例,可以采用以下中的一种或多种作为辅料:糖类,例如蔗糖、甘露糖醇、山梨糖醇、木糖醇或其混合物;纤维素和纤维素衍生物,例如微晶纤维素、羧甲基纤维素钠或其混合物;麦芽糖糊精、环糊精和/或菊粉。可以采用以下中的一种或多种:淀粉和淀粉衍生物,例如大米淀粉、马铃薯淀粉、玉米淀粉、预胶化淀粉或其混合物;润滑剂,例如硬脂酸、硬脂酸镁、甘油山嵛酸酯或其混合物;天然和合成的香料,例如草莓香料、柠檬香料、橙香料、树莓香料、桃香料、樱桃香料、复合莓果香料或其混合物;精油,例如柠檬精油、橙精油、薄荷精油、桉树精油或其混合物;冻干的果汁,例如苹果汁、梨汁、橙汁、柠檬汁、树莓汁、蓝莓汁、草莓汁、接骨木汁(elderjuice)或其混合物;青柠(树)、锦葵、芦荟、蜀葵的粉末或冻干天然提取物或其混合物;甜味剂,例如蜂蜜、糖类、阿斯巴甜、环己氨基磺酸盐、乙酰磺胺酸钾、甜叶菊提取物、三氯蔗糖或其混合物。在说明书和权利要求书中的任何地方,术语“包括(comprising)”可以由术语“由...组成(consistingin)”或“由......制成(madeof)”替代。提供以下实施例是为了进一步阐明本发明而不是为了限制性目的。实施例1.粘膜粘附测定法良好的粘膜粘附效果是最重要的要求,从而该产品可以保留在预期的作用部位(咽粘膜),并在该处以物理性方式实施其保护性和治疗性作用,如以上描述中已经解释的。该测定法的主要目的是评估以不同配方的本发明组合物对合适的细胞模型(设想采用口颊细胞)的体外粘附性。该测定法的第二个目的是确定随着时间推移对人工唾液溶液流的抗生物粘附能力。通过评估产品粘附细胞的能力(通过抑制凝集素(对葡萄糖苷残基和甘露糖苷残基具有较强亲和力的蛋白)与膜糖蛋白结合)来确定以不同配方的本发明组合物的粘膜粘附作用。通过比色反应来测定粘膜粘附作用的程度,该比色反应能够量化未被凝集素结合而是被粘膜粘附产品结合的糖蛋白位点。基于如下图所示的特定凝集素标记系统,可以进行该比色反应:吸光度值的降低与产品粘附(“粘膜粘附”)细胞的能力成正比。将粘膜粘附能力表示为抑制糖蛋白/凝集素结合的百分比,并且根据以下等式表示由产品占据的粘膜位点的百分比:产品的粘膜粘附百分比=(1-样品吸光度/对照吸光度)×100考虑到在实际使用中是在将产品递送后立即发生产品与口咽腔中存在的唾液混合的事实,因而在将产品稀释后施用。以下图表描绘了以不同配方的根据本发明组合物的不同样品所获得的结果。表1-根据1∶2.5稀释的实例(实例固体组合物3)以口服溶解片剂形式的产品对人口颊细胞的粘膜粘附百分比。样品稀释1∶2.5稀释1∶5a69.555.3b71.458.8c65.652.7平均值±s.d.(%)68.8±3.055.6±1.8稀释度1∶2,5相对于1∶5p<0.01表2-实例固体组合物4以1∶2.5和1∶5稀释的产品对人口颊细胞的粘膜粘附百分比。样品稀释1∶2.5稀释1∶5a63.848.5b57.740.6c66.452.3平均值±s.d.62.6±4.547.1±3.5稀释度1∶2.5相对于1∶5p<0.01表3-实例液体组合物4的未稀释或(1∶2和1∶5)稀释的产品对人口颊细胞的粘膜粘附百分比。样品未稀释稀释1∶2稀释1∶5a74.764.258.3b82.473.456.6c71.861.748.8平均值±s.d.(%)76.3±5.466.4±6.154.6±5.1未稀释相对于稀释1∶2p>0.05,未稀释相对于稀释1∶5p<0.05;稀释1∶2相对于稀释1∶5p>0.05表4-实例液体组合物3的未稀释或(1∶2和1∶5)稀释的产品对人口颊细胞的粘膜粘附百分比。样品未稀释稀释1∶2稀释1∶5a75.661.653.6b73.864.849.7c70.358.751.5平均值±s.d.73.2±2.761.7±3.151.6±2.0未稀释相对于稀释1∶2p<0.01;稀释1∶2相对于稀释1∶5p<0.01在实验的第二阶段,通过使该系统经受2ml/min的人工唾液流(由含有ph7的磷酸盐缓冲液和0.5%粘蛋白的等渗水溶液制成)来评估组合物随时间推移保持粘附于粘膜的能力。所获得的结果突出强调了在施用后第一个小时期间令人感兴趣的产品保持生物粘附于粘膜的能力。以下表5报道了利用1∶2.5稀释的组合物(实例固体组合物3)所获得的粘膜粘附层在不同时间(0.5小时、1小时和2小时)对模拟的唾液溶液(0.9%nacl生理溶液)的抗性。样品0小时0.5小时1小时2小时a69.563.454.743.3b71.455.848.834.8c65.652.347.540.2平均值±s.d.(%)68.8±3.057.2±5.650.3±3.839.4±4.3时间0小时相对于时间0.5小时p<0.05;时间0.5小时相对于时间1小时p>0.05时间2小时相对于时间1小时p<0.05表6:利用1∶2.5稀释的组合物(儿童片剂(配方150728/1))所获得的粘膜粘附层在不同时间(0.5小时、1小时和2小时)对模拟的唾液溶液(0.9%nacl生理溶液)的抗性。样品0小时0.5小时1小时2小时a63.858.552.335.5b57.752.847.931.6c66.462.253.538.2平均值±s.d.62.6±4.557.8±4.751.2±2.935.1±3.3时间0小时相对于时间0.5小时p>0.05;时间0.5小时相对于时间1小时p<0.05时间2小时相对于时间1小时p<0.01表7:利用1∶2稀释的组合物(实例液体组合物4)所获得的粘膜粘附层在不同时间(0.5-2小时)对人工唾液溶液的抗性。样品0小时0.5小时1小时2小时a64.263.555.647.2b73.368.952.843.7c61.758.446.338.5平均值±s.d.66.4±6.163.6±5.351.6±4.843.1±4.4时间0小时相对于时间0.5小时p>0.05;时间0.5小时相对于时间1小时p<0.05时间1小时相对于时间0小时p<0.01;时间2小时相对于时间1小时p>0.05表8:利用1∶2稀释的产品(实例液体组合物3)所获得的粘膜粘附层在不同时间(0.5-2小时)对人工唾液溶液的抗性。样品0小时0.5小时1小时2小时a61.655.350.545.2b64.851.848.340.6c58.747.441.638.5平均值±s.d.61.7±3.151.5±4.046.8±4.741.4±3.4时间0小时相对于时间0.5小时p<0.05;时间0.5小时相对于时间1小时p>0.05时间1小时相对于时间0小时p=0.01;时间2小时相对于时间1小时p>0.05在该实验中获得的结果表明,本发明组合物的不同配方对口颊细胞具有较高的粘膜粘附能力。此外,粘膜粘附保护层对人工唾液溶液流的抗性的评估,能够突出强调在施用后第一个小时期间具有良好的粘膜粘附保持能力。根据所获得的结果,可以表明本发明的组合物被证明具有良好的粘膜粘附抗性,其可以在口咽粘膜上发挥真正的保护性作用。2.阻隔测定法该测定法的目的是通过测定其与已知刺激剂相比的成膜和保护性能力来证明本发明组合物的作用机理,所采用的刺激剂是脂多糖(lps)膜,一种经典的炎症诱导模型。所述测定法旨在突出强调该产品限制粘膜与外部刺激剂之间接触的有效能力。所选择的刺激剂是从大肠杆菌(escherichiacoli)细胞膜中分离出来的。lps尺寸使得能够考虑到该阻隔能有效地防止粘膜免受灰尘、烟雾、花粉和同时产生刺激并因此导致因该特定微妙环境引起的不同病理学发作的其它物质。更详细地分析实验方案,通过测定il6产生来评估样品作为阻隔的能力,并且该il6的产生是细胞(成纤维细胞)层与lps之间接触的结果。该实验系统提供了采用特定的transwell孔,该transwell孔配备有涂覆胶原蛋白的半透膜,以防止沉积在底部的细胞与在悬垂的半透膜上分层的样品之间直接接触,该半透膜代表孔的两部分之间的唯一交流途径。将lps置于样品上方的空间,由此穿膜越是困难,样品本身发挥的阻隔效应越强。因此,对在添加lps后+24个小时所产生的白细胞介素的定量是由经测定样品所发挥的阻隔效应的直接证据。il6抑制是阻隔效应的直接测定结果。将阻隔效应(be)表示为il-6释放减少的百分比,并且通过与阳性对照(c+)获得的值(即,在不存在样品下仅用lps处理的细胞所获得的)比较而获得。%be=产生的il-6(pg/ml)抑制%以下表格报道了用本发明组合物的不同实施方式以一式三份实施实验所获得的结果。由于存在高浓度的树脂,对以1:2.5稀释的产品和1:5稀释的产品进行该阻隔测定法。首先是lps激发后细胞分泌il6(皮克),随后在下表中报道了与阳性对照相比的%抑制。表9:根据本发明详述部分所报道的实施例利用以成人片剂形式的本发明组合物(实例固体组合物3)的配方进行阻隔测定法产生的il6。从结果看出,很明显的是在存在所测定产品的实验中所产生的il-6浓度在两种稀释度下都显著降低,表明随时间延长的阻隔,在产品部分损失的情况下(由于无法将片剂缓慢溶解在口中)也是有效的。阴性对照所检测到的il-6值等于64.6pg/μl,其可同化为正常基础值,即非炎性病症。图2a中的图表清楚地显示了产品对细胞发挥的保护作用:数据以相比于对照c-的倍数(f.o.)表示。根据在阻隔测定法和阳性对照中所测定的il-6平均值,如下计算il-6释放减少的百分比:100-[(il-6样品)/il-6c+)×100]因此,通过应用该公式,得到在所测定样品存在下il-6产生减少的值,如表10所报道的,对于按照上面详述部分描述的以成人片剂形式制备的本发明组合物(实例固体组合物3),与阳性对照相比,其在1:5稀释下为54%,在1:2.5稀释下为48%。阻隔效应表11根据本发明详述部分中报道的实施例利用以儿童片剂形式的本发明组合物(实例固体组合物4)的配方在阻隔测定法中产生的il6。根据在阻隔测定法和阳性对照中测定的il-6平均值,如下计算il-6释放减少的百分比:100-[(il-样品)/il-6c+)×100]因此,通过应用该公式,得到在所测定样品存在下il-6产生减少的值,如表12所报道的,对于按照上面详述部分描述的以儿童片剂形式制备的本发明组合物(实例固体组合物4),与阳性对照相比,其在1∶5稀释下为49%,在1∶2.5稀释下为51%。阻隔效应将值四舍五入为3位小数表13:根据在本发明详述部分中报道的实施例利用以强效喷雾剂形式的本发明组合物(实例液体组合物3)的配方在阻隔测定法中产生的il6。根据在阻隔测定法和阳性对照中测定的il-6平均值,如下计算il-6释放减少的百分比:100-[(il-样品)/il-6c+)×100]因此,通过应用该公式,得到在所测定样品存在下il-6产生减少的值,如表14所报道的,对于按照上面详述部分描述的以强效喷雾剂形式制备的本发明组合物(实例液体组合物3),与阳性对照相比,其为39%。下表15示出了根据本发明详述部分中报道的实施例利用以无醇喷雾剂形式的本发明组合物(实例液体组合物4)的配方在阻隔测定法中产生的il6。根据在阻隔测定法和阳性对照中测定的il-6平均值,如下计算il-6释放减少的百分比:100-[(il-6样品)/il-6c+)×100]因此,通过应用该公式,得到在所测定样品存在下il-6产生减少的值,如表16所报道的,对于按照上面详述部分描述的以无醇喷雾剂形式制备的本发明组合物(实例液体组合物4),与阳性对照相比,其为56%。为了验证所采用的方法,并证实结果唯一取决于所测定样品的阻隔效应,并不具有任何药理学、免疫学或代谢方面的作用(例如,细胞因子合成调节),通过同时对每个样品进行的内部对照(ic)来辅助阻隔测定法。在ic测定法中,首先用lps刺激细胞,然而随后仅将样品加入transwell中:在这种情况下,0%的il6抑制将清楚地表明所测定组合物的存在提供了物理性保护作用,而绝不干扰细胞的细胞因子合成。下表17报道了在内部对照实验中测定的il-6浓度值,其中在lps激发后用以成人片剂形式的组合物(实例固体组合物3)进行所述处理:相比于内部对照c-的倍数将值四舍五入为3位小数下表18报道了在内部对照实验中测定的il-6浓度值,其中在lps激发后用以儿童片剂形式的组合物(实例固体组合物4)进行所述处理:相比于内部对照c-的倍数将值四舍五入为3位小数下表19报道了在内部对照实验中测定的il-6浓度值,其中在lps激发后用以强效喷雾剂形式的组合物(实例固体组合物3)进行所述处理:下表20报道了在内部对照实验中测定的il-6浓度值,其中在lps激发后用以无醇喷雾剂形式的组合物(实例液体组合物4)进行所述处理:发现在这些实验中获得的值与用于阻隔测定法的阳性对照(不存在样品)的那些值相同,并且证实在lps激发后施加的样品如何不影响炎症调节因子的产生,因而不具有直接的抗炎效应。这在图5报道的图中得以更好地表示,其中图5表示了以相对于c的倍数表示的细胞产生的il-6的值。3.用于自由基清除活性的dpph测定法通过dpph(2,2-二苯基-1-苦肼基)测定法评估由根据本说明书的杨树芽提取物(通过以上描述的方法获得的,并具有以上描述的性能)引导的清除剂抗氧化活性;dpph是一种有色的稳定基团:当与抗氧化化合物发生化学反应时,它会改变颜色,并可通过分光光度读数进行检测。因此,该测定法的目的是证明所测定样品具有良好的抗氧化活性,其是以纯化学方式(氢转移至自由基)进行的,当施加于生物基质时不涉及药理学、免疫学或代谢方面的机制。所测定样品是根据本说明书的杨树芽的提取物,浓度为1000μg/ml、100μg/ml和10μg/ml。将活性与用于用作阳性对照的维生素c的活性进行比较。从图6中可以看出,根据本发明的杨树芽提取物在1000μg/ml和100μg/ml的较高浓度下表现出优异的抗氧化活性,且在10μg/ml的较低浓度下表现出良好的活性。4.生物膜形成抑制测定法在该测定法中采用的方法利用了微生物粘附于聚苯乙烯板孔并形成生物膜的能力,然后通过结晶-紫染色测定生物膜质量。在该测定法中采用的细菌是涉及咽部粘膜感染最常见的一种细菌,即酿脓链球菌(streptococcuspyogenes);所测定样品是根据本说明书的杨树芽提取物(可通过以上描述的方法获得,并具有以上描述的性能)。该测定法的第一阶段是评估最小抑制浓度(mic),即抑制微生物生长的最低样品浓度。选择抗菌的庆大霉素作为阳性对照。在第二阶段,测定抑制生物膜形成的能力;将所测定样品以等于或低于mic的浓度添加到培养基中,以排除抗生物膜活性是由于微生物生长抑制引起的。在足够的培养期后,用结晶紫将形成的生物膜染色;染色后,用水去除过量的染料,并用乙醇溶解粘附于生物膜上的染料。通过分光光度计在570nm处分析所得的溶液:所形成的生物膜质量越大,由分析获得的吸光度强度将越大;因此,抗生物膜活性和记录的吸光度彼此成反比。对于每个样品,所采用的浓度是1×mic、0.5×mic和0.1mic。报道的数据是以一式三份进行的9次测定的平均值。用t检验计算统计学显著性,*p<0.01和**p<0.001(处理的细菌相对于未处理的细菌)。该测定法显示出与标准的50%水-醇提取物相比,本发明的提取物如何更有效。5.在其不同实施方式中的根据本发明的组合物与蜂胶喷雾剂之间的粘膜粘附和抗洗涤性的比较性测定按照以上实施例1的描述进行该测定法,从而测定在不同稀释度下的本发明组合物和蜂胶喷雾剂。表中报道的数据显示,尤其在较高的稀释度下本发明的组合物与蜂胶相比,如何具有更大的粘膜粘附效果。表21表22表23表24从以上报道的测定法中明显看出的,所测定组合物在经过测定的任何实施方式中(固体,含醇喷雾剂,无醇喷雾剂)显示出杨树芽的提取物比蜂胶具有更大的粘膜粘附能力,特别是在较高稀释度的所测定产品中可知的,如从用1:5稀释度获得的数据是显而易见的。6.水醇多级分提取物的制备将黑杨(populusnigra)芽破碎,并通过配备有机械搅拌器的提取器以浓度降低的乙醇进行两步提取,用85%乙醇进行第一步并用13%乙醇进行第二步。采用的d/s比等于1:6。提取温度等于40℃。用85°乙醇提取的时间等于8个小时,用13°乙醇提取的时间等于8个小时。将按照描述所获得的醇提取物以50:50的比率重新合并。设想将13°醇提取物加入至85°醇提取物中(添加速率等于16l/min)以进行混合。在20°±5℃下进行混合。在添加结束时,将混合物在20°±5℃下倾析72个小时,然后回收上清液,并在配备有截留值为30μm的纤维素过滤器的板式过滤器上进一步过滤。在过滤结束时,检查醇浓度,并调节至62°±1°醇度。7.冻干的多级分提取物的制备不更改按照实施例1的描述所获得的澄清醇提取物的醇浓度,根据标准方案通过使用薄膜蒸馏系统以乙醇蒸发来进行浓缩,其中设想将待浓缩的提取物以约500l/h的流速进行进料;通过设定0.6-0.8巴的残余真空(residualvacuum)进行操作,并将加热蒸发壁的流体设定在140℃,从而在去除乙醇后得到浓缩的含水提取物。将由此获得的含水提取物进行冷冻干燥。8.由阿拉伯胶负载的冻干多级分提取物的制备将按照实施例1的描述所获得的澄清的醇提取物与阿拉伯胶混合,并按照实施例2的描述进行浓缩和冻干。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1