一种抗血小板聚集的爵床提取物及其制备方法和用途与流程
本发明涉及一种抗血小板聚集的中药提取物及其制备方法和用途,具体涉及一种抗血小板聚 集的爵床提取物及其制备方法和用途,属于医药技术领域。
背景技术:
爵床来源于爵床属植物爵床Justicia procumbens L.的干燥全草。又名爵卿、香苏、赤 眼老母草、苍蝇翅等,曾收录于《中华人民共和国药典》(1977年版)一部。爵床为一年生 匍匐草本,地上部分一般长15~50cm,生长于阴湿处,主要分布于中国华中、东南沿海、西 南部及台湾省,国外主要分布于东南亚和非洲,资源丰富。本品长于清热解毒、利湿消积、 活血止痛。临床上常用来治疗感冒发热、咽喉肿痛、疳积、湿热泻痢、疟疾、肠炎、肾炎水 肿等。学术论文“爵床属植物的化学成分和药理活性研究进展”,公开了爵床属植物中木脂素、 黄酮等化学成分及其药理作用,披露了爵床属植物化学成分具有抗肿瘤、抗病毒和抗血小板 凝集的活性,其中抗肿瘤活性最为显著。
心脑血管系统疾病为严重危害人类健康的重大疾病,具有高复发率、高致残率、高死亡 率的特点。抗血小板治疗是心脑血管系统疾病重要的防治手段,抗血小板活化药物的研发已 成为本科学领域的热点。目前临床上有效的药物种类繁多,如阿司匹林、氯吡格雷等,但这 些化学药物不良反应时常发生,使传统中药受到越来越多的关注。学术论文“Antiplatelet arylnaphthalide lignans from Justicia procumbens”(Journal of Natural Products,1996) 公开了学者Chen从爵床的乙醇提取物中获得Justicidin A(爵床脂定A)、Chinensinaphthol (金不换萘酚)等8个木脂素,离体药理活性研究结果显示新爵床脂定A、金不换萘酚都能 明显抑制由花生四烯酸诱导的血小板聚集作用,优于阳性药阿司匹林,但花生四烯酸仅为能 引起血小板聚集的多种诱导剂中的一种,这些化学物质能否抑制其他诱导剂引起的血小板聚 集还需要展开深入研究。学术论文“爵床属植物的化学成分和药理活性研究进展”,公开了爵 床脂定A具有抗肿瘤和抗病毒双重作用,爵床脂定B具有抗肿瘤、抗病毒、抗血小板凝聚三 重作用,但对爵床脂定A、爵床脂定B的研究信息披露甚少。
中国发明专利CN104086537A公开了一种从爵床草中提取爵床定A(即爵床脂定A)的方 法,具体方法为:1)将爵床草粉碎加入7~10倍量80~95%乙醇回流提取,提取液回收乙醇, 浓缩液上大孔树脂,用5~10倍柱体积50~90%乙醇溶液洗脱,洗脱液减压浓缩得浓缩液;2) 上述浓缩液加入乙酸乙酯萃取,萃取液继续浓缩成浸膏采用高速逆流色谱分离,根据图谱收 集流分,流分减压干燥即得爵床定A。
但是CN104086537A技术方案仍然存在缺陷与不足:(1)该制备方法所制备的爵床定A为 单一活性成分,导致爵床药材中其他具有抗血小板聚集的活性成分丢失,使得爵床药材未得 到充分利用,利用率低;(2)制备爵床定A的工序繁琐,制备方法需配备高速逆流色谱,降 低了制备方法的通用性。因此,我们迫切需要开发一种爵床药材利用率高、制备工艺简便的 具有抗血小板聚集活性的爵床提取物。
技术实现要素:
本发明的目的是提供一种具有抗血小板聚集活性的爵床提取物及其制备方法和用途,所 制备的爵床提取物抗血小板聚集活性高、毒性低,且爵床药材利用率高,能作为活性成分用 于制备心血管药物或保健食品;本发明爵床提取物制备方法简单、条件温和、通用性高。
实现本发明技术目的采用的技术方案是:
一种抗血小板聚集的爵床提取物,所述爵床提取物包含6′-羟基爵床脂定B、新爵床脂 定B。
优选的,所述爵床提取物中还包含(2R,3R)-3-(3,4-二甲氧基苄基)-4-羟基-2-(3,4,5- 三甲氧基苄基)乙酸丁酯,(2R,3R)-2,3-二(3,4-二甲氧基苄基)-4-羟丁基乙酯。
优选的,所述爵床提取物中还包含爵床苷L、爵床脂定B、金不换甲醚和新爵床脂定A。
6′-羟基爵床脂定B英文名6′-Hydroxy Justicidin B;爵床脂定B英文名Justicidin B;新爵床脂定B英文名Neojusticin B;(2R,3R)-2-(3,4-二甲氧基苄基)-4-羟基-3-(3,4,5- 三甲氧苄基)丁基单醋酸盐为新发现的化合物,按系统命名法为 (2R,3R)-2-(3,4-dimethoxybenzyl)-4-hydroxy-3-(3,4,5-trimethoxybenzyl)butyl acetate;(2R,3R)-2,3-二(3,4-二甲氧苄基)-4-羟基丁基单醋酸盐为新发现的化合物,按系 统命名法为(2R,3R)-2,3-bis(3,4-dimethoxybenzyl)-4-hydroxybutyl acetate;爵床苷L英 文名Procumbenoside L;金不换甲醚英文名Chinensinaphthol methyl ether;新爵床脂定 A英文名Neojusticin A。爵床提取物中所含的化合物化学结构式如表1所示。
表1爵床提取物化合物化学结构式
优选的,所述爵床提取物中6′-羟基爵床脂定B的含量不低于0.2wt%、新爵床脂定B的 含量不低于0.3wt%。
爵床提取物中化合物的鉴别和含量测定采用液相色谱–质谱联用技术(LC-MS),又叫液 质联用技术,也可以采用其他光谱和色谱技术,如高效液相色谱法(HPLC)。
爵床提取物具有较强的抗血小板聚集功效,其抗血小板聚集的能力不仅强于阿司匹林, 同时也强于爵床脂定B。说明爵床提取物中富集了多种具有抗血小板聚集的活性成分,它们 的活性或协同作用强于爵床脂定B。爵床提取物不仅提高了药物活性,同时最大程度地提高 了药材的利用率,减少了资源的浪费。
爵床提取物毒性小,安全性高。爵床提取物的LD50值为2.16g/kg,相当于180.00g生药 /kg,符合低毒化合物标准。解剖死亡及存活小鼠,肉眼观察心、肝、脾、肺、肾等重大脏器 的变化,发现部分给药组死亡小鼠肾脏上出现白色小点且颜色偏白,其余重要脏器未见明显 异常。给药组存活小鼠体重较空白组增长慢,喂养14天后,各组存活动物体重增长趋势均与 空白组相接近。表明爵床提取物的毒性较低,临床用药安全。
一种爵床提取物的制备方法,包括如下步骤:
(1)爵床药材用5~20倍量(W/V)50~90%(V/V)有机溶剂提取,得到提取液,所述有 机溶剂为甲醇、乙醇、丙酮或甲醇、乙醇、丙酮含酸溶液,提取方法为渗漉、回流或超声;
(2)将步骤(1)所得提取液减压回收有机溶剂得到浓缩液,所述浓缩液用乙酸乙酯萃 取,萃取液减压回收乙酸乙酯,干燥后得到乙酸乙酯部位浸膏;
(3)将步骤(2)所得乙酸乙酯部位浸膏上色谱柱纯化,洗脱液合并后干燥得到爵床提 取物,色谱柱填料为硅胶、大孔吸附树脂、凝胶或聚酰胺。
用比浊法检测爵床提取物的抗聚集率,用二磷酸腺苷(ADP)作为诱导剂诱导血小板聚 集。实验结果表明爵床提取物聚集抑制率高于阿司匹林。
步骤(1)优选乙醇渗漉法提取,渗漉液的流速为每公斤爵床药材10~20mL/min。
优选的,步骤(2)浓缩液先用石油醚萃取,弃去石油醚,再用乙酸乙酯萃取。发明人曾 采用系统溶剂法,浓缩液分别用石油醚、乙酸乙酯、正丁醇萃取,萃取液减压回收溶剂,干 燥后得到石油醚部位、乙酸乙酯部位、正丁醇部位、水部位浸膏;所述石油醚部位、乙酸乙 酯部位、正丁醇部位、水部位浸膏分别通过比浊法测定对花生四烯酸(Arachidonic acid)、 二磷酸腺苷(ADP)、凝血酶(Thrombin)和血小板活化因子(Platelet-activating factor)诱 导的血小板聚集的抵抗作用,结果乙酸乙酯部位浸膏活性最好。爵床提取物有效物质群能多 靶点抑制不同诱导剂诱导的血小板聚集,取得了意想不到的效果。
优选的,步骤(3)乙酸乙酯部位浸膏用大孔吸附树脂柱纯化,大孔吸附树脂柱纯化以乙 醇-水洗脱,弃去30wt%~60wt%乙醇洗脱液,收集80wt%~95wt%乙醇洗脱液,80wt%~ 95wt%乙醇洗脱液体积为1~6倍柱体积。发明人曾采用硅胶柱纯化以混合溶剂石油醚-乙酸 乙酯或石油醚-丙酮洗脱,石油醚-乙酸乙酯或石油醚-丙酮的体积比为4:1~1:3,洗脱体积为 爵床药材重量的6~10倍;凝胶柱纯化以氯仿-甲醇洗脱,氯仿-甲醇体积比为2:1~1:1,氯仿 -甲醇洗脱液体积为3~10倍柱体积;聚酰胺柱纯化以乙醇-水或甲醇-水洗脱,洗脱液浓度为 50wt%~80wt%,体积为8~10倍柱体积。结果上述方法均能制得有效成分含量相当的爵床 提取物,但大孔吸附树脂柱有效成分富集效率高、成本低、毒性小。
优选的,步骤(3)大孔吸附树脂柱填料为D101型大孔树脂。
优选的,步骤(2)所述石油醚、乙酸乙酯、水饱和的正丁醇的用量与浓缩液的体积比为 0.5:1~2:1。
优选的,爵床提取物作为活性成分用于制备心血管药物或保健食品,如抗血小板聚集和 抗凝血药物或保健食品。将抗血小板聚集爵床提取物作为活性成分可提高抗血小板聚集的疗 效,同时能减少制剂的服用剂量,抗血小板聚集爵床提取物作为原料与药学上可接受的辅料 制备成药学上所接受的制剂,如软胶囊、颗粒、胶囊、片剂、注射剂或口服液。
本发明的有益效果在于:
(1)本发明制备的爵床提取物中含6′-羟基爵床脂定B、新爵床脂定B,其抗血小板聚 集活性强于阿司匹林、爵床脂定B,取得了意想不到的效果。
(2)本发明制备的爵床提取物含有多种有效成分,且药理活性较爵床脂定B更高,不仅 富集了活性较爵床脂定B更高的新的具有抗血小板聚集的化合物,同时也提高了爵床药材的 利用率。
(3)本发明制备的爵床提取物不仅对花生四烯酸诱导的血小板聚集有抑制作用,还对二 磷酸腺苷、凝血酶、血小板活化因子诱导的血小板聚集同样有抑制作用。相对于单体化合物 作用于单靶点(例如氯吡格雷的体内代谢物作用靶点是血小板膜上二磷酸腺苷受体P2Y12, 因而只能抑制二磷酸腺苷诱导的血小板聚集),爵床提取物有效物质群能多靶点抑制不同诱导 剂诱导的血小板聚集,取得了意想不到的效果。
(4)本发明制备的爵床提取物是在药理活性试验的指导下完成的,获取爵床提取物目标 性强,准确性高。
(5)本发明制备的爵床提取物安全性高,爵床提取物的LD50值为2.16g/kg,相当于180.00 g生药/kg,符合低毒化合物标准;解剖死亡及存活小鼠,发现部分给药组死亡小鼠肾脏上出 现白色小点且颜色偏白,其余重要脏器未见明显异常。
(6)本发明制备方法简单、高效。含水有机溶剂能有效提取抗血小板聚集的活性成分, 乙酸乙酯能有效萃取活性成分,萃取物再经色谱柱纯化,整个制备方法操作简便易行、工艺 稳定,较新爵床脂定A活性单体的制备简便。
(7)本发明制备方法对仪器设备的要求的低,具有普适性和通用性强的优势。
附图说明
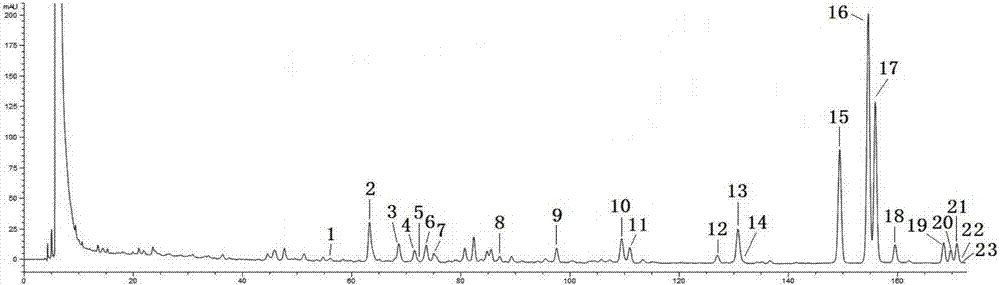
图1为爵床提取物HPLC图。
图2为乙酸乙酯部位HPLC-DAD-ESI-QTOF/MS 205nm紫外色谱图。
图3为乙酸乙酯部位HPLC-DAD-ESI-QTOF/MS正离子模式下的总离子流图。
图4为乙酸乙酯部位HPLC-DAD-ESI-QTOF/MS正离子模式下的总离子流图局部A放大图。
图5为乙酸乙酯部位HPLC-DAD-ESI-QTOF/MS正离子模式下的总离子流图局部B放大图。
图6为乙酸乙酯部位HPLC-DAD-ESI-QTOF/MS正离子模式下的总离子流图局部C放大图。
附图标记:1.爵床苷L;2.Justicidinoside C;3.爵床苷K;
4.5-methoxy-4,4-di-O-methylsecolariciresinol;5.Secoisolariciresinol dimethyl ether;6.Justicidinoside B;7.爵床苷B;8.爵床苷H;9.Tuberculatin;10.(2R,3R)-2-(3,4- 二甲氧基苄基)-4-羟基-3-(3,4,5-三甲氧苄基)丁基单醋酸盐;11.(2R,3R)-2,3-二(3,4-二甲 氧苄基)-4-羟基丁基单醋酸盐;12.6′-羟基爵床脂定B;13.Justin C;14.Diphyllin apioside-5-acetate;15.爵床脂定B;16.5-methoxy-4,4-di-O-methylsecolariciresinol diacetate;17.Secoisolariciresinol dimethyl ether diacetate;18.金不换甲醚; 19.新爵床脂定B;20.(-)-dihydroclusin diacetate;21.2,3-demethoxysecisolintetralin acetate;22.爵床脂定E;23.新爵床脂定A。
具体实施方式
为使本领域的技术人员可以更好的理解本发明并能予以实施,下面结合具体实施例对本 发明作进一步说明。
实施例1
(1)500g爵床药材用10倍量(W/V)80%(V/V)乙醇渗漉提取,渗漉提取速度为每公 斤爵床药材10mL/min,得到提取液;
(2)提取液减压回收乙醇,得到浓缩液,浓缩液依次用石油醚、乙酸乙酯各萃取2次, 每次用量与浓缩液体积比为1:1,弃去石油醚液,乙酸乙酯萃取液减压回收溶剂,干燥后得 到乙酸乙酯部位浸膏;
(3)将乙酸乙酯部位浸膏上硅胶柱,以混合溶剂石油醚-乙酸乙酯(1:3)洗脱,洗脱体 积为3L,洗脱液干燥后得到抗血小板聚集爵床提取物。
实施例2
(1)500g爵床药材用5倍量(W/V)50%(V/V)乙醇超声处理(功率250W,频率40kHz) 30分钟,得到提取液;
(2)提取液减压回收乙醇,得到浓缩液,浓缩液用乙酸乙酯萃取3次,每次用量与浓缩 液体积比为0.5:1,乙酸乙酯萃取液减压回收溶剂,干燥后得到乙酸乙酯部位浸膏;
(3)将乙酸乙酯部位浸膏上硅胶柱,以混合溶剂石油醚-丙酮(4:1)洗脱,洗脱体积为 5L,洗脱液干燥后得到抗血小板聚集爵床提取物。
实施例3
(1)500g爵床药材用20倍量(W/V)90%(V/V)甲醇回流提取2次,每次1小时,合 并两次提取液;
(2)提取液减压回收甲醇,得到浓缩液,浓缩液用正己烷、乙酸乙酯萃取2次,每次正 己烷、乙酸乙酯用量与浓缩液体积比为1.5:1,弃去正己烷液,乙酸乙酯萃取液减压回收溶剂, 干燥后得到乙酸乙酯部位浸膏;
(3)将乙酸乙酯部位浸膏上凝胶柱,以混合溶剂氯仿-甲醇(2:1)洗脱,洗脱体积为10 倍柱体积,洗脱液干燥后得到抗血小板聚集爵床提取物。
实施例4
(1)500g爵床药材用15倍量(W/V)50%(V/V)丙酮回流提取2小时;
(2)提取液减压回收丙酮,得到浓缩液,浓缩液用石油醚、乙酸乙酯萃取3次,石油醚、 乙酸乙酯用量与浓缩液体积比为0.5:1,弃去石油醚液,乙酸乙酯萃取液减压回收溶剂,干燥 后得到乙酸乙酯部位浸膏;
(3)将乙酸乙酯部位浸膏上凝胶柱,以混合溶剂氯仿-甲醇(1:1)洗脱,洗脱体积为3 倍柱体积,洗脱液干燥后得到抗血小板聚集爵床提取物。
实施例5
(1)500g爵床药材用9倍量(W/V)含0.5mol/L盐酸的78%(V/V)乙醇回流提取2小时, 得到提取液;
(2)提取液减压回收乙醇,得到浓缩液,浓缩液用乙酸乙酯萃取2次,每次用量与浓缩 液体积比为1.1:1,萃取液减压回收溶剂,干燥后得到乙酸乙酯部位浸膏;
(3)将乙酸乙酯部位浸膏上硅胶柱,以混合溶剂石油醚-乙酸乙酯(1:1)洗脱,洗脱体 积为3L,洗脱液干燥后得到抗血小板聚集爵床提取物。
实施例6
(1)500g爵床药材用10倍量(W/V)75%(V/V)乙醇渗漉提取,渗漉提取速度为每公 斤爵床药材10mL/min,得到提取液;
(2)提取液减压回收乙醇,得到浓缩液,浓缩液依次用正己烷、乙酸乙酯各萃取3次, 每次正己烷、乙酸乙酯的用量与浓缩液体积比为1:1,弃去正己烷液,乙酸乙酯萃取液减压回 收溶剂,干燥后得到乙酸乙酯部位浸膏;
(3)将乙酸乙酯部位浸膏上聚酰胺柱,以8倍柱体积80wt%乙醇洗脱,洗脱液干燥后得 到抗血小板聚集爵床提取物。
实施例7
(1)500g爵床药材用10倍量(W/V)90%(V/V)甲醇超声处理(功率200W,频率40kHz) 60分钟,得到提取液;
(2)提取液减压回收乙醇,得到浓缩液,浓缩液用乙酸乙酯萃取2次,每次乙酸乙酯的 用量与浓缩液体积比为1.5:1,乙酸乙酯萃取液减压回收溶剂,干燥后得到乙酸乙酯部位浸膏;
(3)将乙酸乙酯部位浸膏上聚酰胺柱,以10倍柱体积50wt%乙醇洗脱,洗脱液干燥后 得到抗血小板聚集爵床提取物。
实施例8
(1)500g爵床药材用10倍量(W/V)85%(V/V)乙醇渗漉提取,渗漉提取速度为每公 斤爵床药材15mL/min,得到提取液;
(2)提取液减压回收乙醇,得到浓缩液,浓缩液依次用石油醚、乙酸乙酯各萃取2次, 每次石油醚、乙酸乙酯的用量与浓缩液体积比为1.5:1,弃去石油醚液,乙酸乙酯萃取液减压 回收溶剂,干燥后得到乙酸乙酯部位;
(3)将乙酸乙酯部位上AB-8型大孔树脂,先用4倍柱体积30wt%乙醇洗脱、再用1倍 柱体积95wt%乙醇洗脱,95wt%乙醇洗脱液减压浓缩、干燥,得到抗血小板聚集爵床提取物。
实施例9
(1)500g爵床药材用10倍量(W/V)80%(V/V)乙醇渗漉提取,渗漉提取速度为每公 斤爵床药材20mL/min,得到提取液;
(2)提取液减压回收乙醇,得到浓缩液,浓缩液依次用石油醚、乙酸乙酯、正丁醇各萃 取1次,每次石油醚、乙酸乙酯、正丁醇的用量与浓缩液体积比为2:1,各萃取液分别减压回 收溶剂,干燥后得到石油醚部位、乙酸乙酯部位、正丁醇部位、水部位浸膏;
(3)比浊法测定80%乙醇部位、石油醚部位、乙酸乙酯部位、正丁醇部位、水部位浸膏 对花生四烯酸、二磷酸腺苷、凝血酶和血小板活化因子诱导的血小板聚集的抵抗作用;
(4)HPLC-DAD-ESI-MS法鉴定乙酸乙酯部位浸膏中的化学成分;
(5)将乙酸乙酯部位浸膏上硅胶柱,以混合溶剂石油醚-丙酮(2:1)洗脱,洗脱体积为 5L,洗脱液干燥后得到抗血小板聚集爵床提取物。
实施例10
(1)500g爵床药材用10倍量(W/V)80%(V/V)乙醇渗漉提取,渗漉提取速度为每公 斤爵床药材20mL/min,得到提取液;
(2)提取液减压回收乙醇至无醇味,得到浓缩液,浓缩液依次用石油醚、乙酸乙酯各萃 取3次,每次石油醚、乙酸乙酯的用量与浓缩液体积比为1:1,弃去石油醚液,乙酸乙酯萃取 液减压回收溶剂,干燥后得到乙酸乙酯部位;
(3)将乙酸乙酯部位上D101型大孔树脂,先用1倍柱体积50wt%乙醇洗脱、再用6倍 柱体积80wt%乙醇洗脱,80wt%乙醇洗脱液减压浓缩、干燥得到抗血小板聚集爵床提取物。
实施例11实施例9爵床抗血小板聚集活性部位的筛选
试验方法:对大鼠腹腔注射2%戊巴比妥钠(40mg·kg-1)麻醉,采用一次性负压采血容 器腹主动脉取血,混合均匀,低速离心得富血小板血浆(PRP),再高速离心得贫血小板血浆 (PPP)。按照血小板聚集仪操作规程,与样品孵育后加入不同诱导剂(花生四烯酸、二磷酸 腺苷、凝血酶和血小板活化因子)诱导聚集,每个浓度的样品平行测3次,记录5min内血小 板最大聚集率,血小板聚集抑制率(%)=(空白对照组血小板聚集率—试药组血小板聚集率) /空白对照组血小板聚集率×100%。80%醇提取物、乙酸乙酯部位、正丁醇部位和水部位浸膏 分别用DMSO溶解,再加pH7.4等渗溶液稀释。
试验结果:抑制四种诱导剂诱导的血小板聚集试验结果显示,乙酸乙酯部位的IC50值最 低,说明爵床抗血小板聚集的活性部位为乙酸乙酯部位。爵床不同部位抑制花生四烯酸诱导 的血小板聚集结果见表2、爵床不同部位抑制二磷酸腺苷诱导的血小板聚集结果见表3、爵床 不同部位抑制凝血酶诱导的血小板聚集结果见表4、爵床不同部位抑制血小板活化因子诱导 的血小板聚集结果见表5。
表2爵床不同部位抑制花生四烯酸诱导的血小板聚集结果
表3爵床不同部位抑制二磷酸腺苷诱导的血小板聚集结果
表4爵床不同部位抑制凝血酶诱导的血小板聚集结果
表5爵床不同部位抑制血小板活化因子诱导的血小板聚集结果
实施例12实施例9乙酸乙酯部位化学成分鉴定
试验方法:采用HPLC-DAD-ESI-MS法。高效液相色谱仪为安捷伦1200Infinity系列;质 谱仪为布鲁克匹配电喷雾(ESI)离子源的四级杆飞行时间(micrOTOF-Q)质谱仪;色谱柱为 菲罗门Synergi Polar-RP 80 A(4.6mm×250mm,4μm);流动相为乙腈-水系统梯度洗脱; 毛细管电压4500V、载气压力0.8bar、干燥气体流速8L/min、干燥气体加热温度200℃、质 谱扫描范围m/z 50~1600;乙酸乙酯部位加甲醇配制成0.3mg/mL的溶液;进样量10μL。
试验结果:共检测到23个化合物,其中9个为二芳基丁烷型木脂素,14个为苯代萘内 酯型木脂素。部分化合物因存在同分异构体,经化学分离后通过核磁共振谱确定结构。化合 物10和11为首次鉴定的新化合物。结果见图2~图6、表6。
表6 23个化合物名称
实施例13实施例10爵床提取物与乙酸乙酯部位、爵床脂定B和阿司匹林抗血小板聚集的比 较
试验方法:取健康的日本大耳兔,兔耳采血,混合均匀,低速离心得富血小板血浆(PRP), 再高速离心得贫血小板血浆(PPP)。按照血小板聚集仪操作规程,与样品孵育后加入二磷酸 腺苷诱导聚集,每个浓度的样品平行测3次,记录5min内血小板最大聚集率,血小板聚集抑 制率(%)=(空白对照组血小板聚集率—试药组血小板聚集率)/空白对照组血小板聚集率 ×100%。以5%DMSO溶液为空白对照,阿司匹林为阳性对照。爵床提取物、乙酸乙酯部位、 爵床脂定B和阿司匹林用DMSO溶解,再加pH7.4等渗溶液稀释。
试验结果:爵床提取物抗血小板聚集的活性强于乙酸乙酯部位、爵床脂定B和阳性对照 药阿司匹林。爵床提取物抗血小板聚集的活性强于乙酸乙酯部位,说明在过柱色谱时有效成 分得到进一步富集,低活性成分被舍弃;爵床提取物抗血小板聚集的活性强于爵床脂定B, 说明不仅富集了活性更高的新的具有抗血小板聚集的化合物,同时也提高了爵床药材的利用 率。结果见表7。
表7爵床提取物抗血小板聚集结果
实施例14实施例10爵床提取物单次给药毒性试验并初步评价毒性
试验方法:昆明小鼠60只,体重17.8~22.5g,雌雄各半。爵床提取物以0.5%的CMC-Na 溶液配置成不同浓度的受试药物。给药组和空白组均按照40mL/kg进行灌胃,对照组给予 0.5%的CMC-Na。给药组的给药剂量为1.37~3.62g/kg。
试验结果:根据各剂量结果,计算得到爵床提取物的LD50值为2.16g/kg,相当于180.00g 生药/kg,符合低毒化合物标准。解剖死亡及存活小鼠,肉眼观察心、肝、脾、肺、肾等重大 脏器的变化,发现部分给药组死亡小鼠肾脏上出现白色小点且颜色偏白,其余重要脏器未见 明显异常。给药组存活小鼠体重较空白组增长慢,喂养14天后,各组存活动物体重增长趋势 均与空白组相接近。表明爵床提取物的单次给药毒性较低,临床用药安全。
实施例15实施例10爵床提取物HPLC检测
试验方法:采用安捷伦1260液相色谱仪;色谱柱为菲罗门Synergi Polar-RP 80 A column (4.6mm×250mm,4μm);流动相采用乙腈-水系统,梯度洗脱程序为:0分钟15%乙腈, 130分钟35%乙腈,175分钟45%乙腈;检测波长为205nm;流速为1mL/min。
实施例10爵床提取物HPLC图见图1,提取物中6′-羟基爵床脂定B的含量为0.6wt%、 新爵床脂定B的含量为1.9wt%。
- 还没有人留言评论。精彩留言会获得点赞!