贝壳杉烯酸在制备抗抑郁症药物中的应用的制作方法
本发明属于药物技术领域,涉及贝壳杉烯酸的医药用途,具体涉及一种贝壳杉烯酸在有效治疗抑郁症的药物中的应用。
背景技术:
抑郁症是一种常见的心境障碍,以显著而持久的心境低落为主要临床特征,其患病率呈全球性增加,预计到2020年可能成为仅次于冠心病的第二大疾患。我国抑郁症的发病率大约为4%,抑郁症患者表现出无法适应社会,思维迟钝、记忆力下降等,是自杀、自残、自虐的高危人群,构成社会重大健康危机。不仅如此,临床研究发现,抑郁症与多种疾病如帕金森症、糖尿病等并存,给患者带来严重的神经精神负担。因此,抑郁症已成为一个凸显的社会问题,抑郁症的研究成为国内外关注的热点。
目前国内外研究认为抑郁症的发病机制复杂,与遗传、环境、社会等多种因素有关。主要涉及以下几种假说:1神经递质假说,中枢5-羟色胺神经系统功能紊乱、突触间隙5-羟色胺(serotonin,5-ht)、去甲肾上腺素(norepinephrine,ne)、多巴胺(dopamine,da)水平降低是导致抑郁症的主要发病机制之一。2神经营养因子假说,神经生长因子(nervegrowthfactor,ngf)、脑源性神经营养因子(brain-derivedneurotrophicfactor,bdnf)、胶质细胞源性神经营养因子(glial-derivedneurotrophicfactor,gdnf)等对神经元的生长、分化和维持神经元功能具有重要作用。海马区神经营养因子及其受体表达水平降低可降低神经发生和神经元存活,引发抑郁症。3神经内分泌假说,其中下丘脑-垂体-肾上腺(hypothalamic-pituitary-adrenal,hpa)轴功能亢进,皮质醇分泌过多,造成海马区神经元受损,进而引发抑郁症。
目前现代医学以提升突触间隙神经递质水平为抑郁症治疗的主要策略。代表的抗抑郁症药物主要有:三环类抗抑郁药(tricyclicantidepressant,tcas),如丙咪嗪等;选择性五羟色胺重摄取抑制剂(selectiveserotoninreuptakeinhibitor,ssri),如氟西汀等;单胺氧化酶抑制剂(monoamineoxidaseinhibitor,maoi),如苯乙肼等。这些药物具有多种副作用和较高的耐受性,且在治疗时间上存在延迟,提示仅通过调节神经递质水平防治抑郁症难以达到良好的效果。神经营养因子假说认为抑郁症的发病与神经发生受损密切相关,上调神经营养因子及其受体表达,促进神经发生可有效缓解抑郁症,这也有助于解释抗抑郁症药需要数周以恢复神经发生才能发挥疗效。因此,需以神经递质和神经营养因子为作用靶点,寻找新的抗抑郁症药物以有效的防治抑郁症。
贝壳杉烯酸(kaurenoicacid)是一种二萜类化合物,主要分布于五加科五加属植物中。但刺五加的主要有效成分为木脂素及其苷类、三萜及其苷类、香豆素、黄酮等,贝壳杉烯酸在刺五加中含量很低。贝壳杉烯酸为白色粉末,分子式:c20h30o2,分子量:302.46,其结构如下,具有舒缓血管平滑肌、抗痉挛、抗血小板聚集、抗肿瘤、降压、利尿、抗炎等作用。目前尚未有见将贝壳杉烯酸用于制备抗抑郁症药物中的应用。
技术实现要素:
本发明所要解决的技术问题是提供贝壳杉烯酸在制备抗抑郁症药物中的应用。所述的贝壳杉烯酸具有如下结构:
本发明涉及贝壳杉烯酸抗抑郁症的应用,其可显著上调神经递质水平、促进神经营养因子及其受体表达,并且在用于上述用途时具有使用安全和可长期服用等特点。因此,贝壳杉烯酸可在制备抗抑郁症药物中应用,该药物具有治疗抑郁症的用途。
贝壳杉烯酸可来源于市售或采用现有技术制备得到。
本发明应用的贝壳杉烯酸可以和药学上允许的任意一种辅料或药物赋形剂制成药物,其制剂可以是药学上允许的任意一种剂型,包括但不限于颗粒剂、片剂、冲剂、软胶丸、软胶囊、滴丸剂、软膏剂或注射剂。
本发明提供的药物,其给药形式主要包括口服给药、经皮给药或注射给药。
本发明中贝壳杉烯酸的给药量,因患者的状态、体重、给药方式等不同而异。比如在非口服情况下,肌肉、静脉、肠内给药0.1-200mg/(kg•d),口服情况下0.4-800mg/(kg•d)。
本发明中贝壳杉烯酸采用最大耐受量法给小鼠进行灌胃试验,结果表明,作用后小鼠均健康无异常反应,解剖无明显病变,脏器指数和血清指标与正常组无显著差异,贝壳杉烯酸对小鼠的经口ld50>15g/kg,说明贝壳杉烯酸对小鼠无毒性作用,是安全的。
与现有技术比较本发明的有益效果:贝壳杉烯酸可显著缩短正常小鼠强迫游泳和悬尾累积不动时间,对慢性应激抑郁大鼠具有显著的抗抑郁作用,可显著提高抑郁大鼠海马区5-羟色胺、去甲肾上腺素、5-羟吲哚乙酸/5-羟色胺水平和纹状体多巴胺水平,显著上调抑郁大鼠海马区神经营养因子及其受体表达,并且通过急性毒性实验表明,贝壳杉烯酸属于无毒级。因此,贝壳杉烯酸可在制备抗抑郁症药物中应用。本发明为贝壳杉烯酸提供了临床新用途,扩大了其应用范围。
附图说明
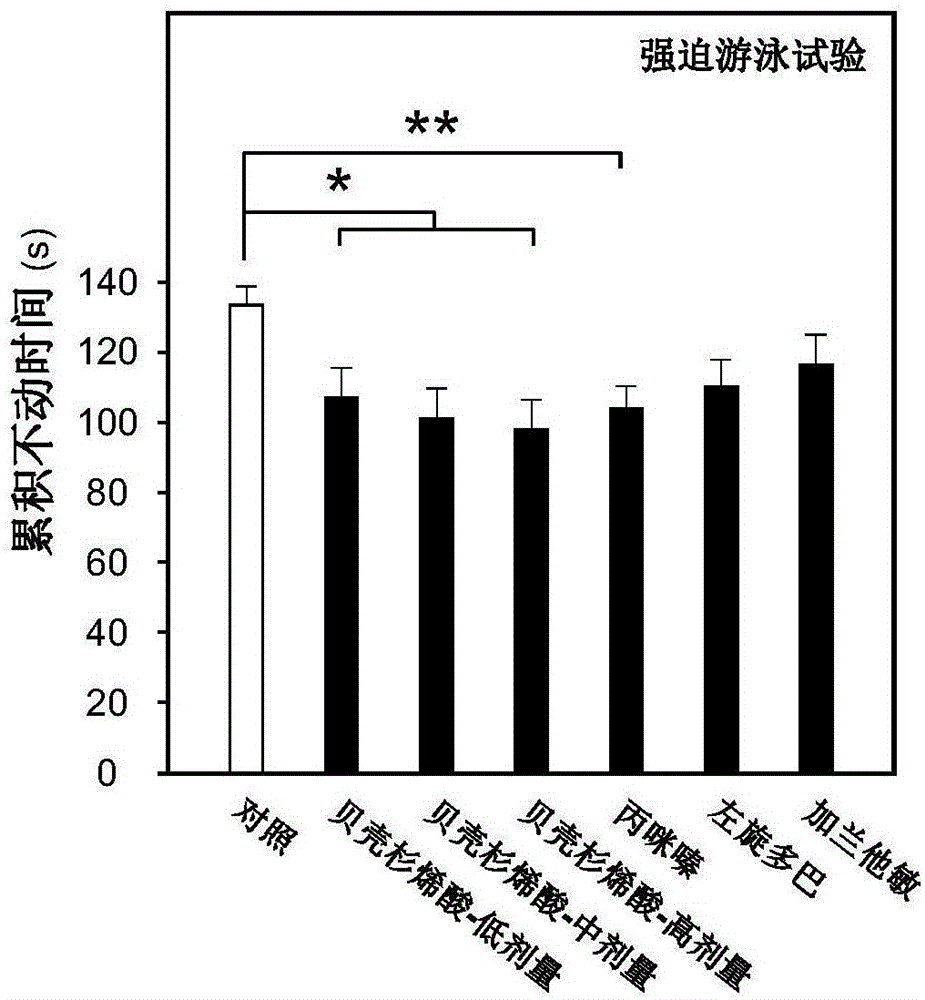
图1为小鼠强迫游泳试验结果图。
图2为小鼠悬尾试验结果图。
图3为慢性应激抑郁大鼠体重检测结果图。
图4为慢性应激抑郁大鼠糖水偏嗜度试验结果图。
图5为慢性应激抑郁大鼠强迫游泳试验结果图。
图6为慢性应激抑郁大鼠神经递质检测结果图。
图7为慢性应激抑郁大鼠海马区神经营养因子检测结果图。
图8为慢性应激抑郁大鼠海马区神经营养因子受体检测结果图。
具体实施方式
以下将结合具体实施例对本发明做进一步阐述,这些实例仅用于说明目的,而不用于限制本发明范围。本发明的实验动物,购自常州卡文斯实验动物有限公司(生产许可证号:scxk(苏)2016-0010),选用临床具有较好疗效的丙咪嗪为阳性对照,另设抗帕金森症药物左旋多巴和抗老年痴呆药物加兰他敏组。贝壳杉烯酸对照品自制,纯度≥98%,溶于水配制成给药浓度(0.75,1.5,3mg/ml或5,10,20mg/ml)。
[实施例一]贝壳杉烯酸对小鼠强迫游泳累积不动时间的影响
采用icr小鼠,雄性,饲养7日以适应新环境。小鼠分为空白对照组、贝壳杉烯酸组[7.5,15,30mg/(kg•d)]、丙咪嗪组[30mg/(kg•d)]、左旋多巴组[60mg/(kg•d)]和加兰他敏组[1.5mg/(kg•d)],每组各12只,每日上午10:00灌胃给药,持续7日。末次给药1h后,进行强迫游泳试验。该试验分2天进行:第1天让小鼠在22±2℃的深水中预游泳15min,24h后在同样的条件下进行强迫游泳6min,统计后4min内游泳累积不动时间(即小鼠停止挣扎或小鼠呈漂浮状态、四肢有轻微动作以保持头部在水面),结果见图1。结果显示阳性药、贝壳杉烯酸[7.5,15,30mg/(kg•d)]作用后小鼠强迫游泳累积不动时间与模型组有显著性差异(p<0.05或p<0.01)。
[实施例二]贝壳杉烯酸对小鼠悬尾累积不动时间的影响
采用icr小鼠,雄性,饲养7日以适应新环境。小鼠分为空白对照组、贝壳杉烯酸组[7.5,15,30mg/(kg•d)]、丙咪嗪组[30mg/(kg•d)]、左旋多巴组[60mg/(kg•d)]和加兰他敏组[1.5mg/(kg•d)],每组各12只,每日上午10:00灌胃给药,持续7日。末次给药1h后,进行悬尾试验。距小鼠尾尖部约1cm处用胶布贴于悬尾箱(25×25×30cm)支架上,使小鼠呈倒挂状态,悬挂时间为6min,统计小鼠6min内悬尾累积不动时间(即小鼠停止挣扎不动或无任何活动),结果见图2。结果显示阳性药、贝壳杉烯酸[7.5,15,30mg/(kg•d)]、左旋多巴、加兰他敏作用后小鼠悬尾累积不动时间与模型组有显著性差异(p<0.05或p<0.01)。
[实施例三]贝壳杉烯酸对慢性应激抑郁大鼠体重的影响
采用sd大鼠,雄性,饲养7日以适应新环境。除空白对照组动物外,其余各组动物给予以下一系列慢性应激刺激:(1)食物剥夺24h;(2)水剥夺24h;(3)暴露于一个空瓶1h;(4)笼倾斜(45°)7h;(5)照明过夜;(6)污笼(笼内加200ml水和100g锯末)24h;(7)8℃下强迫游泳6min;(8)身体限制2h;(9)暴露于外来物体(例如,一个塑料片)24h。以上应激刺激随机被安排在1周内完成,并重复至少4周。建模完成后,通过糖水偏嗜度、体重试验,评价模型的抑郁程度。大鼠分为空白对照组、贝壳杉烯酸组[5,10,20mg/(kg•d)]、丙咪嗪组[20mg/(kg•d)]、左旋多巴组[40mg/(kg•d)]和加兰他敏组[1mg/(kg•d)],每组各12只,每日上午10:00灌胃给药,持续4周。建模完成和给药结束后进行各组大鼠的体重测定,结果见图3。结果显示模型组与正常对照组有显著性差异(p<0.01),灌服阳性药、贝壳杉烯酸[5,10,20mg/(kg•d)]4周后体重与模型组有显著性差异(p<0.05)。
[实施例四]贝壳杉烯酸对慢性应激抑郁大鼠糖水偏嗜度的影响
糖水偏嗜度=蔗糖水消耗量/总液体消耗×100%。
给药完成后,糖水偏嗜度试验前72h,对大鼠进行培训,以适应1%的蔗糖水溶液(重量/体积):2瓶1%蔗糖水溶液置于每个笼子,并在24h后,其中1个瓶子1%的蔗糖水换为饮用水24h。适应培训完成之后,将大鼠剥夺水和食物24h。糖水偏嗜试验在上午9:00开始,每笼1只大鼠,大鼠可以自由地选择2个水瓶(分别含有100ml蔗糖溶液(1%,重量/体积)和100ml的饮用水)。3h后,记录大鼠所消耗的蔗糖水和饮用水的体积。糖水偏嗜度计算公式如下:糖水偏嗜度=1%蔗糖水消耗体积/(水消耗体积+1%蔗糖水消耗体积)×100%,结果见图4。结果显示模型组与正常对照组有显著性差异(p<0.01),灌服阳性药、贝壳杉烯酸[5,10,20mg/(kg•d)]4周后糖水偏嗜度与模型组有显著性差异(p<0.01)。
[实施例五]贝壳杉烯酸对慢性应激抑郁大鼠强迫游泳累积不动时间的影响
给药完成后,进行大鼠强迫游泳试验。该试验分两天进行:第1天让大鼠在22±2℃的深水中预游泳15min,24h后在同样的条件下观测5min的游泳行为,记录累积不动时间。不动时间的判定以大鼠附在水面,只限于做维持身体平衡并将头部露出水面的微小动作为准,结果见图5。结果显示模型组与正常对照组有显著性差异(p<0.01),灌服阳性药、贝壳杉烯酸[5,10,20mg/(kg•d)]4周后强迫游泳累积不动时间与模型组有显著性差异(p<0.05、p<0.01或p<0.001)。
[实施例六]贝壳杉烯酸对慢性应激抑郁大鼠神经递质水平的影响
行为学评价后,处死动物,取海马、纹状体组织样品,检测去甲肾上腺素、5-羟色胺、5-羟吲哚乙酸/5-羟色胺和多巴胺水平。样品经组织裂解液(0.6mol/l高氯酸、0.5mmol/lna2edta、0.1g/ll-半胱氨酸的混合水溶液)处理后,冷冻离心得到上清液;上清液中加入高氯酸沉淀剂(1.20mol/lk2hpo4、2.00mmol/lna2edta的混合水溶液)处理后,冷冻离心、过滤。色谱条件和荧光检测参数如下:agilenthplc1260,shim-packc18柱(250mm×4.6mm,5μm)(日本岛津公司);流动相为柠檬酸-乙酸钠缓冲液(50mmol/l柠檬酸、50mmol/l乙酸钠、0.5mmol/l1-庚烷磺酸钠、5mmol/l三乙胺、0.5mmol/lna2edta)-甲醇(83:13,v/v)(ph8.3);流速为1.0ml/min;进样量为10μl;发射波长为330nm,激发波长为280nm,结果见图6。结果显示模型组与正常对照组有显著性差异(p<0.05或p<0.01),灌服阳性药、贝壳杉烯酸[5,10,20mg/(kg•d)]4周后5-羟色胺、去甲肾上腺素和5-羟吲哚乙酸/5-羟色胺和多巴胺水平与模型组有显著性差异(p<0.05或p<0.01)。
[实施例七]贝壳杉烯酸对慢性应激抑郁大鼠海马区神经营养因子表达的影响
行为学评价后,处死动物,取海马组织样品,检测海马区神经生长因子、脑源性神经营养因子和胶质细胞源性神经营养因子表达水平。样品经rna分离试剂盒提取总rna,nanodrop检测rna含量。取1μgrna样品,经逆转录试剂盒逆转录成cdna,采用sybrgreeni嵌合荧光法进行实时定量pcr试验,结果见图7。结果显示模型组与正常对照组有显著性差异(p<0.05或p<0.01),灌服阳性药、贝壳杉烯酸[5,10,20mg/(kg•d)]4周后神经营养因子表达水平与模型组有显著性差异(p<0.05或p<0.01)。
[实施例八]贝壳杉烯酸对慢性应激抑郁大鼠海马区神经营养因子受体表达的影响
行为学评价后,处死动物,取海马组织样品,检测海马区神经营养因子受体(trka、b和c)表达水平。样品经rna分离试剂盒提取总rna,nanodrop检测rna含量。取1μgrna样品,经逆转录试剂盒逆转录成cdna,采用sybrgreeni嵌合荧光法进行实时定量pcr试验,结果见图8。结果显示模型组与正常对照组有显著性差异(p<0.05),灌服阳性药、贝壳杉烯酸[5,10,20mg/(kg•d)]4周后神经营养因子受体表达水平与模型组有显著性差异(p<0.05、p<0.01或p<0.001)。
[实施例九]贝壳杉烯酸急性毒性试验
按照最大耐受剂量法进行试验,20只icr小鼠,随机分为2组:空白对照组、贝壳杉烯酸试验组,每组10只,雌雄各半。根据食品安全性评价中的急性毒性分级标准,试验前小鼠禁食12h,以0.4ml/只灌胃给药,24h内给药2次,日用量为15g,空白对照组小鼠灌胃相同剂量的生理盐水。给药后,观察小鼠72h内是否死亡,以及未来7日内的进食情况和体重变化;7日后,将小鼠脱颈椎处死,解剖后观察主要脏器病变情况。试验后发现小鼠灌胃后未出现中毒和死亡情况,在以后的7日观察中,小鼠无一死亡,外观健康,被毛光滑,呼吸及大小便正常,鼻、眼和口腔未发现异常分泌物,精神状态良好。与正常对照组小鼠相对比,无明显差别。7日称重后,逐只处死解剖,观察心、肝、脾、肺、肾、胃、肠及胸腔、腹腔情况,各器官均无异常。根据中华人民共和国国标规定:当受试物在试验小鼠体内的剂量达到15g/kg时,仍不会引起动物死亡,则无须精确测定其半数致死剂量,确认受试物的半数致死剂量ld50>15g/kg。根据国家急性毒性分级标准,贝壳杉烯酸属于无毒级别。
[实施例十]贝壳杉烯酸胶囊
贝壳杉烯酸100g,淀粉80g,羧甲基淀粉钠24g,糊精17g,70%乙醇适量,按照常规方法制成1000粒胶囊(每粒含贝壳杉烯酸100mg)。
[实施例十一]贝壳杉烯酸胶囊
贝壳杉烯酸15g,淀粉10g,羧甲基淀粉钠4g,糊精12g,70%乙醇适量,按照常规方法制成1000粒胶囊(每粒含贝壳杉烯酸15mg)。
[实施例十二]贝壳杉烯酸片
贝壳杉烯酸20g,乳糖6g,可压性淀粉3g,羟丙纤维素3g,硬脂酸镁1g,70%乙醇适量,按照常规压片方法制成1000片(每片含贝壳杉烯酸20mg)。
[实施例十三]贝壳杉烯酸胶囊
贝壳杉烯酸20g,淀粉13g,羧甲基淀粉钠5g,糊精5g,70%乙醇适量,按照常规方法制成1000粒胶囊(每粒含贝壳杉烯酸20mg)。
[实施例十四]贝壳杉烯酸胶囊
贝壳杉烯酸40g,淀粉17g,羧甲基淀粉钠17g,糊精5g,70%乙醇适量,按照常规方法制成1000粒胶囊(每粒含贝壳杉烯酸40mg)。
[实施例十五]贝壳杉烯酸片
贝壳杉烯酸150g,乳糖55g,可压性淀粉15g,羟丙纤维素10g,硬脂酸镁5g,70%乙醇适量,按照常规压片方法制成1000片(每片含贝壳杉烯酸150mg)。
[实施例十六]贝壳杉烯酸颗粒剂
贝壳杉烯酸6g,乳糖粉800g,硬脂酸镁194g,70%乙醇适量,按照常规颗粒剂的制备方法制成1000克颗粒(每g颗粒制中含贝壳杉烯酸6mg)。
[实施例十七]贝壳杉烯酸软胶囊
贝壳杉烯酸20g,大豆油10g,明胶5g,甘油5g,蒸馏水7g,按照常规软胶囊的制备方法制成1000粒(每粒含贝壳杉烯酸20mg)。
[实施例十八]贝壳杉烯酸乳膏
贝壳杉烯酸0.5g,硬脂酸100g,十六醇20g,单硬脂酸甘油酯10g,液体石腊10g,羟苯甲酯0.8g,羟苯丁酯0.2g,甘油140g,氢氧化钾5g,乙醇10g,蒸馏水加至1000g。
[实施例十九]贝壳杉烯酸注射液
贝壳杉烯酸25.0g,溶于1000ml注射用水中,充分搅拌溶解,补加注射用水至2000ml,加入针用活性碳2.5g,加热至60℃搅拌30min,碳棒过滤,滤液经0.25μm微孔滤膜过滤除菌,分装于1000支西林瓶中,装量2.0ml/支,封口,灭菌,即得。
- 还没有人留言评论。精彩留言会获得点赞!