香豆酸类化合物的应用、药物组合物及其应用的制作方法
本发明涉及药物化学
技术领域:
,尤其涉及香豆酸类化合物的应用、药物组合物及其应用。
背景技术:
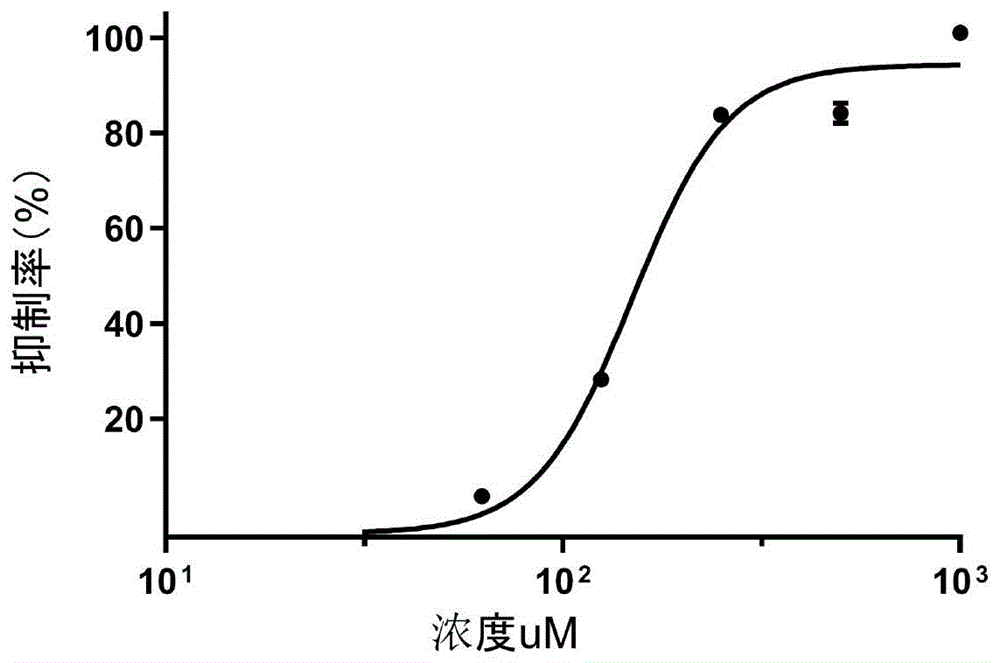
:糖尿病(diabetesmellitus)是一组由遗传与环境因素相互作用而引起的常见的内分泌代谢性疾病,主要是由于胰岛素分泌的绝对或相对不足以及靶细胞对胰岛素敏感性降低而引起的糖、脂肪和蛋白质代谢紊乱。糖尿病人常会出现多尿、口渴、持续饥饿、体重减轻、视力改变和疲劳等症状。临床上以空腹时血糖浓度大于7.0mmol/l,一天中任意时间血糖值大于11.1mmol/l以及餐后2h血糖浓度大于7.0mmol/l这三种症状作为糖尿病的判定依据。根据世界卫生组织(who)的报道,全球糖尿病病人数量呈持续上涨趋势,1980年为1.08亿到2014年已增至4.22亿,全球18岁以上成人糖尿病患病率从1980年的4.7%增加到2014年的8.5%。在2015年,据估计,糖尿病直接造成了160万例死亡,世界卫生组织预测2030年糖尿病将成为第七位主要死因。糖尿病患者需要终身服用降血糖药物来维持血糖水平,根据作用机制的不同,治疗糖尿病的药物主要有胰岛素及其类似物、胰岛素促进剂、胰岛素增敏剂、α-葡萄糖苷酶抑制剂等。胰岛素促进剂临床使用较多的有格列吡嗪和格列美脲。其中,α-葡萄糖苷酶抑制剂是一类控制糖尿病患者餐后血糖的峰值的口服降糖药物。α-葡萄糖苷酶抑制剂可对非胰岛素依赖型糖尿病患者有益,广泛应用于ii型糖尿病治疗,α-葡萄糖苷酶抑制剂根据结构特点,可以分为二糖类、亚氨基糖、碳环糖及假氨基糖、硫糖和其他非糖构型,均为糖类似物。目前,α-葡萄糖苷酶抑制剂的种类较少,不能满足临床需求。技术实现要素:本发明的目的在于提供香豆酸类化合物的应用、药物组合物及其应用,本发明将香豆酸类化合物用于制备α-葡萄糖苷酶抑制剂,表现出了良好的抑制作用,扩宽了α-葡萄糖苷酶抑制剂的选择范围。为了实现上述发明目的,本发明提供以下技术方案:本发明提供了香豆酸类化合物在制备α-葡萄糖苷酶抑制剂中的应用,所述香豆酸类化合物为式1~5所示化合物中的任意一种:本发明还提供了香豆酸类化合物在制备治疗和/或预防糖尿病的药物中的应用,所述香豆酸类化合物为上述技术方案所述的应用中式1~5所示化合物中的任意一种。本发明还提供了香豆酸类化合物在改善糖尿病的保健品中的应用,所述香豆酸类化合物为上述技术方案所述的应用中式1~5所示化合物中的任意一种。本发明还提供了一种药物组合物,包括香豆酸类化合物和药学上可接受的辅料,所述香豆酸类化合物包括上述技术方案所述的应用中式1~5所示化合物中的至少一种。优选地,所述香豆酸类化合物包括上述技术方案所述的应用中式1~5所示化合物中的至少两种。优选地,所述辅料包括载体或赋形剂。本发明还提供了上述技术方案所述的药物组合物在制备α-葡萄糖苷酶抑制剂中的应用。本发明还提供了上述技术方案所述的药物组合物在制备治疗和/或预防糖尿病的药物中的应用。优选地,所述药物的剂型为注射液、粉针剂、粉剂、片剂、口服液、胶囊或颗粒剂。本发明还提供了上述技术方案所述的药物组合物在改善糖尿病的保健品中的应用。本发明提供了香豆酸类化合物在制备α-葡萄糖苷酶抑制剂中的应用,所述香豆酸类化合物为式1~5所示化合物中的任意一种。本发明发现式1~5所示化合物对α-葡萄糖苷酶具有优异的抑制活性,尤其是式2所示化合物的抑制活性甚至超过了阿卡波糖,可用于制备α-葡萄糖苷酶抑制剂、治疗和/或预防糖尿病的药物、以及改善糖尿病的保健品。附图说明图1实施例1所得化合物2的抑制率变化曲线图。具体实施方式本发明提供了香豆酸类化合物在制备α-葡萄糖苷酶抑制剂中的应用,所述香豆酸类化合物为式1~5所示化合物中的任意一种:在本发明中,式1所示化合物的cas号为114590-54-4,式2所示化合物的cas号为72944-19-5,式3所示化合物的cas号为85819-51-8,式4所示化合物的cas号为135117-97-4,式5所示化合物的cas号为210979-34-3。本发明还提供了香豆酸类化合物在制备治疗和/或预防糖尿病的药物中的应用,所述香豆酸类化合物为上述技术方案所述的应用中式1~5所示化合物中的任意一种。本发明还提供了香豆酸类化合物在改善糖尿病的保健品中的应用,所述香豆酸类化合物为上述技术方案所述的应用中式1~5所示化合物中的任意一种。本发明对所述香豆酸类化合物的来源没有特殊限定,可以购买或通过自制得到。在本发明中,所述香豆酸类化合物优选从茵陈蒿的地上部分提取得到,所述提取的方法优选包括如下步骤:将茵陈蒿的地上部分粉碎后,用体积浓度为90%的乙醇水溶液冷浸提取,得到提取液;所述冷浸提取优选在室温进行,所述冷浸提取的次数为3次,每次冷浸提取的时间为3天;将三次提取得到的乙醇提取液合并,得到提取液;将所述提取液中的溶剂去除,然后用水溶解去除溶剂后的固体,得到比重为1.1~1.2的提取物水溶液;使用乙酸乙酯对提取物水溶液进行萃取,将所得有机相中的溶剂去除后,用乙醇溶解所得固体,得到提取物的乙醇溶液;将所述提取物的乙醇溶液与柱色谱硅胶混合后,挥干溶剂,然后依次经研磨、过筛和硅胶柱层析,得到8个流分,按照洗脱出的先后顺序,依次记为a、b、c、d、e、f、g和h;所述硅胶柱层析用洗脱液为石油醚-丙酮溶液,所述石油醚-丙酮溶液中石油醚和丙酮的体积比依次为90:10、80:20、70:30、60:40、50:50、0:100,每个梯度洗脱时所用洗脱液的量为4个柱体积;将流分b在50~100psi的压力下进行mcichp-20p凝胶柱中压制备,使用甲醇-水溶液进行梯度洗脱,得到3个流分,按照洗脱的先后顺序,依次记为b-1、b-2和b-3;所述梯度洗脱过程中,所用甲醇-水溶液中甲醇和水的体积比依次为70:30、80:20、100:0,每个梯度洗脱时所用洗脱液的量为4个柱体积;将流分b-3进行硅胶柱层析,以石油醚-乙酸乙酯溶液洗脱,收集第二流分,得到式2所示化合物;其中石油醚-乙酸乙酯溶液中石油醚和乙酸乙酯的体积比为90:10;将流分c在50~100psi的压力下进行mcichp-20p凝胶柱中压制备,使用甲醇-水溶液进行梯度洗脱,得到5个流分,按照洗脱的先后顺序,依次记为c-1、c-2、c-3、c-4和c-5;所述梯度洗脱过程中,所用甲醇-水溶液中甲醇和水的体积比依次为50:50、60:40、70:30、80:20和100:0,每个梯度洗脱时所用洗脱液的量为4个柱体积;以石油醚-乙酸乙酯溶液(石油醚和乙酸乙酯的体积比优选为80:20)为洗脱液,将流分c-3进行硅胶柱层析,再以rp-c18柱为色谱柱进行液相色谱纯化,流动相为乙腈-水溶液,其中乙腈和水体积比为60:40,取保留时间为16min的流分,得到式1所示的化合物;以石油醚-乙酸乙酯溶液(石油醚和乙酸乙酯的体积比优选为80:20)为洗脱液,将流分c-3进行硅胶柱层析,再以rp-c18柱为色谱柱进行液相色谱纯化,流动相为乙腈-水溶液,其中乙腈和水体积比为65:35,取保留时间为12min的流分,得到式4所示的化合物;将流分d在50~100psi的压力下进行mcichp-20p凝胶柱中压制备,使用甲醇-水溶液梯度洗脱,得到5个流分,按照洗脱出的先后顺序,依次记为d-1、d-2、d-3、d-4和d-5;所述梯度洗脱过程中,所用甲醇-水溶液中甲醇和水的体积比优选为依次为50:50、60:40、70:30、80:20和100:0,每个梯度洗脱时所用洗脱液的量为4个柱体积;以石油醚-乙酸乙酯溶液为洗脱液将流分d-3进行硅胶柱层析,其中石油醚和乙酸乙酯的体积比为70:30,取第二个流分,得到式3所示的化合物,取第三个流分,得到式5所示的化合物。在本发明中,所述柱色谱硅胶优选为薄层色谱硅胶gf254;本发明对所述硅胶柱层析所用硅胶、薄层色谱硅胶gf254和凝胶柱中的mcichp-20p凝胶的来源没有特殊限定,在本发明实施例中,所述硅胶柱层析用硅胶优选为临沂海祥化工有限公司生产的硅胶,所述硅胶粒径为200~300目;所述薄层色谱硅胶gf254购于烟台江友化工有限公司;所述mcichp-20p凝胶购自三菱化学株式会社(日本东京)。本发明还提供了一种药物组合物,包括香豆酸类化合物和药学上可接受的辅料,所述香豆酸类化合物包括上述技术方案所述的应用中式1~5所示化合物中的至少一种。在本发明中,所述香豆酸类化合物优选包括上述技术方案所述的应用中式1~5所示化合物中的至少两种。在本发明中,所述辅料优选包括载体或赋形剂,所述载体或赋形剂优选为固体、半固体和液体稀释剂、填料和药物制品辅剂中的一种或多种。本发明对所述载体和赋形剂的具体种类没有特殊限定,本领域技术人员可以根据需要制备的剂型选择合适的载体和赋形剂。在本发明中,所述药物组合物中,所述香豆酸类化合物的质量百分含量优选为0.1~99%,更优选为0.5~90%。本发明还提供了上述技术方案所述的药物组合物在制备α-葡萄糖苷酶抑制剂中的应用。本发明还提供了上述技术方案所述的药物组合物在制备治疗和/或预防糖尿病的药物中的应用。在本发明中,所述药物的剂型优选为注射液、粉针剂、粉剂、片剂、口服液、胶囊或颗粒剂。本发明所提供的药物组合物可制备成不同的剂型,以用于不同的给药方式,可经注射(静注、肌注)和口服两种形式给药。本发明还提供了本发明还提供了上述技术方案所述的药物组合物在改善糖尿病的保健品中的应用。下面结合实施例对本发明提供的香豆酸类化合物的应用、药物组合物及其应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。实施例1将茵陈蒿的地上部分粉碎后,用体积浓度为90%的乙醇水溶液冷浸提取,得到提取液;所述冷浸提取在室温进行,所述冷浸提取的次数为3次,每次冷浸提取的时间为3天;将三次提取得到的乙醇提取液合并,得到提取液;将所述提取液中的溶剂去除,然后用水溶解去除溶剂后的固体,得到比重为1.1~1.2的提取物水溶液;使用乙酸乙酯对提取物水溶液进行萃取,将所得有机相中的溶剂去除后,用乙醇溶解所得固体,得到提取物的乙醇溶液;将所述提取物的乙醇溶液与柱色谱硅胶混合后,挥干溶剂,然后依次经研磨、过筛和硅胶柱层析,得到8个流分,按照洗脱出的先后顺序,依次记为a、b、c、d、e、f、g和h;所述硅胶柱层析用洗脱液为石油醚-丙酮溶液,所述石油醚-丙酮溶液中石油醚和丙酮的体积比依次为90:10、80:20、70:30、60:40、50:50、0:100,每个梯度洗脱时所用洗脱液的量为4个柱体积;将流分b在50~100psi的压力下进行mcichp-20p凝胶柱中压制备,使用甲醇-水溶液进行梯度洗脱,得到3个流分,按照洗脱的先后顺序,依次记为b-1、b-2和b-3;所述梯度洗脱过程中,所用甲醇-水溶液中甲醇和水的体积比依次为70:30、80:20、100:0,每个梯度洗脱时所用洗脱液的量为4个柱体积;将流分b-3进行硅胶柱层析,以石油醚-乙酸乙酯溶液洗脱,收集第二流分,得到化合物2;其中石油醚-乙酸乙酯溶液中石油醚和乙酸乙酯的体积比为90:10;将流分c在50~100psi的压力下进行mcichp-20p凝胶柱中压制备,使用甲醇-水溶液进行梯度洗脱,得到5个流分,按照洗脱的先后顺序,依次记为c-1、c-2、c-3、c-4和c-5;所述梯度洗脱过程中,所用甲醇-水溶液中甲醇和水的体积比依次为50:50、60:40、70:30、80:20和100:0,每个梯度洗脱时所用洗脱液的量为4个柱体积;以石油醚-乙酸乙酯溶液(石油醚和乙酸乙酯的体积比为80:20)为洗脱液,将流分c-3进行硅胶柱层析,再以rp-c18柱为色谱柱进行液相色谱纯化,流动相为乙腈-水溶液,其中乙腈和水体积比为60:40,取保留时间为16min的流分,得到化合物1;以石油醚-乙酸乙酯溶液(石油醚和乙酸乙酯的体积比为80:20)为洗脱液,将流分c-3进行硅胶柱层析,再以rp-c18柱为色谱柱进行液相色谱纯化,流动相为乙腈-水溶液,其中乙腈和水体积比为65:35,取保留时间为12min的流分,得到化合物4;将流分d在50~100psi的压力下进行mcichp-20p凝胶柱中压制备,使用甲醇-水溶液梯度洗脱,得到5个流分,按照洗脱出的先后顺序,依次记为d-1、d-2、d-3、d-4和d-5;所述梯度洗脱过程中,所用甲醇-水溶液中甲醇和水的体积比优选为依次为50:50、60:40、70:30、80:20和100:0,每个梯度洗脱时所用洗脱液的量为4个柱体积;以石油醚-乙酸乙酯溶液为洗脱液将流分d-3进行硅胶柱层析,其中石油醚和乙酸乙酯的体积比为70:30,取第二个流分,得到化合物3,取第三个流分,得到化合物5。将化合物1~5进行质谱分析和核磁共振检测(以tms(四甲基硅烷)为内标),结果如下:化合物1:分子量:316性状:无色针状晶体形1h-nmr和13c-nmr数据如下:1h-nmr(400mhz,cd3od)δh:7.58(1h,d,j=16hz,h-17),7.26(1h,brs,h-6),7.13(1h,brs,h-2),6.26(1h,d,j=16hz,h-18),3.73(1h,m,h-10a),3.60(1h,m,h-10b),3.33(1h,m,h-7a),3.23(1h,m,h-12),3.02(1h,m,h-7b),1.73(6h,s,h-15,16),0.99(3h,d,j=6.4hz,h-11);13c-nmr(100mhz,cd3od)δc:171.2(s,c-19),161.3(s,c-4),147.0(d,c-17),133.7(s,c-14),130.4(d,c-6),129.0(s,c-1),128.4(s,c-3),124.5(s,c-5),123.3(d,c-2),123.0(d,c-13),115.5(d,c-18),86.5(d,c-8),64.7(t,c-10),43.0(d,c-9),33.5(t,c-7),29.2(t,c-12),26.0(q,c-11),18.0(q,c-15),12.5,(q,c-16)。将上述分析可知,化合物1的结构如式1所示。化合物2:分子式:c19h24o3分子量:300性状:棱状晶体1h-nmr和13c-nmr数据如下:1h-nmr(500mhz,cd3od)δh:7.54(1h,d,j=16hz,h-17),7.11(1h,brs,h-2,h-6),6.19(1h,d,j=16hz,h-18),5.31(2h,brt,h-8,h-13),3.30(4h,m,h-7,h-12),1.74(12h,s,h-10,h-11,h-15,h-16);13c-nmr(125mhz,cd3od)δc:127.4(s,c-1),128.5(d,c-2,c-6),130.1(s,c-3,c-5),29.5(t,c-7,c-12),123.3(d,c-8,c-13),133.9(s,c-9,c-14),25.9(q,c-10,c-16),147.3(d,c-17),115.3(d,c-18),171.2(s,c-19)。将上述分析可知,化合物2的结构如式2所示。化合物3:分子式:c19h24o4分子量:316性状:棱状晶体1h-nmr和13c-nmr数据如下:1h-nmr(500mhz,cd3od)δh:7.54(1h,d,j=16hz,h-13),7.22(2h,brs,h-2,h-6),6.22(1h,d,j=16hz,h-18),5.41(1h,brt,h-18),5.34(1h,brt,h-17),3.42(2h,d,j=7.5hz,h-7),3.37(2h,d,j=7.0hz,h-12),1.74(9h,s,h-10,h-15,h-16);13c-nmr(125mhz,cd3od)δc:126.8(s,c-1),128.7(d,c-2),133.9(s,c-3),156.4(s,c-4),129.2(s,c-5),129.0(d,c-6),29.9(t,c-7),127.4(d,c-8),136.5(s,c-9),22.0(q,c-10),61.9(t,c-11),29.4(t,c-12),123.3(d,c-13),130.3(s,c-14),17.9(q,c-15),25.9(q,c-16),147.1(d,c-17),115.4(d,c-18),171.2(s,c-19)。将上述分析可知,化合物3的结构如式3所示。化合物4:分子式:c21h26o5分子量:358性状:无色油状物1h-nmr和13c-nmr数据如下:1h-nmr(600mhz,cd3od)δh:7.54(1h,d,j=15.6hz,h-19),7.26(1h,brs,h-6),7.16(1h,s,h-2),7.14(1h,s,h-6),6.24(1h,d,j=15.6hz,h-20),5.55(1h,brt,h-8),5.32(1h,brt,h-15),2.03(3h,s,h-13),1.78(3h,s,h-10),1.75(3h,s,h-17),1.71(3h,s,h-18);13c-nmr(125mhz,cd3oh)δc:173.1(s,c-12),171.6(s,c-21),156.3(s,c-4),146.9(d,c-19),134.2(s,c-16),132.4(s,c-9),130.3(s,c-1),129.5(d,c-8),129.4(s,c-3),128.9(d,c-2),128.8(d,c-6),127.7(s,c-5),123.2(d,c-15),116.1(d,c-20),64.4(t,c-11),29.6(t,c-14),29.6(t,c-7),26.1(q,c-10),21.8(q,c-18),20.9(q,c-13),18.0(q,c-17)。将上述分析可知,化合物4的结构如式4所示。化合物5:分子式:c19h24o4分子量:316性状:无色油状物1h-nmr和13c-nmr数据如下:1h-nmr(400mhz,cd3od)δh:7.56(1h,d,j=16.0hz,h-17),7.17(1h,d,j=1.6hz,h-2),7.16(1h,d,j=1.6hz,h-6),6.27(1h,d,j=16.0hz,h-18),,5.27(1h,brt,j=7.6hz,h-13),3.78(1h,dd,j=5.6,7.2hz,h-8),3.27(2h,d,j=7.2hz,h-12),3.03(1h,dd,j=5.2,16.8hz,h-7a),2.74(1h,dd,j=7.6,16.8hz,h-7b),1.74(6h,s,h-10,11),1.37(3h,s,h-16),1.28(3h,s,h-15);13c-nmr(100mhz,cd3oh)δc:127.5(s,c-1),129.2(d,c-2),121.4(s,c-3),154.4(s,c-4),131.4(s,c-5),128.3(d,c-6),32.1(t,c-7),70.2(d,c-8),78.8(s,c-9),26.1(q,c-10),21.3(q,c-11),29.5(t,c-12),123.7(d,c-13),133.1(s,c-14),18.0(q,c-15),26.0(q,c-16),146.8(d,c-17),115.9(d,c-18),171.2(s,c-19)。将上述分析可知,化合物5的结构如式5所示。实施例2化合物1~5的活性测试:将待测样品溶解于甲醇-磷酸盐缓冲液(其中甲醇和磷酸盐缓冲液的体积比为1:1,磷酸盐缓冲液的ph值为6.8)中,得到所需浓度的待测样品溶液;将对硝基苯基-α-d-吡喃葡萄糖苷(pnpg)溶于ph值为6.8的磷酸盐缓冲液中,得到底物浓度为5mmol/l的底物溶液;将20μl待测样品溶液和20μl的α-葡萄糖苷酶溶液(浓度为2.0u/ml,ph值为6.8的磷酸盐溶液为溶剂)加入到96孔板中,在37℃的恒温箱中孵育5min,然后加入20μl底物溶液,振摇后再在37℃恒温箱中孵育15min,然后用40μl浓度为0.1m的na2co3水溶液终止反应,用酶标仪在405nm处测定吸光值,记录结果。空白实验:使用ph值为6.8的磷酸盐缓冲溶液代替α-葡萄糖苷酶溶液,其他测试条件与上述活性测试的方法相同。阳性对照实验:使用阿卡波糖代替待测样品,其他测试条件与上述活性测试的方法相同;阴性对照实验:使用ph值为6.8的磷酸盐缓冲溶液代替待测样品溶液,其他测试条件与上述活性测试的方法相同。根据上述测试的结果,按照下式计算α-葡萄糖苷酶抑制率:α-葡萄糖苷酶抑制率=(△酶-△样)/(△酶-△阴)×100%其中:△酶为空白实验测试得到的吸光度值变化量;△样为待测样品的吸光度值变化量;△阴为阴性对照实验测试得到的吸光度值变化量。表1为化合物1~5的α-葡萄糖苷酶抑制率结果,由表1可知式1~5所示的香豆酸类化合物具有α-葡萄糖苷酶抑制活性,尤其是化合物2表现出了优异的抑制活性,可用于制备α-葡萄糖苷酶抑制剂、治疗和/或预防糖尿病的药物、以及改善糖尿病的保健品。表1化合物1~5的α-葡萄糖苷酶抑制率结果化合物抑制率(%)171.07±1.06299.19±2.06339.22±4.32480.18±1.45542.79±1.21测试化合物2的半抑制浓度(ic50),结果如图1所示,由图1可知,化合物2的ic50值可达149μmol/l,低于阳性对照(阿卡波糖)的ic50值(190μmol/l)。实施例3按照如下方法制备不同剂型的药物:1.将实施例1制备得到化合物1~5,分别用dmso溶解后,加入注射用水,然后精滤,灌封灭菌得到5种注射液。2.将实施例1制备得到化合物1~5,分别用dmso溶解后,将其溶于无菌注射用水中,搅拌使溶解,用无菌抽滤漏斗过滤,再无菌精滤,分装于安瓿瓶中,低温冷冻干燥后无菌熔封得到5种粉针剂。3.将实施例1制备得到化合物1~5分别与赋形剂按照重量比为9:1的比例混合,制成5种粉剂。4.将实施例1制备得到化合物1~5分别与赋形剂按照重量比为5:1的比例混合,然后依次经制粒和压片,得到5种片剂。5.将实施例1制备得到化合物1~5分别按常规口服液制法制成口服液。6.将实施例1制备得到化合物1~5分别与赋形剂按照重量比为5:1的比例混合后,制成5种胶囊。以上所述仅是本发明的优选实施方式,应当指出,对于本
技术领域:
的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1