用于神经特异性成像的基于噁嗪的荧光团化合物
用于神经特异性成像的基于噁嗪的荧光团化合物
1.关于联邦资助的研究或开发的声明
2.本发明是根据国立卫生研究院(national institutes of health)授予的授权r01eb021362在政府支持下进行的。政府拥有本发明的某些权利。
技术领域
3.本发明涉及可用于体内神经成像的新型基于噁嗪的荧光团化合物以及包括所述化合物的组合物及所述化合物和所述组合物的使用方法。
背景技术:
4.全世界每年进行超过3亿台外科手术。尽管最近在癌症和其它疾病的治疗上取得了许多进展,但外科手术仍然是许多疾病和损伤最有效的治疗选择。外科手术的最终目标是切除或修复组织,同时通过保留如神经和血管等重要结构来最大限度地减少合并症。包含微创性机器人辅助腹腔镜外科手术的最新技术进步改善了结果,并且使得可以稳健地以最小的风险进行困难的手术。此外,如磁共振成像(mri)和计算机断层扫描(ct)等术前三维成像技术极大地改善了诊断准确性、分期和术前计划。
5.尽管已经取得了进展,但仍然难以在外科手术期间识别要保留的重要结构(例如,神经)或要完全切除的组织(例如,肿瘤)。由于患者解剖构造的差异,以及在外科手术领域通常几乎没有直接神经可视化的能力,在术中可能难以进行神经识别和保留。当前,通过肉眼可视化、触诊和肌电图监测的组合来进行术中神经检测。若干种成像模式已经在临床研究中用于神经检测,包含超声波、光学相干断层扫描和共聚焦显微内镜。然而,这些成像模式缺乏特异性、分辨率和宽视场成像功能,使得难以实时识别神经组织。因此,神经损伤继续困扰着外科手术结果。医源性神经损伤每年影响着全世界多达6300万患者,引起了急性疼痛和慢性疼痛以及运动机能和感觉功能的受损或丧失。根治性前列腺切除术(rp),一种涉及切除整个前列腺作为前列腺癌治疗手段的外科手术,尤其受到神经损伤的困扰。此外,尽管如机器人辅助rp等微创性方法可以达到与开放性rp等效的癌症控制,同时使得失血降低、输血速率更低和康复期更快,但是这些进展对于神经保留结果没有益处,并且事实上去除了直接触诊组织的能力。
6.能够在术中对神经组织进行宽视场、实时识别的成像模式将极大地有益于外科医生进行神经保留并且降低医源性神经损伤的比率,从而改善患者术后的生活质量。
7.当前,不存在nir神经特异性荧光团,并且需要进一步开发荧光团来获得用于临床转化的适当候选物。已经研究了用于fgs的若干种类别的神经特异性荧光团。参见例如:吉布斯-斯特劳斯(gibbs-strauss)等人分子成像(molecular imaging)10,91-101(2011);吴(wu)等人医药化学杂志(journal of medicinal chemistry)51,6682-6688(2008);王(wang)等人组织化学与细胞化学杂志:组织化学学会官方杂志(the journal of histochemistry and cytochemistry:official journal of the histochemistry society)58,611-621(2010);吉布斯(gibbs)等人公共科学图书馆综合(plos one)8,
e73493(2013);斯坦科夫(stankoff)等人美国国家科学院院刊(proceedings of the national academy of sciences of the united states of america)103,9304-9309(2006);科特罗(cotero)等人分子成像与生物学:mib:分子成像学会官方出版物(molecular imaging and biology:mib:the official publication of the academy of molecular imaging)14,708-717(2012);科特罗等人公共科学图书馆综合10,e0130276(2015);巴贾吉(bajaj)等人组织化学与细胞化学杂志:组织化学学会官方杂志61,19-30(2013);吉布斯-斯特劳斯等人分子成像9,128-140(2010);梅耶斯(meyers)等人神经科学杂志:神经科学学会官方杂志(the journal of neuroscience:the official journal of the society for neuroscience)23,4054-4065(2003);王等人神经科学杂志:神经科学学会官方杂志31,2382-2390(2011);以及帕克(park)等人治疗诊断学(theranostics)4,823-833(2014)。其中,噁嗪4是最有希望的开发候选物,其显示出高神经特异性和接近nir的红移吸收和发射光谱(帕克等人治疗诊断学4,823-833(2014))。
8.在国际申请pct/us2019/045347中公开了有用的噁嗪神经保留荧光团,但仍然需要此类化合物,具体地用于水性组合物中的化合物。
技术实现要素:
9.一个实施例提供了一种式(i)的化合物:
[0010][0011]
其中:
[0012]
r1和r2各自独立地选自以下的群组:直链或支链c
1-c6烷基;
[0013]-(ch2)
n1-so
3-、-(ch2)
n1-n
+
(ch3)3、-ch
2-ch
2-o-x1、-ch
2-ch
2-o-[ch
2-ch
2-o]
n2-x1、-ch
2-ch
2-ch
2-o-x1以及-ch
2-ch
2-ch
2-o-[ch
2-ch
2-ch
2-o]
n3-x1;或选自以下的群组的部分:
[0014]
a)
[0015]
b)
[0016]
c)以及
[0017]
d)
[0018]
r3是氢,或者r2和r3一起形成稠环,从而产生式(ii)的核心:
[0019][0020]
r4和r5与其结合的氮原子一起形成选自以下的群组的环:
[0021]
以及
[0022]
或者当所述化合物具有式(ii)时,r4和r5可以独立地选自c
1-c6烷基,条件是当r1是甲基并且r4是乙基时,r5不是乙基;
[0023]
r6是氢;
[0024]
或者当r2和r3一起形成稠环以产生式(ii)的核心时,r5和r6也可以与r5结合的氮原子一起形成稠环以产生式(iii)的核心:
[0025][0026]
条件是当r4和r5与其结合的氮原子一起用于环并且r3是h时,r1和r2与其结合的氮原子一起可以形成吡咯烷基环;
[0027]
每个实例中的x1独立地选自c
1-c6直链或支链烷基、c
1-c6直链或支链烯基、c
1-c6直链或支链炔基以及-si(c
1-c4烷基)3;
[0028]
n是选自1和2的群组的整数;
[0029]
n1是在每个实例中独立地选自1、2、3和4的群组的整数;
[0030]
n2是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;
[0031]
n3是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;
[0032]
n4是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;并且
[0033]
条件是n2+n2的总和不大于10;
[0034]
条件是n2+n3的总和不大于10;
[0035]
条件是n2+n4的总和不大于10;
[0036]
条件是n3+n4的总和不大于10;
[0037]
条件是当r4和r5与其结合的氮原子一起形成环时,r1和r2不都是甲基,r1和r2不都是乙基,r1和r2不都是正丙基,r1和r2不都是正丁基,并且r1和r2不都是正戊基;并且
[0038]
条件是当所述化合物具有式(iii)时,当r1是甲基时,r4不是甲基。
附图说明
[0039]
图1表示了pbs中噁嗪衍生物的归一化的吸收和荧光发射光谱,分别为化合物(a)lgw13-79、(b)lgw14-42、(c)lgw14-47、(d)lgw14-51、(e)lgw14-53和(f)lgw14-83的归一化的吸收和荧光发射光谱。
[0040]
图2a提供了将(共溶剂调配物中的125μm)所指示化合物直接施加到暴露的臂丛神经和坐骨神经之后nir噁嗪衍生物的代表性照片和荧光图像。
[0041]
图2b表示了与未经染色的对照组相比,量化每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度。
[0042]
图2c表示了针对筛选的噁嗪衍生物与未经染色的对照组之间的比较所计算的量化的神经信号与背景比率(sbr)。
[0043]
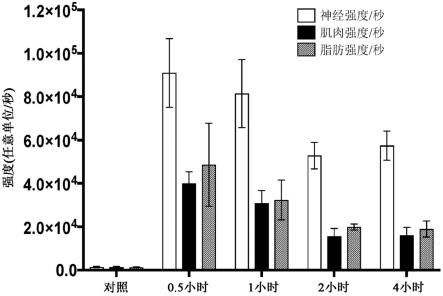
图3a提供了全身施用之后0.5小时、1小时、2小时和4小时时间点处nir神经特异性候选物lgw03-76的照片和荧光图像。
[0044]
图3b表示了量化并且与对照组织自体荧光相比的每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度。
[0045]
图3c表示了针对lgw03-76与对照组织自体荧光之间的比较所计算的量化的神经sbr。
[0046]
图4a提供了全身施用之后0.5小时、1小时、2小时和4小时时间点处nir神经特异性候选物lgw13-79的照片和荧光图像。
[0047]
图4b表示了量化并且与对照组织自体荧光相比的每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度。
[0048]
图4c表示了针对lgw13-79与对照组织自体荧光之间的比较所计算的量化的神经sbr。
[0049]
图5a提供了全身施用之后0.5小时、1小时、2小时和4小时时间点处nir神经特异性候选物lgw14-42的代表性照片和荧光图像。
[0050]
图5b表示了量化并且与对照组织自体荧光相比的每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度。
[0051]
图5c表示了针对lgw14-42与对照组织自体荧光之间的比较所计算的量化的神经sbr。
具体实施方式
[0052]
第二实施例提供了一种式(iv)的化合物:
[0053][0054]
其中:
[0055]
r1和r2各自独立地选自以下的群组:直链或支链c
1-c6烷基;
[0056]-(ch2)
n1-so
3-、-(ch2)
n1-n
+
(ch3)3、-ch
2-ch
2-o-x1、-ch
2-ch
2-o-[ch
2-ch
2-o]
n2-x1、-ch
2-ch
2-ch
2-o-x1以及-ch
2-ch
2-ch
2-o-[ch
2-ch
2-ch
2-o]
n3-x1;或选自以下的群组的部分:
[0057]
a)
[0058]
b)
[0059]
c)以及
[0060]
d)
[0061]
r3是氢,或者r2和r3一起形成稠环,从而产生式(v)的核心:
[0062][0063]
条件是当n是1并且r3是h时,r1和r2与其结合的氮原子一起可以形成吡咯烷基环;
[0064]
每个实例中的x1独立地选自c
1-c6直链或支链烷基、c
1-c6直链或支链烯基、c
1-c6直链或支链炔基以及-si(c
1-c4烷基)3;
[0065]
n是选自1和2的群组的整数;
[0066]
n1是在每个实例中独立地选自1、2、3和4的群组的整数;
[0067]
n2是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;
[0068]
n3是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;
[0069]
n4是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;并且
[0070]
条件是n2+n2的总和不大于10;
[0071]
条件是n2+n3的总和不大于10;
[0072]
条件是n2+n4的总和不大于10;
[0073]
条件是n3+n4的总和不大于10;并且
[0074]
条件是当n是2时,r1和r2不都是甲基,r1和r2不都是乙基,r1和r2不都是正丙基,r1和r2不都是正丁基,并且r1和r2不都是正戊基。
[0075]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和都不大于10。
[0076]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和都不大于8。
[0077]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和都不大于6。
[0078]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和都不大于4。
[0079]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和的组中的组合都不大于10。
[0080]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和的组中的组合都不大于8。
[0081]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和的组中的组合都不大于6。
[0082]
在本文的具体实施例中的每个具体实施例内,存在另外的实施例,所述另外的实施例提供了如由所讨论的具体实施例的所有变量和条件所定义的化合物,其中进一步的条件是n1+n2的总和、n1+n3的总和以及n1+n4的总和的组中的组合都不大于4。
[0083]
两个另外且单独的实施例分别提供了式(vi)的化合物和式(vii)的化合物:
[0084][0085]
其中所有变量,包含r1、r2、r3、x1、n、n1、n2、n3以及n4连同所有条件,都如以上针对式(i)所定义。
[0086]
又两个单独的实施例分别提供了式(vi)的化合物和式(vii)的化合物,其中在每个实施例中,r3是h,并且r1和r2各自独立地选自以下的群组:甲基、乙基、正丙基、异丙基、正丁基、仲丁基以及叔丁基。
[0087]
又两个单独的实施例分别提供了式(vi)的化合物和式(vii)的化合物,其中在每个实施例中,r3是h,并且r1和r2各自独立地选自以下的群组:甲基、乙基、正丙基、异丙基、正丁基、仲丁基以及叔丁基,条件是r1和r2不相同。
[0088]
又两个单独的实施例分别提供了式(vi)的化合物和式(vii)的化合物,其中在每个实施例中,r3是h,并且r1和r2各自独立地选自以下的群组:甲基、乙基、正丙基和异丙基,条件是r1和r2不相同。
[0089]
又两个单独的实施例分别提供了式(vi)的化合物和式(vii)的化合物,其中在每个实施例中,r3是h,并且r1选自以下的群组:甲基、乙基、正丙基、异丙基、正丁基、仲丁基以及叔丁基,并且r2选自以下的群组:-(ch2)
n1-so
3-、-(ch2)
n1-n
+
(ch3)3、-ch
2-ch
2-o-x1、-ch
2-ch
2-o-[ch
2-ch
2-o]
n2-x1、-ch
2-ch
2-ch
2-o-x1以及-ch
2-ch
2-ch
2-o-[ch
2-ch
2-ch
2-o]
n3-x1;或选自以下的群组的部分:
[0090]
a)
[0091]
b)
[0092]
c)并且
[0093][0094]
每个实例中的x1独立地选自c
1-c6直链或支链烷基、c
1-c6直链或支链烯基、c
1-c6直链或支链炔基以及-si(c
1-c4烷基)3;
[0095]
n1是在每个实例中独立地选自1、2、3和4的群组的整数;
[0096]
n2是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;
[0097]
n3是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;
[0098]
n4是在每个实例中独立地选自1、2、3、4、5、6、7、8、9和10的群组的整数;并且
[0099]
条件是当r2是由上述k)所表示的部分时,n2+n4的总和不大于10。
[0100]
另外的实施例包括式(via)的化合物:
[0101]
[0102]
其中r1和r2独立地选自c
1-c6烷基。
[0103]
另一个实施例提供了一种式(via)的化合物,其中r1和r2各自独立地选自c
1-c4烷基。
[0104]
另一个实施例提供了一种式(via)的化合物,其中r1和r2各自独立地选自c
1-c3烷基。
[0105]
另一个实施例提供了一种式(via)的化合物,其中r1是乙基并且r2是c
1-c4烷基。
[0106]
另一个实施例提供了一种式(via)的化合物,其中r1是乙基并且r2是c
1-c3烷基。
[0107]
另一个实施例提供了一种式(via)的化合物,其中r1是甲基并且r2是c
1-c4烷基。
[0108]
另一个实施例提供了一种式(via)的化合物,其中r1是甲基并且r2是c
1-c3烷基。
[0109]
另一个实施例提供了一种式(ii)的化合物:
[0110][0111]
其中r1、r4、r5、r6以及所有相关变量和条件都如以上针对式(i)所定义。
[0112]
另外的实施例提供了一种上式(ii)的化合物,其中r1如以上针对式(i)所定义,r6是氢,并且r4和r5各自独立地选自直链或支链c
1-c6烷基的组,条件是当r1是甲基并且r4是乙基时,r5不是乙基。
[0113]
另外的实施例提供了一种式(viii)的化合物:
[0114][0115]
其中n和r1连同所有其它相关变量和条件都如以上针对式(i)所定义。
[0116]
另外的实施例提供了一种式(viiia)的化合物:
[0117][0118]
其中r1连同所有其它相关变量和条件都如以上针对式(i)所定义。
[0119]
另外的实施例提供了一种上式(viiia)的化合物,其中r1是c
1-c4烷基。
[0120]
另一个实施例提供了一种上式(viiia)的化合物,其中r1是c
1-c3烷基。
[0121]
另外的实施例提供了一种上式(viiia)的化合物,其中r1是c
1-c2烷基。
[0122]
另一个另外的实施例提供了一种式(viii)的化合物:
[0123][0124]
其中r1连同所有其它相关变量和条件都如以上针对式(i)所定义。
[0125]
另外的实施例提供了一种上式(viiib)的化合物,其中r1是c
1-c4烷基。
[0126]
另一个实施例提供了一种上式(viiib)的化合物,其中r1是c
1-c3烷基。
[0127]
另外的实施例提供了一种上式(viiib)的化合物,其中r1是c
1-c2烷基。
[0128]
仍另外的实施例提供了一种式(iii)的化合物:
[0129][0130]
其中r1和r4连同所有相关变量和条件都如以上针对式(i)所定义,条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0131]
另一个实施例提供了一种上式(iii)的化合物,其中r1是c
1-c6烷基,并且r4连同所有其它相关变量和条件都如以上针对式(i)所定义,并且条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0132]
仍另一个实施例提供了一种上式(iii)的化合物,其中r1是c
1-c4烷基,并且r4连同所有其它相关变量和条件都如以上针对式(i)所定义,并且条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0133]
仍另一个实施例提供了一种上式(iii)的化合物,其中r1是c
1-c3烷基,并且r4连同所有其它相关变量和条件都如以上针对式(i)所定义,并且条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0134]
仍另一个实施例提供了一种上式(iii)的化合物,其中r1是c
1-c2烷基,并且r4连同所有其它相关变量和条件都如以上针对式(i)所定义,并且条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0135]
又另一个实施例提供了一种上式(iii)的化合物,其中r1和r2各自独立地选自c
1-c6烷基,条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0136]
另外的实施例提供了一种上式(iii)的化合物,其中r1和r2各自独立地选自c
1-c4烷基,条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0137]
另一个实施例提供了一种上式(iii)的化合物,其中r1和r2各自独立地选自c
1-c3烷基,条件是当r1是甲基时,r4不是甲基,并且条件是当r1是乙基时,r4不是乙基。
[0138]
另外的实施例提供了一种式(ix)的化合物:
[0139][0140]
其中r1和r4各自独立地选自c
1-c6烷基。
[0141]
另外的实施例提供了一种式(ix)的化合物,其中r1和r4各自独立地选自c
1-c4烷基。
[0142]
另一个实施例提供了一种式(ix)的化合物,其中r1和r4各自独立地选自c
1-c3烷基。
[0143]
另外的实施例提供了一种式(ix)的化合物,其中r1和r4各自独立地选自c
1-c2烷基。
[0144]
另外的实施例提供了一种式(ix)的化合物,其中r1连同所有定义的相关变量和条件都如以上针对式(i)所定义。
[0145]
定义
[0146]“受试者”或“患者”是指任何动物。所述动物可以是哺乳动物。合适的哺乳动物的实例包含人和非人灵长类动物、狗、猫、羊、牛、猪、马、小鼠、大鼠、兔子和豚鼠。在一些实施例中,所述受试者或患者是人,具体地包含正进行或需要外科手术或检查的人。
[0147]
本文所使用的术语“神经”是指神经轴突束。在神经内,每个轴突被称为神经内膜的结缔组织层所围绕。轴突被捆扎成称为束的群组,并且每个束被包裹在称为神经束膜的结缔组织层中。整个神经被包裹在称为神经外膜的结缔组织层中。术语“神经”旨在包含任何组织(例如,窦房结或房室结)或与其相关的结构(例如,神经肌肉接点)。
[0148]
本文中的术语“神经特异性(nerve-specific或nerve specific)”是指被吸取到神经或神经组织并且可以用于荧光成像技术以帮助对比和区分神经或神经组织与周围的细胞和/或组织的药剂。术语“神经特异性(nerve specificity)”是指药剂的性质或活性是神经特异性的。
[0149]
术语“近红外”或首字母缩略词“(nir)”是指近红外光谱处的光,通常在约0.65到约1.4μm(700nm-1400nm)的波长处的光。其还可以是指由国际标准化组织指定的从约0.78μm到约3μm的波长范围。在一些实施例中,优选的近红外光谱和成像(nirs)范围为约650nm到约950nm。在其它实施例中,优选的近红外光谱和成像(nirs)范围为约650nm到约900nm。
[0150]
在一些实施例中,药剂和/或包括所述药剂的组合物打算直接/局部施用。在本文中将直接或局部施用理解为包括将药剂或组合物直接施用到组织、器官、神经束或其它身体组成部分的表面。在一些方法中,施用可以通过用适当的化合物或组合物刷涂、喷涂或冲洗来完成。
[0151]
在其它实施例中,药剂和/或组合物可以如通过静脉内注射或输注全身施用到患者或受试者。
[0152]
在其它实施例中,药剂和/或组合物可以如通过注射局部施用到期望的组织或器
官。
[0153]
术语“有效量”或“药物有效量”或“成像有效量”或类似术语是指如本文所述的化合物或组合物充分覆盖靶标区域以完成与一或多个神经的结合,使得所述神经可以通过相关成像技术,尤其是近红外成像技术来识别的量。
[0154]
术语“烷基”是指直链或支链烃。例如,烷基基团可以包含具有1个到6个碳原子(即,c
1-c6烷基或c
1-6
烷基)、1个到4个碳原子(即,c
1-c4烷基或c
1-4
烷基)、1个到3个碳原子(即,c
1-c3烷基或c
1-3
烷基)或1个到2个碳原子(即,c
1-c2烷基或c
1-2
烷基)的烷基。合适的烷基基团的实例包含但不限于甲基、乙基、正丙基、异丙基(-ch(ch3)2)、1-丁基(n-bu、正丁基、
‑‑
ch2ch2ch2ch3)、2-甲基-1-丙基(i-bu、异丁基、
‑‑
ch2ch(ch3)2)、2-丁基(s-bu、仲丁基、
‑‑
ch(ch3)ch2ch3)、2-甲基-2-丙基(t-bu、叔丁基、
‑‑
c(ch3)3)、1-戊基(正戊基、
‑‑
ch2ch2ch2ch2ch3)、2-戊基(
‑‑
ch(ch3)ch2ch2ch3)、3-戊基(
‑‑
ch(ch2ch3)2)、2-甲基-2-丁基(-c(ch3)2ch2ch3)、3-甲基-2-丁基(
‑‑
ch(ch3)ch(ch3)2)、3-甲基-1-丁基(
‑‑
ch2ch2ch(ch3)2)、2-甲基-1-丁基(-ch2ch(ch3)ch2ch3)、1-己基(
‑‑
ch2ch2ch2ch2ch2ch3)、2-己基(
‑‑
ch(ch3)ch2ch2ch2ch3)、3-己基(-ch(ch2ch3)(ch2ch2ch3))、2-甲基-2-戊基(-c(ch3)2ch2ch2ch3)、3-甲基-2-戊基(-ch(ch3)ch(ch3)ch2ch3)、4-甲基-2-戊基(-ch(ch3)ch2ch(ch3)2)、3-甲基-3-戊基(
‑‑
c(ch3)(ch2ch3)2)、2-甲基-3-戊基(-ch(ch2ch3)ch(ch3)2)、2,3-二甲基-2-丁基(
‑‑
c(ch3)2ch(ch3)2)以及3,3-二甲基-2-丁基(-ch(ch3)c(ch3)3)。
[0155]
术语“烯基”是指具有至少一个不饱和位点,即碳-碳sp2双键的直链或支链烃。例如,烯基基团可以具有2到4个碳原子(即,c
2-c4烯基)。合适的c
2-c4烯基基团的实例包含但不限于乙烯基(ethenyl或vinyl)(-ch=ch2)、烯丙基(-ch2ch=ch2)、丁-1-烯基(
–
ch=ch-ch
2-ch3)、丁-2-烯基(ch
2-ch=ch-ch3)、丁-3-烯基(-ch
2-ch
2-ch=ch)。
[0156]
术语“炔基”是指具有至少一个不饱和位点,即碳-碳sp三键的直链或支链烃。例如,炔基基团可以具有2到6个碳原子(即,c
2-c6炔烃)或2到4个碳原子(即,c
2-c4炔基)。合适的炔基基团的实例包含但不限于乙炔(-c≡ch)、丙炔基(-ch2c≡ch)等。
[0157]
还应理解,本文一般和具体描述和/或示出的化合物结构包含此类化合物的所有对应共振结构。作为使用以下结构的实例,当化合物a可以命名为3-(二甲基-|4-氮烷亚基)-7-(吡咯烷-1-基)-3h-吩噁嗪并且化合物b可以命名为n,n-二甲基-7-(1|4-吡咯烷-1-亚基)-3h-7|5-吩噁嗪-3-胺时,每个化合物落入式(i)的化合物的本定义之内,其中r1和r2形成吡咯烷基环,r4和r5各自是甲基,并且r3和r6都是氢,并且化合物结构a、b、c和d中的每个包含并表示本文中的其它化合物结构。
[0158][0159]
本文中的术语“成像”是指荧光化合物在常规医学成像技术中的用途,包含但不限于与荧光图像导引外科手术(包含微创性腹腔镜检查或内窥镜检查技术)、计算机辅助外科手术或外科手术导航、放射外科手术或放射疗法、介入放射学、荧光显微术和激光共聚焦显微术相关的那些用途。这些技术可以包含从约650nm到900nm的近红外波长。
[0160]
术语“标记”是指促进本文所公开的靶向分子的可视化和/或检测的分子。在一些实施例中,所述标记是荧光部分。术语“标记”是指将标记成功施用到靶标以允许此类检测。
[0161]
如本文所使用的,术语“机器人外科手术”、“机器人辅助外科手术”或“计算机辅助外科手术”是指涉及机器人系统的外科手术技术,所述机器人系统控制医疗器械的运动以利用旨在限制外科手术创伤、失血、疼痛、结疤和术后患者恢复时间和/或并发症(如外科手术区域感染)的量的精确、灵活和/或微创性动作进行外科手术。机器人外科手术的实例包含使用由美国食品和药物管理局(u.s.food and drug administration)于2000年批准的达芬奇外科手术系统(da vinci surgical system)(美国加利福尼亚州桑尼维尔直觉外科手术公司(intuitive surgical,sunnyvale,ca,usa))进行的那些外科手术。
[0162]
如本文所使用的,术语“外科手术”或“外科手术方法”是指用于通过物理干预来操纵、改变或引起效果的任何方法。这些方法包含但不限于开放性外科手术、内窥镜外科手术、腹腔镜外科手术、微创性外科手术、机器人外科手术、任何可能影响任何神经元或神经的手术,如脊柱外科手术期间牵开器的放置、导电心肌组织或神经切除、硬膜外注射、鞘内注射、神经元或神经阻断、如神经元或神经刺激器等装置的植入以及泵的植入。这些方法还可以包含用于如出于诊断目的而收集细胞或组织样品的活检或其它侵入性技术。
[0163]
如本文所使用的,术语“靶向分子”是指与所关注的靶标缔合(例如,结合)的任何药剂(例如,肽、蛋白质、核酸聚合物、适体或小分子)。所关注的靶标可以是神经细胞或与一或多个神经细胞或神经结构相关的器官或组织。在一些实施例中,靶向分子是与包括一或多个神经元、神经或与所述神经元、神经相关的组织或结构,即神经组织、神经系统组织、神经束等的靶标缔合(例如,结合)的任何药剂。应当理解,神经和神经相关靶标包含与中枢神经系统(cns)的脑和脊髓以及周围神经系统(pns)的神经相关的那些靶标。
[0164]
术语“前列腺切除术”是指切除受试者前列腺的全部或部分的外科手术技术。“根
治性前列腺切除术”涉及切除受试者的整个前列腺连同周围组织,通常包含精囊和附近的淋巴结。
[0165]
术语“矫形肢体修复”或“矫形肢体修复外科手术”是指对受试者的肢体肌肉骨骼系统进行的外科手术技术。这些技术包含肢体重建外科手术、关节置换手术、翻修关节外科手术、清创术、骨融合、肌腱或韧带修复、骨内固定和截骨术。
[0166]
本文中的术语“荧光团”是指本文所述的用于成像技术,具体地用于神经成像技术的化合物中的任何一种化合物。本文所述的作为具体合成的产物或在一般描述中描述的化合物中的每种化合物被认为是用于方法、用途和组合物的荧光团。
[0167]
在本文的一般描述和权利要求中使用的术语“变量”是指在一些实例中可以选自具体组的实体或部分。此类变量可以包含r1、r2、r3、r4、r5、r6、n1、n2、n3、n4、x1等。
[0168]
本文所公开和/或要求保护的所有范围包含所陈述的端点并且可独立地组合(例如,“2到10”和“2-10”的范围包含端点2和10,以及所有中间值)。例如,对“权利要求2到5”的提及包含所有权利要求2、3、4和5。
[0169]
如在本文描述方法或用途中使用的术语“术中”是指在外科手术期间或在此类手术的即时准备中发生的活动。
[0170]
如本文所使用的,关于调配物或组合物组分使用的术语“药学上可接受的”或“生理学上可接受的”等是指药学上可接受的媒剂,所述媒剂包含但不限于任何和所有载剂、溶剂、分散介质、涂料、抗细菌剂和抗真菌剂、等渗剂和吸收延迟剂等。此类材料提供了可接受水平的所讨论的荧光团/化合物的活性,并且与其接触的细胞、组织、器官等相容并且对所述细胞、组织、器官等基本上无毒。此类介质和药剂对药物活性物质的用途是本领域众所周知的。除非任何常规介质或药剂与活性成分不相容,否则设想了将其用于治疗性组合物中。还可以将补充性活性成分掺入到组合物中。
[0171]
术语“载剂”是指赋形剂或媒剂,其包含但不限于与所讨论的化合物一起施用的稀释剂、崩解剂、沉淀抑制剂、表面活性剂、助流剂、乳化剂、缓冲剂、稳定剂、润滑剂等。载剂在本文中进行了一般描述并且还描述于e.w.马丁(e.w.martin)的“雷明顿药物科学(remington's pharmaceutical sciences)”中。然而,应当理解,为药物组合物所选择的载剂以及所述组合物中此类载剂的量可以根据调配方法而变化。
[0172]
术语“稀释剂”通常是指用于在递送前稀释所关注的化合物的物质。
[0173]
使用方法
[0174]
提供了一种检测组织或器官中的神经的方法,所述方法包括
[0175]
a)将有效量的包括如本文所描述的荧光团的组合物施用到所述组织或所述器官以形成经染色的组织或经染色的器官;以及
[0176]
b)对所述经染色的组织或所述经染色的器官进行成像,从而在术中检测所述经染色的组织或所述经染色的器官中的神经。
[0177]
提供了一种在术中检测进行外科手术的受试者的神经的方法,所述方法包括:
[0178]
c)在外科手术前或外科手术期间向所述受试者施用有效量的包括如本文所描述的荧光团的组合物以形成经染色的组织;以及
[0179]
d)对所述受试者的进行外科手术的所述经染色的组织进行成像,从而在手术中检测进行外科手术的所述受试者的神经。
[0180]
还提供了一种在术中检测进行前列腺切除术外科手术的受试者的神经的方法,所述方法包括:
[0181]
e)在所述前列腺切除术外科手术之前或期间向所述受试者施用有效量的包括如本文所描述的荧光团的组合物以形成经染色的组织;以及
[0182]
f)对所述受试者的进行外科手术的所述经染色的组织进行成像,从而在手术中检测进行前列腺切除术外科手术的所述受试者的神经。
[0183]
在一个实施例中,提供了一种在术中检测进行前列腺切除术外科手术的受试者的海绵体神经的方法,所述方法包括:
[0184]
g)在所述前列腺切除术外科手术之前或期间向所述受试者施用有效量的包括如本文所描述的荧光团的组合物以形成经染色的组织;以及
[0185]
h)对所述受试者的进行外科手术的所述经染色的组织进行成像,从而在手术中检测进行前列腺切除术外科手术的所述受试者的海绵体神经。
[0186]
对于本文涉及前列腺切除术外科手术或手术的方法中的每种方法,存在其中所述外科手术或手术是根治性前列腺切除术的另一个实施例。
[0187]
对于以上和本文中的方法中的每种方法,存在其中将包括荧光团的组合物全身施用到受试者的实施例。
[0188]
对于以上和本文中的方法中的每种方法,存在其中将包括荧光团的组合物直接或局部,即通过直接施用或局部施用而施用到受试者的实施例。
[0189]
在本文的方法中的每种方法中,存在其中在前列腺切除术外科手术之前或期间向受试者施用有效量的包括如本文所描述的荧光团的组合物以形成经染色的组织可以在十五分钟或更短时间内完成的另外的实施例。在仍进一步的实施例中,在前列腺切除术外科手术之前或期间向受试者施用有效量的包括如本文所描述的荧光团的组合物以形成经染色的组织可以在十分钟或更短时间内完成。
[0190]
本文还提供了对神经组织肿瘤(赘生物)进行成像的方法,所述神经组织肿瘤包含神经胶质瘤,如bliomatosis cerbri、少突星形细胞瘤、脉络丛乳突瘤、室管膜瘤、星形细胞瘤(毛细胞星形细胞瘤和多形性胶质母细胞瘤)、胚胎发育不良性神经上皮肿瘤、少突神经胶质细胞瘤、髓母细胞瘤和原始神经外胚层肿瘤;神经上皮瘤,如神经节细胞瘤、神经母细胞瘤、非典型畸胎样横纹肌样瘤、视网膜母细胞瘤和嗅神经母细胞瘤;以及神经鞘瘤,如神经纤维瘤(神经纤维肉瘤和神经纤维瘤病)、许旺氏细胞瘤、神经鞘瘤(neurinomas)、听神经瘤和神经瘤。
[0191]
提供了一种对受试者的靶标区域进行成像的方法,所述方法包括使所述受试者的所述靶标区域与选自本文的那些化合物的化合物接触并使用荧光或近红外成像检测所述靶标中的所述化合物。
[0192]
还提供了一种对受试者的靶标区域中的一或多个神经进行成像的方法,所述方法包括使所述受试者的所述靶标区域与选自本文中的那些化合物的化合物接触并使用荧光成像检测所述靶标中的所述化合物。
[0193]
还提供了一种对受试者的靶标区域中的一或多个神经进行成像的方法,所述方法包括使所述受试者的所述靶标区域与选自本文中的那些化合物的化合物接触并使用近红外成像检测所述靶标中的所述化合物。
simultaneous near-infrared fluorescence imaging of bile duct and arterial anatomy).外科手术研究杂志(the journal of surgical research)176,7-13(2012);费尔贝克(verbeek)等人泌尿学杂志190,574-579(2013);吉布斯-斯特劳斯等人分子成像10,91-101(2011);赫希(hirche)等人外科创新(surgical innovation)20,516-523(2013);高多(gotoh)等人外科肿瘤学杂志(journal of surgical oncology)100,75-79(2009);以及喜多川(kitagawa)等人抗癌研究(anticancer research)35,6201-6205(2015)。重要的是,经常用于机器人辅助根治性前列腺切除术(rp)的达芬奇外科手术机器人可以配备fda批准的荧光成像通道。
[0203]
直接施用(有时也称为局部施用)是荧光探针的全身施用的有吸引力的替代方案,用于最大限度地减少潜在毒性并减轻首次人体临床研究中的监管负担。通过选择性地标记外科手术区域内的组织,直接施用所需的剂量明显低于全身施用。已开发出一种直接施用方法,所述方法在15分钟染色方案后提供了与全身施用等效的神经信号与背景比率(sbr)。巴斯(barth)和吉布斯.治疗诊断学7,573-593(2017)。此方法已成功应用于自主神经模型,所述模型密切模仿前列腺周围的神经。此方法在rp的应用中具有另外的益处,因为在rp期间通过全身施用进行神经标记会从无法保留的前列腺神经和肾脏荧光团清除中产生高背景,从而在相邻的膀胱内的尿液中产生明显的荧光信号。这两种无关的荧光信号都会降低识别神经血管束(nvb)内海绵体神经的能力,所述海绵体神经负责节制力和效力(巴斯和萨默(summer).治疗诊断学(2016)。特瓦里(tewari)等人英国国际泌尿学杂志(bju international)98,314-323(2006);帕特(patel)等人欧洲泌尿学61,571-576(2012))。也许最重要的是,直接施用方法所需的剂量为全身施用的1/16,并且当按体表面积缩放到人体时,所述剂量属于在向fda的探索性试验性新药(eind)申请下临床转化的要求的范围内。在eind下进行的研究需要最少的临床前毒性测试,因为仅向每个患者施用微剂量(《100μg),从而明显降低了首次人体研究的成本。
[0204]
虽然直接施用方法已在临床前啮齿动物模型中以短染色方案提供了高神经特异性和sbr(巴斯和吉布斯.治疗诊断学7,573-593(2017)),但在大型动物模型中的初步染色研究产生了明显的背景。为了促进临床转化,需要fda批准并有助于加强对各种组织表面进行染色、角度和形态的应用控制的改良调配物策略。
[0205]
包括一或多种本文公开的化合物的调配物可以用于对神经或神经组织进行成像。在特定实施例中,本公开的调配物可以用于对受试者的神经或神经组织进行成像。在特定实施例中,神经的图像可以在fgs期间在术中获得。在特定实施例中,在fgs期间神经的可视化允许对所关注的组织进行外科手术,同时保留神经以便降低外科手术期间神经损伤的发生率。可以通过外科手术暴露进行外科手术的区域或附近区域。可以对器官进行外科手术,所述器官包含如神经组织、肌肉组织和脂肪组织等组织。外科手术可以是腹腔镜检查,所述腹腔镜检查是微创性的并且包含使用薄的管状装置(腹腔镜),所述装置通过锁孔切口插入受试者身体的一部分,如腹部或骨盆。外科手术可以由机器人辅助。机器人辅助外科手术可以提供更高的精确度、灵活性和控制力,并且通常与微创性外科手术相关。
[0206]
在特定实施例中,直接施加到神经组织的调配物中荧光团的浓度包含40到300μg/ml的浓度范围。在特定实施例中,用于直接施加的调配物中荧光团的浓度包含40μg/ml、50μg/ml、60μg/ml、70μg/ml、80μg/ml、90μg/ml、100μg/ml、110μg/ml、120μg/ml、130μg/ml、140μ
g/ml、150μg/ml、160μg/ml、170μg/ml、180μg/ml、190μg/ml和200μg/ml。在特定实施例中,用于直接施加的调配物中荧光团的浓度为50μg/ml。在特定实施例中,用于直接施加的调配物中荧光团的浓度为200μg/ml。
[0207]
本公开的调配物可以全身施加到受试者用于神经成像。在特定实施例中,调配物的全身施加包含将所述调配物静脉内注射到受试者体内。
[0208]
可以允许直接施加到组织的调配物在直接施加后渗透组织,持续给定量的时间。在特定实施例中,可以允许调配物渗透组织,持续30秒到15分钟、持续1分钟到10分钟、持续1分钟到5分钟、持续1分钟、持续2分钟、持续3分钟、持续4分钟或持续5分钟。在特定实施例中,可以允许调配物渗透组织,持续1分钟到2分钟。全身施加到受试者的调配物可以在成像前施用足够的时间,使得调配物可以到达要成像的区域并且在成像时存在于此区域中。在特定实施例中,全身施用到受试者的调配物可以在成像之前施用足够的时间,以允许调配物被受试者的组织所吸收。在特定实施例中,调配物可以在成像之前施用至多或少于30分钟、1小时、2小时、3小时、4小时、5小时、6小时、7小时或8小时。所需时间量可能取决于神经成像施加和施用位点。在特定实施例中,在成像前施用调配物不超过30分钟、1小时、2小时、3小时或4小时。在特定实施例中,在成像前施用调配物不超过2小时。
[0209]
通过直接施加而由包含荧光团的调配物染色的组织可以在对经染色的组织进行成像之前用缓冲液洗涤。洗涤由包含荧光团的调配物染色的组织可以包含用适当的缓冲液冲洗所述组织并去除所述缓冲液。在特定实施例中,经染色的组织可以用洗涤缓冲液洗涤1到18次、1到10次、1到6次、1次、2次、3次、4次、5次或6次。在特定实施例中,经染色的组织可以洗涤6次。在特定实施例中,洗涤缓冲液是磷酸盐缓冲盐水(pbs)。在特定实施例中,洗涤经染色的组织去除了未结合的荧光团。在特定实施例中,与不洗涤经染色的组织相比,洗涤经染色的组织增加了神经信号强度和/或信号与背景比率(sbr)。在特定实施例中,洗涤经染色的组织使荧光团重新溶解并允许荧光团进一步扩散到神经组织中。
[0210]
对由包含荧光团的调配物染色的组织进行成像包含将光施加到已经用本公开的调配物染色的组织。所述光的波长可以足以激发调配物中的荧光团发出荧光。在特定实施例中,用于激发荧光团的光处于近红外光谱中的波长处。在特定实施例中,调配物的荧光团在近红外光谱中的波长处发射。在特定实施例中,近红外光谱包含650到900nm的波长。在一些实施例中,所关注的红外光谱为约700nm。在其它实施例中,所关注的红外光谱包含约725nm到约875nm的波长。
[0211]
对由包含荧光团的调配物染色的组织进行成像包含通过光学成像系统(如实例中描述的那些)获得经染色的组织的荧光图像。
[0212]
在特定实施例中,对组织进行成像包含观察经染色的组织的荧光图像。荧光图像可以包含静止图像(无论是打印的还是屏幕上的),或视频监视器上的实时图像。在特定实施例中,通过用本调配物对神经进行染色所获得的单个神经图像可以用于诊断目的并且用于记录神经位置。通过观察荧光图像,外科手术团队可以确定所述图像中不存在或存在神经。因此,外科手术团队可以使用关于存在/不存在一或多个神经或一或多个神经的位置的信息来确定将如何进行外科手术。例如,基于通过公开的方法获得的信息,外科手术团队可以决定在组织中的某一点处进行外科手术切割,其中不太可能基于感知到的组织的区域中神经的缺失而无意地切割或手术接触特定神经。
[0213]
如果神经末端被横断,则从获得的图像中获得的信息可以帮助移植所述神经末端。在横断的情况下,可以将神经移植物直接施加到所述末端,以促进再生神经纤维的萌发。在这种情况下,从横断神经的末端的荧光中可见的光提供了靶标以指导神经移植物对神经的吻合。
[0214]
提供了一种调配物,所述调配物包括有效量的如本文所描述的化合物以及药学上或生理学上可接受的载剂。在一些实施例中,药学上或生理学上可接受的载剂是水性载剂。
[0215]
水性载体可以包含盐水溶液,如缓冲盐水溶液,以及葡萄糖水溶液和甘油水溶液。合适的药物载剂还可以包含赋形剂,如葡萄糖、乳糖、蔗糖、单硬脂酸甘油酯、氯化钠、甘油、丙烯、乙二醇、水、乙醇等。如果需要,本组合物还可以含有少量的润湿剂或乳化剂(如可从巴斯夫(basf)获得的产品家族)或ph缓冲剂。
[0216]
用于检测神经组织的本公开的调配物也可以以试剂盒的形式提供。用于检测神经组织的试剂盒在不同的容器中可以包含:(i)包括荧光团的基于水的调配物,以及(ii)一或多种洗涤缓冲液。试剂盒还可以包含由管理药物或生物制品的制造、使用或销售的政府机构规定的形式的公告,所述公告反映了机构针对人类施用在制造、使用或销售方面的许可。所述公告可以声明所提供的活性成分可以施用到受试者。试剂盒可以包含用于使用试剂盒的另外的说明书,例如关于以下的说明书;将调配物直接施加到组织;洗涤以去除多余的调配物;将调配物全身施用到受试者;应用光来可视化荧光团;捕获组织的荧光图像;妥善处置相关废物;等。说明书可以呈试剂盒内提供的印刷说明书的形式,或者说明书可以印刷在试剂盒本身的一部分上。说明书可以呈表格、小册子、手册、cd-rom或计算机可读装置的形式,或者可以在如网站等远程位置处提供对说明书的指导。在特定实施例中,试剂盒还可以包含有效使用试剂盒所需的一些或全部必要的实验室和/或医疗用品,如注射器、安瓿、管件、手套、导管、缓冲液等。可以对本文所述的任何试剂盒的内容进行更改。
[0217]
概述
[0218]
所有试剂均购自西格玛奥德里奇(sigma aldrich)、飞世尔科技公司(fisher scientific)或东京化成工业株式会社(tci)。除非另有说明,否则所有可商购获得的起始材料均直接使用而无需进一步纯化。分析型tlc在具有硅胶60(f254,32-63μm)的millipore即用型板上进行。在使用预装硅胶柱的biotage isolera flash系统上或在反相制备型hplc(agilent 1250infinity hplc)上进行纯化。
[0219]
lcms表征
[0220]
在具有二极管阵列检测器vl+的安捷伦6244飞行时间lcms上表征噁嗪化合物的质荷比和纯度。将样品(10ul)注射到c18柱(poroshell 120,4.6
×
50mm,2.7微米)中,并用a(h2o,0.1%fa)和b(mecn,01.%fa)的溶剂体系以0.4毫升/分钟进行洗脱,10分钟内从a/b=90/10到5/95,在a/b=5/95下维持另外的5分钟。通过将毛细管电压设置为4kv并将气体温度设置为350℃,在正离子模式下检测离子。
[0221]
使用直接/局部施用进行神经特异性筛选
[0222]
使用先前发表的鼠臂丛神经和坐骨神经中的直接/局部施用策略针对组织特异性筛选每种化合物。6将来自噁嗪文库的每种化合物在先前使用的共溶剂调配物(10%dmso,5%kolliphor,65%血清和20%磷酸盐缓冲盐水)中以125μm进行调配。将100μl调配的噁嗪在暴露的臂丛神经或坐骨神经上温育5分钟。去除含有所述荧光团的溶液,并用盐水冲洗所
述区域18次以去除任何未结合的荧光团。在噁嗪直接/局部施用后30分钟,使用具有620/60nm激发和700/75nm带通发射滤光片的定制宏观成像系统收集每个经染色的区域的共配准荧光和彩色图像。使用自定义编写的matlab代码分析组织特异性荧光,其中使用白光图像在神经、肌肉和脂肪组织上选择所关注的区域。然后在共配准匹配荧光图像上分析这些所关注的区域,从而允许评估神经与肌肉和神经与脂肪的比率。
[0223]
使用全身施用进行神经特异性筛选
[0224]
使用先前发表的鼠臂丛神经和坐骨神经中的全身施用策略针对组织特异性筛选每种化合物。6将来自噁嗪文库的每种化合物在先前使用的共溶剂调配物(10%dmso,5%kolliphor,65%血清和20%磷酸盐缓冲盐水)中以2mm进行调配。在暴露臂丛神经和坐骨神经前4小时静脉内施用100μl调配的噁嗪。使用具有620/60nm激发和700/75nm带通发射滤光片的定制宏观成像系统收集每个神经部位的共配准荧光和彩色图像。使用自定义编写的matlab代码分析组织特异性荧光,其中使用白光图像在神经、肌肉和脂肪组织上选择所关注的区域。然后在共配准匹配荧光图像上分析这些所关注的区域,从而允许以盲检方式评估神经与肌肉和神经与脂肪的比率。
[0225]
化学合成
[0226][0227]
方案:lgw11-98的合成路线。试剂和条件:a)6m hcl,nano2,0℃;b)氯乙酰氯,tbab、nahco3,h2o,0℃;c)1m bbr3,dcm,0℃到室温;d)nah,thf,0℃到室温;e)bh
3-thf,thf,0℃到室温;f)ac2o,h2o,50℃到室温;g)bh
3-thf,thf,0℃到室温;h)化合物2,hclo4,90%i-proh,80℃。
[0228]
5-(二甲氨基)-2-亚硝基苯酚(2):将化合物1(1.00g,7.29mmol)溶解在冰冷的6mhcl溶液(5ml)中。在1小时内向上述溶液中分批添加nano2(0.513g,7.44mmol),同时将溶液的温度保持低于5℃,使得未观察到棕色nox蒸气。将反应混合物搅拌另外的2小时。之后,将沉淀物通过布赫纳漏斗(b
ü
chner funnel)过滤并用小部分冰冷的2m hcl溶液洗涤。将产
物留在漏斗中并风干过夜,以提供呈黄色固体的化合物2(1.01g,84%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0229]
2-氯-n-(2,5-二甲氧基苯基)乙酰胺(4):在n2下将化合物3(20.0g,130mmol)溶解在无水mecn(60ml)中,并在冰浴中冷却。向溶液中小心添加et3n(40ml,287mmol)和氯乙酰氯(12.7ml,159mmol)。将反应混合物搅拌1小时,然后用500ml di水进行稀释。滤出固体悬浮液,以产生呈浅棕色固体的化合物4(21.0g,70%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0230]
2-氯-n-(2,5-二羟苯基)乙酰胺(5):在n2下将化合物4(10.0g,43.5mmol)溶解在无水dcm(20ml)中,并在冰浴中冷却。使用注射泵在1小时内向上述溶液中滴加bbr3(1m于dcm中,130ml,130mmol)。将反应混合物缓慢温热到室温并搅拌过夜。将反应烧瓶放置于冰浴中,在足够的冷却时间后,小心地将水添加到反应混合物中以破坏过量的bbr3。通过真空过滤收集所得沉淀物并用小部分di水洗涤所述沉淀物。将产物留在漏斗中并风干过夜,以提供化合物5(7.96g,91%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0231]
6-羟基-2h-苯并[b][1,4]噁嗪-3(4h)-酮(6):在n2下将化合物5(6.00g,29.8mmol)溶解在无水thf(50ml)中,并在冰浴中冷却。在足够的冷却时间后,在10分钟内将nah(60%,4.17g,104mmol)分4份添加到溶液中。将反应混合物缓慢温热到室温并搅拌过夜。反应完成后,小心地向反应烧瓶中添加冰冷的水以破坏过量的nah。将反应混合物用2m hcl酸化,然后用etoac(5
×
100ml)萃取。将合并的有机层用盐水冲洗并经无水na2so4干燥。使用旋转蒸发器去除溶剂,并且将残留物通过利用硅胶的快速柱色谱法,使用etoac/dcm/己烷作为洗脱液来进行纯化以得到呈浅棕色固体的化合物6(3.12g,63%)。
[0232]
3,4-二氢-2h-苯并[b][1,4]噁嗪-6-醇(7):在n2下将6(2.2g,13.3mmol)于无水thf(40ml)中的溶液在冰浴中搅拌30分钟。使用注射泵在30分钟内将硼烷四氢呋喃络合物溶液(1m,40ml)添加到上述溶液中,同时保持溶液温度低于5℃。将所得反应混合物留在冰浴中并缓慢温热到室温。24小时后,将溶液再次放置于冰浴中,并且通过小心地添加meoh直至没有气体逸出来破坏过量的硼烷试剂。在减压下蒸发溶剂,将残留物通过利用硅胶的快速柱色谱法,使用eroac/己烷作为洗脱液来进行纯化以获得7(1.91g,95%)。
[0233]
1-(6-羟基-2,3-二氢-4h-苯并[b][1,4]噁嗪-4-基)乙-1-酮(8):将化合物7(1.00g,6.62mmol)悬浮在10ml di水中,向其中滴加乙酸酐(2.5ml,26.5mmol)。将反应混合物放置于超声浴中持续1分钟,然后在水浴(50℃)中搅拌10分钟。将所得溶液在室温下搅拌过夜。之后,通过真空过滤收集固体并用小部分di水洗涤所述固体。将产物留在漏斗中并风干过夜,以提供呈白色固体的化合物8(1.21g,95%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0234]
4-乙基-3,4-二氢-2h-苯并[b][1,4]噁嗪-6-醇(9):在n2下将8(900mg,10.0mmol)于无水thf(14ml)中的溶液在冰浴中搅拌30分钟。使用注射泵在30分钟内将硼烷四氢呋喃络合物溶液(1m,14ml)添加到所述溶液中,同时保持溶液温度低于5℃。将所得反应混合物留在冰浴中并缓慢温热到室温。24小时后,将溶液再次放置于冰浴中,并且通过小心地添加meoh直至没有气体逸出来破坏过量的硼烷试剂。在减压下蒸发溶剂,将残留物通过利用硅胶的快速柱色谱法,使用dcm/己烷作为洗脱液来进行纯化以得到呈棕色油状物的9(756mg,91%)。
[0235]
n-(4-乙基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)-n-甲基甲铵(lgw11-98):在80℃将化合物9(40mg,0.22mmol)溶解在i-proh/h2o的溶液(9/1,3ml)中持续30分钟。在15分钟内将化合物2(73mg,0.22mmol)分5份添加到溶液中。然后用hclo4(70%,20μl)处理反应混合物。将所得溶液搅拌过夜。在减压下蒸发深蓝色溶液,并将残留物通过利用硅胶的快速柱色谱法,使用含有0.5%甲酸的chcl3和meoh的流动相(线性梯度,2-15%的meoh/chcl3)来进行纯化。合并含有产物的级分并将所述级分蒸发,从而提供呈深蓝色固体的lgw11-98(26mg,38%)。ms(esi):c
18h20
n3o2[m]
+
的计算值:310.1550;实测值:310.1563。
[0236][0237]
方案:lgw13-79的合成路线。试剂和条件:a)mei,nah,thf,0℃到室温;b)2m hcl,nano2,0℃;ii)k2co3,0℃;c)pd(oac)2,verkade碱,lihmds,氮杂环丁烷,甲苯,80℃。d)化合物12,hclo4,90%i-proh,80℃。
[0238]
n,n-二乙基-3-甲氧基苯胺(11):在n2下将化合物10(5.00g,30.3mmol)溶解在无水thf(50ml)中,并在冰浴中冷却30分钟。在10分钟内将nah(60%,3.63g,90.8mmol)分3份添加到溶液中,同时将温度保持低于5℃。10分钟后,将mei(7.54ml,121mmol)一次性添加到反应混合物中。将所得悬浮液缓慢温热到室温并搅拌过夜。完成后,将di水添加到反应混合物中以破坏过量的nah。在减压下去除有机溶剂并且用dcm(3
×
100ml)萃取残留物。将合并的有机层用盐水冲洗,经无水na2so4干燥,并且使用旋转蒸发器去除溶剂。将残留物通过利用硅胶的快速柱色谱法,使用dcm/己烷作为洗脱液来进行纯化,以得到呈透明油状物的化合物11(4.70g,88%)。
[0239]
n,n-二乙基-3-甲氧基-4-亚硝基苯胺(12):将化合物11(1.08g,6.02mmol)溶解在冰冷的2m hcl溶液(15ml)中。在1小时内向上述溶液中分批添加nano2(457mg,6.63mmol),同时将溶液的温度保持低于5℃,使得未观察到棕色nox蒸气。将反应混合物搅拌另外的2小时。用固体k2co3小心地将溶液碱化,直到溶液的ph值升到8以上。之后,将沉淀物通过布赫纳漏斗过滤并用小部分di水洗涤。将产物留在漏斗中并风干过夜,以提供呈绿色固体的化合物12(1.05g,84%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0240]
3-(氮杂环丁烷-1-基)苯酚(14):化合物14按照由格里姆(grimm)等人公布的稍作修改的方案合成7。向烘干烧瓶中装入pd(oac)2(52mg,0.231mmol)。将烧瓶密封,在真空下抽真空并用n2回填5次,然后添加甲苯(40ml)。然后向化合物13(2.00g,11.6mmol)于甲苯(10ml)中的溶液中依次添加含2,8,9-三异丁基-2,5,8,9-四氮杂-1-磷杂双环[3.3.3]十一烷(159mg,0.463mmol)的甲苯(10ml)和lihmds溶液(1.3m,20ml,26mmol)。在添加氮杂环丁烷(792mg,13.9mmol)后,将反应在80℃下搅拌过夜。然后将其冷却到室温,沉积在硅藻土上
并浓缩至干燥。通过硅胶快速色谱法,使用etoac和己烷的流动相进行的纯化提供了呈灰白色固体的化合物14(1.38g,80%)。
[0241]
1-(7-(二乙氨基)-3h-吩噁嗪-3-亚基)氮杂环丁烷-1-正离子(lgw13-79):在80℃将化合物14(40mg,0.268mmol)溶解在i-proh/h2o的溶液(9/1,4ml)中持续30分钟。在15分钟内将化合物12(56mg,0.268mmol)分5份添加到溶液中。然后用hclo4(70%,20μl)处理反应混合物。将所得溶液搅拌过夜。然后将深蓝色溶液冷却到室温,在减压下蒸发,并将残留物通过利用硅胶的快速柱色谱法,使用含有0.5%甲酸的chcl3和meoh的流动相(线性梯度,2-15%的meoh/chcl3)来进行纯化。合并含有产物的级分并将所述级分蒸发,从而提供呈深蓝色固体的lgw13-79(25mg,30%)。ms(esi):c
19h22
n3o[m]
+
的计算值:308.1757;实测值:308.1763。
[0242][0243]
方案:lgw14-42的合成路线。试剂和条件:a)氯乙酰氯,k2co3,mecn,80℃;b)bh
3-thf,thf,0℃到室温;c)eti,na2co3,mecn,80℃;d)i)2m hcl,对硝基苯重氮四氟硼酸盐,0℃;ii)k2co3,0℃;e)化合物14,ppse,cf3ch2oh,80℃。
[0244]
6-甲氧基-2h-苯并[b][1,4]噁嗪-3(4h)-酮(16):化合物16是按照由张(zhang)等人报道的稍微修改的方案合成的8。在n2气氛下,将化合物15(2.00g,14.4mmol)溶解在无水mecn(20ml)中,向其中滴加2-氯乙酰氯(1.37ml,17.3mmol)。添加k2co3(4.97g,25.9mmol)后,将反应混合物加热至80℃并搅拌过夜。然后将其冷却到室温,用dcm稀释,并通过硅藻土过滤。在真空下去除溶剂,并将残留物通过硅胶快速色谱法,使用etoac和己烷的流动相来进行纯化,从而提供呈棕色固体的化合物16(2.21g,86%)。
[0245]
6-甲氧基-3,4-二氢-2h-苯并[b][1,4]噁嗪(17):将化合物16(2.00g,11.2mmol)于无水thf(30ml)中的溶液在n2下在冰浴中搅拌30分钟。使用注射泵在30分钟内将硼烷四氢呋喃络合物溶液(1m,30ml)滴加到上述溶液中,同时将溶液的温度保持低于5℃。将所得反应混合物留在冰浴中搅拌并缓慢温热到室温。24小时后,将溶液再次放置于冰浴中,并且通过小心地添加meoh直至没有气体逸出来破坏过量的硼烷试剂。在减压下蒸发溶剂,并且将残留物通过利用硅胶的快速柱色谱法,使用dcm/己烷作为洗脱液来进行纯化,从而提供呈淡粉色固体的化合物17(1.62g,88%)。
[0246]
4-乙基-6-甲氧基-3,4-二氢-2h-苯并[b][1,4]噁嗪(18):在室温下在n2下向化合物17(1.00g,6.05mmol)和na2co3(1.28g,12.1mmol)于无水mecn(10ml)中的悬浮液中添加eti(0.501ml,6.17mmol)。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温,用dcm稀释,并通过硅藻土过滤。在真空下去除溶剂,并且将残留物通过利用硅胶的硅胶快速色谱法,使用dcm/己烷作为洗脱液来进行纯化,以得到呈浅棕色油状物的化合物18(1.01g,86%)。
[0247]
(e)-4-乙基-6-甲氧基-7-((4-硝基苯基)二氮烯基)-3,4-二氢-2h-苯并[b][1,4]噁嗪(19):将化合物18(400mg,2.07mmol)溶解于meoh(1ml)中。将溶液在冰浴中冷却,然后用hcl(2m,10ml)处理。15分钟后,在另外15分钟内将对硝基苯重氮四氟硼酸盐(515mg,2.17mmol)分3份添加到溶液中,然后在0℃搅拌1小时。在此时间期间,反应混合物的颜色从橙色变为深红色。两小时后,将溶液小心地用固体k2co3中和,直到溶液的ph值升至7以上。通过真空过滤收集沉淀物并用小部分di水洗涤所述沉淀物。将产物留在漏斗中,风干过夜,提供呈绿色固体的化合物19(537mg,76%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0248]
1-(4-乙基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)氮杂环丁烷-1-正离子(lgw14-42):将化合物14(30mg,0.201mmol)和19(69mg,0.201mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h20
n3o2[m]
+
的计算值:322.1550;实测值:322.1584。
[0249][0250]
方案:lgw14-45合成。试剂和条件:a)mei,na2co3,mecn,80℃;b)i)2m hcl,对硝基苯重氮四氟硼酸盐,0℃;ii)k2co3,0℃;c)化合物1,ppse,cf3ch2oh,80℃。
[0251]
6-甲氧基-4-甲基-3,4-二氢-2h-苯并[b][1,4]噁嗪(20):在室温下在n2下向化合物17(1.00g,6.05mmol)和na2co3(1.28g,12.1mmol)于无水mecn(10ml)中的悬浮液中添加mei(400μl,6.36mmol)。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温,用dcm稀释,并通过硅藻土过滤。在真空下去除溶剂,并且将残留物通过利用硅胶的硅胶快速色谱法,使用dcm/己烷作为洗脱液来进行纯化,以得到呈深红色油状物的化合物20(0.814g,75%)。
[0252]
(e)-6-甲氧基-4-甲基-7-((4-硝基苯基)二氮烯基)-3,4-二氢-2h-苯并[b][1,4]噁嗪(21):将化合物20(400mg,2.23mmol)溶解于meoh(1ml)中。将溶液在冰浴中冷却,然后用hcl(2m,10ml)处理。15分钟后,在另外15分钟内将对硝基苯重氮四氟硼酸盐(555mg,2.34mmol)分3份添加到溶液中,然后在0℃搅拌1小时。在此时间期间,反应混合物的颜色从橙色变为深红色。两小时后,将溶液小心地用固体k2co3中和,直到溶液的ph值升至7以上。通过真空过滤收集沉淀物并用小部分di水洗涤所述沉淀物。将产物留在漏斗中,风干过夜,提供呈深红色固体的化合物21(693mg,95%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0253]
n-甲基-n-(4-甲基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)甲铵(lgw14-45):将化合物1(30mg,0.219mmol)和21(72mg,0.219mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
17h18
n3o2[m]
+
的
计算值:296.1394;实测值:296.1441。
[0254][0255]
方案:lgw14-46的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0256]
n-乙基-n-(4-甲基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)乙铵(lgw14-46):将化合物10(30mg,0.182mmol)和21(60mg,0.182mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h22
n3o2[m]
+
的计算值:324.1707;实测值:324.1746。
[0257][0258]
方案:lgw14-47的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0259]
1-(4-甲基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)氮杂环丁烷-1-正离子(lgw14-47):将化合物14(30mg,0.201mmol)和21(66mg,0.201mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
18h18
n3o2[m]
+
的计算值:308.1394;实测值:308.1436。
[0260][0261]
方案:lgw14-49的合成路线。试剂和条件:a)ac2o,h2o,50℃到室温;b)bh
3-thf,thf,0℃到室温;c)mei,na2co3,mecn,80℃;d)i)2m hcl,对硝基苯重氮四氟硼酸盐,0℃;ii)k2co3,0℃;e)化合物10,ppse,cf3ch2oh,80℃。
[0262]
n-(3-甲氧基苯基)乙酰胺(23):将化合物22(2.00g,16.2mmol)悬浮在20ml di水中,向其中滴加乙酸酐(4.61ml,48.7mmol)。将反应混合物放置于超声浴中1分钟,然后在热水浴(50℃)中搅拌10分钟。将所得溶液在室温下搅拌过夜。通过真空过滤收集固体产物并用小部分di水洗涤所述固体产物。将产物留在漏斗中,风干过夜,提供呈灰白色固体的化合物23(2.37g,88%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0263]
n-乙基-3-甲氧基苯胺(24):将化合物23(2.00g,12.1mmol)于无水thf(30ml)中的溶液在n2下在冰浴中搅拌30分钟。使用注射泵在30分钟内将硼烷四氢呋喃络合物溶液(1m,30ml)滴加到上述溶液中,同时将溶液的温度保持低于5℃。将所得反应混合物留在冰浴中搅拌并缓慢温热到室温。24小时后,将溶液再次放置于冰浴中,并且通过小心地添加meoh直至没有气体逸出来破坏过量的硼烷试剂。在减压下蒸发溶剂,并且将残留物通过利用硅胶的快速柱色谱法,使用dcm/己烷作为洗脱液来进行纯化,从而提供呈油状物的化合物24(1.47g,80%)。
[0264]
n-乙基-3-甲氧基-n-甲基苯胺(25):在室温下在n2下向化合物24(1.00g,6.61mmol)和na2co3(1.05g,9.92mmol)于无水mecn(10ml)中的悬浮液中添加mei(424μl,6.75mmol)。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温,用dcm稀释,并通过硅藻土过滤。在真空下去除溶剂,并且将残留物通过利用硅胶(25g)的硅胶快速色谱法,使用dcm/己烷作为洗脱液来进行纯化,以得到呈淡黄色固体的化合物25(917mg,84%)。
[0265]
(e)-n-乙基-3-甲氧基-n-甲基-4-((4-硝基苯基)二氮烯基)苯胺(26):将化合物25(400mg,2.42mmol)溶解于meoh(1ml)中。将溶液在冰浴中冷却,然后用hcl(2m,10ml)处理。15分钟后,在另外15分钟内将对硝基苯重氮四氟硼酸盐(602mg,2.54mmol)分3份添加到溶液中,然后在0℃搅拌1小时。在此时间期间,反应混合物的颜色从橙色变为深红色。两小时后,将溶液小心地用固体k2co3中和,直到溶液的ph值升至7以上。通过真空过滤收集沉淀物并用小部分di水洗涤所述沉淀物。将产物留在漏斗中,风干过夜,提供呈深红色固体的化合物26(714mg,94%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0266]
n-乙基-n-(7-(乙基(甲基)氨基)-3h-吩噁嗪-3-亚基)乙铵(lgw14-49):将化合物10(30mg,0.182mmol)和26(57mg,0.182mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h24
n3o[m]
+
的计算值:310.1914;实测值:310.1943。
[0267][0268]
方案:lgw14-50的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0269]
n-(7-(乙基(甲基)氨基)-3h-吩噁嗪-3-亚基)-n-甲基甲胺(lgw14-50):将化合物1(30mg,0.219mmol)和26(69mg,0.219mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
17h20
n3o[m]
+
的计算值:282.1601;实测值:282.1626。
[0270][0271]
方案:lgw14-51的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0272]
(e)-n-(7-(氮杂环丁烷-1-基)-3h-吩噁嗪-3-亚基)-n-甲基乙铵(lgw14-51):将化合物14(30mg,0.201mmol)和26(63mg,0.201mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
18h20
n3o[m]
+
的计算值:294.1601;实测值:294.1634。
[0273][0274]
方案:lgw14-53的合成路线。试剂和条件:a)pd2(dba)3、xphos、cs2co3、氮杂环丁烷、二噁烷、100℃;b)i)2m hcl,对硝基苯重氮四氟硼酸盐,0℃;ii)k2co3,0℃;c)化合物14,ppse,cf3ch2oh,80℃。
[0275]
1-(3-甲氧基苯基)氮杂环丁烷(28):向火焰干燥的烧瓶中装入磁力搅拌棒、化合物27(2.00g,10.7mmol)、pd2(dba)3(979mg,1.07mmol)、xphos(1.53g,3.21mmol)和cs2co3(4.88g,14.97mmol)。将烧瓶密封,在真空下抽真空并用n2回填5次,然后通过注射器递送氮杂环丁烷(800μl,11.8mmol)和无水二噁烷(20ml)。将反应加热到100℃并搅拌6小时,然后冷却到室温,用dcm(20ml)稀释。通过硅藻土过滤去除固体,然后将滤液沉积在硅藻土上,并且浓缩至干燥。通过硅胶快速色谱法,使用etoac和己烷的流动相进行的纯化提供了呈橙黄色固体的化合物28(1.58g,91%)。
[0276]
(e)-1-(3-甲氧基-4-((4-硝基苯基)二氮烯基)苯基)氮杂环丁烷(29):将化合物28(400mg,2.45mmol)溶解于meoh(1ml)中。将溶液在冰浴中冷却,然后用hcl(2m,10ml)处理。15分钟后,在另外15分钟内将对硝基苯重氮四氟硼酸盐(639mg,2.70mmol)分3份添加到溶液中,然后在0℃搅拌1小时。在此时间期间,反应混合物的颜色从橙色变为深红色。两小时后,将溶液小心地用固体k2co3中和,直到溶液的ph值升至7以上。通过真空过滤收集沉淀物并用小部分di水洗涤所述沉淀物。将产物留在漏斗中,风干过夜,提供呈黑色固体的化合物29(630mg,82%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0277]
1-(7-(氮杂环丁烷-1-基)-3h-吩噁嗪-3-亚基)氮杂环丁烷-1-正离子(lgw14-53):将化合物14(29mg,0.192mmol)和29(60mg,0.192mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷
却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
18h18
n3o[m]
+
的计算值:292.1444;实测值:292.1481。
[0278][0279]
方案:lgw14-57的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0280]
n-(7-(氮杂环丁烷-1-基)-3h-吩噁嗪-3-亚基)-n-甲基甲铵(lgw14-57):将化合物14(30mg,0.201mmol)和2(34mg,0.201mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
17h18
n3o[m]
+
的计算值:280.1444;实测值:280.1491。
[0281][0282]
方案:lgw14-61的合成路线。试剂和条件:a)i)1,4-二氯丁烷,甲苯,回流;ii)et3n,na2co3,回流;b)6m hcl,nano2,0℃;c)化合物1,ppse,cf3ch2oh,80℃。
[0283]
3-(吡咯烷-1-基)苯酚(31):按照由高尚(ghashang)报告的方案9,向化合物30(5.00g,45.82mmol)于无水甲苯中的悬浮液中添加1,4-二氯丁烷(5.52ml,50.4mmol)。将反应混合物回流24小时,然后冷却到室温。一旦冷却,就将含et3n(9.58ml,68.7mmol)和na2co3(4.86g,45.8mmol)的10ml di水添加到反应烧瓶中。将所得反应混合物回流另外24小时。一旦反应完成,就在减压下去除有机溶剂,并且用dcm(3
×
100ml)萃取水相。将合并的有机层用盐水冲洗,经无水na2so4干燥,并且使用旋转蒸发器去除溶剂。将残留物通过利用硅胶的快速柱色谱法,使用dcm/己烷作为洗脱液来进行纯化,以得到呈浅灰色固体的化合物31(5.37g,72%)。
[0284]
2-亚硝基-5-(吡咯烷-1-基)苯酚(32):将化合物31(400mg,2.45mmol)溶解在冰冷的6m hcl溶液(4ml)中。在1小时内向所述溶液中分批添加nano2(178mg,2.57mmol),同时将溶液的温度保持低于5℃,使得未观察到棕色nox蒸气。将反应混合物搅拌另外的2小时。之后,将沉淀物通过布赫纳漏斗过滤并用小部分冰冷的2m hcl溶液洗涤。将产物留在漏斗中并风干过夜,以提供呈亮黄色固体的化合物32(0.403g,86%),所述化合物在不进一步纯化的情况下用于下一步骤。
[0285]
1-(7-(二甲氨基)-3h-吩噁嗪-3-亚基)吡咯烷-1-正离子(lgw14-61):将化合物1(30mg,0.219mmol)和32(42mg,0.219mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的
三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
18h20
n3o[m]
+
的计算值:294.1601;实测值:294.1622。
[0286][0287]
方案:lgw14-63的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0288]
1-(4-甲基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)吡咯烷-1-正离子(lgw14-63):将化合物31(30mg,0.184mmol)和21(61mg,0.184mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h20
n3o2[m]
+
的计算值:322.1550;实测值:322.1591。
[0289][0290]
方案:lgw14-72的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0291]
1-(7-(乙基(甲基)氨基)-3h-吩噁嗪-3-亚基)吡咯烷-1-正离子(lgw14-72):将化合物31(30mg,0.184mmol)和26(58mg,0.184mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h22
n3o[m]
+
的计算值:308.1757;实测值:308.1783。
[0292][0293]
方案:lgw14-76的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0294]
1-(4-乙基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)吡咯烷-1-正离子(lgw14-76):将化合物31(30mg,0.184mmol)和19(63mg,0.184mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
20h22
n3o2[m]
+
的计算值:336.1707;实测值:336.1753。
[0295][0296]
方案:lgw14-83的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0297]
1-(7-(吡咯烷-1-基)-3h-吩噁嗪-3-亚基)氮杂环丁烷-1-正离子(lgw14-83):将化合物14(30mg,0.201mmol)和32(39mg,0.201mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h20
n3o[m]
+
的计算值:306.1601;实测值:306.1627。
[0298][0299]
方案:lgw14-88的合成路线。试剂和条件:a)1m bbr3,dcm,0℃到室温;b)化合物26,ppse,cf3ch2oh,80℃。
[0300]
4-甲基-3,4-二氢-2h-苯并[b][1,4]噁嗪-6-醇(33):在n2下将化合物20(100mg,0.558mmol)溶解在无水dcm(5ml)中,并在冰浴中冷却。向上述溶液中滴加bbr3(dcm中1m,2ml,1.95mmol)。将反应混合物缓慢温热到室温并搅拌过夜。将反应烧瓶放置于冰浴中,在足够的冷却时间后,小心地向反应混合物中添加水以破坏过量的bbr3并用na2co3中和到ph为约7。然后用etoac(4
×
10ml)萃取水相。将合并的有机物经无水na2so4干燥,过滤并在真空下浓缩。利用硅胶的快速色谱法产生了呈深红色油状物的化合物33(61mg,66%)。
[0301]
(e)-n-甲基-n-(4-甲基-3,4-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-8(2h)-亚基)乙铵(lgw14-88):将化合物33(10mg,0.061mmol)和26(19mg,0.061mmol)溶解在含有多磷酸三甲基甲硅烷基酯(10μl)的三氟乙醇溶液(1ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
18h20
n3o2[m]
+
的计算值:310.1550;实测值:310.1578。
[0302][0303]
方案:lgw14-90的合成路线。试剂和条件:a)1m bbr3,dcm,0℃到室温;b)化合物26,ppse,cf3ch2oh,80℃。
[0304]
3-(乙基(甲基)氨基)苯酚(34):在n2下将化合物25(100mg,0.605mmol)溶解在无水dcm(5ml)中,并在冰浴中冷却。向上述溶液中滴加bbr3(dcm中1m,2.2ml,2.12mmol)。将反应混合物缓慢温热到室温并搅拌过夜。将反应烧瓶放置于冰浴中,在足够的冷却时间后,小心地向反应混合物中添加水以破坏过量的bbr3并用na2co3中和到ph为约7。然后用etoac(4
×
10ml)萃取水相。将合并的有机物经无水na2so4干燥,过滤并在真空下浓缩。利用硅胶的快速色谱法产生了呈透明油状物的化合物34(75mg,82%)。
[0305]
(e)-n-(7-(乙基(甲基)氨基)-3h-吩噁嗪-3-亚基)-n-甲基乙铵(lgw14-90):将化合物34(30mg,0.198mmol)和26(62mg,0.198mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
18h22
n3o[m]
+
的计算值:296.1757;实测值:296.1800。
[0306][0307]
方案:lgw14-92的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0308]
4,8-二甲基-3,8,9,10-四氢-2h-双([1,4]噁嗪并)[2,3-b:3',2'-i]吩噁嗪-4-正离子(lgw14-92):将化合物33(10mg,0.061mmol)和21(20mg,0.061mmol)溶解在含有多磷酸三甲基甲硅烷基酯(10μl)的三氟乙醇溶液(1ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
18h18
n3o3[m]
+
的计算值:324.1343,实测值:324.1361。
[0309][0310]
方案:lgw14-95的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0311]
4-乙基-8-甲基-3,8,9,10-四氢-2h-双([1,4]噁嗪并)[2,3-b:3',2'-i]吩噁嗪-4-正离子(lgw14-95):将化合物33(10mg,0.061mmol)和19(21mg,0.061mmol)溶解在含有多磷酸三甲基甲硅烷基酯(10μl)的三氟乙醇溶液(1ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h20
n3o3[m]
+
的计算值:338.1499;实测值:338.1529。
[0312][0313]
方案:lgw14-98的合成路线。试剂和条件:a)ppse,cf3ch2oh,80℃。
[0314]
4-乙基-8-(乙基(甲基)氨基)-2,3-二氢-[1,4]噁嗪并[2,3-b]吩噁嗪-4-正离子(lgw14-98):将化合物34(30mg,0.198mmol)和19(68mg,0.198mmol)溶解在含有多磷酸三甲基甲硅烷基酯(30μl)的三氟乙醇溶液(3ml)中。将反应混合物加热到80℃并搅拌过夜。然后将其冷却到室温并在真空下去除溶剂。将残留物通过硅胶快速色谱法,使用含有1%甲酸的chcl3和meoh的流动相(梯度,2-15%的meoh/chcl3)来进行纯化。ms(esi):c
19h22
n3o2[m]
+
的
计算值:324.1707;实测值:324.1722。
[0315]
噁嗪衍生物文库的hplc-ms表征。hplc-ms用于通过对254nm下的吸光度(左)和正离子模式下的质荷比(m/z)(右)进行曲线下面积(auc)分析来量化每种噁嗪衍生物的纯度。将样品(5μl)注射到c18柱(poroshell 120,2.1
×
50mm,2.7微米)中,并用a(h2o,0.1%甲酸)和b(乙腈,0.1%甲酸)的溶剂体系以0.4毫升/分钟洗脱,在6分钟内从a/b=95/5到5/95,在a/b=5/95下维持另外的2分钟。通过将毛细管电压设置为4kv并将气体温度设置为350℃,在正离子模式下检测离子。确定lgw-76的纯度为97%,并且lgw-13-79、lgw14-42、lgw14-47、lgw14-51、lgw14-53和lgw14-83的纯度》99%。
[0316][0317]
图1a到1f表示pbs中噁嗪衍生物的归一化的吸收和荧光发射光谱。化合物lgw14-42和lgw14-27都在nir中吸收并且发射,而其它化合物仅在nir中发射。在7种筛选的候选化合物中,lgw14-42是最大红移的荧光团。
[0318]
图2-体内直接施用神经特异性筛选。a.将(共溶剂调配物中的125μm)直接施加到暴露的臂丛神经和坐骨神经之后nir噁嗪衍生物的代表性照片和荧光图像。所有图像都代表了每个荧光团的针对n=6个神经位点所收集的数据。b.与未经染色的对照组相比,量化每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度。c.针对筛选的噁嗪衍生物与未经染色的对照组之间的比较所计算的量化的神经sbr。所有量化的数据呈现为平均值
±
标准偏差。
[0319]
图3-nir神经特异性候选物lgw03-76的药代动力学研究。a.全身施用之后0.5小时、1小时、2小时和4小时时间点处nir神经特异性候选物lgw03-76的代表性照片和荧光图像。b.量化每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度并将其与对照组织自体荧光进行比较。c.针对lgw03-76与对照组织自体荧光之间的比较所计算的量化的神经sbr。所有量化的数据呈现为平均值
±
标准偏差。
[0320]
图4-nir神经特异性候选物lgw13-79的药代动力学研究。a.全身施用之后0.5小时、1小时、2小时和4小时时间点处nir神经特异性候选物lgw13-79的代表性照片和荧光图像。b.量化每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度并将其与对照组织自体荧光进行比较。c.针对lgw13-79与对照组织自体荧光之间的比较所计算的量化的神经sbr。所有量化的数据呈现为平均值
±
标准偏差。
[0321]
图5-nir神经特异性候选物lgw14-42的药代动力学研究。a.全身施用之后0.5小时、1小时、2小时和4小时时间点处nir神经特异性候选物lgw14-42的代表性照片和荧光图
像。b.量化每秒平均神经(白色)、肌肉(黑色)和脂肪(灰色)组织强度并将其与对照组织自体荧光进行比较。c.针对lgw14-42与对照组织自体荧光之间的比较所计算的量化的神经sbr。所有量化的数据呈现为平均值
±
标准偏差。
[0322]
实验性logd测量。将每种筛选候选物以10mm的浓度溶解在dmso中。对储备溶液进行取样(2μl)并且将其添加到1-辛醇和pbs缓冲液(等体积)的1ml混合物中。然后将所述溶液在室温下涡旋30分钟,然后以13,000rpm离心5分钟。将pbs缓冲液和1-辛醇层分离,并且使用具有微板读数器的spectramax m5光谱仪(加利福尼亚州桑尼维尔分子装置公司(molecular devices,sunnyvale,ca))测量吸光度。然后使用吸光度与浓度的比尔定律(beer's law)绘图来计算每个相中的样品浓度。使用以下等式计算每种筛选候选物的实验性logd值。
[0323][0324]
参考文献
[0325]
1.查斯,b.(chance,b.)使用连续、相位调制和脉冲光与血液和血液氧合的量化的近红外图像(near-infrared images using continuous,phase-modulated,and pulsed light with quantitation of blood and blood oxygenation).纽约科学院年报(annals of the new york academy of sciences)838,29-45(1998)。
[0326]
2.瓦尔迈杰,a.l.(vahrmeijer,a.l.),赫特曼,m.(hutteman,m.),范德沃斯特,j.r.(van der vorst,j.r.),范德维尔德,c.j.(van de velde,c.j.)和弗兰吉奥尼,j.v.(frangioni,j.v.)使用近红外荧光的图像导引癌症外科手术(image-guided cancer surgery using near-infrared fluorescence).自然评论:临床肿瘤学10,507-518(2013)。
[0327]
3.弗兰吉奥尼,j.v.体内近红外荧光成像(in vivo near-infrared fluorescence imaging).化学生物学新见(current opinion in chemical biology)7,626-634(2003)。
[0328]
4.吉布斯,s.l.(gibbs,s.l.)用于图像导引外科手术的近红外荧光(near infrared fluorescence for image-guided surgery).医学和外科手术中的定量成像2,177-187(2012)。
[0329]
5.惠特尼,m.a.(whitney,m.a.)等人荧光肽在小鼠外科手术期间突出显示外周神经(fluorescent peptides highlight peripheral nerves during surgery in mice).自然生物技术(nature biotechnology)29,352-356(2011)。
[0330]
6.吴,c.(wu,c.)等人用于对cns中有髓鞘白质进行成像的分子探针(molecular probes for imaging myelinated white matter in cns).医药化学杂志51,6682-6688(2008)。
[0331]
7.王,c.(wang,c.)等人髓鞘形成的原位荧光成像(in situ fluorescence imaging of myelination).组织化学与细胞化学杂志:组织化学学会官方杂志58,611-621(2010)。
[0332]
8.斯坦科夫,b.(stankoff,b.)等人通过正电子发射断层扫描对cns髓鞘进行成像(imaging of cns myelin by positron-emission tomography).美国国家科学院院刊
103,9304-9309(2006)。
[0333]
9.科特罗,v.e.(cotero,v.e.)等人通过髓鞘选择性造影剂对外周和中枢神经进行术中荧光成像(intraoperative fluorescence imaging of peripheral and central nerves through a myelin-selective contrast agent).分子成像与生物学:mib:分子成像学会官方出版物14,708-717(2012)。
[0334]
10.吉布斯,s.l.等人突出显示神经的荧光团的构效关系(structure-activity relationship of nerve-highlighting fluorophores).公共科学图书馆综合8,e73493(2013)。
[0335]
11.吉布斯-斯特劳斯,s.l.(gibbs-strauss,s.l.)等人用于图像导引外科手术的突出显示神经的荧光造影剂(nerve-highlighting fluorescent contrast agents for image-guided surgery).分子成像10,91-101(2011)。
[0336]
12.梅耶斯,j.r.(meyers,j.r.)等人点亮感官:fm1-43通过非选择性离子通道加载感觉细胞(lighting up the senses:fm1-43 loading of sensory cells through nonselective ion channels).神经科学杂志:神经科学学会官方杂志23,4054-4065(2003)。
[0337]
13.吉布斯-斯特劳斯,s.l.等人对椎间盘的纤维环具有特异性的分子成像剂(molecular imaging agents specific for the annulus fibrosus of the intervertebral disk).分子成像9,128-140(2010)。
[0338]
14.帕克,m.h.(park,m.h.)等人原型神经特异性近红外荧光团(prototype nerve-specific near-infrared fluorophores).治疗诊断学4,823-833(2014)。
[0339]
15.王,c.(wang,c.)等人髓鞘形成的纵向近红外成像(longitudinal near-infrared imaging of myelination).神经科学杂志:神经科学学会官方杂志31,2382-2390(2011)。
[0340]
16.巴斯,c.w.(barth,c.w.)和吉布斯,s.l.直接施用神经特异性造影剂以改善保留神经的根治性前列腺切除术(direct administration of nerve-specific contrast to improve nerve sparing radical prostatectomy).治疗诊断学7,573-593(2017)。
[0341]
17.高尚,m.(ghashang,m.)作为高效催化剂用于新型4h-色烯-3-甲腈的多组分、一锅法、水性介质制备的znal2o4
–
bi2o3复合纳米粉末(znal2o4
–
bi2o3 composite nano-powder as an efficient catalyst for the multi-component,one-pot,aqueous media preparation of novel 4h-chromene-3-carbonitriles).化学中间体研究(research on chemical intermediates)42,4191-4205(2016)。
[0342]
18.格里姆,j.b.(grimm,j.b.)等人用于改进活细胞和单分子显微术的荧光团的一般方法(a general method to improve fluorophores for live-cell and single-molecule microscopy).自然方法(nat methods)12,244-250,250之后243页(2015)。
[0343]
19.张,h.(zhang,h.)等人具有双重抗增殖和抗血管生成活性的强效微管抑制剂的设计、合成和表征(design,synthesis and characterization of potent microtubule inhibitors with dual anti-proliferative and anti-angiogenic activities).欧洲医药化学杂志(european journal of medicinal chemistry)157,380-396(2018)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1