适用于治疗的脂质体RNA制剂的制备和储存的制作方法
本公开内容涉及用于制备用于在肠胃外施用之后(特别是在静脉内施用之后)将rna递送至靶组织的rna lipoplex颗粒的方法,以及包含这样的rna lipoplex颗粒的组合物。本公开内容还涉及允许以符合工业gmp的方式制备rna lipoplex颗粒的方法。此外,本公开内容涉及用于储存rna lipoplex颗粒而基本上不损失产品品质,并且特别是基本上不损失rna活性的方法和组合物。本文中所述的rna lipoplex颗粒制剂可通过冷冻干燥、喷雾干燥或相关方法冷冻或脱水,使得能够获得与液体储存相比延长的产品货架期(shelf-life)。在一个实施方案中,rna lipoplex颗粒包含单链rna,例如编码目的肽或蛋白质(例如药物活性肽或蛋白质)的mrna。rna被靶组织的细胞吸收,并且rna被翻译成可表现出其生理活性的编码的肽或蛋白质。目的肽或蛋白质可以是包含一个或更多个表位的肽或蛋白质,以用于诱导或增强针对所述一个或更多个表位的免疫应答。本文中所述的方法和组合物适合于以符合药物产品的要求,更具体地,符合gmp制造的要求和用于肠胃外施加的药物产品的品质的要求的方式使用。
背景技术:
1、使用rna将外来遗传信息递送到靶细胞中提供了dna的有吸引力的替代方案。使用rna的优点包括瞬时表达和非转化特征。rna不需要进入细胞核以进行表达,并且此外,rna不会整合到宿主基因组中,从而消除肿瘤发生的风险。
2、rna可通过所谓的lipoplex制剂递送,其中rna与由阳离子脂质与辅助脂质(helper lipid)的混合物构成的脂质体结合以形成可注射的纳米颗粒制剂。然而,即使在制剂的储存之后,用于将生物活性rna递送至靶组织的制剂的开发是未满足的需求。另外,用于符合gmp来制造可注射rna lipoplex颗粒制剂的提供长货架期的方法的开发仍是未满足的需求。
3、因此,需要提供用于将生物活性rna递送至靶组织的制剂,其中所递送的rna被有效地翻译成其编码的肽或蛋白质。此外,需要提供这样的制剂,其是货架稳定的基本上不损失产品品质,并且特别是基本上不损失rna的生物学活性。
4、本发明人出人意料地发现,本文中所述的rna lipoplex颗粒制剂满足上述要求。
技术实现思路
1、i.用于制备rna lipoplex颗粒的方法、rna lipoplex颗粒和包含rna lipoplex颗粒的组合物
2、在第一方面,本公开内容涉及用于制备具有改善的生物学活性的rna lipoplex颗粒的方法、根据本公开内容制备的rna lipoplex颗粒以及包含这样的rna lipoplex颗粒的组合物。rna lipoplex颗粒和包含rna lipoplex颗粒的组合物可用于在肠胃外施用之后,特别是在静脉内施用之后将rna递送至靶组织。rna lipoplex颗粒使用通过将在乙醇中的高度浓缩的脂质溶液注入到水或合适的水相中而获得的脂质体来制备。在一个实施方案中,rna lipoplex产物的特征在于x射线散射中的特定模式,其中观察到在约1nm-1处的单个布拉格峰(bragg peak),其中峰宽小于0.2nm-1。
3、在一个实施方案中,脂质体和rna lipoplex颗粒包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。脂质混合物中dope的浓度高于单独的乙醇中dope的平衡溶解度。在室温下,dope单独具有约50mm的溶解度,与dotma一起其则具有100mm或更高的溶解度。形成从中获得高活性lipoplex的脂质体的脂质溶液可具有270mm或更高的总脂质浓度(例如,90mm或更高的dope)。通过提高温度可获得乙醇中甚至更高浓度的溶液。从其中dope的浓度高于平衡溶解度的脂质溶液获得的脂质体显著大于来自其中dope的浓度处于平衡溶解度和以下的脂质溶液的脂质体。脂质体尺寸随在乙醇中的浓度而单调提高。
4、根据本公开内容制备的脂质体可通过将该脂质体与rna混合而用于制备rnalipoplex颗粒。在一个实施方案中,在混合之前将rna与nacl一起孵育以调整lipoplex的活性提高所需的特定离子强度。由这些较大的脂质体形成的lipoplex具有显著更高的生物学活性,如通过体外和体内实验所证明的。可通过某些物理化学参数将这些具有较高活性的lipoplex与具有较低活性的那些清楚地区分开,所述物理化学参数例如(i)较低的布拉格峰峰宽,以及(ii)在用于尺寸测量的分散分析方法,如场-流分级(field-flowfractionation)中的不同分离谱。具有较低活性的lipoplex平均更小。另外,它们还具有不同的洗脱曲线,这可能与参数如分子构象、形状以及与本体相(bulk phase)的相互作用相关。
5、因此,在这个方面,本公开内容涉及产生脂质体胶体的方法,其包括将在乙醇中的脂质溶液注入到水相中以产生脂质体胶体,其中所述脂质溶液中至少一种脂质的浓度对应于或高于所述至少一种脂质在乙醇中的平衡溶解度。
6、在一个实施方案中,所述方法包括将脂质溶液加热以提高脂质溶液中脂质的浓度。在一个实施方案中,将脂质溶液加热至至少约40℃或至少约60℃的温度。
7、在一个实施方案中,脂质溶液是两种或更多种不同脂质的混合物的溶液。
8、在一个实施方案中,脂质溶液中一种脂质的浓度对应于或高于脂质在乙醇中的平衡溶解度。
9、在一个实施方案中,脂质溶液中的总脂质浓度为约180mm至约600mm、约300mm至约600mm,或约330mm。
10、在一个实施方案中,脂质溶液包含至少一种阳离子脂质和至少一种另外的脂质。
11、在一个实施方案中,脂质溶液中的另外的脂质的浓度对应于或高于所述另外的脂质在乙醇中的平衡溶解度。
12、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
13、在一个实施方案中,所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
14、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
15、在一个实施方案中,所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
16、在一个实施方案中,脂质溶液包含摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope。
17、在一个实施方案中,脂质溶液中dope的浓度为至少约60mm或至少约90mm。
18、在一个实施方案中,将脂质溶液注入到约50rpm至约150rpm的水相搅拌速度的水相中。
19、在一个实施方案中,水相是水。
20、在一个实施方案中,水相具有酸性ph。在一个实施方案中,水相包含例如量为约5mm的乙酸。
21、在一个实施方案中,所述方法还包括搅拌脂质体胶体。
22、在一个实施方案中,将脂质体胶体搅拌约15分钟至约60分钟,或搅拌约30分钟。
23、本公开内容还涉及产生脂质体胶体的方法,所述方法包括将在乙醇中包含摩尔比为约2∶1的dotma和dope的脂质溶液注入到以约150rpm的搅拌速度搅拌的水中以产生脂质体胶体,其中在所述脂质溶液中dotma和dope的浓度为约330mm。
24、在一个实施方案中,产生脂质体的方法不包括将脂质体挤出的步骤。
25、本公开内容还涉及可通过产生脂质体的方法获得的脂质体胶体。
26、在一个实施方案中,脂质体的平均直径为至少约250nm。
27、在一个实施方案中,脂质体的平均直径为约250nm至约800nm。
28、在一个实施方案中,脂质体具有小于约0.5、小于约0.4,或小于约0.3的多分散性指数。
29、在一个实施方案中,脂质体是阳离子脂质体。
30、在一个实施方案中,脂质体包含至少一种阳离子脂质和至少一种另外的脂质。
31、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
32、在一个实施方案中,所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
33、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
34、在一个实施方案中,所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
35、在一个实施方案中,脂质体包含摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope。
36、本公开内容还涉及制备rna lipoplex颗粒的方法,所述方法包括将上述脂质体胶体添加至包含rna的溶液。
37、在一个实施方案中,在x射线散射模式中,rna lipoplex的特征在于在约1nm-1处的单个布拉格峰,其中峰宽小于0.2nm-1。
38、在一个实施方案中,rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
39、本公开内容还涉及包含rna lipoplex颗粒的组合物,所述rna lipoplex颗粒可如上所述获得。
40、在一个实施方案中,rna lipoplex颗粒包含至少一种阳离子脂质和至少一种另外的脂质。
41、在一个实施方案中,rna编码包含至少一个表位的肽或蛋白质,其中所述rnalipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
42、本公开内容还涉及组合物,其包含:
43、rna lipoplex颗粒,其包含:
44、编码包含至少一个表位的肽或蛋白质的rna,以及
45、至少一种阳离子脂质和至少一种另外的脂质,
46、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0,并且
47、其中所述rna lipoplex颗粒的特征在于在约1nm-1处的单个布拉格峰,其中峰宽小于0.2nm-1。
48、在一个实施方案中,所述组合物还包含浓度为约10mm至约300mm、约45mm至约300mm、约10mm至约50mm,或约80mm至约150mm的氯化钠。
49、在一个实施方案中,所述组合物还包含缓冲剂。
50、在一个实施方案中,所述组合物还包含螯合剂。
51、在一个实施方案中,在i.下的该方面中所述的rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
52、在一个实施方案中,rna lipoplex颗粒具有小于约0.5、小于约0.4,或小于约0.3的多分散性指数。
53、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
54、在一个实施方案中,所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
55、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
56、在一个实施方案中,所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
57、在一个实施方案中,rna lipoplex颗粒包含摩尔比为约10∶0至1∶9、约4∶1至1∶2、约3∶1至约1:1、或约2∶1的dotma和dope,并且其中dotma中正电荷与rna中负电荷的电荷比为约1∶2至1.9∶2。
58、在一个实施方案中,螯合剂是乙二胺四乙酸(edta)。
59、在一个实施方案中,edta的浓度为约0.25mm至约5mm,或约2.5mm。
60、在一个实施方案中,组合物还包含辅料。
61、在一个实施方案中,组合物配制成用于全身性施用。
62、在一个实施方案中,全身性施用是通过静脉内施用。
63、本公开内容还涉及用于治疗用途的如前所述的组合物。
64、ii.用于以符合工业gmp的方式制备rna lipoplex颗粒的方法
65、在第二方面,本公开内容涉及允许以符合工业gmp的方式制备rna lipoplex颗粒的方法。
66、在本公开内容的一个实施方案中,将流体路径(fluid path)系统用于药物rnalipoplex颗粒产品的gmp制造,这使得能够精确控制rna与脂质体的混合比,这对于产品品质是重要的。在一个实施方案中,流体路径包括以1∶1(体积/体积)的方式将脂质体溶液与rna溶液混合,其中选择组分的浓度以精确地维持期望的电荷比。在一个实施方案中,在混合之前将rna与nacl一起孵育以调整lipoplex的活性所需的特定离子强度。在一个实施方案中,实现了y型混合设置,其完全基于单一使用材料。使流体动力学最优化以维持颗粒特征并避免堵塞。相反,当使用市售微流体装置时,在一段时间后会发生堵塞,这使得gmp的应用变得不可能。
67、在一个实施方案中,通过将rna与阳离子脂质体一起孵育来制造lipoplex,其中通过使用注射器泵(灌注泵)精确地控制混合比和混合条件,其中将两个注射器(一个包含脂质体并且一个包含rna)插入注射器泵中,优先地平行地插入到同一泵中。两个泵的活塞由同一驱动器向前移动,从而精确地控制了所混合的相对体积。在选定的工艺条件下,这两种溶液均使用相同的注射器,由此使实现精确的一对一(v/v)混合条件。通过在混合之前调整两种溶液的浓度,即可精确控制rna与脂质体(阳离子脂质)之间的比。
68、因此,在这个方面,本公开内容涉及用于连续流制造rna lipoplex颗粒的方法,其包括在rna和阳离子脂质体的受控混合条件下将包含rna的溶液与包含阳离子脂质体的溶液混合。
69、在一个实施方案中,包含阳离子脂质体的溶液是如上所述的脂质体胶体。
70、在一个实施方案中,包含rna的溶液和包含阳离子脂质体的溶液是水性溶液。
71、在一个实施方案中,使用允许包含rna的溶液与包含阳离子脂质体的溶液混合的流量(flow rate)。
72、在一个实施方案中,所述流的特征在于雷诺数大于300,或约500至约2100。
73、在一个实施方案中,所述受控混合条件包括控制包含rna的溶液与包含阳离子脂质体的溶液的混合比。
74、在一个实施方案中,所述受控混合条件包括控制待混合的包含rna的溶液与包含阳离子脂质体的溶液的相对体积。
75、在一个实施方案中,通过使用相同混合体积(v/v)的包含rna的溶液和包含阳离子脂质体的溶液以及调整相应溶液中rna和阳离子脂质体的浓度来控制rna与阳离子脂质体的混合比。
76、在一个实施方案中,选择所述受控混合条件以在避免堵塞的同时维持rnalipoplex颗粒的特征。
77、在一个实施方案中,所述方法包括使用y型或t型混合元件。
78、在一个实施方案中,y型或t型混合元件的直径为约1.2mm至约50mm。
79、在一个实施方案中,所述方法包括使用混合元件,例如y型或t型混合元件,其中将来自两个管或软管的流体放在一起,并且其中不存在内部静态混合元件如例如裂缝,以及重组、交错的人字形、之字形或扭曲的通道,或者三维蛇纹石(serpentine)。混合元件的直径可为1.2至50.0mm。
80、在一个实施方案中,所述方法包括使用装置,其中将两个注射器(一个包含所述包含阳离子脂质体的溶液并且一个包含所述包含rna的溶液)平行地插入到同一或两个保持物中,并且所述装置的活塞通过一个或两个精密致动器(actuator)伸出。在一个实施方案中,所述方法包括使用注射器泵,其中将两个注射器平行地插入到同一泵中,所述两个注射器一个包含所述包含阳离子脂质体的溶液并且一个包含所述包含rna的溶液。
81、在一个实施方案中,所述方法包括将压力容器、膜泵、齿轮泵、磁悬浮泵、蠕动泵、hplc/fplc泵或任何其他活塞泵任选地与流量传感器组合使用,所述流量传感器任选地具有用于在线控制和实时调整流量的反馈回路。
82、在一个实施方案中,包含rna的溶液与包含脂质体的溶液的混合物包含浓度为约45mm至约300mm的氯化钠,或包含对应于浓度为约45mm至约300mm的氯化钠的离子强度。
83、在一个实施方案中,rna溶液包含浓度为约90mm至约600mm的氯化钠,或包含对应于浓度为约90mm至约600mm的氯化钠的离子强度。
84、在一个实施方案中,包含rna的溶液与包含脂质体的溶液的混合物具有至少约50mm的离子强度。
85、在一个实施方案中,在x射线散射模式中,rna lipoplex的特征在于在约1nm-1处的单个布拉格峰,其中峰宽小于0.2nm-1。
86、在一个实施方案中,rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
87、本公开内容还涉及包含rna lipoplex颗粒的组合物,所述rna lipoplex颗粒可如上所述获得。
88、在一个实施方案中,rna lipoplex颗粒包含至少一种阳离子脂质和至少一种另外的脂质。
89、在一个实施方案中,rna编码包含至少一个表位的肽或蛋白质,其中所述rnalipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
90、本公开内容还涉及组合物,其包含:
91、rna lipoplex颗粒,其包含:
92、编码包含至少一个表位的肽或蛋白质的rna,以及
93、至少一种阳离子脂质和至少一种另外的脂质,
94、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0,并且
95、其中rna lipoplex颗粒的特征在于在约1nm-1处的单个布拉格峰,其中峰宽小于0.2nm-1。
96、在一个实施方案中,组合物还包含浓度为约10至约300mm、约45mm至约300mm、约10mm至约50mm,或约80mm至约150mm的氯化钠。
97、在一个实施方案中,组合物还包含缓冲剂。
98、在一个实施方案中,组合物还包含螯合剂。
99、在一个实施方案中,在ii.下的该方面中所述的rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
100、在一个实施方案中,rna lipoplex颗粒具有小于约0.5、小于约0.4,或小于约0.3的多分散性指数。
101、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
102、在一个实施方案中,所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
103、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
104、在一个实施方案中,所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
105、在一个实施方案中,rna lipoplex颗粒包含摩尔比为约10∶0至1∶9、约4∶1至1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope,并且其中dotma中正电荷与rna中负电荷的电荷比为约1∶2至1.9∶2。
106、在一个实施方案中,螯合剂是乙二胺四乙酸(edta)。
107、在一个实施方案中,edta的浓度为约0.25mm至约5mm,或约2.5mm。
108、在一个实施方案中,组合物还包含辅料。
109、在一个实施方案中,组合物配制成用于全身性施用。
110、在一个实施方案中,全身性施用是通过静脉内施用。
111、本公开内容还涉及用于治疗用途的如前所述的组合物。
112、iii.用于储存rna lipoplex颗粒的方法和组合物
113、在第三方面,本公开内容涉及用于储存rna lipoplex颗粒而基本上不损失产品品质,并且特别是基本上不损失rna活性的方法和组合物。特别地,本公开内容涉及允许rnalipoplex颗粒的冷冻、冻干或喷雾干燥而基本上不损失rna lipoplex颗粒的品质,并且特别是基本上不损失rna活性的制剂。
114、本文中所述的rna lipoplex颗粒制剂可通过冷冻干燥、喷雾干燥或相关方法冷冻或脱水,使得能够获得与液体储存相比延长的产品货架期。
115、为了使得能够冷冻,添加了稳定剂(冷冻保护剂)。在一个实施方案中,在制造之后,用稳定剂(冷冻保护剂)对lipoplex进行稀释,从而使得能够调整离子强度,优先降低离子强度并调整稳定剂的适当浓度。为了冷冻产品,稳定剂浓度可高于获得生理渗量浓度(osmolality)的值。在那种情况下,为了施用,将产品用合适的水相(例如注射用水、盐水)稀释以调整期望的渗量浓度和离子强度。可使用糖如葡萄糖、蔗糖或海藻糖作为稳定剂,还可使用其他化合物如葡聚糖作为稳定剂。
116、出乎意料的是,根据本公开内容发现,包含如本文中所述的稳定剂的rnalipoplex制剂也可被冻干。对于冻干,所需的稳定剂(冷冻保护剂)浓度可低于冷冻所需的浓度,并且耐受的nacl浓度(离子强度)可高于冷冻所需的浓度。如果需要大规模的经济脱水,也可将产品喷雾干燥。
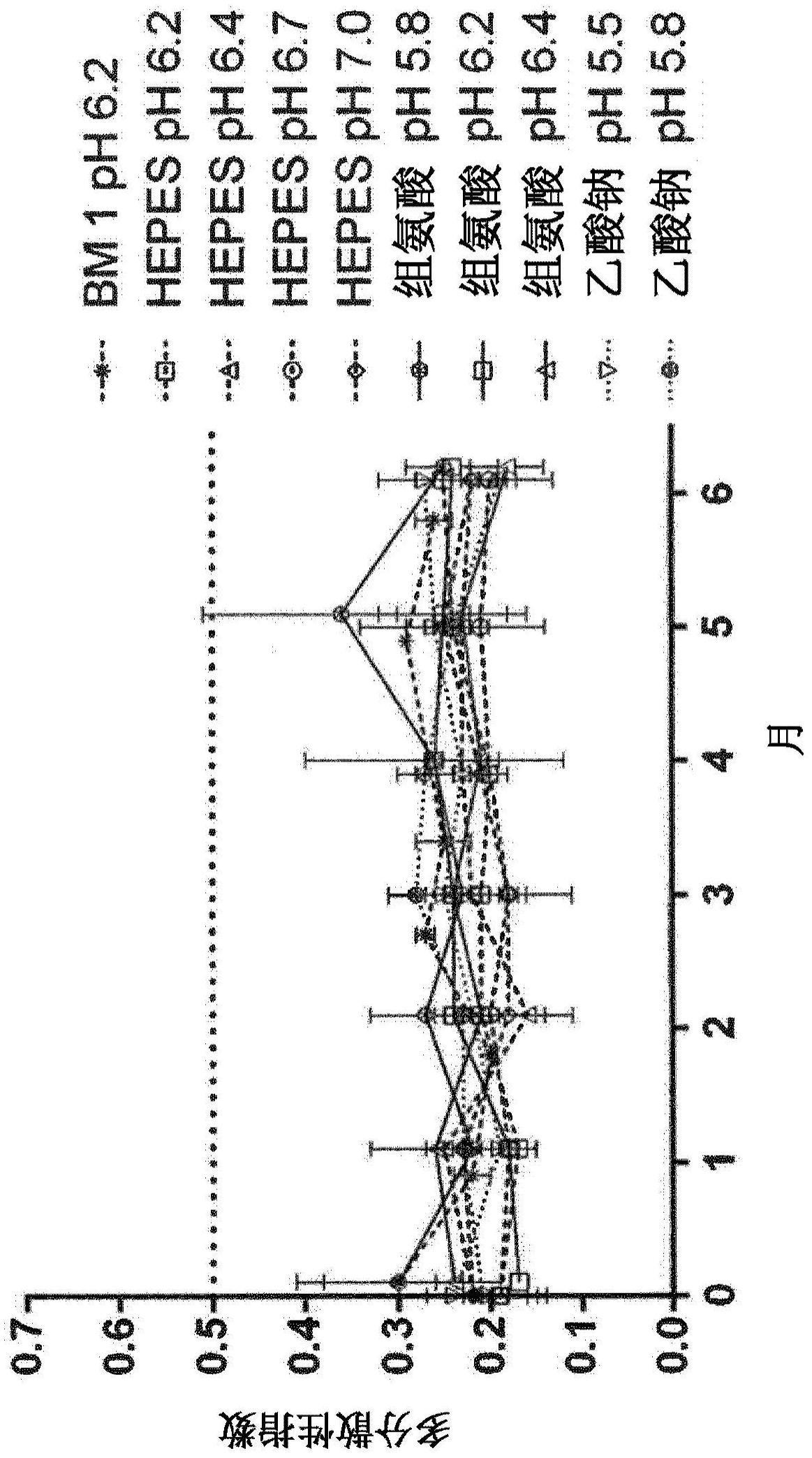
117、将一些rna lipoplex制剂的ph调整至低于通常的生理范围和在本体相(bulkphase)中通常对于rna储存而言最佳的ph的值。最佳ph为约6.2,合适的范围为约5.7至约6.7。对于其他制剂,理想的ph可甚至更低。据推测,由于阳离子脂质的正电荷,rnalipoplex内部的局部ph高于本体相ph。
118、在其中将rna lipoplex组合物冷冻用于储存的本公开内容的那些实施方案中,可将组合物解冻,并且任选地,可通过添加水性液体来调整组合物的渗量浓度、离子强度和/或ph。所得组合物可施用于对象。
119、在其中将rna lipoplex组合物冻干或冷冻干燥用于储存的本公开内容的那些实施方案中,可通过添加水性液体来使组合物重构,并且任选地,可通过添加水性液体来调整组合物的渗量浓度、离子强度和/或ph。所得组合物可施用于对象。
120、因此,在这个方面,本公开内容涉及制备包含rna lipoplex颗粒的冷冻组合物的方法,其包括(i)提供包含rna lipoplex颗粒和稳定剂的水性组合物,以及(ii)冷冻所述组合物。
121、在一个实施方案中,冷冻在约-15℃至约-40℃,或在约-30℃的温度下进行。
122、在一个实施方案中,组合物例如在约-15℃至约-40℃,或约-20℃的储存温度下储存。
123、在一个实施方案中,稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
124、在一个实施方案中,提供包含rna lipoplex颗粒和稳定剂的水性组合物包括提供包含rna lipoplex颗粒的水性组合物并向所述包含rna lipoplex颗粒的水性组合物添加所述稳定剂。因此,制备用于冷冻的组合物的方法包括提供包含rna lipoplex颗粒的水性组合物,并向所述包含rna lipoplex颗粒的水性组合物添加稳定剂。
125、在一个实施方案中,向包含rna lipoplex颗粒的水性组合物添加稳定剂降低了所述包含rna lipoplex颗粒的水性组合物的离子强度。
126、在一个实施方案中,在包含rna lipoplex颗粒和稳定剂的水性组合物中稳定剂的浓度高于生理渗量浓度所需的值。
127、在一个实施方案中,在包含rna lipoplex和稳定剂的水性组合物中稳定剂的浓度足以维持rna lipoplex颗粒的品质,并且特别地避免在将所述组合物在约-15℃至约-40℃的温度下储存至少一个月、至少6个月、至少12个月、至少24个月,或至少36个月之后rna活性的实质性损失。
128、在一个实施方案中,在包含rna lipoplex和稳定剂的水性组合物中稳定剂的浓度为约5%至约35.0%(w/v)、约10%至约30.0%(w/v)、约12.5%至约25.0%(w/v),或约22.0%(w/v)。
129、在一个实施方案中,包含rna lipoplex和稳定剂的水性组合物中的ph低于通常对于rna储存而言最佳的ph。
130、在一个实施方案中,包含rna lipoplex和稳定剂的水性组合物包含浓度为约10mm至约50mm的氯化钠,或包含对应于浓度为约10mm至约50mm的氯化钠的离子强度。
131、在一个实施方案中,包含rna lipoplex和稳定剂的水性组合物具有对应于浓度为约20mm的氯化钠的离子强度。
132、在一个实施方案中,rna lipoplex颗粒可通过如上在i.和ii.下所述的方法获得。
133、在一个实施方案中,制备冷冻组合物的方法还包括储存包含rna lipoplex颗粒的冷冻组合物。所述组合物可在对应于或基本对应于冷冻温度的温度或者高于或低于该冷冻温度的温度下储存。一般来说,组合物在约-15℃至约-40℃的温度下,例如在约-20℃下储存。
134、本公开内容还涉及包含rna lipoplex颗粒的组合物,其可通过上述制备冷冻组合物的方法获得。本公开内容还涉及包含rna lipoplex颗粒的组合物,其可通过上述制备用于冷冻的组合物的方法获得。
135、在一个实施方案中,rna lipoplex颗粒包含至少一种阳离子脂质和至少一种另外的脂质。
136、在一个实施方案中,rna编码包含至少一个表位的肽或蛋白质,其中所述rnalipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
137、在一个实施方案中,组合物还包含浓度为约10mm至约50mm的氯化钠。
138、本公开内容还涉及组合物,其包含:
139、rna lipoplex颗粒,其包含:
140、编码包含至少一个表位的肽或蛋白质的rna,
141、至少一种阳离子脂质和至少一种另外的脂质,
142、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0,
143、浓度为0mm至约40mm的氯化钠,以及
144、稳定剂。
145、在一个实施方案中,所述组合物还包含缓冲剂。
146、在一个实施方案中,所述组合物中rna的量为约0.01mg/ml至约1mg/ml、约0.05mg/ml至约0.5mg/ml,或约0.05mg/ml。
147、在一个实施方案中,氯化钠的浓度为约20mm至约30mm。
148、在一个实施方案中,氯化钠的浓度为约20mm。
149、在一个实施方案中,氯化钠的浓度为约30mm。
150、在一个实施方案中,所述组合物中稳定剂的浓度高于生理渗量浓度所需的值。
151、在一个实施方案中,所述组合物中稳定剂的浓度为约5至约35重量/体积百分比(%w/v),或约12.5至约25重量/体积百分比(%w/v)。
152、在一个实施方案中,稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
153、在一个实施方案中,稳定剂是蔗糖,其浓度为约5至约25重量/体积百分比(%w/v)。
154、在一个实施方案中,蔗糖的浓度为约15%(w/v)至约25%(w/v)。
155、在一个实施方案中,蔗糖的浓度为约20%(w/v)至约25%(w/v)。
156、在一个实施方案中,蔗糖的浓度为约22%(w/v)。
157、在一个实施方案中,蔗糖的浓度为约20%(w/v)。
158、在一个实施方案中,组合物的ph低于通常对于rna储存而言最佳的ph。
159、在一个实施方案中,组合物的ph为约5.7至约6.7,或约6.2。
160、在一个实施方案中,缓冲剂是2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)。
161、在一个实施方案中,hepes的浓度为约2.5mm至约10mm,或约7.5mm。
162、在一个实施方案中,组合物还包含螯合剂。
163、本公开内容还涉及组合物,其包含:
164、rna lipoplex颗粒,其包含:
165、编码包含至少一个表位的肽或蛋白质的rna,浓度为约0.05mg/ml,以及
166、摩尔比为约2∶1的dotma和dope,
167、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1.3∶2.0,
168、浓度为约20mm的氯化钠,
169、浓度为约22%(w/v)的蔗糖,
170、浓度为约7.5mm、ph为约6.2的hepes,以及
171、浓度为约2.5mm的edta。
172、在一个实施方案中,组合物为液体或冷冻状态。
173、在一个实施方案中,冷冻组合物在约-15℃至约-40℃的温度下至少一个月、至少6个月、至少12个月、至少24个月、或至少36个月保持稳定。
174、在一个实施方案中,冷冻组合物在约-15℃的温度下至少一个月、至少6个月、至少12个月、至少24个月、或至少36个月保持稳定。
175、在一个实施方案中,冷冻组合物在约-15℃的温度下至少两个月保持稳定。
176、在一个实施方案中,冷冻组合物在约-20℃的温度下至少一个月、至少6个月、至少12个月、至少24个月、或至少36个月保持稳定。
177、在一个实施方案中,冷冻组合物在约-20℃的温度下至少两个月保持稳定。
178、在一个实施方案中,冷冻组合物在约-30℃的温度下至少一个月、至少6个月、至少12个月、至少24个月、或至少36个月保持稳定。
179、在一个实施方案中,冷冻组合物在约-30℃的温度下至少两个月保持稳定。
180、本公开内容还涉及包含rna lipoplex颗粒的水性组合物,所述水性组合物可通过将上述冷冻组合物解冻,以及任选地通过添加水性液体来调整渗量浓度和离子强度来获得。
181、在一个实施方案中,组合物的渗量浓度为约200mosmol/kg至约450mosmol/kg。
182、在一个实施方案中,组合物包含浓度为约80mm至约150mm的氯化钠。
183、在一个实施方案中,rna lipoplex颗粒可通过如上在i.和ii.下所述的方法获得。
184、本公开内容还涉及制备包含rna lipoplex颗粒的脱水的(例如冻干或喷雾干燥的)组合物的方法,其包括(i)提供包含rna lipoplex颗粒和稳定剂的水性组合物,以及(ii)对所述组合物进行脱水例如冻干或喷雾干燥。
185、在一个实施方案中,稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
186、在一个实施方案中,提供包含rna lipoplex颗粒和稳定剂的水性组合物包括提供包含rna lipoplex颗粒的水性组合物并向所述包含rna lipoplex颗粒的水性组合物添加所述稳定剂。因此,制备用于脱水(例如冻干或喷雾干燥)的组合物的方法包括:提供包含rna lipoplex颗粒的水性组合物并向所述包含rna lipoplex颗粒的水性组合物添加稳定剂。
187、在一个实施方案中,向所述包含rna lipoplex颗粒的水性组合物添加稳定剂降低了所述包含rna lipoplex颗粒的水性组合物的离子强度。
188、在一个实施方案中,在包含rna lipoplex颗粒和稳定剂的水性组合物中稳定剂的浓度高于生理渗量浓度所需的值。
189、在一个实施方案中,在包含rna lipoplex和稳定剂的水性组合物中稳定剂的浓度足以维持rna lipoplex颗粒的品质,并且特别地避免在将所述组合物储存至少一个月、至少6个月、至少12个月、至少24个月,或至少36个月之后rna活性的实质性损失。
190、在一个实施方案中,包含rna lipoplex和稳定剂的水性组合物中稳定剂的浓度为约5%至约35.0%(w/v)、约10%至约30.0%(w/v)、约12.5%至约25.0%(w/v),或约22.0%(w/v)。
191、在一个实施方案中,包含rna lipoplex和稳定剂的水性组合物中的ph低于通常对于rna储存而言最佳的ph。
192、在一个实施方案中,包含rna lipoplex和稳定剂的水性组合物包含浓度为约10mm至约80mm,或约10mm至约50mm的氯化钠,或者包含对应于浓度为约10mm至约80mm,或约10mm至约50mm的氯化钠的离子强度。
193、在一个实施方案中,包含rna lipoplex和稳定剂的水性组合物具有对应于浓度为约20mm、约40mm、约60mm,或约80mm的氯化钠的离子强度。
194、在一个实施方案中,rna lipoplex颗粒可通过如上在i.和ii.下所述的方法获得。
195、在一个实施方案中,制备脱水的(例如冻干或喷雾干燥的)组合物的方法还包括储存包含rna lipoplex颗粒的冻干或喷雾干燥的组合物。一般来说,组合物在约-15℃至约-40℃的温度下,例如在约-20℃下储存。在某些实施方案中,组合物在高于0℃的温度下,例如在约25℃或约4℃下,或例如在室温下储存。
196、本公开内容还涉及包含rna lipoplex颗粒的组合物,其可通过上述制备脱水的(例如冻干或喷雾干燥的)组合物的方法获得。本公开内容还涉及包含rna lipoplex颗粒的组合物,其可通过上述制备用于脱水(例如冻干或喷雾干燥)的组合物的方法获得。
197、在一个实施方案中,rna lipoplex颗粒包含至少一种阳离子脂质和至少一种另外的脂质。
198、在一个实施方案中,rna编码包含至少一个表位的肽或蛋白质,其中所述rnalipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
199、在一个实施方案中,组合物还包含浓度为约10mm至约80mm或约10mm至约50mm的氯化钠。
200、本公开内容还涉及组合物,其包含:
201、rna lipoplex颗粒,其包含:
202、编码包含至少一个表位的肽或蛋白质的rna,
203、至少一种阳离子脂质和至少一种另外的脂质,
204、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0,
205、浓度为10mm至约80mm的氯化钠,以及
206、稳定剂。
207、在一个实施方案中,组合物还包含缓冲剂。
208、在一个实施方案中,组合物中rna的量为约0.01mg/ml至约1mg/ml、约0.05mg/ml至约0.5mg/ml,或约0.05mg/ml。
209、在一个实施方案中,氯化钠的浓度为约20mm至约30mm。
210、在一个实施方案中,氯化钠的浓度为约20mm。
211、在一个实施方案中,氯化钠的浓度为约30mm。
212、在一个实施方案中,组合物中稳定剂的浓度高于生理渗量浓度所需的值。
213、在一个实施方案中,组合物中稳定剂的浓度为约5至约35重量/体积百分比(%w/v),或约10至约25重量/体积百分比(%w/v)。
214、在一个实施方案中,稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
215、在一个实施方案中,稳定剂是海藻糖,其浓度为约5至约35重量/体积百分比(%w/v)。
216、在一个实施方案中,海藻糖的浓度为约5%(w/v)至约25%(w/v)。
217、在一个实施方案中,海藻糖的浓度为约10%(w/v)至约25%(w/v)。
218、在一个实施方案中,海藻糖的浓度为约10%(w/v)。
219、在一个实施方案中,海藻糖的浓度为约15%(w/v)。
220、在一个实施方案中,组合物的ph低于通常对于rna储存而言最佳的ph。
221、在一个实施方案中,组合物的ph为约5.7至约6.7,或约6.2。
222、在一个实施方案中,缓冲剂是2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)。
223、在一个实施方案中,hepes的浓度为约2.5mm至约10mm,或约7.5mm。
224、在一个实施方案中,组合物还包含螯合剂。
225、本公开内容还涉及组合物,其包含:
226、rna lipoplex颗粒,其包含:
227、编码包含至少一个表位的肽或蛋白质的rna,浓度为约0.05mg/ml,以及
228、摩尔比为约2∶1的dotma和dope,
229、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1.3∶2.0,
230、浓度为约20mm的氯化钠,
231、浓度为约10%(w/v)的海藻糖,
232、浓度为约7.5mm、ph为约6.2的hepes,以及
233、浓度为约2.5mm的edta。
234、在一个实施方案中,组合物为液体或脱水的,例如冻干或冷冻干燥的状态。
235、在一个实施方案中,脱水的(例如冻干或冷冻干燥的)组合物至少一个月、至少6个月、至少12个月、至少24个月、或至少36个月保持稳定。在一个实施方案中,组合物在高于0℃的温度下,例如在约25℃或约4℃下,或例如在室温下储存。
236、在一个实施方案中,脱水的(例如冻干或冷冻干燥的)组合物至少一个月保持稳定。
237、在一个实施方案中,脱水的(例如冻干或冷冻干燥的)组合物至少两个月保持稳定。
238、本公开内容还涉及包含rna lipoplex颗粒的水性组合物,所述水性组合物可通过使上述脱水的(例如冻干或冷冻干燥的)组合物重构,以及任选地通过添加水性液体来调整渗量浓度和离子强度来获得。
239、在一个实施方案中,组合物的渗量浓度为约150mosmol/kg至约450mosmol/kg。
240、在一个实施方案中,组合物包含浓度为约80mm至约150mm的氯化钠。
241、在一个实施方案中,rna lipoplex颗粒可通过如上在i.和ii.下所述的方法获得。
242、在一个实施方案中,在iii.下的该方面中所述的rna lipoplex颗粒的特征在于在约1nm-1处的单个布拉格峰,其中峰宽小于0.2nm-1。
243、在一个实施方案中,在iii.下的该方面中所述的rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
244、在一个实施方案中,rna lipoplex颗粒具有小于约0.5、小于约0.4,或小于约0.3的多分散性指数。
245、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
246、在一个实施方案中,所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
247、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
248、在一个实施方案中,所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
249、在一个实施方案中,rna lipoplex颗粒包含摩尔比为约10∶0至1∶9、约4∶1至1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope,并且其中dotma中正电荷与rna中负电荷的电荷比为约1∶2至1.9∶2。
250、在一个实施方案中,螯合剂是乙二胺四乙酸(edta)。
251、在一个实施方案中,edta的浓度为约0.25mm至约5mm,或约2.5mm。
252、在一个实施方案中,组合物还包含辅料。
253、在一个实施方案中,组合物配制成用于全身性施用。
254、在一个实施方案中,全身性施用是通过静脉内施用。
255、本公开内容还涉及用于治疗用途的如前所述的组合物。
256、本公开内容还涉及制备包含rna lipoplex颗粒的水性组合物的方法,其包括将上述冷冻组合物解冻或使上述冻干或喷雾干燥的组合物重构,以及任选地通过添加水性液体来调整渗量浓度和离子强度。
257、在一个实施方案中,添加水性液体以使所述组合物获得约200mosmol/kg至约450mosmol/kg的渗量浓度。
258、在一个实施方案中,添加水性液体以获得浓度为约80mm至约150mm的氯化钠。
259、本文中所述的适合储存rna lipoplex颗粒而基本上不损失产品品质,并且特别是基本上不损失rna活性的一些rna lipoplex制剂不需要对产品进行修饰,特别是将产品用水相(例如注射用水、盐水)稀释以在施用之前调整期望的渗量浓度和离子强度。这样的rnalipoplex制剂可在储存之后并且任选地在产品解冻或重构之后直接施用。在其中将rnalipoplex组合物冷冻用于储存的本公开内容的那些实施方案中,可将组合物解冻,并且在无需调整组合物的渗量浓度、离子强度和/或ph的情况下施用。
260、因此,本公开内容涉及组合物,其包含:
261、rna lipoplex颗粒,其包含:
262、rna,以及
263、至少一种阳离子脂质和至少一种另外的脂质,
264、浓度为约10mm或更低的氯化钠,
265、浓度为约10%重量/体积百分比(%w/v)或更低的稳定剂,以及
266、缓冲剂。
267、在一个实施方案中,氯化钠的浓度为约5mm至约10mm。在一个实施方案中,氯化钠的浓度为约7.5mm或更低,例如约5mm至约7.5mm。在一个实施方案中,氯化钠的浓度为约6.5mm或约7.5mm。
268、在一个实施方案中,组合物中盐和/或稳定剂的浓度约为生理渗量浓度所需的值。在一个实施方案中,由溶解的组分,包括离子和非离子组分产生的渗量浓度约为生理渗量浓度所需的值。
269、在一个实施方案中,组合物中稳定剂的浓度为约5至约10%(w/v)。在一个实施方案中,组合物中稳定剂的浓度为约5至约7.5%(w/v)。在一个实施方案中,组合物中稳定剂的浓度为约7.5至约10%(w/v)。
270、在一个实施方案中,稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
271、在一个实施方案中,稳定剂是蔗糖或海藻糖。在一个实施方案中,稳定剂是蔗糖,其浓度为约5至约10%(w/v)。在一个实施方案中,蔗糖的浓度为约10%(w/v)。在一个实施方案中,稳定剂是海藻糖,其浓度为约5至约10%(w/v)。在一个实施方案中,海藻糖的浓度为约10%(w/v)。
272、在一个实施方案中,缓冲剂选自:2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)、组氨酸、乙酸/乙酸钠和mes(2-(n-吗啉代)乙磺酸)。在一个实施方案中,缓冲剂是hepes、组氨酸或mes。在一个实施方案中,缓冲剂是hepes或mes。在一个实施方案中,缓冲剂是hepes。
273、在一个实施方案中,组合物的ph为6.0至7.2、6.0至7.0、6.2至7.0、6.5至7.0或6.5至6.7。在一个实施方案中,组合物的ph为约6.5或6.7。
274、在一个实施方案中,缓冲剂以2.5mm至10mm的浓度存在。在一个实施方案中,缓冲剂以2.5mm至5mm的浓度存在。在一个实施方案中,缓冲剂以5mm至10mm的浓度存在。在一个实施方案中,缓冲剂以5mm至7.5mm的浓度存在。在一个实施方案中,缓冲剂以7.5mm至10mm的浓度存在。在一个实施方案中,缓冲剂以约7.5mm的浓度存在。
275、在一个实施方案中,缓冲剂是hepes,其浓度为约7.5mm或更低,例如2.5mm至7.5mm或5mm至7.5mm、ph为约6.5或约6.7。
276、在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。在一个实施方案中,所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)v-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。在一个实施方案中,所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
277、在一个实施方案中,所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1到约1∶1、或约2∶1。
278、在一个实施方案中,所述rna lipoplex颗粒包含摩尔比为约10∶0至1∶9、约4∶1至1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope。
279、在一个实施方案中,组合物还包含螯合剂。在一个实施方案中,螯合剂是乙二胺四乙酸(edta)。在一个实施方案中,edta的浓度为约3.5mm或更低,或约0.25mm至约3.5mm,或约0.25mm至约2.5mm。
280、在本文中所述的组合物的一个实施方案中,所述rna编码包含至少一个表位的肽或蛋白质,其中所述组合物中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
281、本公开内容还涉及组合物,其包含:
282、rna lipoplex颗粒,其包含:
283、编码包含至少一个表位的肽或蛋白质的rna,
284、摩尔比为约2∶1的dotma和dope,
285、其中所述组合物中正电荷与负电荷之比为约1.3∶2.0,
286、浓度为约7.5mm的氯化钠,
287、浓度为约10%(w/v)的蔗糖,
288、浓度为约7.5mm、ph为约6.5或约6.7的hepes,以及
289、浓度为约2.5mm的edta。
290、在本文中所述的组合物的一个实施方案中,所述rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
291、在本文中所述的组合物的一个实施方案中,所述组合物中rna的量为约0.01mg/ml至约1mg/ml、约0.05mg/ml至约0.5mg/ml、约0.05mg/ml,或约0.02mg/ml。
292、在本文中所述的组合物的一个实施方案中,组合物还包含辅料。
293、在本文中所述的组合物的一个实施方案中,组合物为液体、冷冻或脱水状态。
294、在一个实施方案中,组合物是冷冻组合物并且在约-15℃的温度下至少一个月保持稳定。在一个实施方案中,组合物是冷冻组合物并且在约-15℃的温度下至少两个月保持稳定。在一个实施方案中,组合物是冷冻组合物并且在约-15℃的温度下至少四个月保持稳定。在一个实施方案中,组合物是冷冻组合物并且在约-15℃的温度下至少六个月保持稳定。
295、本公开内容还涉及包含rna lipoplex颗粒的液体组合物,所述液体组合物可通过将本文中所述的冷冻组合物解冻来获得。在一个实施方案中,所述液体组合物具有如上所述的组成。
296、本公开内容还涉及包含rna lipoplex颗粒的液体组合物,所述液体组合物可通过将本文中所述的脱水组合物溶解来获得。在一个实施方案中,所述液体组合物具有如上所述的组成。
297、在一个实施方案中,本文中所述的液体组合物是水性组合物。
298、在一个实施方案中,本文中所述的组合物,特别是液体组合物可直接施用于对象。
299、在一个实施方案中,本文中所述的组合物是药物组合物。
300、在一个实施方案中,本文中所述的组合物配制成用于全身性施用。
301、在一个实施方案中,全身性施用是通过静脉内施用。
302、本公开内容还涉及用于治疗用途的本文中所述的组合物。
303、本公开内容还涉及制备用于直接施用于对象的包含rna lipoplex颗粒的液体组合物的方法,其包括将本文中所述的冷冻组合物解冻。本公开内容还涉及制备用于直接施用于对象的包含rna lipoplex颗粒的液体组合物的方法,其包括将本文中所述的脱水组合物溶解。在本文中所述的方法的一个实施方案中,所述液体组合物是水性组合物。在一个实施方案中,所述液体组合物具有如上所述的组成。对于如本文中所述的治疗应用,将本文中所述的液体组合物施用于对象。
304、本公开内容还涉及组合物,其包含:
305、rna lipoplex颗粒,其包含
306、rna,以及
307、至少一种阳离子脂质和至少一种另外的脂质,
308、浓度为约10mm或更低的氯化钠,
309、浓度为超过约10%重量/体积百分比(%w/v)且低于约15%重量/体积百分比(%w/v)的稳定剂,以及
310、缓冲剂。
311、在一个实施方案中,氯化钠的浓度为约5mm至约10mm。在一个实施方案中,氯化钠的浓度为约8.5mm或更低,例如约5mm至约8.5mm。在一个实施方案中,氯化钠的浓度为约8.2mm
312、在一个实施方案中,组合物中盐和/或稳定剂的浓度约为生理渗量浓度所需的值。在一个实施方案中,由溶解的组分(包括离子和非离子组分)产生的渗量浓度约为生理渗量浓度所需的值。
313、在一个实施方案中,组合物中稳定剂的浓度为约11%至约14%(w/v)。在一个实施方案中,组合物中稳定剂的浓度为约12至约14%(w/v)。在一个实施方案中,组合物中稳定剂的浓度为约13%(w/v)。
314、在一个实施方案中,稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
315、在一个实施方案中,稳定剂是蔗糖或海藻糖。在一个实施方案中,稳定剂是浓度为约12至约14%(w/v)的蔗糖。在一个实施方案中,蔗糖的浓度为约13%(w/v)。在一个实施方案中,稳定剂是浓度为约12至约14%(w/v)的海藻糖。在一个实施方案中,海藻糖的浓度为约13%(w/v)。
316、在一个实施方案中,缓冲剂选自:2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)、组氨酸、乙酸/乙酸钠和mes(2-(n-吗啉代)乙磺酸)。在一个实施方案中,缓冲剂是hepes、组氨酸或mes。在一个实施方案中,缓冲剂是hepes或mes。在一个实施方案中,缓冲剂是hepes。
317、在一个实施方案中,组合物的ph为6.0至7.5、6.5至7.5、6.5至7.3、6.5至7.2、6.7至7.2或6.5至7.0。在一个实施方案中,组合物的ph为约6.7。
318、在一个实施方案中,缓冲剂以2.5mm至10mm的浓度存在。在一个实施方案中,缓冲剂以2.5mm至7.5mm的浓度存在。在一个实施方案中,缓冲剂以4mm至6mm的浓度存在。在一个实施方案中,缓冲剂以约5mm的浓度存在。
319、在一个实施方案中,缓冲剂是浓度为约7.5mm或更低(例如2.5mm至7.5mm或4mm至6mm,例如约5mm)且ph为约6.7的hepes。
320、在一个实施方案中,至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。在一个实施方案中,至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。在一个实施方案中,至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
321、在一个实施方案中,至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
322、在一个实施方案中,rna lipoplex颗粒包含摩尔比为约10∶0至1∶9、约4∶1至1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope。
323、在一个实施方案中,组合物还包含螯合剂。在一个实施方案中,螯合剂是乙二胺四乙酸(edta),特别是edta二钠盐。在一个实施方案中,edta的浓度为约3.5mm或更低,或约0.25mm至约3.5mm,或约0.25mm至约2.5mm。
324、在本文中所述组合物的一个实施方案中,rna编码包含至少一个表位的肽或蛋白质,其中所述组合物中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
325、本公开内容还涉及组合物,其包含:
326、rna lipoplex颗粒,其包含:
327、编码包含至少一个表位的肽或蛋白质的rna,
328、摩尔比为约2∶1的dotma和dope,
329、其中所述组合物中正电荷与负电荷之比为约1.3∶2.0,
330、浓度为约8.2mm的氯化钠,
331、浓度为约13%(w/v)的蔗糖,
332、浓度为约5mm、ph为约6.7的hepes,以及
333、浓度为约2.5mm的edta。
334、在本文中所述组合物的一个实施方案中,rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
335、在本文中所述组合物的一个实施方案中,组合物中rna的量为约0.01mg/ml至约1mg/ml、约0.05mg/ml至约0.5mg/ml、或约0.025mg/ml。
336、在本文中所述组合物的一个实施方案中,组合物还包含酸。在一个实施方案中,酸以使脂质体稳定的量存在。在一个实施方案中,酸以降低dope水解的量存在。在一个实施方案中,酸是乙酸或hcl。在一个实施方案中,酸是乙酸。在一个实施方案中,酸是浓度为约0.09mm的乙酸。
337、在本文中所述组合物的一个实施方案中,组合物还包含辅料。
338、在本文中所述组合物的一个实施方案中,组合物为液体、冷冻或脱水状态。
339、在一个实施方案中,组合物是冷冻组合物,并且在约-15℃的温度下至少一个月保持稳定。在一个实施方案中,组合物是冷冻组合物,并且在约-15℃的温度下至少两个月保持稳定。在一个实施方案中,组合物是冷冻组合物,并且在约-15℃的温度下至少四个月保持稳定。在一个实施方案中,组合物是冷冻组合物,并且在约-15℃的温度下至少六个月保持稳定。
340、本公开内容还涉及包含rna lipoplex颗粒的液体组合物,其可通过将本文中所述的冷冻组合物解冻来获得。在一个实施方案中,所述液体组合物具有如上所述的组成。
341、本公开内容还涉及包含rna lipoplex颗粒的液体组合物,其可通过将本文中所述的脱水组合物溶解来获得。在一个实施方案中,所述液体组合物具有如上所述的组成。
342、在一个实施方案中,本文中所述的液体组合物是水性组合物。
343、在一个实施方案中,本文中所述的组合物,特别是液体组合物,可直接施用于对象。
344、在一个实施方案中,本文中所述的组合物是药物组合物。
345、在一个实施方案中,本文中所述的组合物配制成用于全身性施用。
346、在一个实施方案中,全身性施用是通过通过静脉内施用。
347、本公开内容还涉及用于治疗用途的本文中所述的组合物。
348、本公开内容还涉及制备用于直接施用于对象的包含rna lipoplex颗粒的液体组合物的方法,所述方法包括将本文中所述的冷冻组合物解冻。本公开内容还涉及制备用于直接施用于对象的包含rna lipoplex颗粒的液体组合物的方法,所述方法包括将本文中所述的脱水组合物溶解。在本文中所述方法的一个实施方案中,液体组合物是水性组合物。在一个实施方案中,液体组合物具有如上所述的组成。对于本文中所述的治疗应用,将本文中所述的液体组合物施用于对象。
349、另一些实施方案如下:
350、1.产生脂质体胶体的方法,其包括将在乙醇中的脂质溶液注入到水相中以产生所述脂质体胶体,其中所述脂质溶液中至少一种脂质的浓度对应于或高于所述至少一种脂质在乙醇中的平衡溶解度。
351、2.实施方案1所述的方法,其中所述脂质溶液是两种或更多种不同脂质的混合物的溶液。
352、3.实施方案1或2所述的方法,其中所述脂质溶液中一种脂质的浓度对应于或高于室温下所述脂质在乙醇中的平衡溶解度。
353、4.实施方案1至3中任一项所述的方法,其中所述脂质溶液中的总脂质浓度为约180mm至约600mm、约300mm至约600mm,或约330mm。
354、5.实施方案1至4中任一项所述的方法,其中所述脂质溶液包含至少一种阳离子脂质和至少一种另外的脂质。
355、6.实施方案5所述的方法,其中所述脂质溶液中的另外的脂质的浓度对应于或高于所述另外的脂质在乙醇中的平衡溶解度。
356、7.实施方案5或6所述的方法,其中所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
357、8.实施方案5至7中任一项所述的方法,其中所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
358、9.实施方案5至8中任一项所述的方法,其中所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
359、10.实施方案5至9中任一项所述的方法,其中所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
360、11.实施方案1至10中任一项所述的方法,其中所述脂质溶液包含摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope。
361、12.实施方案8至11中任一项所述的方法,其中所述脂质溶液中dope的浓度为至少约60mm或至少约90mm。
362、13.实施方案1至12中任一项所述的方法,其中将所述脂质溶液注入到约50rpm至约150rpm的水相搅拌速度的水相中。
363、14.实施方案1至13中任一项所述的方法,其中所述水相是水。
364、15.实施方案1至14中任一项所述的方法,其中所述方法还包括搅拌所述脂质体胶体。
365、16.实施方案1至15中任一项所述的方法,其中将所述脂质体胶体搅拌约15分钟至约60分钟,或搅拌约30分钟。
366、17.产生脂质体胶体的方法,其包括将在乙醇中包含摩尔比为约2∶1的dotma和dope的脂质溶液注入到以约150rpm的搅拌速度搅拌的水中以产生所述脂质体胶体,其中在所述脂质溶液中dotma和dope的浓度为约330mm。
367、18.脂质体胶体,其可通过实施方案1至17中任一项所述的方法获得。
368、19.实施方案18所述的脂质体胶体,其中所述脂质体的平均直径为至少约250nm。
369、20.实施方案18或19所述的脂质体胶体,其中所述脂质体的平均直径为约250nm至约800nm。
370、21.实施方案18至20中任一项所述的脂质体胶体,其中所述脂质体是阳离子脂质体。
371、22.实施方案18至21中任一项所述的脂质体胶体,其中所述脂质体包含至少一种阳离子脂质和至少一种另外的脂质。
372、23.实施方案22所述的脂质体胶体,其中所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
373、24.实施方案22或23所述的脂质体胶体,其中所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
374、25.实施方案22至24中任一项所述的脂质体胶体,其中所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
375、26.实施方案22至25中任一项所述的脂质体胶体,其中所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
376、27.实施方案18至26中任一项所述的脂质体胶体,其中所述脂质体包含摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope。
377、28.制备rna lipoplex颗粒的方法,其包括将实施方案18至27中任一项所述的脂质体胶体添加至包含rna的溶液。
378、29.用于连续流制备rna lipoplex颗粒的方法,其包括在rna和阳离子脂质体的受控混合条件下将包含rna的溶液与包含阳离子脂质体的溶液混合。
379、30.实施方案29所述的方法,其中所述包含阳离子脂质体的溶液是实施方案18至27中任一项所述的脂质体胶体。
380、31.实施方案29或30所述的方法,其中所述包含rna的溶液和所述包含阳离子脂质体的溶液是水性溶液。
381、32.实施方案29至31中任一项所述的方法,其中使用允许所述包含rna的溶液与所述包含阳离子脂质体的溶液混合的流量。
382、33.实施方案29至32中任一项所述的方法,其中所述流的特征在于雷诺数大于300,或为约500至约2100。
383、34.实施方案29至33中任一项所述的方法,其中所述受控混合条件包括控制所述包含rna的溶液与所述包含阳离子脂质体的溶液的混合比。
384、35.实施方案29至34中任一项所述的方法,其中所述受控混合条件包括控制待混合的所述包含rna的溶液与所述包含阳离子脂质体的溶液的相对体积。
385、36.实施方案29至35中任一项所述的方法,其中通过使用相同混合体积(v/v)的所述包含rna的溶液和所述包含阳离子脂质体的溶液以及调整相应溶液中rna和阳离子脂质体的浓度来控制所述rna与所述阳离子脂质体的混合比。
386、37.实施方案29至36中任一项所述的方法,其中选择所述受控混合条件以在避免堵塞的同时维持所述rna lipoplex颗粒的特征。
387、38.实施方案29至37中任一项所述的方法,其中所述方法包括使用y型或t型混合元件。
388、39.实施方案29至38中任一项所述的方法,其中所述y型或t型混合元件的直径为约1.2mm至约50mm。
389、40.实施方案29至39中任一项所述的方法,其中所述方法包括使用注射器泵,其中将两个注射器平行地插入到同一泵中,所述两个注射器的一个包含所述包含阳离子脂质体的溶液并且一个包含所述包含rna的溶液。
390、41.实施方案29至40中任一项所述的方法,其中所述方法包括将压力容器、膜泵、齿轮泵、磁悬浮泵或蠕动泵与流量传感器组合使用,所述流量传感器任选地具有用于在线控制和实时调整流量的反馈回路。
391、42.实施方案29至41中任一项所述的方法,其中所述包含rna的溶液与所述包含脂质体的溶液的混合物包含浓度为约45mm至约300mm的氯化钠,或包含对应于浓度为约45mm至约300mm的氯化钠的离子强度。
392、43.实施方案29至42中任一项所述的方法,其中所述包含rna的溶液与所述包含脂质体的溶液的混合物具有至少约50mm的离子强度。
393、44.实施方案28至43中任一项所述的方法,其中在x射线散射模式中,所述rnalipoplex的特征在于在约1nm-1处的单个布拉格峰,其中所述峰宽小于0.2nm-1。
394、45.实施方案28至44中任一项所述的方法,其中所述rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
395、46.制备包含rna lipoplex颗粒的冷冻组合物的方法,其包括(i)提供包含rnalipoplex颗粒和稳定剂的水性组合物,以及(ii)冷冻所述组合物。
396、47.实施方案46所述的方法,其中冷冻在约-15℃至约-40℃,或在约-30℃的温度下进行。
397、48.实施方案47所述的方法,其中所述稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
398、49.实施方案46至48中任一项所述的方法,其中提供包含rna lipoplex颗粒和稳定剂的水性组合物包括提供包含rna lipoplex颗粒的水性组合物并向所述包含rnalipoplex颗粒的水性组合物添加所述稳定剂。
399、50.实施方案46至49中任一项所述的方法,其中向所述包含rna lipoplex颗粒的水性组合物添加所述稳定剂降低所述包含rna lipoplex颗粒的水性组合物的离子强度。
400、51.实施方案46至50中任一项所述的方法,其中在所述包含rna lipoplex颗粒和稳定剂的水性组合物中稳定剂的浓度高于生理渗量浓度所需的值。
401、52.实施方案46至51中任一项所述的方法,其中在所述包含rna lipoplex和稳定剂的水性组合物中稳定剂的浓度足以维持所述rna lipoplex颗粒的品质,并且特别地足以避免在将所述组合物在约-15℃至约-40℃的温度下储存至少一个月、至少6个月、至少12个月、至少24个月,或至少36个月之后rna活性的实质性损失。
402、53.实施方案46至52中任一项所述的方法,其中所述包含rna lipoplex和稳定剂的水性组合物中的ph低于通常对于rna储存而言最佳的ph。
403、54.实施方案46至53中任一项所述的方法,其中所述包含rna lipoplex和稳定剂的水性组合物包含浓度为约10mm至约50mm的氯化钠,或包含对应于浓度为约10mm到约50mm的氯化钠的离子强度。
404、55.实施方案46至54中任一项所述的方法,其中所述包含rna lipoplex和稳定剂的水性组合物具有对应于浓度为约20mm的氯化钠的离子强度。
405、56.实施方案46至55中任一项所述的方法,其中所述rna lipoplex颗粒可通过实施方案28至44中任一项所述的方法获得。
406、57.包含rna lipoplex颗粒的组合物,所述rna lipoplex颗粒可通过实施方案28至45中任一项所述的方法获得。
407、58.实施方案57所述的组合物,其中所述rna lipoplex颗粒包含至少一种阳离子脂质和至少一种另外的脂质。
408、59.实施方案57或58所述的组合物,其中所述rna编码包含至少一个表位的肽或蛋白质,其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
409、60.组合物,其包含:
410、rna lipoplex颗粒,其包含:
411、编码包含至少一个表位的肽或蛋白质的rna,以及
412、至少一种阳离子脂质和至少一种另外的脂质,
413、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0,并且
414、其中所述rna lipoplex颗粒的特征在于在约1nm-1处的单个布拉格峰,其中所述峰宽小于0.2nm-1。
415、61.实施方案57至60中任一项所述的组合物,其中所述组合物还包含浓度为约10至约300mm、约45mm至约300mm、约10mm至约50mm,或约80mm至约150mm的氯化钠。
416、62.实施方案57至61中任一项所述的组合物,其中所述组合物还包含缓冲剂。
417、63.实施方案57至62中任一项所述的组合物,其中所述组合物还包含螯合剂。
418、64.包含rna lipoplex颗粒的组合物,其可通过实施方案46至56中任一项所述的方法获得。
419、65.实施方案64所述的组合物,其中所述rna lipoplex颗粒包含至少一种阳离子脂质和至少一种另外的脂质。
420、66.实施方案64或65所述的组合物,其中所述rna编码包含至少一个表位的肽或蛋白质,其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0。
421、67.实施方案64至66中任一项所述的组合物,其中所述组合物还包含浓度为约10mm至约50mm的氯化钠。
422、68.组合物,其包含:
423、rna lipoplex颗粒,其包含:
424、编码包含至少一个表位的肽或蛋白质的rna,
425、至少一种阳离子脂质和至少一种另外的脂质,
426、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1∶2至约1.9∶2,或约1.3∶2.0,
427、浓度为0mm至约40mm的氯化钠,以及
428、稳定剂。
429、69.实施方案64至68中任一项所述的组合物,其中所述组合物还包含缓冲剂。
430、70.实施方案64至69中任一项所述的组合物,其中所述组合物中rna的量为约0.01mg/ml至约1mg/ml、约0.05mg/ml至约0.5mg/ml,或约0.05mg/ml。
431、71.实施方案67至70中任一项所述的组合物,其中所述氯化钠的浓度为约20mm至约30mm。
432、72.实施方案67至71中任一项所述的组合物,其中所述氯化钠的浓度为约20mm。
433、73.实施方案67至71中任一项所述的组合物,其中所述氯化钠的浓度为约30mm。
434、74.实施方案64至73中任一项所述的组合物,其中所述组合物中稳定剂的浓度高于生理渗量浓度所需的值。
435、75.实施方案64至74中任一项所述的组合物,其中所述组合物中稳定剂的浓度为约5至约35重量/体积百分比(%w/v),或约12.5至约25重量/体积百分比(%w/v)。
436、76.实施方案64至75中任一项所述的组合物,其中所述稳定剂是选自单糖、二糖、三糖、糖醇、寡糖或其相应糖醇以及直链多元醇的碳水化合物。
437、77.实施方案64至76中任一项所述的组合物,其中所述稳定剂是蔗糖,其浓度为约5至约25重量/体积百分比(%w/v)。
438、78.实施方案77所述的组合物,其中所述蔗糖的浓度为约15%(w/v)至约25%(w/v)。
439、79.实施方案77所述的组合物,其中所述蔗糖的浓度为约20%(w/v)至约25%(w/v)。
440、80.实施方案77所述的组合物,其中所述蔗糖的浓度为约22%(w/v)。
441、81.实施方案77所述的组合物,其中所述蔗糖的浓度为约20%(w/v)。
442、82.实施方案64至81中任一项所述的组合物,其中所述组合物的ph低于通常对于rna储存而言最佳的ph。
443、83.实施方案64至82中任一项所述的组合物,其中所述组合物的ph为约5.7至约6.7,或约6.2。
444、84.实施方案68至83中任一项所述的组合物,其中所述缓冲剂是2-[4-(2-羟基乙基)哌嗪-1-基]乙磺酸(hepes)。
445、85.实施方案84所述的组合物,其中所述hepes的浓度为约2.5mm至约10mm,或约7.5mm。
446、86.实施方案64至85中任一项所述的组合物,其中所述组合物还包含螯合剂。
447、87.组合物,其包含:
448、rna lipoplex颗粒,其包含:
449、编码包含至少一个表位的肽或蛋白质的rna,所述rna浓度为约0.05mg/ml,以及
450、摩尔比为约2∶1的dotma和dope,
451、其中所述rna lipoplex颗粒中正电荷与负电荷之比为约1.3∶2.0,浓度为约20mm的氯化钠,
452、浓度为约22%(w/v)的蔗糖,
453、浓度为约7.5mm、ph为约6.2的hepes,以及
454、浓度为约2.5mm的edta。
455、88.实施方案64至87中任一项所述的组合物,其中所述组合物为液体或冷冻状态。
456、89.实施方案88所述的冷冻组合物,其中所述组合物在约-15℃至约-40℃的温度下至少一个月保持稳定。
457、90.实施方案88所述的冷冻组合物,其中所述组合物在约-15℃的温度下至少一个月保持稳定。
458、91.实施方案88所述的冷冻组合物,其中所述组合物在约-15℃的温度下至少两个月保持稳定。
459、92.实施方案88所述的冷冻组合物,其中所述组合物在约-20℃的温度下至少一个月保持稳定。
460、93.实施方案88所述的冷冻组合物,其中所述组合物在约-20℃的温度下至少两个月保持稳定。
461、94.实施方案88所述的冷冻组合物,其中所述组合物在约-30℃的温度下至少一个月保持稳定。
462、95.实施方案88所述的冷冻组合物,其中所述组合物在约-30℃的温度下至少两个月保持稳定。
463、96.包含rna lipoplex颗粒的水性组合物,所述水性组合物可通过将实施方案88至95中任一项所述的冷冻组合物解冻,以及任选地通过添加水性液体来调整渗量浓度和离子强度来获得。
464、97.实施方案96所述的组合物,其中所述组合物的渗量浓度为约200mosmol/kg至约450mosmol/kg。
465、98.实施方案96或97所述的组合物,其中所述组合物包含浓度为约80mm至约150mm的氯化钠。
466、99.实施方案64至98中任一项所述的组合物,其中所述rna lipoplex颗粒可通过实施方案28至45中任一项所述的方法获得。
467、100.实施方案64至99中任一项所述的组合物,其中所述rna lipoplex颗粒的特征在于在约1nm-1处的单个布拉格峰,其中所述峰宽小于0.2nm-1。
468、101.实施方案57至100中任一项所述的组合物,其中所述rna lipoplex颗粒的平均直径为约200至约800nm、约250至约700nm、约400至约600nm、约300nm至约500nm,或约350nm至约400nm。
469、102.实施方案58至63、65至86和88至101中任一项所述的组合物,其中所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma)和/或1,2-二油酰基-3-三甲基铵丙烷(dotap)。
470、103.实施方案58至63、65至86和88至102中任一项所述的组合物,其中所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)、胆固醇(chol)和/或1,2-二油酰基-sn-甘油基-3-磷酸胆碱(dopc)。
471、104.实施方案58至63、65至86和88至103中任一项所述的组合物,其中所述至少一种阳离子脂质包含1,2-二-o-十八碳烯基-3-三甲基铵丙烷(dotma),并且所述至少一种另外的脂质包含1,2-二-(9z-十八碳烯酰基)-sn-甘油基-3-磷酸乙醇胺(dope)。
472、105.实施方案58至63、65至86和88至104中任一项所述的组合物,其中所述至少一种阳离子脂质与所述至少一种另外的脂质的摩尔比为约10∶0至约1∶9、约4∶1至约1∶2、约3∶1至约1∶1、或约2∶1。
473、106.实施方案58至63、65至86和88至105中任一项所述的组合物,其中所述rnalipoplex颗粒包含摩尔比为约10∶0至1∶9、约4∶1至1∶2、约3∶1至约1∶1、或约2∶1的dotma和dope,并且其中dotma中正电荷与所述rna中负电荷的电荷比为约1∶2至1.9∶2。
474、107.实施方案63、86和88至106中任一项所述的组合物,其中所述螯合剂是乙二胺四乙酸(edta)。
475、108.实施方案107所述的组合物,其中所述edta的浓度为约0.25mm至约5mm,或约2.5mm。
476、109.实施方案57至108中任一项所述的组合物,其还包含辅料。
477、110.实施方案57至109中任一项所述的组合物,其配制成用于全身性施用。
478、111.实施方案110所述的组合物,其中所述全身性施用是通过静脉内施用。
479、112.实施方案57至111中任一项所述的组合物,其用于治疗用途。
480、113.制备包含rna lipoplex颗粒的水性组合物的方法,其包括将实施方案88至112中任一项所述的冷冻组合物解冻,以及任选地通过添加水性液体来调整渗量浓度和离子强度。
481、114.实施方案113所述的方法,其中添加水性液体以使所述组合物获得约200mosmol/kg至约450mosmol/kg的渗量浓度。
482、115.实施方案113或114所述的方法,其中添加水性液体以获得氯化钠浓度为约80mm至约150mm。
- 还没有人留言评论。精彩留言会获得点赞!