感光性树脂组合物及其固化物的制作方法
本发明涉及感光性树脂组合物,该感光性树脂组合物包含通过照射活化能量线而产生碱的光产碱剂。
背景技术:
以往,通过照射光、红外线、电子束或X射线等活性能量线而发生化学结构变化的感光性树脂组合物被用于各种用途。
作为像这样的感光性树脂组合物,例如已知配合了通过照射活性能量线而产生强酸的光产酸剂的化学放大型抗蚀剂。该化学放大型抗蚀剂中,通过照射活性能量线而产生的强酸作为催化剂作用于树脂成分,使相对于显像液的溶解性发生变化,由此进行图案形成。以往,为了高灵敏度化、高分辨率化的目的开发了各种抗蚀剂材料,但是,光产酸剂与树脂的组合受限,要求开发出新的化学放大型抗蚀剂。
通过照射活性能量线而使单体、预聚物光固化的技术大致分为自由基系、阳离子系及阴离子系3种。这些技术中成为最广泛开发对象的是对光自由基引发剂照射光而使乙烯基单体聚合的技术。另外,还研究了因光的作用而产生酸并以该酸为催化剂进行阳离子聚合的技术。
但是,像这样的自由基聚合系的情况下,因空气中的氧而妨碍聚合反应,所以需要在阻断氧的方面特别下工夫。另外,阳离子聚合系的情况下,虽然从没有氧带来的妨碍方面考虑非常有利,但是,指出有可能存在:由固化后还残留的光产酸剂产生的强酸的腐蚀性或树脂改性。因此,强烈希望开发出一种不包含像强酸这样的腐蚀性物质、且不被空气中的氧妨碍、以高效率迅速地进行反应的感光性树脂组合物。
从像这样的状况考虑,提出了包含将通过光的作用而产生的碱用于聚合反应、化学反应的阴离子系光产碱剂的感光性树脂组合物。但是,与自由基系光聚合引发剂、阳离子系光产酸剂相比,阴离子系光产碱剂可以举出如下缺点:光灵敏度差,必须照射强活性能量。
专利文献1中公开了感光性树脂组合物,该感光性树脂组合物含有:通过光的作用而产生碱的光产碱剂、具有羧基的环氧树脂以及具有巯基的固化剂。首先,对该感光性树脂照射光,产生作为碱的胺化合物,接下来,通过实施加热处理使产生的胺化合物与环氧基反应,得到固化膜。
但是,像专利文献1中使用的那样的光产碱剂,由于通过光照射产生的胺为单官能,所以为了以高残膜率得到固化膜,需要并用多官能硫醇单体。由于该多官能伯硫醇单体即便在常温下也具有与环氧树脂的反应性,因此,存在感光性树脂组合物的适用期短的问题。
进而,专利文献1中使用的光产碱剂由于分子内具有酚性羟基,所以没有进行光照射的部位也因加热而进行环氧基的反应。因此,将感光性树脂组合物用于抗蚀剂用途的情况下,即便是未曝光部也形成了固化膜,难以忠实地再现掩膜图案。
现有技术文献
专利文献
专利文献1:日本特开2013-95706号公报
非专利文献
非专利文献1:Angew.Chem.Int.2000,39,No.19
技术实现要素:
本发明是鉴于以上的课题而完成的,目的是提供一种由于即便是在使用光产碱剂的体系中也具有高灵敏度所以容易固化、进而得到的固化膜具有高分辨率、高残膜率、并且保存稳定性优异的感光性树脂组合物。
本发明的发明人为了解决上述课题进行了潜心研究,结果发现,含有特定结构的光产碱剂和碱可溶性环氧树脂这两者的感光性树脂组合物的灵敏度、分辨率及保存稳定性优异,并且通过使用该树脂组合物能够以高残膜率得到固化膜,从而完成本发明。
即,本发明涉及如下内容:
(1)一种感光性树脂组合物,其包含(A)光产碱剂和(B)碱可溶性环氧化合物,其中,所述(A)光产碱剂包含由下式(2-1)表示的化合物:
[化学式1]
(式(2-1)中,n表示0~4的整数。R1表示从由碳原子数1~18的烷基、碳原子数2~18的烯基、碳原子数2~18的炔基、碳原子数6~12的芳基、碳原子数1~18的酰基、碳原子数7~18的芳酰基、硝基、氰基、碳原子数1~18的烷氧基、碳原子数1~18的烷硫基、羟基及卤素原子构成的组中选择的至少1种取代基。R2表示氢原子、碳原子数1~18的烷基、碳原子数2~18的炔基、碳原子数6~12的芳基、碳原子数1~18的酰基、碳原子数7~18的芳酰基、硝基、氰基、碳原子数1~18的烷氧基、碳原子数1~18的烷硫基、羟基或卤素原子。X表示氨基。)
所述(B)碱可溶性环氧化合物是:使(a)1分子中具有至少2个以上环氧基的环氧化合物和(b)1分子中具有至少1个以上羟基及1个羧基的化合物的反应物、与(c)多元酸酐反应而得到的环氧化合物。
(2)根据前项(1)所述的感光性树脂组合物,其中,式(2-1)中的X为由下式(3-1)表示的基团:
[化学式2]
(式(3-1)中,R3及R4分别独立地表示氢原子、碳原子数1~12的烷基、碳原子数5~10的环烷基、碳原子数6~14的芳基或碳原子数7~15的芳基烷基,或者R3及R4彼此键合而形成构成原子数为3~12的含氮环。)。
(3)根据前项(1)所述的感光性树脂组合物,其中,由式(2-1)表示的化合物为由下式(4-1)或(4-2)表示的化合物:
[化学式3]
[化学式4]
(式(4-1)及(4-2)中,R1分别独立地表示与式(2-1)中的R1相同的含义。n分别独立地表示0~4的整数。p表示1~6的整数。)。
(4)根据前项(1)~(3)中的任意一项所述的感光性树脂组合物,其中,(B)碱可溶性环氧化合物包含由式(5-1)表示的环氧化合物:
[化学式5]
(式(5-1)中,r表示1以上的实数。s表示0以上的实数。其中,r与s的和为30以下。D1及D2分别独立地表示由下式(6-1)~(6-10):
[化学式6]
表示的二价连接基团中的任意一种。)。
(5)根据前项(1)~(4)中的任意一项所述的感光性树脂组合物,其中,所述感光性树脂组合物还包含具有至少1个尿烷键的化合物作为(C)碱增殖剂。
(6)根据前项(5)所述的感光性树脂组合物,其中,具有至少1个尿烷键的化合物为具有由下式(7-1)表示的碱增殖基的化合物:
[化学式7]
(7)一种固化物,其是前项(1)~(6)中的任意一项所述的感光性树脂组合物的固化物。
(8)一种图案形成方法,其包括:将前项(1)~(6)中的任意一项所述的感光性树脂组合物涂布在支撑体上的工序、对通过涂布得到的感光性树脂组合物层进行干燥的工序、干燥后曝光为规定图案的工序、曝光后进行烘烤的工序、使所述树脂组合物层显像的工序、以及对得到的树脂图案进行加热处理而得到固化树脂图案的工序。
本发明的感光性树脂组合物的灵敏度、分辨率及保存稳定性优异,并且,通过使用该树脂组合物能够以高残膜率得到固化膜。
附图说明
图1表示实施例1~4的感光性树脂组合物在各曝光量下的残膜率(曝光前的膜厚为1的情形下的、图案化后得到的图案的膜厚)的测定结果。
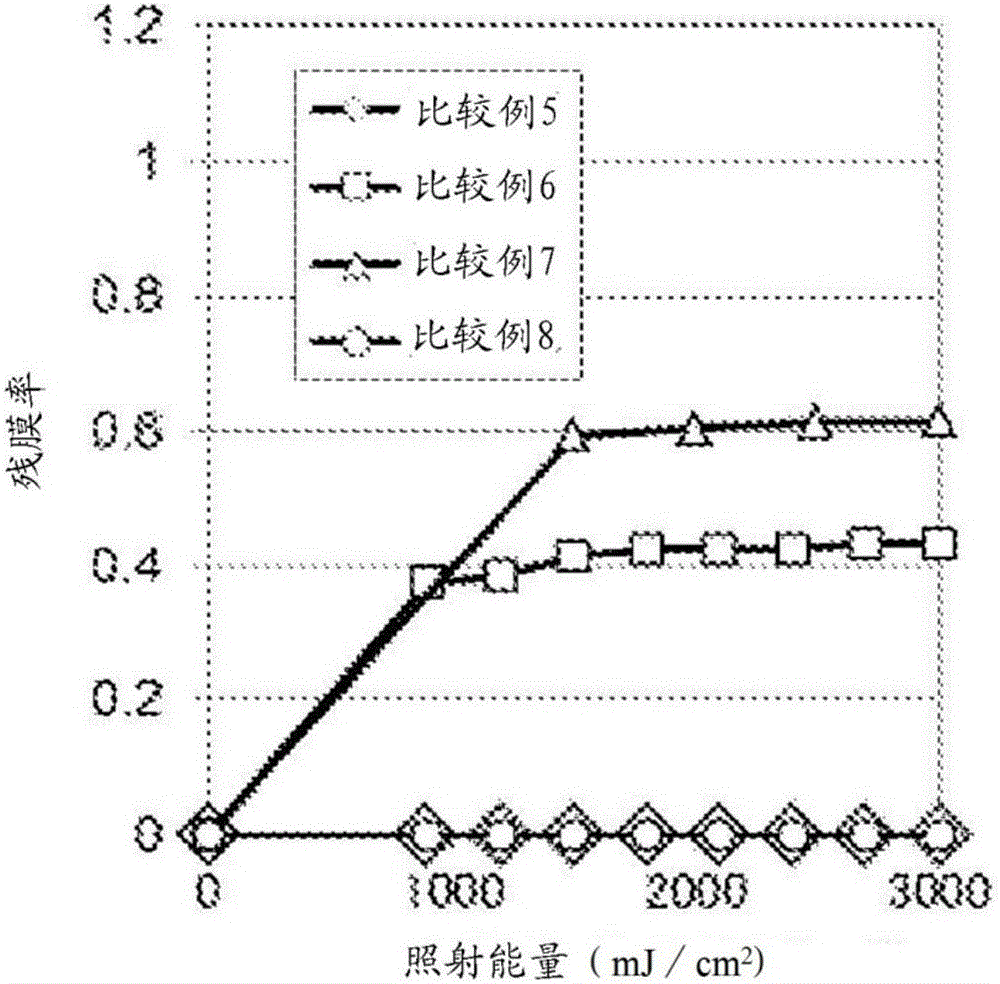
图2表示比较例5~8的感光性树脂组合物在各曝光量下的残膜率(曝光前的膜厚为1的情形下的、图案化后得到的图案的膜厚)的测定结果。
图3表示实施例1~4的感光性树脂组合物在各曝光量下的分辨率(与基板紧密接触的最细图案的线宽)的测定结果。
图4表示比较例5~8的感光性树脂组合物在各曝光量下的分辨率(与基板紧密接触的最细图案的线宽)的测定结果。
具体实施方式
以下,对本发明详细地进行说明。
本发明的一个方案是感光性树脂组合物,该感光性树脂组合物包含(A)光产碱剂(以下,也仅记载为“(A)成分”)和(B)碱可溶性环氧化合物(以下,也仅记载为“(B)成分”),该(A)成分包含由上述式(2-1)表示的化合物,该(B)成分是:使(a)1分子中具有至少2个以上环氧基的环氧化合物和(b)1分子中具有至少1个以上羟基和1个羧基的化合物的反应物、与(c)多元酸酐反应而得到的环氧化合物。
本发明的感光性树脂组合物包含至少一种由下式(2-1)表示的(A)成分。(A)成分是通过照射活性能量线而能够产生作为碱的单官能胺或者多官能胺的化合物。
[化学式8]
式(2-1)中,n通常表示0~4的整数,优选为1~2的整数,更优选为2。另外,n为2时R1的取代位置优选为:以式(2-1)中清楚记载的苯环上的与-CHR2-的键合位置为1位、与-NO2的键合位置为2位时的4位及5位。
式(2-1)中,R1表示从由碳原子数1~18的烷基、碳原子数2~18的烯基、碳原子数2~18的炔基、碳原子数6~12的芳基、碳原子数1~18的酰基、碳原子数7~18的芳酰基、硝基、氰基、碳原子数1~18的烷氧基、碳原子数1~18的烷硫基、羟基及卤素原子构成的组中选择的至少1种取代基,具有多个R1的情况下,彼此可以不同。
作为式(2-1)的R1表示的碳原子数1~18的烷基,可以举出:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、正己基、正庚基、正辛基、正壬基、正癸基、正十一烷基及正十二烷基等,优选为碳原子数2~6的烷基。
作为式(2-1)的R1表示的碳原子数2~18的烯基,可以举出:乙烯基、丙烯基、1-丁烯基、异丁烯基、1-戊烯基、2-戊烯基、2-甲基-1-丁烯基、3-甲基-1-丁烯基、2-甲基-2-丁烯基、2,2-二氰基乙烯基、2-氰基-2-甲基羧基乙烯基及2-氰基-2-甲基磺酸基乙烯基等。
作为式(2-1)的R1表示的碳原子数2~18的炔基,可以举出:乙炔基、1-丙炔基及1-丁炔基等。
作为式(2-1)的R1表示的碳原子数6~12的芳基,可以举出:苯基、萘基及甲苯基等,优选为碳原子数6~10的芳基。
作为式(2-1)的R1表示的碳原子数1~18的酰基,可以举出:甲酰基、乙酰基、乙基羰基、正丙基羰基、异丙基羰基、正丁基羰基、正戊基羰基、异戊基羰基、新戊基羰基、2-甲基丁基羰基及硝基苄基羰基等。
作为式(2-1)的R1表示的碳原子数7~18的芳酰基,可以举出:苯甲酰基、甲苯酰基、萘甲酰基及邻苯二甲酰基等。
作为式(2-1)的R1表示的碳原子数1~18的烷氧基,可以举出:甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基、叔丁氧基、正戊氧基、异戊氧基、新戊氧基、正己氧基及正十二烷氧基等。
作为式(2-1)的R1表示的碳原子数1~18的烷硫基,可以举出:甲硫基、乙硫基、正丙硫基、异丙硫基、正丁硫基、异丁硫基、仲丁硫基、叔丁硫基、正戊硫基、异戊硫基、2-甲基丁硫基、1-甲基丁硫基、新戊硫基、1,2-二甲基丙硫基及1,1-二甲基丙硫基等。
作为式(2-1)的R1表示的卤素原子,可以举出:氟原子、氯原子、溴原子及碘原子。
作为式(2-1)中的R1,优选为碳原子数1~18的烷氧基,更优选为碳原子数1~10的烷氧基,进一步优选为碳原子数1~4的烷氧基,特别优选为甲氧基。具有多个R1的情况下,优选至少一个R1为烷氧基,更优选全部R1均为烷氧基。
式(2-1)中,R2表示氢原子、碳原子数1~18的烷基、碳原子数2~18的炔基、碳原子数6~12的芳基、碳原子数1~18的酰基、碳原子数7~18的芳酰基、硝基、氰基、碳原子数1~18的烷氧基、碳原子数1~18的烷硫基、羟基或卤素原子。
作为式(2-1)的R2表示的碳原子数1~18的烷基、碳原子数2~18的炔基、碳原子数6~12的芳基、碳原子数1~18的酰基、碳原子数7~18的芳酰基、碳原子数1~18的烷氧基、碳原子数1~18的烷硫基及卤素原子,可以举出与式(2-1)的R1表示的碳原子数1~18的烷基、碳原子数2~18的炔基、碳原子数6~12的芳基、碳原子数1~18的酰基、碳原子数7~18的芳酰基、碳原子数1~18的烷氧基、碳原子数1~18的烷硫基及卤素原子相同的基团。
作为式(2-1)中的R2,优选为氢原子或碳原子数1~18的烷基,更优选为氢原子或碳原子数1~10的烷基,进一步优选为氢原子或碳原子数1~4的烷基,特别优选为氢原子。
式(2-1)中,X表示氨基。
式(2-1)中的X表示的氨基可以为取代氨基及非取代氨基(NH2基)中的任意一种,另外,该取代氨基可以为单取代氨基及二取代氨基中的任意一种。
式(2-1)中的X优选为由下式(3-1)表示的氨基。
[化学式9]
式(3-1)中,R3及R4分别独立地表示氢原子、碳原子数1~18的烷基、碳原子数5~10的环烷基、碳原子数6~12的芳基或碳原子数7~15的芳基烷基,或者R3及R4可以彼此键合而形成构成原子数为3~12的含氮环。应予说明,R3及R4彼此键合没有形成含氮环的情况下,各R3及R4可以包含取代基X从由上述式(2-1)表示的化合物上脱离得到的残基。
作为式(3-1)的R3及R4表示的碳原子数1~18的烷基,可以举出与式(2-1)的R1表示的碳原子数1~18的烷基相同的基团,优选为碳原子数2~6的烷基。
式(3-1)的R3及R4表示的碳原子数1~18的烷基可以具有从由氨基、烷氧基、烷氧基羰基、酰基、酰氧基及羟基构成的组中选择的取代基。
对于作为式(3-1)的R3及R4表示的碳原子数1~18的烷基可以具有的取代基的氨基而言,可以举出:氨基、单或二甲基氨基、单或二乙基氨基、单或二(正丙基)氨基等烷基取代氨基;单或二苯基氨基、单或二萘基氨基等芳香族取代氨基;单烷基单苯基氨基等烷基和芳香族残基各取代一个得到的氨基或苄基氨基;以及乙酰基氨基、苯基乙酰基氨基等。
对于作为式(2-1)的R3及R4表示的碳原子数1~12的烷基可以具有的取代基的烷氧基而言,可以举出:甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、仲丁氧基及叔丁氧基等。
对于作为式(3-1)的R3及R4表示的碳原子数1~18的烷基可以具有的取代基的烷氧基羰基而言,可以举出:甲氧基羰基、乙氧基羰基、正丙氧基羰基、异丙氧基羰基、正丁氧基羰基、异丁氧基羰基、仲丁氧基羰基、叔丁氧基羰基、正戊氧基羰基、正己氧基羰基、正庚氧基羰基、正壬氧基羰基及正癸氧基羰基等。
对于作为式(3-1)的R3及R4表示的碳原子数1~18的烷基可以具有的取代基的酰基而言,例如可以举出:碳原子数1~10的烷基羰基、芳基羰基等,优选为碳原子数1~4的烷基羰基,具体而言,可以举出:乙酰基、丙酰基、三氟甲基羰基、五氟乙基羰基、苯甲酰基、萘甲酰基等。
对于作为式(3-1)的R3及R4表示的碳原子数1~18的烷基可以具有的取代基的酰氧基而言,可以举出作为式(2-1)的R3及R4表示的碳原子数1~12的烷基可以具有的取代基的酰基与氧原子键合而得到的酰氧基。
作为式(3-1)的R3及R4表示的碳原子数5~10的环烷基,可以举出:环戊基、环己基、环庚基及环辛基等,优选为碳原子数6~8的环烷基。
式(3-1)的R3及R4表示的碳原子数5~10的环烷基可以具有从由氨基、烷氧基、烷氧基羰基、酰基、酰氧基及羟基构成的组中选择的取代基,对于作为该可以具有的取代基的氨基、烷氧基、烷氧基羰基、酰基及酰氧基而言,可以举出与作为式(2-1)的R3及R4表示的碳原子数1~18的烷基可以具有的取代基的氨基、烷氧基、烷氧基羰基、酰基及酰氧基相同的基团。
作为式(3-1)的R3及R4表示的碳原子数6~12的芳基,可以举出与式(2-1)的R1表示的碳原子数6~12的芳基相同的基团,优选为碳原子数6~10的芳基。
式(3-1)的R3及R4表示的碳原子数6~12的芳基可以具有从由氨基、烷氧基、烷氧基羰基、酰基、酰氧基及羟基构成的组中选择的取代基,对于作为该可以具有的取代基的氨基、烷氧基、烷氧基羰基、酰基及酰氧基而言,可以举出与作为式(2-1)的R3及R4表示的碳原子数1~18的烷基可以具有的取代基的氨基、烷氧基、烷氧基羰基、酰基及酰氧基相同的基团。
式(3-1)的R3及R4表示的碳原子数7~15的芳基烷基是烷基上的氢原子被芳基取代得到的碳原子数为7~15的取代基,优选为碳原子数7~11的芳基烷基。作为该烷基及该芳基的具体例,可以举出与式(2-1)的R1表示的碳原子数1~18的烷基及碳原子数6~12的芳基相同的基团。
式(3-1)的R3及R4表示的碳原子数7~15的芳基烷基可以具有从由氨基、烷氧基、烷氧基羰基、酰基、酰氧基及羟基构成的组中选择的取代基,对于作为该可以具有的取代基的氨基、烷氧基、烷氧基羰基、酰基及酰氧基而言,可以举出与作为式(2-1)的R3及R4表示的碳原子数1~18的烷基可以具有的取代基的氨基、烷氧基、烷氧基羰基、酰基及酰氧基同样的基团。
式(3-1)的R3及R4可以彼此键合而形成含氮环。构成该含氮环的原子数包含氮原子在内通常为3~12个,优选为5~8个。另外,构成该含氮环的原子中可以包含多个杂原子(氮原子、氧原子及硫原子等)。
另外,式(2-1)中的X还优选为由下式(3-2)表示的取代基。
[化学式10]
式(3-2)中,n及m分别独立地为1~6的整数,优选分别独立地为2~4的整数。另外,n+m优选为4~12,更优选为4~8。
式(3-2)中,R5表示氢原子、碳原子数1~18的烷基、碳原子数1~18的烷氧基、碳原子数5~10的环烷基、碳原子数5~10的环烷氧基、碳原子数6~12的芳基、碳原子数6~12的芳氧基、碳原子数7~15的芳基烷基、碳原子数7~15的芳基烷氧基或碳原子数1~18的酰基,还可以包含取代基X从由上述式(2-1)表示的化合物上脱离得到的残基。
作为式(3-2)的R5表示的碳原子数1~18的烷基、碳原子数1~18的烷氧基、碳原子数6~12的芳基及碳原子数1~18的酰基,可以举出与式(2-1)的R1表示的碳原子数1~18的烷基、碳原子数1~18的烷氧基、碳原子数6~12的芳基及碳原子数1~18的酰基相同的基团。
作为式(3-2)的R5表示的碳原子数5~10的环烷基及碳原子数7~15的芳基烷基,可以举出与式(2-1)的R3及R4表示的碳原子数5~10的环烷基及碳原子数7~15的芳基烷基相同的基团。
式(3-2)的R5表示的碳原子数5~10的环烷氧基是环烷基与氧原子键合得到的碳原子数为5~10的取代基,作为该环烷基的具体例,可以举出与式(2-1)的R3及R4表示的碳原子数5~10的环烷基相同的基团。
式(3-2)的R5表示的碳原子数6~12的芳氧基是芳基与氧原子键合得到的碳原子数为6~12的取代基,作为该芳基的具体例,可以举出与式(2-1)的R1表示的碳原子数6~12的芳基相同的基团。
式(3-2)的R5表示的碳原子数7~15的芳基烷氧基是烷氧基上的氢原子被芳基取代得到的碳原子数为7~15的取代基,作为该烷氧基及芳基的具体例,分别可以举出与式(2-1)的R1表示的碳原子数1~18的烷氧基及碳原子数6~12的芳基相同的基团。
作为本发明的感光性树脂组合物含有的(A)成分,特别优选由下式(4-1)或(4-2)表示的化合物。
[化学式11]
[化学式12]
式(4-1)及(4-2)中,R1分别独立地表示与式(2-1)中的R1相同的含义。作为式(4-1)及(4-2)中的R1,优选分别独立地为碳原子数1~18的烷氧基,更优选两者为相同的碳原子数1~18的烷氧基,进一步优选两者为相同的碳原子数1~4的烷氧基,特别优选两者均为甲氧基。
式(4-1)及(4-2)中,R2分别独立地表示与式(2-1)中的R2相同的含义。作为式(4-1)及(4-2)中的R2,优选为氢原子。
式(4-1)及(4-2)中,n分别独立地表示0~4的整数,优选为1~2的整数,更优选为2。p表示1~6的整数,优选为2~4的整数,更优选为3。
将(A)成分含有的由上述式(2-1)表示的化合物的具体例示于下式(8-1)~(8-6),但是,本发明并不限定于这些例子。
[化学式13]
本发明的感光性树脂组合物含有的(B)成分是:使(a)1分子中具有至少2个以上环氧基的环氧化合物(以下,仅记载为“原料化合物(a)”)和(b)1分子中具有至少1个以上羟基和1个羧基的化合物(以下,仅记载为“原料化合物(b)”)的反应物、与(c)多元酸酐(以下,仅记载为“原料化合物(c)”)反应得到的环氧化合物。
此处,作为原料化合物(a),只要1分子中具有至少2个以上环氧基的环氧化合物即可,没有特别限定,例如可以举出:酚醛清漆型环氧树脂、双酚型环氧树脂、三酚甲烷型环氧树脂、三(2,3-环氧丙基)异氰脲酸酯、联苯二缩水甘油醚、脂环式环氧树脂、共聚型环氧树脂等。
酚醛清漆型环氧树脂可以通过如下公知的方法得到:使例如苯酚、甲酚、卤代酚及烷基酚等酚类与甲醛、乙醛等醛类在酸性催化剂下进行反应,得到酚醛清漆类,使该酚醛清漆类与表氯醇、表溴醇等表卤醇类反应而得到酚醛清漆型环氧树脂,不过,还可以直接使用市售品。作为该市售品的具体例,可以举出:EOCN-103、EOCN-104S、EOCN-102、EOCN-1027、EOCN-4400H、EPPN-201及BREN-S(商品名、日本化药株式会社制)、DEN-431及DEN-439(商品名、Dow Chemical公司制)、N-730、N-770、N-865、N-665、N-673及VH-4150(商品名、DIC株式会社制)、YDCN-700-3、YDCN-700-5、YDCN-700-7及YDCN-700-10(商品名、新日铁住金化学株式会社制)等。
双酚型环氧树脂可以通过如下公知的方法得到:使例如双酚A、双酚F、双酚S及四溴双酚A等双酚类与表氯醇、表溴醇等表卤醇类进行反应,或者使双酚A、双酚F等双酚类的二缩水甘油醚和所述双酚类形成的缩合物与表氯醇、表溴醇等表卤醇类进行反应,从而得到双酚型环氧树脂,不过,还可以直接使用市售品。作为该市售品的具体例,可以举出:jER1004、jER1002、jER4002及jER4004(商品名、JER株式会社制)等。
三酚甲烷型环氧树脂可以通过如下公知的方法得到:使例如三苯酚甲烷、三甲酚甲烷等三(羟基)芳基甲烷类与表氯醇、表溴醇等表卤醇类进行反应而得到三酚甲烷型环氧树脂,不过,还可以直接使用市售品。作为该市售品的具体例,可以举出:EPPN-501、EPPN-501HY及EPPN-502(商品名、日本化药株式会社制)等。
作为脂环式环氧树脂,例如可以举出:Celloxide 2021及EHPE3150(商品名、Daicel化学工业株式会社制)、E-1031S(商品名、JER株式会社制)、日本曹达(株)制、EPB-13及EPB-27(商品名、日本曹达株式会社制)等。
作为共聚型环氧树脂,例如可以举出:CP-50M及CP-50S(商品名、日本油脂株式会社制、甲基丙烯酸缩水甘油酯、苯乙烯以及甲基苯乙烯的共聚物)、甲基丙烯酸缩水甘油酯和环己基马来酰亚胺等的共聚物等。
其中,作为本发明中使用的原料化合物(a),优选甲酚酚醛清漆型的环氧树脂。
作为原料化合物(b),例如可以举出:二羟甲基丙酸、二羟甲基乙酸、二羟甲基丁酸、二羟甲基戊酸、二羟甲基己酸等多羟基单羧酸类;羟基新戊酸、对羟基苯甲酸等单羟基单羧酸类等。这些物质可以2种以上并用。
其中,作为本发明中使用的原料化合物(b),优选二羟甲基丙酸。
关于原料化合物(a)和原料化合物(b)的反应,相对于原料化合物(a)中的环氧基1摩尔而言,优选使用原料化合物(b)中的羧酸为0.01~0.5摩尔的量,更优选使用羧酸为0.1~0.3摩尔的量。反应温度通常为60~150℃,反应时间通常为5~30小时。
另外,以下将原料化合物(a)和原料化合物(b)的反应物记载为“中间体(ab)”。
作为原料化合物(c),例如可以举出由下式表示的化合物等。这些化合物可以2种以上并用。
[化学式14]
其中,作为本发明中使用的原料化合物(c),优选由下式表示的化合物。
[化学式15]
关于中间体(ab)和原料化合物(c)的反应,相对于中间体(ab)中的羟基1摩尔而言,优选使用0.1~1.0摩尔的原料化合物(c)。反应温度通常为60~150℃,反应时间通常为3~24小时。
在上述原料化合物(a)和(b)的反应时和/或中间体(ab)和原料化合物(c)的反应时,优选使用有机溶剂作为稀释剂。作为该有机溶剂的具体例,可以举出:乙基甲基酮、环己酮及环戊酮等酮类;甲苯、二甲苯及四甲基苯等芳香族烃类;二丙二醇二甲醚及二丙二醇二乙醚等二醇醚类;乙酸乙酯、乙酸丁酯、丁基溶纤剂乙酸酯及乙酸卡必醇酯等酯类;辛烷及癸烷等脂肪族烃;石油醚、石脑油、氢化石脑油及溶剂石脑油等石油系溶剂等。
另外,为了促进反应,例如使用三苯基膦、苄基二甲胺、甲基三乙基氯化铵、三苯基及辛酸铬等催化剂也是优选的方案。使用催化剂的情况下,优选通过在反应结束后使用有机过氧化物等进行氧化处理而使所使用的催化剂实质上钝化。催化剂的使用量相对于反应原料混合物而言优选为0.1~10质量%。
进而,为了防止反应中的聚合,还优选并用例如对苯二酚、甲基对苯二酚、对甲氧基苯酚、邻苯二酚及邻苯三酚等阻聚剂,其使用量相对于反应原料混合物而言优选为0.01~1质量%。
作为这样得到的(B)成分,优选由下式(5-1)表示的环氧化合物:
[化学式16]
(式(5-1)中,r为括弧内的重复单元数的平均值,表示1以上的实数。s为括弧内的重复单元数的平均值,表示0以上的实数。其中,r与s的和为30以下。D1及D2分别独立地表示由下式(6-1)~(6-10):
[化学式17]
表示的二价连接基团中的任意一种。),更优选D1及D2为由上述式(6-1)表示的二价连接基团的环氧化合物。
关于本发明的感光性树脂组合物中的(A)成分及(B)成分的含量,相对于(B)成分100质量份,(A)成分通常为1质量份~60质量份,优选为2质量份~30质量份。(A)成分相对于100质量份(B)成分的配合量低于1质量份的情况下,反应有时会不充分,而超过60质量份的情况下,不仅(A)成分自身有可能对(A)成分的溶解性造成较大的影响,而且感光性树脂组合物的成本相对变高。
本发明的感光性树脂组合物中可以并用(C)碱增殖剂(以下,还有时仅记载为“(C)成分”)。(C)成分是能够在通过照射活性能量线而由(A)成分释放的极少量的碱的作用下,最终其总量自增殖性分解而产生大量碱的化合物。
可并用的(C)成分只要是能够在由(A)成分释放的碱的作用下分解而产生碱的化合物即可,没有特别限定,优选为其结构中含有至少1个尿烷键的尿烷系化合物。该尿烷系化合物的特征是:因源自(A)成分的氨基的碱(氨或胺)的作用而分解,产生源自尿烷键的碱(氨或胺)。
作为本发明的感光性树脂组合物中可并用的(C)成分,更优选具有由下述通式(7-1)表示的碱增殖基的化合物。
[化学式18]
将具有由上述式(7-1)表示的碱增殖基的(C)成分的具体例示于下式(9-1)~(9-6),但并不限定于此。
[化学式19]
这些(C)成分可以仅使用1种,还可以将2种以上混合使用。
本发明的感光性树脂组合物中的(C)成分的含量相对于(B)成分100质量份而言,通常为60质量份以下,优选为1~30质量份。如果加入1质量份以上的(C)成分,则能够使(B)成分迅速反应。另一方面,如果是60质量份以下、优选为30质量份以下,则(C)成分自身不会对(B)成分的溶解性造成较大的影响,能够抑制感光性树脂组合物的成本。
本发明的感光性树脂组合物中,还可以根据需要使用溶剂、反应性环氧单体、光敏剂、无机填充剂、着色剂、阻聚剂、增粘剂、消泡剂、密接性赋予剂、流平剂及光自由基引发剂等添加剂中的1种,或者将多个组合并用。配合添加剂时的配合量相对于(A)成分100份而言,优选合计为0.01~20质量份。
本发明的感光性树脂组合物可以溶解在有机溶剂中而制备感光性树脂组合物溶液。可并用的有机溶剂没有特别限制,例如可以举出:二乙醚、四氢呋喃及二噁烷等代表的醚类;乙二醇单甲醚、乙二醇单乙醚及二乙二醇单乙醚等代表的二醇单醚类(所谓的溶纤剂类);甲基乙基酮、丙酮、甲基异丁基酮、环戊酮及环己酮等代表的酮类;乙酸乙酯、乙酸丁酯、乙酸正丙酯及乙酸异丙酯、丙二醇单甲醚乙酸酯等代表的酯类;甲醇、乙醇、异丙醇、丁醇、环己醇、乙二醇及甘油等代表的醇类;二氯甲烷、氯仿、1,1-二氯乙烷、1,2-二氯乙烷及1-氯丙烷、氯苯等代表的卤代烃类;N,N-二甲基甲酰胺、N,N-二甲基乙酰胺及N-甲基吡咯烷酮等代表的酰胺类;γ-丁内酯等代表的内酯类;二甲基亚砜等代表的亚砜类;己烷、环己烷及庚烷等代表的链状或环状饱和烃类;其它的有机极性溶剂类。进而,作为有机溶剂,可以举出:苯、甲苯及二甲苯等代表的芳香族烃类;以及其它的有机非极性溶剂类。这些有机溶剂可以单独使用1种,或者将2种以上组合使用。其中,从(A)成分的溶解性容易变得良好的方面考虑,优选酰胺类、内酯类、亚砜类、酯类、酮类及醇类。
为了改良图案的性能、抗蚀剂的反应性、固化膜的物性等的目的,可以在本发明的感光性树脂组合物中并用反应性环氧单体。本说明书中,所谓反应性环氧单体,是指重均分子量为约1000以下且在室温下为液体或半固体状的具有环氧基的化合物,作为其具体例,可以举出:二乙二醇二缩水甘油醚、己二醇二缩水甘油醚、二羟甲基丙烷二缩水甘油醚、聚丙二醇二缩水甘油醚(株式会社ADEKA制、ED506)、三羟甲基丙烷三缩水甘油醚(株式会社ADEKA制、ED505)、三羟甲基丙烷三缩水甘油醚(低氯型、Nagase ChemteX株式会社制、EX321L)、季戊四醇四缩水甘油醚、双酚A二缩水甘油醚、双酚F二缩水甘油醚及3,4-环氧环己烯基甲基-3',4'-环氧环己烯羧酸酯(Daicel化学工业株式会社制、Celloxide 2021P)等。这些物质可以单独使用,或者2种以上混合使用。反应性环氧单体为液体的情况下,如果相对于树脂组合物的总量配合大于20质量%的量,则除去溶剂后的被膜会产生粘性,容易发生掩膜粘接等,并不合适。从这方面考虑,本发明的树脂组合物中的反应性环氧单体的配合比例优选在感光性树脂组合物中为20质量%以下。
作为可并用的光敏剂,例如优选噻吨酮类、在9位和10位具有烷氧基的蒽化合物(9,10-二烷氧基蒽衍生物)。作为所述烷氧基,例如可以举出:甲氧基、乙氧基、丙氧基、丁氧基等C1~C4的烷氧基。9,10-二烷氧基蒽衍生物还可以具有取代基。作为取代基,例如可以举出:氟原子、氯原子、溴原子、碘原子等卤素原子;甲基、乙基、丙基等碳原子数1~4的烷基;磺酸烷基酯基、羧酸烷基酯基等。作为磺酸烷基酯基、羧酸烷基酯中的烷基,例如可以举出:甲基、乙基、丙基等碳原子数1~4的烷基。这些取代基的取代位置优选为2位。
作为可并用的无机填充剂,例如可以举出:硫酸钡、钛酸钡、氧化硅粉、微粉状氧化硅、无定形二氧化硅、滑石、粘土、碳酸镁、氧化铝、氢氧化铝、云母等公知的物质,为了提高固化物与基材的密接性、固化物的硬度等各种物性的目的而使用上述无机填充剂。
作为可并用的着色剂,例如可以举出:酞菁蓝、酞菁绿、碘绿、双偶氮黄、结晶紫、氧化钛、炭黑、萘黑等。
作为可并用的阻聚剂,例如可以举出:对苯二酚、对苯二酚单甲醚、叔丁基邻苯二酚、邻苯三酚、吩噻嗪等。
作为可并用的增粘剂,例如可以举出:石棉、Orbene、Benton、蒙脱石等。
作为可并用的消泡剂,例如可以举出:有机硅系、氟系及高分子系等的消泡剂。
作为可并用的密接性赋予剂,可以使用硅烷偶联剂或钛偶联剂等偶联剂,优选举出硅烷偶联剂。
使用感光性树脂组合物的基材没有特别限制,作为其具体例,可以举出:聚对苯二甲酸乙二醇酯、聚对苯二甲酸丁二醇酯、聚对苯二甲酸四亚甲酯、聚萘二甲酸乙二醇酯等聚酯系基材;缩合型聚酰亚胺、加成型聚酰亚胺、高温加成型聚酰亚胺等聚酰亚胺系基材;BA型环氧树脂、BF型环氧树脂、苯氧树脂等环氧树脂系基材;苯酚酚醛清漆树脂、甲酚酚醛清漆树脂、聚羟基苯乙烯等酚醛树脂系基材;聚乙烯、聚丙烯、聚苯乙烯、聚环烯烃等聚烯烃系基材;尼龙6,6、尼龙6、尼龙6,T、尼龙4,6、尼龙12、尼龙6,12等聚酰胺系基材等,以及聚氨酯系、聚碳酸酯系、聚缩醛系、聚苯醚系、聚(甲基)丙烯酸酯系、丙烯腈-丁二烯-苯乙烯共聚物系、聚苯硫醚系、聚醚醚酮系、聚醚酰亚胺系、聚醚砜系、聚苯并噁唑系等基材;由玻璃纤维等强化后的树脂基材;Si、Cu、Ag、Au、Ni、Pd、Co、Rh、Fe、In、Sn等金属系基材等。对于本实施方式的感光性树脂组合物而言,在以膜的形式形成在基材上时,高温下的烧结工序不是必须的。因此,基材的耐热性等没有限制。因此,可以将如上所述的各种树脂用作基材。
使用感光性树脂组合物的基材的形态没有特别限制,作为其具体例,例如可以举出:膜、片材、带、微粒、层叠板、立体成型品、以及将Cu、Ag、Au、Ni、Pd、Co、Rh、Fe、In、Sn等金属图案化得到的印刷线路板、膜及带等。
将本发明的感光性树脂组合物涂布于基材的方法没有特别限制,作为其具体例,可以举出:喷墨法、喷雾法、旋涂法、辊涂法、静电涂装法、帘式涂布法、柔版印刷法、凹版印刷法、平版印刷法、凹版胶印法、丝网印刷法等公知的方法。其中,优选柔版印刷法及凹版印刷法。通过利用这些印刷法将感光性树脂组合物涂布于基材,能够以高位置精度形成适合于图案化的膜厚的保护膜。
本发明的另一个方案提供一种具备通过前述的本发明的一个方案所涉及的制造方法得到的基材的电子部件。由前述的方法得到的、形成有图案的基材具有如下优点:与例如通过丝网印刷形成了图案的基材相比,能够形成精细的图案;与使用了非感光性绝缘材料的基材相比,能够减少工时,并且非常简便。这种基材能够优选用作柔性配线基板、IC标签天线电路基板等电子部件。更具体而言,可以应用于RFID用IC标签的天线电路、柔性、硬性、软硬结合等的印刷线路板的电路、电磁波屏蔽用微细配线、半导体的配线、晶体管的配线、电容器的配线、电阻器的配线、电池的配线及电极、有机EL显示器中的配线及电极、无机EL显示器中的配线及电极、数字标牌中的配线及电极、电子纸中的配线及电极、液晶显示器中的配线及电极、等离子显示器的配线及电极、有机EL等面发光照明的配线及电极等用途。
本发明的图案形成方法的特征是:使用上述的含有(A)成分、(B)成分、并且根据需要含有(C)成分的感光性树脂组合物。例如将本发明的感光性树脂组合物溶解在有机溶剂中制作涂布液,将该涂布液涂布在基板等支撑体上,干燥而形成涂膜。接下来,对该涂膜进行图案曝光,使其产生碱。接下来,进行加热处理,使其进行碱反应性树脂的反应。反应结束后,在溶剂(显像液)中浸渍进行显像,由此得到规定形状的固化树脂图案,其中,溶剂(显像液)会在曝光部和未曝光部产生溶解度差异。
加热处理的条件可根据曝光能量、使用的光产碱剂的种类、碱可溶性环氧化合物适当设定。加热温度通常为50~250℃,优选为60~130℃。加热时间优选为10秒~60分钟,更优选为60秒~30分钟。
实施例
以下,利用实施例对本发明详细地进行说明,但是,这些实施例只不过是用于适当地说明本发明的示例,不会对本发明作任何限定。应予说明,合成例及实施例中的份为质量份。
合成例1(4,5-二甲氧基-2-硝基苄基醇的合成)
在具备搅拌机、回流冷却管及搅拌装置的烧瓶中放入4,5-二甲氧基-2-硝基苄基醛12.5份、四氢硼酸钠1.5份及甲醇250份,在室温(23℃)下搅拌3小时后,加入饱和氯化铵溶液38份。然后,过滤回收析出的黄色固体,在滤液中加入氯仿120份进行萃取操作,然后,蒸馏除去溶剂而得到灰色固体。将得到的固体用乙酸乙酯重结晶,由此,得到4,5-二甲氧基-2-硝基苄基醇的黄色固体8.4份。
合成例2(光产碱剂A-1(由上述式(8-3)表示的化合物)的合成)
将合成例1中得到的4,5-二甲氧基-2-硝基苄基醇8.9份、甲苯150份及辛酸锡0.02份放入烧瓶中,进行回流搅拌直至均匀。接下来,在回流下加入异佛尔酮二异氰酸酯4.6份,继续进行回流3小时,然后,冷却,用蒸发器蒸馏除去溶剂。将得到的褐色固体用乙醇重结晶,由此,得到光产碱剂A-1 6.8份。
合成例3(2-硝基-4,5-二甲氧基苄基4’-硝基苯基碳酸酯的合成)
将合成例1中得到的4,5-二甲氧基-2-硝基苄基醇13.0份、三乙基胺12.3份及THF 60份放入烧瓶中,搅拌均匀后,经20分钟滴加对硝基苯基氯甲酸酯的THF溶液55份。滴加结束后,在室温下搅拌3小时,将反应溶液投入水中,用二氯甲烷萃取。将有机层用5质量%HCl水溶液、饱和碳酸氢钠水溶液及饱和食盐水依次清洗后,将有机层用无水硫酸镁干燥,用蒸发器蒸馏除去溶剂。将得到的固体用甲苯重结晶,减压干燥得到2-硝基-4,5-二甲氧基苄基4’-硝基苯基碳酸酯的黄色固体17.6份。
合成例4(光产碱剂A-2(由上述式(8-4)表示的化合物)的合成)
将合成例3中得到的2-硝基-4,5-二甲氧基苄基4’-硝基苯基碳酸酯1.0份、1-羟基三唑0.13份及二氯甲烷60ml放入烧瓶中,边回流,边经30分钟滴加1,3-二-4-哌啶基丙烷的二氯甲烷溶液20ml,然后,回流搅拌4小时。反应结束后,用饱和碳酸氢钠水溶液及饱和食盐水依次清洗,对有机层进行萃取并用无水硫酸镁干燥后,用蒸发器蒸馏除去溶剂,由此得到黄色固体。将得到的固体在过量的甲醇中搅拌后,过滤,将得到的固体用2-丙醇重结晶,由此得到光产碱剂A-2的黄色固体0.25份。
合成例5(碱可溶性环氧化合物B-1的合成)
依据日本特许第4,913,143号的段落[0058]中的“碱可溶性环氧化合物的合成例”的记载,合成碱可溶性环氧化合物(B-1)。应予说明,碱可溶性环氧化合物B-1是由式(5-1)表示的化合物,并且是D1及D2均为式(6-1)的化合物。
合成例6(碱增殖剂C(由上述式(9-4)表示的化合物)的合成)
将氯甲酸9-芴基甲酯10.0份及THF放入烧瓶中,进行搅拌直至均匀。将该溶液用冰浴冷却至2℃后,边冷却,边经20分钟滴加溶解有1,3-双(3-氨基丙基)四甲基二硅氧烷9.6份的THF溶液35份,搅拌3小时。在得到的溶液中加入氯仿60份,用5质量%HCl水溶液、饱和碳酸氢钠水溶液及饱和食盐水依次清洗,对有机层进行萃取并用硫酸镁干燥后,用蒸发器蒸馏除去溶剂,由此得到白色固体。将得到的固体用乙醇重结晶,由此得到由上述式(9-4)表示的化合物、即碱增殖剂C的白色固体10份。
实施例1~4、比较例5~8
(感光性树脂组合物的制备)
按照表1中记载的配合量将各成分混合,得到感光性树脂组合物。
[表1]
(A-1):合成例2中得到的光产碱剂
(A-2):合成例4中得到的光产碱剂
(B-1):合成例5中得到的碱可溶性环氧化合物
(B-2):SU-8(日本化药株式会社制、双酚A酚醛清漆型环氧化合物)
(B-3):EOCN-4400H(日本化药株式会社制、邻甲酚酚醛清漆型环氧化合物)
(B-4):NER-7604(日本化药株式会社制、双酚F型环氧化合物)
(B-5):EHPE-3150(株式会社Daicel制、脂环式环氧化合物)
(C):合成例6中得到的碱增殖剂(由上述式(9-4)表示的化合物)
(D-1):ED-506(株式会社ADEKA制)
(E):S-510(Chisso株式会社制)
(F):Megafac F-470(DIC株式会社制)
(G):环戊酮
感光性树脂组合物的图案化
将实施例1~4及比较例5~8的各树脂组合物用旋涂机涂布在Si基板上后,利用热板于100℃预烘烤2分钟进行干燥,得到膜厚10μm的树脂组合物层。然后,使用i射线曝光装置(Mask Aligner:Ushio电机公司制)进行图案曝光(软接触、宽带曝光),照射900~3000mJ/cm2的UV光。接下来,利用热板进行烘烤,然后,使用显像液利用浸渍法进行显像处理,在基板上得到固化而成的树脂图案。将曝光后的加热温度、加热时间、显像溶剂及显像时间记载在表2中。
[表2]
感光性树脂组合物的残膜率评价
用触针式膜厚测定器测定上述“感光性树脂组合物的图案化”中得到的图案的膜厚,将各曝光量下的残膜率(曝光前的膜厚为1的情形下的、图案化后得到的图案的膜厚)示于图1、图2。实施例1~4的残膜率约为1,大致维持曝光前的膜厚,与此相对,比较例的残膜率相当低,可知在使用光产碱剂的体系中,实施例的感光性树脂组合物非常优异。
感光性树脂组合物的分辨率评价
测定上述“感光性树脂组合物的图案化”中得到的图案的线宽,将各曝光量下的分辨率(与基板紧密接触的最细图案的线宽)示于图3、图4。其中,关于因显像而流失使得基板上没有残留图案的例子,使分辨率为0。由图3、图4可知:当使用实施例的组合物时,与使用比较例的组合物的情形相比,分辨率高。
本发明的感光性树脂组合物能够碱显像,并且,图像分辨率、灵敏度、保存稳定性优异,此外,该树脂组合物的固化物具有热稳定性优异的特性,在要求金属基板的耐腐蚀性的领域中非常有用。
- 还没有人留言评论。精彩留言会获得点赞!
- 着色感光性树脂组合物、包含其的滤色器和显示装置的制造方法
- 红色感光性树脂组合物、使用其制造的滤色器和包含该滤色器的显示元件的制造方法与工艺
- 药液除气装置的制造方法
- 负型感光性树脂组合物、树脂固化膜、隔壁和光学元件的制造方法与工艺
- 感光性树脂组合物、光刻胶层叠体以及它们的固化物(11)的制造方法与工艺
- 感光性非电解镀基底剂的制造方法与工艺
- 感光性树脂组合物、感光性膜、图案基板、感光性导电膜及导电图案基板的制造方法与工艺
- 着色感光性树脂组合物的制造方法与工艺
- 一种感光性树脂组合物及其应用的制造方法与工艺
- 负型感光性树脂组合物、使其固化而成的固化膜及其制造方法、以及具有其的光学设备及背面照射型CMOS图像传感器与制造工艺
- 负型感光性树脂组合物、树脂固化膜、隔壁和光学元件的制造方法与工艺
- 感光性树脂组合物、光刻胶层叠体以及它们的固化物(11)的制造方法与工艺
- 感光性树脂组合物、感光性膜、图案基板、感光性导电膜及导电图案基板的制造方法与工艺
- 着色感光性树脂组合物的制造方法与工艺
- 一种感光性树脂组合物及其应用的制造方法与工艺
- 负型感光性树脂组合物、使其固化而成的固化膜及其制造方法、以及具有其的光学设备及背面照射型CMOS图像传感器与制造工艺
- 着色感光树脂组合物以及使用其的滤色器的制造方法与工艺
- 黑色感光性树脂组合物及其应用的制造方法与工艺
- 含芴的感光性树脂、其制备方法及具有其的光固化组合物和光刻胶与制造工艺
- 感光性树脂层叠体卷的制造方法与工艺
- 负型感光性树脂组合物、树脂固化膜、隔壁和光学元件的制造方法与工艺
- 感光性树脂组合物、光刻胶层叠体以及它们的固化物(11)的制造方法与工艺
- 感光性树脂组合物、感光性膜、图案基板、感光性导电膜及导电图案基板的制造方法与工艺
- 着色感光性树脂组合物的制造方法与工艺
- 一种感光性树脂组合物及其应用的制造方法与工艺
- 负型感光性树脂组合物、使其固化而成的固化膜及其制造方法、以及具有其的光学设备及背面照射型CMOS图像传感器与制造工艺
- 着色感光树脂组合物以及使用其的滤色器的制造方法与工艺
- 黑色感光性树脂组合物及其应用的制造方法与工艺
- 含芴的感光性树脂、其制备方法及具有其的光固化组合物和光刻胶与制造工艺
- 感光性树脂层叠体卷的制造方法与工艺