一种用于骨植入物的可降解复合材料的制作方法
本发明涉及骨再生领域,尤其是涉及一种用于骨植入物的可降解复合材料。
背景技术:
骨科手术中,常需要植入固定材料以便骨质修复和再生,传统的植入骨内的固定材料以金属为主,如钛合金、不锈钢等,这种固定材料需要在骨修复后进行二次手术取出。现今,研究者们将可降解材料纳入植入固定材料的课题。
中国专利文献cn102908672a,公开了一种“高强度可吸收镁基复合骨科内固定器及制备方法”,该专利文献中,在具有一定结构的低孔隙率多孔镁合金基体内填充聚乳酸高分子材料,为可提高植入固定材料的强度,同时为也为降低镁合金的用量,尽量避免溶骨的现象。中国专利文献cn103330959a,公开了一种“预应力增强的轻质高强可控降解医用复合材料及制备方法”,该专利文献中,将经预应力处理过的镁合金丝材作为增强相,但是,由于植入材料中,仍然利用镁合金做基体,其镁合金的用量仍然很高,较为活泼的镁在液体环境内发生电化学反应,大量的金属镁与体液发生反应生成氢气,并未彻底解决溶骨的问题,而且,为了增加机械强度,采用的是镁合金,镁合金中其他成分或元素,并未对骨质修复起到积极作用,造成了浪费。
技术实现要素:
为解决以上技术问题,本发明设计了一种可完全降解的复合材料,该复合材料中可降解的聚己内酯为基体,镁为填充料,能有效控制镁离子的释放速率,促进骨自生长,也避免了溶骨的现象。
本发明是采用如下方案实现的:
一种用于骨植入物的可降解复合材料,成分包括镁和聚己内酯,所述镁 单质与所述聚己内酯的配比为1:2~1:50。。
本发明中,聚己内酯为无毒害可降解物质,在体内与生物细胞相容性好,其降解后产物为二氧化碳和水,并且具有较好的加工性能,能适用于传统的挤出、吹塑、注塑等加工方法。但是同时,聚己内酯较为柔软,具有极大的伸展性,刚性、机械性能不足。镁元素是骨细胞生长必备元素,但是镁合金做支架,镁腐蚀速度过快,又容易产生溶骨现象。因此本发明将少量镁与聚己内酯均匀混合,既能增加聚己内酯材料的机械性能,又由于聚己内酯在生物体内能缓慢且稳定降解,可有效且均匀的控制镁离子的释放速率,有助于骨质细胞生长,又不会发生溶骨现象。
优选地,所述镁包括表面改性过的镁和表面未改性过的镁。
更优选地,所述表面改性过的镁为利用γ-甲基丙烯酰氧丙基三甲氧基硅烷改性过的镁。
更有选地,所述表面改性过的镁与所述表面未改性过的镁的比例为1:9~1:11。
其中,所述镁的粒度为30μm~300μm。
镁活性很高,尤其是在粒径很小时,比表面积大,非常容易氧化,并且溶液发生团聚,不易分散,而镁粒子太大时,释放速度又太快。因此需要对镁进行适度改性和控制镁粒子的粒径范围,一方面是防止镁大量氧化,另一方面镁粒子表面改性过后,不容易集结成块,粒子更加均匀,有助于控制镁粒子的释放速度。
附图说明
图1为镁粒度为45μm时,镁含量与聚己内酯含量比为1:10、2:10、3:10的时候压缩模量
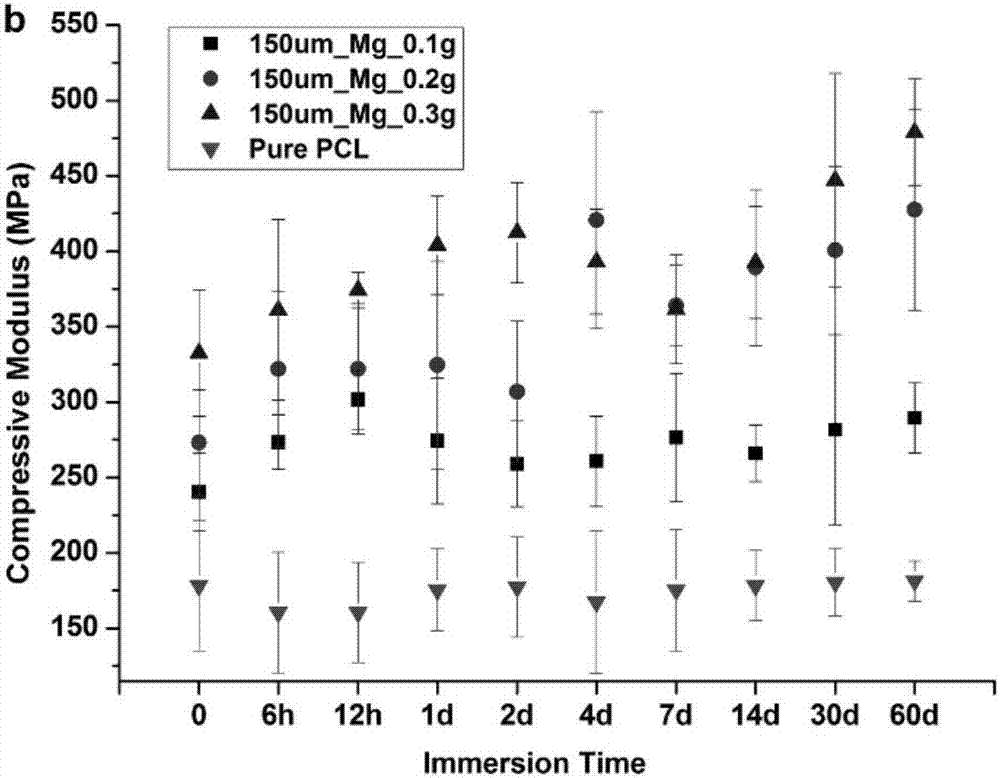
图2为镁粒度为150μm时,镁含量与聚己内酯含量比为1:10、2:10、3:10的时候压缩模量
图3为镁粒子为45μm时,随着时间的积累,模拟体液内镁离子的累积含量
图4为镁粒子为150μm时,随着时间的积累,模拟体液内镁离子的累积含量
图5第一天时,镁粒子分别为45μm和150μm模拟体液内细胞的活性
图6第三天时,镁粒子分别为45μm和150μm模拟体液内细胞的活性
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
实施例1、
本实施例采用两组实验,来进行对比并分析。
第一组为,采用粒径为45μm的金属镁粒子,所采用的镁粒子均由γ-甲基丙烯酰氧丙基三甲氧基硅烷表面改性;第二组为,采用粒径为150μm的金属镁粒子,所采用的镁粒子均由γ-甲基丙烯酰氧丙基三甲氧基硅烷表面改性。
本实施例是在60℃时,将两组镁粒子混合于聚己内酯中,然后在模拟体液中浸泡,测得各种数据。
图1是第一组实验,镁与聚己内酯质量比为1:10、2:10、3:10的时候压缩模量。图2是第二组实验,镁与聚己内酯质量比为1:10、2:10、3:10的时候压缩模量。
根据图1所得知,第一组实验中,镁与聚己内酯形成的复合材料的机械性能,均达到了松质骨的机械强度,而且比纯聚己内酯的机械性能高49%,镁的含量越多聚己内酯复合材料的机械性能越好。
根据图2中所得知,第二组实验中,镁与聚己内酯形成的复合材料的机械性能与第一组,机械性能也达到了松质骨的机械强度,并且对比图2与图1 得知,镁粒径在45μm或150μm,对压缩模量影响不大。
图3为第一组实验,镁粒子为45μm时,随着时间的积累,模拟体液内镁离子的累积含量;图4第二组实验,为镁粒子为150μm时,随着时间的积累,模拟体液内镁离子的累积含量。
由图3中可得知,在第一组实验中,模拟体液中,镁离子的累积从6h的30ppm到2个月的199ppm,说明镁粒子释放可以有效的得到控制,说明随着时间的积累,模拟体液中镁粒子的含量在稳定增长,镁粒子是以比较稳定的速度释放的。
图4为第二组实验中,模拟体液内的镁离子的累积变化。由图3对比图4可以得出,镁粒径在一定的范围内变化,对释放速度没有大的影响,这是由于聚己内酯在稳定的缓慢的降解,有效的控制了混合于聚己内酯内的镁的释放速度,也即镁粒子的释放速度受聚己内酯降解速度的制约。
图5为24小时后,第一组实验和第二组实验所培育的骨细胞的活性,图6为72小时后,第一组实验和第二组实验所培育的骨细胞的活性。
由图5可以得知,模拟体液中,mg/聚己内酯复合材料要比纯聚己内酯对细胞的影响要好,mg/聚己内酯复合材料培养的细胞活性要比纯聚己内酯培育的细胞活性好。镁与聚己内酯复合材料培育的细胞活性比纯聚己内酯高出30%到160%。
本实施例为本发明的最佳实施例,但实际应用中不仅限于这两种粒径的粒子。
本实施例中,采用的是粒径为45μm的镁粒子和粒径为150μm的镁粒子均由γ-甲基丙烯酰氧丙基三甲氧基硅烷表面改性,目的是为了防止镁粒子发生聚合,并且在与聚己内酯混合的过程中,在聚己内酯材料中分散均匀。
在实际应用中,可采用粒径更大的镁粒子,如300μm的镁粒子,当镁粒子更大时,镁粒子之间不易发生团聚,这样可以采用改性后的镁与未改性的镁混合使用,表面改性的镁与表面未改性的镁在1:9~1:11的范围内,这样未改性的镁适度的氧化会在模拟体液中发生复分解反应,调节体液的酸碱性。 而实际应用中也可以采用更小的镁粒子,如30μm或者甚至于纳米级的镁粒子,将镁粒子全部改性,也可以有效的控制镁的释放速率及提高机械性能和细胞活性。
在实际应用中,镁与聚己内酯的配比在1:2到1:50之间的范围内,均能达到有效控制镁释放速率和提高机械性能及细胞活性。
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应该以权利要求的保护范围为准。
- 还没有人留言评论。精彩留言会获得点赞!