从龙脷叶中同时分离槲皮素‑3‑O‑龙胆二糖苷和山柰酚‑3‑O‑龙胆二糖苷的方法与流程
本发明涉及一种植物化合物分离提纯方法,具体涉及从龙脷叶中同时分离槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷的方法,属于中药技术领域。
背景技术:
龙脷叶Sauropus rostratus系大戟科守宫木属植物,又名龙舌叶、龙味叶、龙利叶、牛耳叶,主要分布在广东、广西、福建等地,原产于越南北部,马来半岛有栽培。具有清热润肺、化痰止咳之功效,民间用于治疗肺热咳喘痰多、口干、便秘等疾病。目前对龙利叶的报道仅限于一些初步探讨,对其化学成分及其药理活性的研究较少。而龙脷叶中槲皮素-3-O-龙胆二糖苷与山柰酚-3-O-龙胆二糖苷在中药技术领域中有至关重要作用。
槲皮素-3-O-龙胆二糖苷(Quercetin 3-O-gentiobioside),分子式为C27H30O17,分子量为626.52,结构式如下:
山柰酚-3-O-龙胆二糖苷(Kaempferol 3-O-diglucoside),分子式为C27H30O16,分子量为 610.52,结构式如下:
目前主要采用硅胶柱层析和结晶相结合的方法进行槲皮素-3-O-龙胆二糖苷、山柰酚-3-O-龙胆二糖苷单体的精制,生产周期长,试剂浪费严重,产品收率低。
国家知识产权局于2006年10月11日公开了一种公开号为CN1844116,专利名称为“乌饭树黑色素中黄酮类单体的提取、分离、纯化及鉴定”的发明专利,该专利以乌饭树树叶为原料,经乙醇提取得到乌饭树树叶黑色素溶液,再经大孔吸附树脂对黑色素中的黄酮类化合物进行粗分离,再通过聚酰胺柱和HW-40柱对黄酮类化合物单体进行纯化,再用高效液相色谱-质谱、核磁共振技术对纯化组分进行结构鉴定;从中分离出7种黄酮类化合物单体,分别为A、B、C、D、E、F和G,并对B、C、D、E和F进行了精确的结构鉴定,确定分别为槲皮素、白杨黄素、芹黄素、山奈酚和木犀草素,其相对含量分别为:37.51%,2.26%,9.57%,1.72%和15.16%。
该专利以乌饭树树叶为原料,经乙醇提取得到乌饭树树叶黑色素溶液,再经大孔吸附树脂对黑色素中的黄酮类化合物进行粗分离,再通过聚酰胺柱和HW-40柱对黄酮类化合物单体进行纯化。但该技术方案过程复杂,成本较高,所涉及溶剂种类过多,所提取到黄酮类化合物中槲皮素及山柰酚含量低,纯度不高;且所涉及的槲皮素、白杨黄素、芹黄素、山奈酚和木犀草素为黄酮苷元,而没有提及到黄酮苷类化合物,由于黄酮苷元与黄酮苷类化合物两者极性相差极大,故该技术方案不适用于槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷的提取分离。
技术实现要素:
本发明旨在解决现有技术问题,而提出了从龙脷叶中同时分离槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷的方法。本发明通过成熟的工艺步骤及参数条件,使产品中槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷纯度分别达到99%以上;该方法能快速、高纯度、简便的分离、提纯龙脷叶中槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷。
为了实现上述技术目的,提出如下技术方案:
从龙脷叶中同时分离槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷的方法,包括如下步骤:
(1)提取
以龙脷叶药材为原料,粉碎成1~4mm的粗粉,然后按照每千克原料加入乙醇溶液6升,加入70%乙醇溶液,回流提取3-4次,每次2-3小时,提取液过滤,收集、合并,得提取液Ⅰ;
(2)浓缩
将步骤(1)所得的提取液Ⅰ回收乙醇后,浓缩至原提取液Ⅰ体积的15-25%,为提取液Ⅱ;
(3)大孔树脂柱富集与洗脱
将步骤(2)所得的提取液Ⅱ过大孔吸附树脂柱进行吸附,用纯化水清洗至无色后,再用60-70%乙醇溶液洗脱产品段,至流出液无色,收集、合并洗脱液,然后将洗脱液减压浓缩,回收乙醇,得提取液Ⅲ;
(4)聚酰胺树脂柱富集与洗脱
将步骤(3)所得的提取液Ⅲ过聚酰胺树脂柱进行吸附,先用10%乙醇溶液清洗聚酰胺树脂柱至无色后,再用90%乙醇溶液洗脱产品段,至流出液无色,收集、合并洗脱液,然后将洗脱液减压浓缩,回收乙醇后,得含有两种目标产物的浓缩液,为提取液Ⅳ;
(5)高效制备液相色谱仪分离
取步骤(4)所得的提取液Ⅳ用0.45μm有机膜过滤,收集滤液,然后滤液进样,进行槲皮素-3-0-龙胆二糖苷单体与山柰酚-3-0-龙胆二糖苷单体的制备分离,并针对性收集槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液;在此过程中,紫外检测器以波长350nm,进行在线检测;
(6)产品回收
将步骤(5)中进行高效制备液相色谱分离得到的槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液,加热回收甲醇,槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体在水溶液中大量析出,放置室温后,用漏斗过滤析出晶体,过滤固体于65℃条件下干燥12小时,即得到槲皮素-3-0-龙胆二糖苷单体及山柰酚-3-0-龙胆二糖苷单体目标产物。
在步骤(5)中,色谱条件为:色谱柱填料为C18填料,柱温为30℃,流速为1.0mL/min,流动相为甲醇-0.1%磷酸水溶液,且两者的体积比为46比54。
在进行高效制备液相色谱仪分离前,可通过液-质联用或其它本技术领域常用的方法确定高效液相色谱中槲皮素-3-0-龙胆二糖苷及山柰酚-3-0-龙胆二糖苷单体的峰形。以液-质联用方法为例,可与上述制备分离色谱条件相同,采用填料相同的色谱柱、组成相同的流动相、相同的检测波长等,柱温为室温。取步骤(4)所得的提取液Ⅳ过滤,然后进样,进行槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体的高效液相分离纯化,根据质谱检测结果,可确定槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体在液相色谱中所对应的峰形。
所述槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体产品的纯度复检采用反相分析型液相色谱,色谱条件为:以C18为填充剂;以甲醇-0.1%磷酸水溶液为流动相,两者体积比为46比54;流速1.0mL/min;检测波长为350nm。
槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷纯度分别达到99%以上。
采用上述技术方案,带来的有益技术效果为:
1.本发明通过成熟的工艺步骤及参数条件,使产品中槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷纯度分别达到99%以上;同时,本方法操作简便、分离效率高,原料可回收,可大量、高纯度且同时分离制备槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷单体;
2.在本发明中,针对龙脷叶药材中存在的各种成分的理化性质,本技术方案通过步骤的适当顺序搭配,以及适当的参数组合,有效提取出了槲皮素-3-O-龙胆二糖苷及山柰酚-3-O-龙胆二糖苷成分,并除去了大量杂质,由此获得可以进入制备型高效液相色谱系统的样品溶液,不至对高效液相色谱系统造成很大的影响,尽量延长其使用周期,节约了生产成本;
3.在本发明(1)步骤中,每千克原料加入乙醇溶液6升,在该比例下,既能有效浸泡原料,又能减少乙醇使用量,从而降低溶剂的使用成本;而采用70%乙醇回流提取,既可将槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷这两种黄酮类成分有效的提取出来,又使其他杂质成分溶出率较低,确保制备时杂质干扰少;
4.在本发明(2)步骤中,提取液Ⅰ回收乙醇,能减少浓缩液中的乙醇含量;通过浓缩,既可回收乙醇又减少了后续步骤中富集液的体积;
5.在本发明(3)步骤中,通过大孔吸附树脂柱进行吸附,用纯化水清洗至无色,通过纯化水确保除去大极性杂质和一些糖类成分;而60-70%乙醇溶液在保证产品被洗脱出来的同时,极性较小的杂质却不会被洗脱下来;
6.在本发明(4)步骤中,洗脱液通过聚酰胺树脂柱的吸附,能有效达到分离槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷,又能起到除去一部分杂质的作用;而通过10%乙醇洗脱掉一些大极性的色素和杂质,减少制备时的杂质干扰;90%乙醇既能快速的洗脱产品,浓缩时又能把制备原料减少到最少体积;
7.在本发明(5)步骤中,采用制备型高效液相色谱系统对槲皮素-3-O-龙胆二糖苷、山柰酚-3-O-龙胆二糖苷单体进行分离、纯化,达到了很好的分离效果,高效制备液相色谱相对于其他的常规分离方法(比如硅胶柱洗脱分离)既能对产品快速分离,而且对产品的收率有很大的提高,成本大大降低。并且通过在线紫外检测,针对性的收集槲皮素-3-O-龙胆二糖苷、山柰酚-3-O-龙胆二糖苷单体,目标明确,避免了常规柱层析等造成的资源浪费,而且便于控制产品质量,产品纯度可达99%以上;
8.在高效液相色谱分离过程中,各色谱条件的选择及其组合极为重要,因为它直接影响物质的出峰时间、峰形等;色谱条件主要包括色谱柱(包括填料、柱长、柱温等)、流动相(包括成分、流速等)、检测器及检测波长等。本发明通过大量的试验研究和对比分析,确定了以上所述的色谱条件,从而使物质的出峰时间、峰形、分离效果等达到最佳化,实现了槲皮素-3-O-龙胆二糖苷、山柰酚-3-O-龙胆二糖苷单体的高效分离;
9.在本发明中,各工艺步骤中的有机试剂均可回收再利用,溶剂消耗量少,节约成本。
附图说明
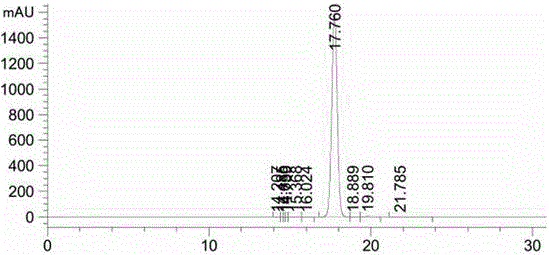
图1为本发明中槲皮素-3-O-龙胆二糖苷单体产品的HPLC图谱
图2为本发明中山柰酚-3-O-龙胆二糖苷单体产品的HPLC图谱。
具体实施方式
下面通过对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
实施例1
如图1、图2所示:从龙脷叶中同时分离槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷的方法,包括如下工艺步骤:
(1)提取
将龙脷叶药材称取1Kg,粉碎成1~4mm的粗粉,然后加入70%乙醇溶液6L,回流提取3次,2小时/次,过滤,合并滤液,共30L,为提取液Ⅰ;
(2)浓缩
将步骤(1)所得的提取液Ⅰ回收乙醇后,浓缩至小体积,所得浓缩液为5L,为提取液Ⅱ;
(3)大孔树脂柱富集与洗脱
将步骤(2)所得的提取液Ⅱ用大孔树脂进行吸附,用10L纯化水清洗树脂至无色后,再用15L的60%乙醇溶液洗脱产品段,至流出液无色,收集、合并洗脱液,将洗脱液减压浓缩,回收乙醇,得5L提取液Ⅲ;
(4)聚酰胺树脂柱富集与洗脱
将步骤(3)所得的提取液Ⅲ过聚酰胺树脂柱进行吸附,先用10L的10%乙醇溶液清洗树脂至无色后,再用16L的90%乙醇溶液洗脱产品,至流出液无色,收集、合并洗脱液,将洗脱液减压浓缩,回收乙醇后,得1L含产品的浓缩液,为提取液Ⅳ;
(5)高效制备液相色谱分离
色谱条件如下:填料为C18的色谱柱;
流动相组成为:甲醇-0.1%磷酸水溶液(V/V),二者体积比为46比54;
检测波长为350nm;取步骤(4)所得的提取液Ⅳ用0.45μm有机膜过滤,收集滤液,然后滤液进样,进行槲皮素-3-0-龙胆二糖苷单体与山柰酚-3-0-龙胆二糖苷单体的制备分离,并针对性收集槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液,分别得槲皮素-3-0-龙胆二糖苷制备溶液5L、山柰酚-3-0-龙胆二糖苷制备溶液6L;在此过程中,紫外检测器在线检测;
(6)产品回收
将步骤(5)中进行高效制备液相色谱分离得到的槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液,加热回收甲醇,槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体在水溶液中大量析出,放置室温后用漏斗过滤析出晶体,过滤固体于65℃条件下干燥12小时,即得到槲皮素-3-0-龙胆二糖苷固体1.1g、山柰酚-3-0-龙胆二糖苷固体1.3g。
所述槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体产品的纯度复检采用反相分析型液相色谱(RP-HPLC)法,色谱条件如下:以C18为填充剂;以甲醇-0.1%磷酸水溶液为流动相,两者体积比为46比54);流速1.0mL/min;检测波长为350nm。
整个生产流程用时约4天。
计算得产品收率为:
槲皮素-3-O-龙胆二糖苷:(1.1/1000)×100%=0.11%;
山柰酚-3-O-龙胆二糖苷:(1.3/1000)×100%=0.13%。
通过更换流动相组分,利用反相分析型液相色谱(RP-HPLC)复检产品纯度,测得结果为槲皮素-3-O-龙胆二糖苷99.15%,山柰酚-3-O-龙胆二糖苷99.35%。
实施例2
从龙脷叶中同时分离槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷的方法,包括如下工艺步骤:
(1)提取
将龙脷叶药材称取10Kg,粉碎成1~4mm的粗粉,加入60L体积浓度为70%乙醇溶液,提取3次,3小时/次,过滤,合并滤液,共90L,为提取液Ⅰ;
(2)浓缩
将步骤(1)所得的提取液Ⅰ回收乙醇后,浓缩至小体积,所得浓缩液为15L,为提取液Ⅱ;
(3)大孔树脂富集与解析
将步骤(2)所得的提取液Ⅱ用大孔树脂进行吸附,用80L纯化水清洗树脂至无色后,再用120L的65%乙醇溶液洗脱产品段,至流出液无色,收集、合并洗脱液,将洗脱液减压浓缩,回收乙醇,得18L提取液Ⅲ;
(4)聚酰胺树脂柱富集与洗脱
将步骤(3)所得的提取液Ⅲ过聚酰胺树脂柱进行吸附,先用100L的10%乙醇溶液清洗树脂至无色后,再用180L的90%乙醇溶液洗脱产品,至流出液无色,收集、合并洗脱液,将洗脱液减压浓缩,回收乙醇后,得20L含产品的浓缩液,为提取液Ⅳ;
(5)高效制备液相色谱分离
色谱条件如下:填料为C18的色谱柱;
流动相组成为:甲醇-0.1%磷酸水溶液(V/V),二者体积比为46比54;
检测波长为350nm;取步骤(4)所得的提取液Ⅳ用0.45μm有机膜过滤,收集滤液,然后滤液进样,进行槲皮素-3-0-龙胆二糖苷单体与山柰酚-3-0-龙胆二糖苷单体的制备分离,并针对性收集槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液,分别得槲皮素-3-0-龙胆二糖苷制备溶液60L、山柰酚-3-0-龙胆二糖苷制备溶液75L;在此过程中,紫外检测器在线检测;
(6)产品回收
将步骤(5)中进行高效制备液相色谱分离得到的槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液,加热回收甲醇,槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体在水溶液中大量析出,放置室温后用漏斗过滤析出晶体,过滤固体于65℃条件下干燥12小时,即得到槲皮素-3-0-龙胆二糖苷固体12、山柰酚-3-0-龙胆二糖苷固体14g。
所述槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体产品的纯度复检采用反相分析型液相色谱(RP-HPLC)法,色谱条件如下:以C18为填充剂;以甲醇-0.1%磷酸水溶液为流动相,两者体积比为46比54;流速1.0mL/min;检测波长为350 nm。
整个生产流程用时约6天。
计算得产品收率为:
槲皮素-3-O-龙胆二糖苷:(12/1000)×100%=0.12%;
山柰酚-3-O-龙胆二糖苷:(14/1000)×100%=0.14%。
通过更换流动相组分,利用反相分析型液相色谱(RP-HPLC)复检产品纯度,测得结果为槲皮素-3-O-龙胆二糖苷99.25%,山柰酚-3-O-龙胆二糖苷99.45%。
实施例3
从龙脷叶中同时分离槲皮素-3-0-龙胆二糖苷和山柰酚-3-0-龙胆二糖苷的方法,包括如下工艺步骤:
(1)提取
将龙脷叶药材称取20Kg,粉碎成1~4mm的粗粉,然后加入120L的70%乙醇溶液,提取4次,3小时/次,过滤,合并滤液,共185L,为提取液Ⅰ;
(2)浓缩
将步骤(1)所得的提取液Ⅰ回收乙醇后,浓缩至小体积,所得浓缩液为30L,为提取液Ⅱ;
(3)大孔树脂富集与解析
将步骤(2)所得的提取液Ⅱ用大孔树脂进行吸附,用150L纯化水清洗树脂至无色后,再用200L的70%乙醇溶液洗脱产品段,至流出液无色,收集、合并洗脱液,将洗脱液减压浓缩,回收乙醇,得25L提取液Ⅲ;
(4)聚酰胺树脂柱富集与洗脱
将步骤(3)所得的提取液Ⅲ过聚酰胺树脂柱进行吸附,先用100L的10%乙醇溶液清洗树脂至无色后,再用200L的90%乙醇溶液洗脱产品,至流出液无色,收集、合并洗脱液,将洗脱液减压浓缩,回收乙醇后,得21L含产品的浓缩液,为提取液Ⅳ;
(5)高效制备液相色谱分离
色谱条件如下:填料为C18的色谱柱;
流动相组成为:甲醇-0.1%磷酸水溶液(V/V),二者体积比为46比54;
检测波长为350nm;
取步骤(4)所得的提取液Ⅳ用0.45μm有机膜过滤,收集滤液,然后滤液进样,进行槲皮素-3-0-龙胆二糖苷单体与山柰酚-3-0-龙胆二糖苷单体的制备分离,并针对性收集槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液,分别得槲皮素-3-0-龙胆二糖苷制备溶液80L、山柰酚-3-0-龙胆二糖苷制备溶液95L;在此过程中,紫外检测器在线检测;
(6)产品回收
将步骤(5)中进行高效制备液相色谱分离得到的槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷两种单体的制备馏分溶液,加热回收甲醇,槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体在水溶液中大量析出,放置室温后用漏斗过滤析出晶体,过滤固体于65℃条件下干燥12小时,即得到槲皮素-3-0-龙胆二糖苷固体25g、山柰酚-3-0-龙胆二糖苷固体27g。
所述槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体产品的纯度复检采用反相分析型液相色谱(RP-HPLC)法,色谱条件如下:以C18为填充剂;以甲醇-0.1%磷酸水溶液为流动相,两者体积比为4比54;流速1.0mL/min;检测波长为350nm。
整个生产流程用时约7天。
计算得产品收率为:
槲皮素-3-O-龙胆二糖苷:(25/2000)×100%=0.125%;
山柰酚-3-O-龙胆二糖苷:(27/2000)×100%=0.135%。
通过更换流动相组分,利用反相分析型液相色谱(RP-HPLC)复检产品纯度,测得结果为槲皮素-3-O-龙胆二糖苷99.45%,山柰酚-3-O-龙胆二糖苷99.35%。
实施例4
在实施例1-3基础上,流动相还可以为乙腈-0.1%磷酸水溶液,且两者体积比为25比75;
在进行高效液相色谱法分离前,通过液-质联用法确定高效液相色谱中槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体的峰形,即,取步骤(5)中所得混合液进样,进行槲皮素-3-0-龙胆二糖苷、山柰酚-3-0-龙胆二糖苷单体的制备分离,根据质谱检测结果,确定槲皮素-3-0-龙胆二糖苷与山柰酚-3-0-龙胆二糖苷单体在液相色谱中对应的峰形。
- 还没有人留言评论。精彩留言会获得点赞!