帕金森病致病基因及检测试剂盒的制作方法
本发明涉及基因检测技术领域,尤其涉及一种帕金森病致病基因及检测试剂盒。
背景技术:
帕金森病(Parkinson’s disease,PD;MIM 168600),又称震颤麻痹,是一种常见的运动系统障碍疾病,是仅次于阿尔茨海默病的第二大常见进行性神经系统退行性疾病。流行病学资料显示其患病率与年龄有一定关系,65岁以上人群的患病率约1%左右,到85岁人群患病率增长至约4%~5%。PD的平均发病年龄为70岁,PD的标准化发病率估计为8~18/10万/年,终生患病风险约为1.5%。此外,性别也可能影响PD的发病率,几项前瞻性研究发现男性的发病率高于女性。PD运动系统典型症状为运动迟缓、静止性震颤、肌强直和姿势步态不稳,这些症状主要由黑质多巴胺能神经元的进行性丢失引起,此外PD患者可表现出如自主神经功能紊乱等非运动系统症状,甚至可能早于运动系统症状出现。PD不仅累及大脑和脑干,对其它器官(心脏、膀胱及肠道)也有影响。目前PD的主要治疗仅能控制症状,常用的药物治疗只能减轻PD的运动系统症状,并不能延缓疾病的进展,甚至会出现一些运动系统的副作用,如开关现象和运动困难等。此外,在PD疾病发展过程中特别是晚期,非运动系统症状也很常见,如自主神经功能紊乱、认知障碍、抑郁、嗅觉和感觉缺失以及睡眠障碍等。PD是一种慢性疾病,其起病隐匿,病情进展缓慢,从诊断到死亡的平均生存期可持续15年甚至更久,但PD病情严重时可出现各种严重并发症,对患者造成严重困扰甚至引起死亡。因PD具有病程长和致残率高等特点,对患者的社会功能和生活质量造成了严重的危害,给患者及其家庭带来沉重的负担和烦恼。
一些环境因素,例如乡下生活、农耕作业、饮用井水和接触杀虫剂等,已被确定是PD发病的危险因素。流行病学研究显示10%~30%的PD患者有家族史,PD患者一级亲属PD的发生风险是正常人2~7倍。双胞胎研究也表明遗传因素在PD发病过程中发挥重要作用。大部分患者的PD是散发的,有5%~10%的患者属于遗传型PD,其遗传模式包括常染色体显性遗传、常染色体隐性遗传和X连锁遗传等。目前已确定的与常染色体显性遗传有关的基因包括SNCA、LRRK2、VPS35、UCHL1、GIGYF2、HTRA2、EIF4G1、DNAJC13、CHCHD2、TMEM230和RIC3。与常染色体隐性遗传相关的基因包括Parkin、PINK1、DJ-1、ATP13A2、DNAJC6、SYNJ1、PRKN、PLA2G6、FBXO7、SYNJ1和VPS13C。PD易感基因包括GBA、MAPT、GAK、HLA-DRA、BST1、FGF20、STX1B和STBD1等。
自1997年第一个致病基因SNCA(theα-synuclein gene)被鉴定可能导致常染色体显性遗传PD以来,遗传因素在PD发生中的作用越来越受到关注。目前报道约10%左右PD患者具有阳性家族史(其中1个以上有血缘关系的亲属表现出类似症状),其余大多数为散发性PD。目前对家族性PD的相关基因及基因突变和遗传因素对散发性PD发生的影响均有一定的研究,此外越来越多的研究证实了一些PD相关基因的基因多态性与PD发病风险相关。
PD遗传机制复杂,具有遗传及临床异质性,目前的遗传学研究表明至少有25个疾病位点和20个致病基因与PD发病有关,其中13个疾病位点和11个致病基因与常染色体显性遗传PD有关,具体发病机制复杂,目前不甚清楚。目前已发现的遗传学病因仅能解释约5%的PD,仍有较多的家族性PD和散发性PD的病因不明,某些已明确的疾病位点如1p32和1q32等尚未鉴定出致病基因。据了解,目前尚无GALNT2基因与PD发病关系的研究报道,也暂无该基因所在位置1q42.13与PD相关的报道。
由于PD遗传机制复杂,具有临床及遗传异质性,目前缺乏快速、准确的检测技术应用于PD致病基因的检测。
技术实现要素:
本发明要解决的技术问题是克服现有技术的不足,提供一种帕金森病致病基因及检测试剂盒,其中帕金森病致病基因为GALNT2;针对其编码区序列设计诊断引物,发明检测试剂盒应用于PCR体外扩增基因组DNA,结合Sanger测序,检测PD致病基因GALNT2基因的突变,应用于临床基因诊断,具有检测方便、便捷,准确率达到100%等优势。
为解决上述技术问题,本发明提供了一种帕金森病致病基因,所述帕金森病致病基因为GALNT2基因编码区(第四外显子)第466位碱基发生G→A改变的基因,包含所述帕金森病致病基因的核苷酸序列为SEQ ID NO.33所示的序列。
作为本发明的同一技术构思,本发明还提供了一种帕金森病致病基因的检测试剂盒,所述检测试剂盒包括引物,所述引物为根据GALNT2基因所有外显子及其外显子-内含子交界区序列设计的引物,所述引物用于PCR扩增,所述PCR扩增的产物包括GALNT2基因外显子及其外显子-内含子交界区的核苷酸序列。
上述的检测试剂盒,优选的,所述引物的核苷酸序列为以下引物对中的至少一对:SEQ ID NO.1和SEQ ID NO.2、SEQ ID NO.3和SEQ ID NO.4、SEQ ID NO.5和SEQ ID NO.6、SEQ ID NO.7和SEQ ID NO.8、SEQ ID NO.9和SEQ ID NO.10、SEQ ID NO.11和SEQ ID NO.12、SEQ ID NO.13和SEQ ID NO.14、SEQ ID NO.15和SEQ ID NO.16、SEQ ID NO.17和SEQ ID NO.18、SEQ ID NO.19和SEQ ID NO.20、SEQ ID NO.21和SEQ ID NO.22、SEQ ID NO.23和SEQ ID NO.24、SEQ ID NO.25和SEQ ID NO.26、SEQ ID NO.27和SEQ ID NO.28、SEQ ID NO.29和SEQ ID NO.30、SEQ ID NO.31和SEQ ID NO.32。
上述的检测试剂盒,优选的,所述检测试剂盒还包括用于PCR的DNA扩增酶和缓冲液。
上述的检测试剂盒,优选的,所述用于PCR的DNA扩增酶为Taq DNA聚合酶。
上述的检测试剂盒,优选的,所述Taq DNA聚合酶的酶活为5U/μl。
上述的检测试剂盒,优选的,所述缓冲液为PCR Buffer、MgCl2和dNTP Mix。
上述的检测试剂盒,优选的,所述MgCl2的浓度为25mM、所述dNTP Mix的浓度为10mM。
上述的检测试剂盒,优选的,所述引物、DNA扩增酶和缓冲液的体积比为2:0.15:4.82。
本发明的创新点在于:
本发明公开了一种在常染色体显性遗传PD患者中发现的致病基因及其编码的蛋白质,首次揭示了定位于1q42.13区间内的GALNT2基因为一个中国汉族常染色体显性遗传PD家系的致病基因,同时鉴定出该家系的致病突变为GALNT2p.V156M的杂合突变。本发明提供了一种常染色体显性遗传PD致病基因突变的检测方法,采用检测试剂盒使检测变得简便和易行,本发明将进一步加深人类在分子病理水平上对PD的认识,为今后开展相应基因诊断、产前筛查、靶向药物设计和临床治疗提供重要的遗传学依据。
与现有技术相比,本发明的优点在于:
(1)本发明提供了一种帕金森病致病基因,通过对PD家系进行外显子组测序及Sanger测序分析,鉴定了一个新的常染色体显性遗传PD致病基因——GALNT2,该基因定位于1q42.13区间内,针对其编码区序列设计诊断引物,发明检测试剂盒应用于PCR体外扩增基因组DNA,结合Sanger测序,检测PD致病基因GALNT2基因的突变,应用于临床基因诊断。
(2)本发明提供了一种用于检测帕金森病致病基因的检测试剂盒,通过设计PCR扩增的致病基因GALNT2所有外显子及其外显子-内含子交界区序列的引物,提供了一种用于PD致病基因突变的检测试剂盒,该试剂盒检测方便、便捷,准确率达到100%。
(3)本发明用于检测帕金森病致病基因的检测试剂盒应用于PD致病基因突变的检测,有利于明确PD患者的分子诊断及分型,用于开展基因诊断和遗传咨询,应用于PD家系患者子代产前诊断,指导优生优育。此外,新的PD致病基因的克隆,结合遗传或表观遗传修饰因素调节基因表达及构建相应的动物模型将为揭示PD的发病机理提供重要线索,进一步阐明该疾患的发病机制,有助个体化诊断及治疗。
附图说明
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整的描述。
图1为PD家系图,其中M表示定位在1号染色体上GALNT2基因c.466G>A(p.V156M)突变,N表示正常(normal)。
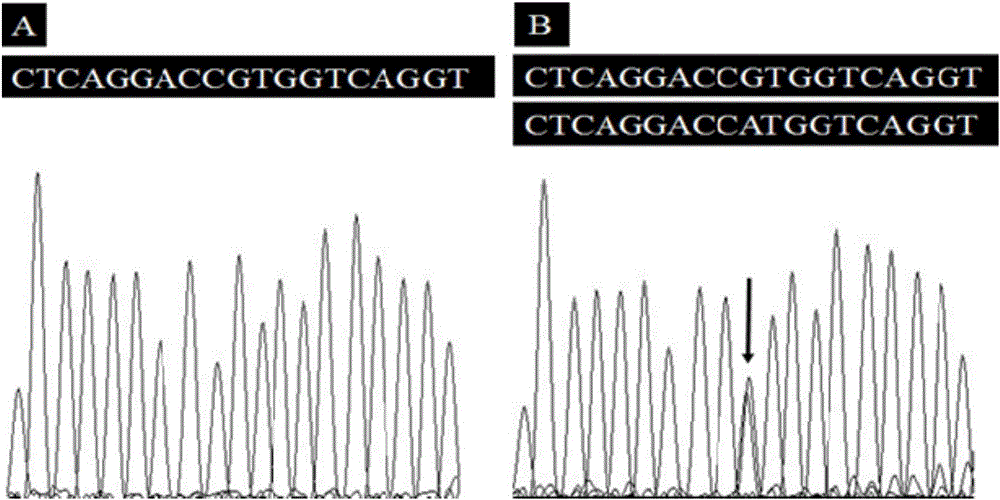
图2为PD家系成员GALNT2基因测序结果图;其中A表示正常者(Ⅲ:6)测序图;B表示患者(Ⅲ:4)测序图示c.466G>A(p.V156M)突变。
图3为GALNT2基因编码蛋白同源性比较分析(BLAST结果)。
具体实施方式
以下结合说明书附图和具体优选的实施例对本发明作进一步描述,但并不因此而限制本发明的保护范围。
实施例
以下实施例中所采用的材料和仪器均为市售。
实施例1:
一种帕金森病致病基因,其包含基因突变的核苷酸序列为(SEQ ID NO.33):
TCTGCCTGTTCTCTGAAGGGctaaacaagctgtggctgctctgggggtcattgttcagaggaccatctttctcttcctgcaggtgtcagcggaagcagtggcgggtggatctgccggccaccagcgtggtgatcacgtttcacaatgaagccaggtcggccctactcaggaccAtggtcaggtgaggccaggagatgcattacctgtcaggggtgttaagacattagctgtgtcCCAGGCACAGTCAGACCAG。
正常的核苷酸序列为(SEQ ID NO.34):
tctgcctgttctctgaagggctaaacaagctgtggctgctctgggggtcattgttcagaggaccatctttctcttcctgcaggtgtcagcggaagcagtggcgggtggatctgccggccaccagcgtggtgatcacgtttcacaatgaagccaggtcggccctactcaggaccGtggtcaggtgaggccaggagatgcattacctgtcaggggtgttaagacattagctgtgtcccaggcacagtcagaccag。
该致病基因是采用以下方法鉴定的:
采集到一个三代常染色体显性遗传PD家系(图1)成员的外周静脉血样本10ml,经EDTA-K2抗凝,常规苯酚-氯仿法提取基因组DNA,将提取得到的基因组DNA经分光光度计测DNA浓度和OD值后稀释至100ng/μl,用于后续外显子组测序。
本次共采集了家系内11名成员(包括4名患者和7名正常者)的血液样本及相关详细临床资料,家系内PD患者临床表现为运动迟缓、静止性震颤和一些非运动系统表现(腿部疼痛、失眠),左旋多巴治疗有效,具有诊断意义的典型症状。详细临床表现列于表1中。
表1:常染色体显性遗传PD家系成员基本信息
+表示症状明显;-表示不详或无明显症状。
将采集到的基因组DNA进行外显子组测序:对PD家系内2个典型患者(Ⅲ:5和Ⅲ:9)的基因组DNA进行外显子组测序,获得核苷酸变异数据。
测序流程为:将基因组DNA随机打断成随机片段并建立随机片段文库;采用NimbleGen SeqCap EZ(生物素化寡DNA核酸探针)人全外显子捕获系统,对目标片段进行富集;运用第二代高通量ABI SOLiDTM4.0测序仪,进行高通量的测序。外显子组测序获得原始数据经过去污染、质量控制等过滤处理后,比对人类参考基因组,获得比对到基因组上的Unique mapped reads(单一定位读取片段),即得到核苷酸变异数据。
生物信息学分析:对外显子组测序获得的核苷酸变异数据,通过与正常人核苷酸变异数据库(如dbSNP132、1000基因组计划、HapMap和中国炎黄一号)对比,排除已知的核苷酸多态和人群中有一定频率的核苷酸多态,优先在两个患者者同时存在的变异,结合生物信息学软件预测结果,进一步缩小候选变异数目为85个,确定候选基因及变异。
通过设计针对候选基因变异的引物、位点特异性PCR扩增、Sanger测序和家系内突变-表型共分离分析等,结果显示,PD家系内2个典型患者(Ⅲ:5和Ⅲ:9)GALNT2基因编码区(NM_004481.4,NP_004472.1)第466位碱基发生G→A改变(c.466G>A,p.V156M),该突变为PD家系的致病基因突变。
引物设计:候选基因变异的基因标准序列来自于UCSC(http://genome.ucsc.edu/),应用Primer3(version 4.0.0,http://primer3.ut.ee/)软件设计用于检测候选基因变异的引物并合成,然后利用Primer-BLAST(http://www.ncbi.nlm.nih.gov/tools/primer-blast/)验证引物特异性。
根据上述方法,本发明合成的正向引物为:5’-tctgcctgttctctgaaggg-3’(即SEQ ID NO.7);反向引物为:5’-ctggtctgactgtgcctgg-3’(即SEQ ID NO.8);引物对SEQ ID NO.7和SEQ ID NO.8仅针对GALNT2基因候选变异c.466G>A(p.V156M)所在外显子(4号外显子),但是在实际的应用过程中,突变位点可能会存在于GALNT2基因的任一位置上。若突变位点出现在该基因其他区域,针对GALNT2基因编码区序列设计的以下引物对中的至少一对也能实现对PD致病基因GALNT2突变的检测,并达到相同或相似的技术效果:SEQ ID NO.1和SEQ ID NO.2、SEQ ID NO.3和SEQ ID NO.4、SEQ ID NO.5和SEQ ID NO.6、SEQ ID NO.9和SEQ ID NO.10、SEQ ID NO.11和SEQ ID NO.12、SEQ ID NO.13和SEQ ID NO.14、SEQ ID NO.15和SEQ ID NO.16、SEQ ID NO.17和SEQ ID NO.18、SEQ ID NO.19和SEQ ID NO.20、SEQ ID NO.21和SEQ ID NO.22、SEQ ID NO.23和SEQ ID NO.24、SEQ ID NO.25和SEQ ID NO.26、SEQ ID NO.27和SEQ ID NO.28、SEQ ID NO.29和SEQ ID NO.30、SEQ ID NO.31和SEQ ID NO.32。
实施例2:一种帕金森病致病基因的检测试剂盒。
前述PD致病基因的检测试剂盒,其具体成分和含量列于表2中。
表2:实施例1的PD致病基因的检测试剂盒成分表
实施例3:一种实施例2的检测试剂盒在帕金森病致病基因检测中的应用。
分别以正常者(Ⅲ:6)和患者(Ⅲ:4)为被检者,进行如下操作:
1、基因组DNA提取:采集两位被检者外周静脉血样本10ml,经EDTA-K2抗凝,常规苯酚-氯仿法提取基因组DNA,分光光度计测DNA浓度和OD值后稀释至100ng/μl备用。
2、PCR扩增:利用实施例2设计的检测试剂盒将步骤1中提取的基因组DNA进行扩增得到PCR扩增产物。PCR反应体系(25μl)的成分为:1μl的DNA模板(即步骤1提取的基因组DNA);2.5μl的10×PCR Buffer;2.0μl的25mM MgCl2;0.32μl的10mM dNTP Mix;1.0μl实施例2的正向引物(10μmol/L);1.0μl实施例2的反向引物(10μmol/L);0.15μl的Taq DNA聚合酶(5U/μl),加灭菌双蒸水(ddH2O)至25μl。PCR反应条件为:95℃预变性3分钟,95℃变性40秒,58℃退火35秒,72℃延伸40秒,重复变性、退火和延伸三个步骤35个循环,最后72℃延伸5分钟,4℃保存。将PCR扩增产物于6%非变性聚丙烯酰胺凝胶电泳,凝胶经固定液(固定液包括450ml的蒸馏水、50ml的无水乙醇和2.5ml的冰醋酸液)固定,染色液(染色液包括1g的硝酸银和500ml的蒸馏水)染色,显色液(显色液包括500ml的蒸馏水、3.75g的氢氧化钠和2.5ml的甲醛)显带,得到电泳图谱。
3、产物纯化:分析步骤2中得到的电泳图谱,选择电泳图谱中带型单一且浓度较高与目标片段大小一致的PCR产物进行产物纯化。产物纯化反应体系:虾碱性磷酸酶(SAP,1U/μl)0.8μl,核酸外切酶I(EXO I,20U/μl)0.2μl,10×SAP Buffer 0.2μl,ddH2O 0.3μl,PCR产物8.5μl。产物纯化反应条件:在温度为37℃下反应120分钟,然后转入80℃下反应15分钟,得到PCR产物纯品,于4℃保温,备用。
4、Sanger测序:将步骤3中制备得到的PCR产物纯品按BigDye 3.1 Sequencing kit(BigDye 3.1 Sequencing kit由Applied Biosystems公司提供)试剂盒进行测序PCR得到测序产物。测序PCR反应体系为1/16反应体系(10μl):2μl PCR产物纯品(DNA),0.5μl的BigDye,1.75μl的5×BigDye Seq Buffer,1μl的测序引物(3.2pmol/μl,测序引物采用实施例2的正向引物或反向引物),4.75μl的ddH2O。测序PCR反应条件:96℃下变性30秒,55℃退火15秒,60℃延伸3分钟,重复变性、退火和延伸步骤33个循环,维持4℃,得到测序产物,取出备用。
将测序产物进行纯化:采用乙醇/EDTA/乙酸钠(NaAc)法纯化测序产物,10μl反应体系,96孔板。具体操作步骤如下:在96孔板中每孔加入1μl 125mM EDTA与1μl 3M NaAc混合液;再于每孔中加入25μl无水乙醇,用铝箔纸密封后震荡混匀4次,于室温放置15分钟;然后置于离心机中以2800×g离心30分钟,马上倒置96孔板,再离心至185×g停止离心(从离心机启动到达185×g停止,离心时间共1分钟);接着于每孔中加入35μl 70%乙醇,于4℃下以1650×g离心15分钟,马上倒置96孔板,离心至185×g停止离心(从离心机启动到达185×g停止,离心时间共1分钟);重复上述步骤一次,置于室温;待乙醇挥发干净后,于每孔中加入10μl高度去离子甲酰胺(Hi-Di Formamide)溶解DNA;待测序产物完全溶解后置于96℃变性5分钟后,迅速置于冰中冷却15分钟。采用美国Applied Biosystems公司自动基因分析仪3500测序分析纯化后的测序产物得到测序图(参见图2)。其中A表示正常者(Ⅲ:6)测序图;B表示患者(Ⅲ:4)测序图。从图2中可知,PD家系患者(Ⅲ:4)1号染色体上GALNT2基因编码区第466位碱基发生G→A改变。
5、突变分析:PCR产物纯品进行Sanger测序后,比对参考基因组标准序列,鉴定GALNT2基因编码区(NM_004481.4,NP_004472.1)第466位碱基是否发生G→A改变(c.466G>A,p.V156M)。进一步使用生物信息学软件SIFT(http://sift.jcvi.org),Polyphen-2(http://genetics.bwh.harvard.edu/pph2/)和MutationMaster(http://www.mutationtaster.org/)进行预测,预测突变是否影响功能和致病,进一步明确基因突变与疾病的关系,预测该突变为致病性突变。
鉴定基因突变后,NCBI-BLAST(http://blast.st-va.ncbi.nlm.nih.gov/Blast.cgi)对比其它生物中的同源基因编码蛋白(图3),从图3中可知:GALNT2基因编码蛋白的156位缬氨酸(V)在多个物种中高度保守。
以上所述,仅是本发明的较佳实施例而已,并非对本发明作任何形式上的限制。虽然本发明已以较佳实施例揭示如上,然而并非用以限定本发明。任何熟悉本领域的技术人员,在不脱离本发明的精神实质和技术方案的情况下,都可利用上述揭示的方法和技术内容对本发明技术方案做出许多可能的变动和修饰,或修改为等同变化的等效实施例。因此,凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所做的任何简单修改、等同替换、等效变化及修饰,均仍属于本发明技术方案保护的范围内。
SEQUENCE LISTING
<110> 中南大学湘雅三医院
<120> 帕金森病致病基因及检测试剂盒
<130> 无
<160> 34
<170> PatentIn version 3.5
<210> 1
<211> 18
<212> DNA
<213> 人工序列
<400> 1
cttcctccgc tcctcccc 18
<210> 2
<211> 18
<212> DNA
<213> 人工序列
<400> 2
gagagggcag gggacagg 18
<210> 3
<211> 19
<212> DNA
<213> 人工序列
<400> 3
tcatcagtgc atccccagg 19
<210> 4
<211> 20
<212> DNA
<213> 人工序列
<400> 4
atgctcagtc cactcccaat 20
<210> 5
<211> 21
<212> DNA
<213> 人工序列
<400> 5
gccatggatg tgatttctgg a 21
<210> 6
<211> 20
<212> DNA
<213> 人工序列
<400> 6
caggtgaaag cgacgtactg 20
<210> 7
<211> 20
<212> DNA
<213> 人工序列
<400> 7
tctgcctgtt ctctgaaggg 20
<210> 8
<211> 19
<212> DNA
<213> 人工序列
<400> 8
ctggtctgac tgtgcctgg 19
<210> 9
<211> 20
<212> DNA
<213> 人工序列
<400> 9
agtgtgtagc tcctccaacc 20
<210> 10
<211> 20
<212> DNA
<213> 人工序列
<400> 10
gttcacgcct cattagcacc 20
<210> 11
<211> 20
<212> DNA
<213> 人工序列
<400> 11
ccaaggagat aatcggccct 20
<210> 12
<211> 21
<212> DNA
<213> 人工序列
<400> 12
tctggtagag ggagacagaa a 21
<210> 13
<211> 18
<212> DNA
<213> 人工序列
<400> 13
ggttggcatg gggttgtg 18
<210> 14
<211> 20
<212> DNA
<213> 人工序列
<400> 14
tactccctgc gttacacctc 20
<210> 15
<211> 20
<212> DNA
<213> 人工序列
<400> 15
ccctgtgcct gcctaatact 20
<210> 16
<211> 20
<212> DNA
<213> 人工序列
<400> 16
gggagtggtg atcagatgct 20
<210> 17
<211> 20
<212> DNA
<213> 人工序列
<400> 17
ttaagctgtg aggaatgggg 20
<210> 18
<211> 20
<212> DNA
<213> 人工序列
<400> 18
caaagaagct ggaacctggg 20
<210> 19
<211> 20
<212> DNA
<213> 人工序列
<400> 19
caagggtgct ggcaatctaa 20
<210> 20
<211> 20
<212> DNA
<213> 人工序列
<400> 20
gcaaggatcg attaagccca 20
<210> 21
<211> 20
<212> DNA
<213> 人工序列
<400> 21
gcttggtgtg tctgctgttg 20
<210> 22
<211> 20
<212> DNA
<213> 人工序列
<400> 22
ctcaaacagc ccaaggtcag 20
<210> 23
<211> 20
<212> DNA
<213> 人工序列
<400> 23
aggtgcaaat ggagtgatgc 20
<210> 24
<211> 20
<212> DNA
<213> 人工序列
<400> 24
gcacctgggt agctgaattc 20
<210> 25
<211> 20
<212> DNA
<213> 人工序列
<400> 25
ccctgttctc ctcagcagat 20
<210> 26
<211> 20
<212> DNA
<213> 人工序列
<400> 26
atttcccctc tgctgcttct 20
<210> 27
<211> 20
<212> DNA
<213> 人工序列
<400> 27
ctctcgttcc tgtcacctgt 20
<210> 28
<211> 20
<212> DNA
<213> 人工序列
<400> 28
caactcctgc tctctctggg 20
<210> 29
<211> 20
<212> DNA
<213> 人工序列
<400> 29
tcgatgcccc ttctttcctt 20
<210> 30
<211> 20
<212> DNA
<213> 人工序列
<400> 30
ctttgagagg cagcacagag 20
<210> 31
<211> 21
<212> DNA
<213> 人工序列
<400> 31
acaaggtcct gaattcacac g 21
<210> 32
<211> 20
<212> DNA
<213> 人工序列
<400> 32
gatcaccaga ctccacccaa 20
<210> 33
<211> 253
<212> DNA
<213> 人类
<400> 33
tctgcctgtt ctctgaaggg ctaaacaagc tgtggctgct ctgggggtca ttgttcagag 60
gaccatcttt ctcttcctgc aggtgtcagc ggaagcagtg gcgggtggat ctgccggcca 120
ccagcgtggt gatcacgttt cacaatgaag ccaggtcggc cctactcagg accatggtca 180
ggtgaggcca ggagatgcat tacctgtcag gggtgttaag acattagctg tgtcccaggc 240
acagtcagac cag 253
<210> 34
<211> 253
<212> DNA
<213> 人类
<400> 34
tctgcctgtt ctctgaaggg ctaaacaagc tgtggctgct ctgggggtca ttgttcagag 60
gaccatcttt ctcttcctgc aggtgtcagc ggaagcagtg gcgggtggat ctgccggcca 120
ccagcgtggt gatcacgttt cacaatgaag ccaggtcggc cctactcagg accgtggtca 180
ggtgaggcca ggagatgcat tacctgtcag gggtgttaag acattagctg tgtcccaggc 240
acagtcagac cag 253
- 还没有人留言评论。精彩留言会获得点赞!