一种铜催化合成三氟甲基‑1,2,4‑三嗪酮化合物的方法与流程
本发明属于有机氟化学合成领域,具体涉及一种铜催化合成三氟甲基-1,2,4-三嗪酮化合物的方法。
背景技术:
三氟甲基引入到有机分子中,能增强分子的脂溶性、提高代谢稳定性、抗氧化性和刚性等,因此含三氟甲基化合物广泛应用于医药、农药、以及先进材料领域。另一方面,1,2,4-三嗪酮化合物在杀虫、杀菌、抗癌、抗溃疡、植物生长调节上具有较好的生物活性。构建含三氟甲基1,2,4-三嗪酮化合物具有重要的理论研究意义和实际应用价值。目前,通过一些廉价易得的原料,高效、简便地合成该类化合物的方法还未见报道。因此发明一种利用简单易得的、廉价的原料合成三氟甲基-1,2,4-三嗪酮化合物的方法,为发展新型的医药、农药、以及先进材料提供了支撑和可能。
技术实现要素:
本发明的目的在于提供一种铜催化合成三氟甲基-1,2,4-三嗪酮化合物的方法,该法催化剂及原料廉价易得,产率普遍较高,官能团的适应性很好,且其反应条件温和,操作简便,具有良好的工业应用前景。
为实现上述目的,本发明采用如下技术方案:
一种铜催化合成三氟甲基-1,2,4-三嗪酮化合物的方法,以铜盐为催化剂,以叠氮、炔烃、三氟乙酸酐为原料,加入三乙基胺,在四氢呋喃溶剂中,反应制得三氟甲基-1,2,4-三嗪酮化合物:
所述的铜盐为碘化亚铜、溴化亚铜、cu(ch3cn)4bf4和cucn中的任一种。
所述叠氮的结构式为:
所述炔烃的结构式为:
铜盐、炔烃、叠氮、三氟乙酸酐、三乙基胺以及溶剂的摩尔比为0.025-0.05:0.5-1:0.65-1.3:0.75-1.5:1-2:12.3-24.6。
优选的,铜盐、炔烃、叠氮、三氟乙酸酐、三乙基胺以及溶剂的摩尔比为0.025:0.5:0.65:0.75:1:12.3。
具体步骤如下:在氮气气氛中,向带有磁力搅拌装置的容器中加入铜盐、叠氮、炔烃、三氟乙酸酐、三乙基胺、以及溶剂,混合均匀后关好塞子,将其放入室温下继续搅拌1-16小时后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯或正戊烷和二氯甲烷为洗脱剂,得到三氟甲基-1,2,4-三嗪酮产物。
本发明的有益效果在于:
本发明以廉价易得的叠氮、炔烃、三氟乙酸酐等为原料,以碘化亚铜为催化剂,一步合成三氟甲基-1,2,4-三嗪酮产物,得到普遍较高的产率,官能团的适应性很好,且其反应条件温和,操作简便,具有良好的工业应用前景。
附图说明
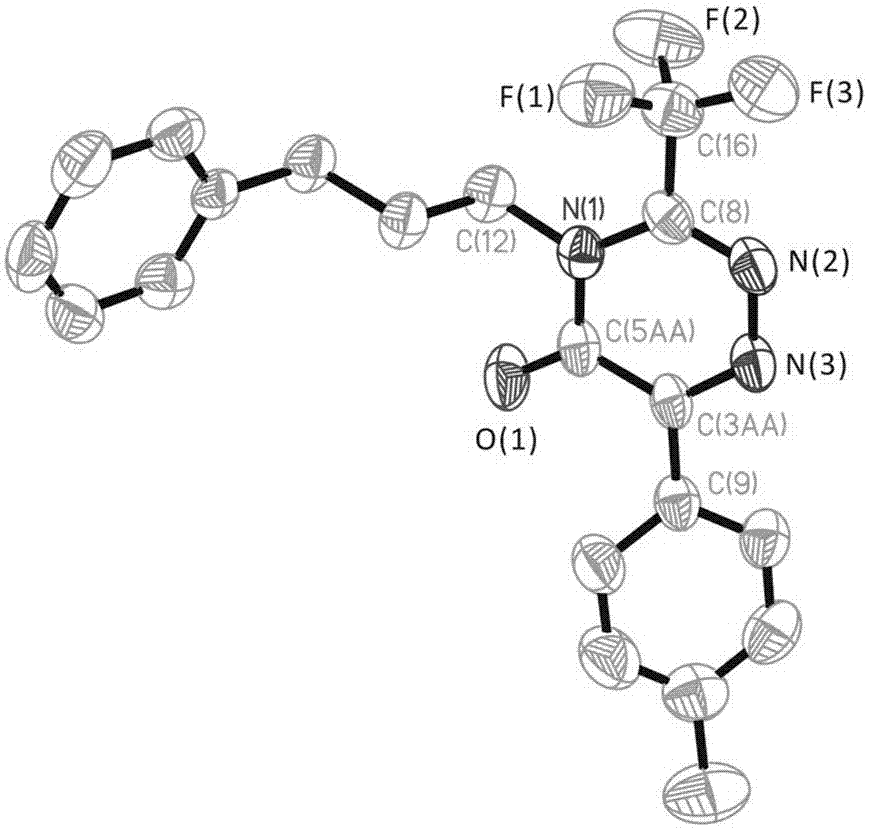
图1为实施例1制得的6-苯基-(3’-苯基丙基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮单晶结构图;
图2实施例13制得的为4-(3’-苯基丙基)-6-(4’’-甲苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮。
具体实施方式
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
实施例1
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到6-苯基-(3’-苯基丙基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率90%)。1hnmr(400mhz,cdcl3)δ8.28(d,j=7.8hz,2h),7.54(t,1h),7.47(t,j=7.5hz,2h),7.29(t,j=7.4hz,2h),7.20(t,j=6.8hz,3h),4.08(t,2h),2.76(t,j=7.6hz,2h),2.20–2.01(dt,2h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
实施例2
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-叔丁基苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到6-(4’-(叔丁基)苯基)-4-(3’’-苯基丙基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率86%)。1hnmr(400mhz,cdcl3)δ8.30(d,j=8.6hz,2h),7.56(d,j=8.6hz,2h),7.34(t,2h),7.25(t,j=6.2hz,3h),4.13(t,2h),2.81(t,j=7.6hz,2h),2.26–2.03(dt,2h),1.41(s,9h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
实施例3
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-乙炔基苯戊醚,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到6-(4’-(戊氧基)苯基)-4-(3’’-苯基丙基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率83%)。1hnmr(400mhz,cdcl3)δ8.41(d,j=9.0hz,2h),7.32(t,2h),7.24(t,j=5.8hz,3h),6.99(d,j=9.0hz,2h),4.16–3.91(m,4h),2.78(t,j=7.6hz,2h),2.12(dt,j=15.6,7.8hz,2h),1.93–1.73(m,2h),1.57–1.37(m,4h),1.00(t,j=7.1hz,3h).19fnmr(376mhz,cdcl3)δ-65.4(s,3f)。
实施例4
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol3-乙炔基噻吩,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-(3’-苯基丙基)-6-(3’’-噻吩基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率72%)。1hnmr(400mhz,cdcl3)δ8.90(d,j=2.1hz,1h),8.04(d,j=5.1hz,1h),7.40(dd,j=5.1,3.0hz,1h),7.33(t,2h),7.24(t,j=6.3hz,3h),4.12(t,2h),2.80(t,j=7.6hz,2h),2.40–2.03(dt,2h).19fnmr(376mhz,cdcl3)δ-65.3(s,3f)。
实施例5
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-氰基苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-(3’-苯基丙基)-6-(4’’-氰基苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率70%)。1hnmr(400mhz,cdcl3)δ8.46(d,j=8.5hz,2h),7.78(d,j=8.5hz,2h),7.32(t,j=7.4hz,2h),7.24(t,j=7.3hz,3h),4.14(t,2h),2.81(t,j=7.6hz,2h),2.27–2.08(dt,2h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
实施例6
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-正丙基苯乙炔,0.65mmol4’-甲基苄基叠氮,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-(4’-甲基苄基)-6-(4’’-正丙基苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率70%)。1hnmr(400mhz,cdcl3)δ8.29(d,j=8.3hz,2h),7.31(d,j=8.3hz,2h),7.22–7.07(m,4h),5.34(s,2h),2.68(t,2h),2.35(s,3h),1.70(dq,j=14.8,7.4hz,2h),0.98(t,j=7.3hz,3h).19fnmr(376mhz,cdcl3)δ-64.6(s,3f)。
实施例7
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol3-氟苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到6-(3’-氟苯基)-4-(3’’-苯基丙基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率90%)。1hnmr(400mhz,cdcl3)δ8.17(dd,j=7.9,0.9hz,1h),8.14–8.07(m,1h),7.47(td,j=8.1,5.9hz,1h),7.37–7.30(m,2h),7.28–7.20(m,4h),4.12(t,2h),2.81(t,j=7.6hz,2h),2.30–2.04(dt,2h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f),-112.0(ddd,1f,j=10.2,8.3,6.0hz)。
实施例8
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-氯苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到6-(4’-氯苯基)-4-(3’’-苯基丙基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率45%)。1hnmr(400mhz,cdcl3)δ8.34(d,j=8.6hz,2h),7.49(d,j=8.6hz,2h),7.33(t,j=7.5hz,2h),7.24(t,j=7.5hz,3h),4.13(t,2h),2.81(t,j=7.6hz,2h),2.15(dt,j=15.6,7.7hz,2h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
实施例9
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-正丙基苯乙炔,0.65mmol环己基叠氮,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-环己基-6-(4’-正丙基苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率90%)。1hnmr(400mhz,cdcl3)δ8.21(d,j=8.3hz,2h),7.30(d,j=8.3hz,2h),4.09(tt,j=11.7,3.5hz,1h),2.79–2.58(m,4h),1.95(d,j=12.4hz,2h),1.80(d,j=11.4hz,2h),1.69(td,j=14.9,7.4hz,3h),1.47–1.22(m,3h),0.97(t,j=7.3hz,3h).19fnmr(376mhz,cdcl3)δ-64.3(s,3f)。
实施例10
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-正丙基苯乙炔,0.65mmol1-叠氮基-2-苯基乙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-苯乙基-6-(4’-正丙基苯基)-3-(三氟甲基)-1,2,4-三唑-5(4h)-酮(分离产率100%)。1hnmr(400mhz,cdcl3)δ8.31(d,j=8.2hz,2h),7.63–6.81(m,7h),4.30(t,2h),3.09(t,2h),2.71(t,j=7.6hz,2h),1.90–1.57(m,2h),1.02(t,j=7.3hz,3h).19fnmr(376mhz,cdcl3)δ-65.3(s,3f)。
实施例11
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-正丙基苯乙炔,0.65mmol1-叠氮基正辛烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-正辛基-6-(4’-正丙基苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率95%)。1hnmr(400mhz,cdcl3)δ8.28(d,j=8.3hz,2h),7.33(d,j=8.3hz,2h),4.09(t,2h),2.68(t,2h),1.75(m,4h),1.52–1.23(m,10h),0.99(t,j=7.3hz,3h),0.91(t,j=6.8hz,3h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
实施例12
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-正丙基苯乙炔,0.65mmol1-叠氮基-2-(4’-硝基苯基)乙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-(4’-硝基苯乙基)-6-(4’’-正丙基苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率98%)。1hnmr(400mhz,cdcl3)δ8.21(d,j=8.2hz,2h),8.13(d,j=8.5hz,2h),7.46(d,j=8.5hz,2h),7.27(d,j=8.2hz,2h),4.26(t,2h),3.15(t,2h),2.63(t,j=7.6hz,2h),1.81–1.48(m,2h),0.95(t,j=7.3hz,3h).19fnmr(376mhz,cdcl3)δ-65.3(s,3f)。
实施例13
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol碘化亚铜,1ml四氢呋喃,0.5mmol4-甲基苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-(3’-苯基丙基)-6-(4’’-甲苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率94%)。1hnmr(400mhz,cdcl3)δ8.26(d,j=8.3hz,2h),7.34(t,j=7.6hz,4h),7.25(t,j=6.6hz,3h),4.12(t,2h),2.80(t,j=7.6hz,2h),2.46(s,3h),2.15(dt,j=15.6,7.8hz,2h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
实施例14
在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol溴化亚铜,1ml四氢呋喃,0.5mmol3-甲基苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-(3’-苯基丙基)-6-(3’’-甲苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率58%)。1hnmr(400mhz,cdcl3)δ8.12(d,j=5.5hz,2h),7.41(dd,j=8.7,5.9hz,2h),7.37–7.31(m,2h),7.25(t,j=6.7hz,3h),4.12(t,2h),2.81(t,j=7.6hz,2h),2.47(s,3h),2.16(dt,j=15.6,7.8hz,2h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
实施例15在氮气气氛中,在一个5ml反应管中放入聚四氟乙烯磁石一粒,加入0.025mmol四氟硼酸四(乙腈)亚铜(cu(ch3cn)4bf4),1ml四氢呋喃,0.5mmol4-甲基苯乙炔,0.65mmol1-叠氮基-3-苯基丙烷,0.75mmol三氟乙酸酐,最后加入1mmol三乙基胺,室温下在密闭体系中搅拌反应9h后,用100-200目硅胶过滤,二氯甲烷冲洗,合并有机相,然后旋蒸除去有机溶剂;得到的粗产物通过硅胶柱层析,以正戊烷和乙酸乙酯洗脱,得到4-(3’-苯基丙基)-6-(4’’-甲苯基)-3-(三氟甲基)-1,2,4-三嗪-5(4h)-酮(分离产率66%)。1hnmr(400mhz,cdcl3)δ8.26(d,j=8.3hz,2h),7.34(t,j=7.6hz,4h),7.25(t,j=6.6hz,3h),4.12(t,2h),2.80(t,j=7.6hz,2h),2.46(s,3h),2.15(dt,j=15.6,7.8hz,2h).19fnmr(376mhz,cdcl3)δ-65.5(s,3f)。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 含离子液体共溶剂介质中制备(R)‑3,5‑双三氟甲基苯乙醇的方法与流程
- 一种邻二氟苯的合成方法与制造工艺
- 2,2,2‑三氟乙硫醇的合成的制造方法与工艺
- 2-氯-3-(甲基硫烷基)-N-(1-甲基-1H-四唑-5-基)-4-(三氟甲基)苯甲酰胺或其盐在耐受HPPD抑制剂除草剂的转基因作物植物的区域中防治不想要的植物的用途的制造方法与工艺
- (R)‑3,5‑双(三氟甲基)苯乙醇的生物制备方法与制造工艺
- 2-(2-吡啶)-6-(2-氯-3-三氟甲基苯甲酰基)-5,7,8-三氢吡啶并[4,3-d]嘧啶及其制备方法与制造工艺
- 一种1,3,4-噻二唑类化合物及其制备方法与制造工艺
- 一种1,3,4-噻二唑类化合物及其制备方法与制造工艺
- 一种阿瑞吡坦中间体及其制备方法与制造工艺
- 一类含4,4’‑二氟二苯甲基的不对称α‑二亚胺镍配合物、其中间体、制备方法及其应用与制造工艺