肿瘤相关巨噬细胞双靶向多肽、纳米颗粒、制备及应用的制作方法
本发明涉及生物科学和药物载体技术领域,具体涉及提供一种肿瘤相关巨噬细胞双靶向多肽、纳米颗粒、制备及应用。
背景技术:
肿瘤相关巨噬细胞(tam)是肿瘤组织中含量最丰富的白细胞之一,但是由于肿瘤微环境的免疫抑制作用,其不能通过正常的吞噬作用和抗原提呈反应阻止肿瘤的发展。相反地,tam通过多种方式促进肿瘤的生长和恶化。如,通过表达血管内皮生长影子(vegf)促进肿瘤血管的新生,从而为肿瘤细胞提供充足的养分;通过表达pd-l1等抑制性配体,抑制具有肿瘤细胞杀伤能力的t细胞的活性;通过分泌il-10等异质性细胞因子,抑制抗肿瘤的免疫反应等等。由于tam的这些特性,导致其在肿瘤组织的大量募集往往与较差的预后直接相关。因此,研究人员普遍认为,将tam作为免疫治疗靶标具有广阔的临床应用前景。
目前,针对tam最广泛使用的治疗策略是使用非靶向药物,如曲妥单抗(trabectedin)和唑来膦酸(zoledronicacid)来剔除tam或扭转它们的分化状态。然而,由于巨噬细胞在先天性免疫反应中的重要作用及其全身分布特性,这些非靶向治疗可能存在安全性问题。因此,迫切需要具有tam靶向能力的运输载体。以前报道的纳米运输平台通过配体结合(如甘露糖和叶酸)或tam的吞噬能力显示出tam亲和力并获得了不错的治疗结果。然而,当靶向tam时,甘露糖和叶酸也会与其他细胞相结合。
因此,急需开发更具特异性的靶向tam的纳米载体,并以此为基础发展新的针对tam的肿瘤免疫疗法。
技术实现要素:
针对现有技术中存在的缺陷,本发明的目的在于提供一种肿瘤相关巨噬细胞双靶向多肽、纳米颗粒、制备及应用,实现高效靶向肿瘤相关巨噬细胞,达到抑制肿瘤生长的目的。
为达到以上目的,本发明采取的技术方案是一种肿瘤相关巨噬细胞双靶向多肽,所述双靶向多肽由α螺旋多肽、连接序列和m2型巨噬细胞靶向肽以共价键的形式串连而成。
在上述技术方案的基础上,所述α螺旋多肽的氨基酸序列为序列表中seqidno.1所示。
在上述技术方案的基础上,所述连接序列的氨基酸序列为gsg。
在上述技术方案的基础上,所述m2型巨噬细胞靶向肽的氨基酸序列为序列表中seqidno.2所示。
本发明还公开了一种靶向肿瘤相关巨噬细胞的纳米颗粒,所述纳米颗粒由双靶向多肽和磷脂、胆固醇脂和脂溶性光学探针组成。
在上述技术方案的基础上,所述磷脂为二肉豆蔻酰磷脂酰胆碱(dmpc)和二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-peg2000)中一种或两种的组合。
在上述技术方案的基础上,所述脂溶性光学探针为dir-boa。
本发明还公开了一种靶向肿瘤相关巨噬细胞的纳米颗粒的制备方法,包括以下步骤:
s1,将所述磷脂、胆固醇脂和脂溶性光学探针混合物溶解于氯仿中;将混合物溶液置于氮吹仪中吹干;将吹干后的混合物置于真空干燥器中干燥;将干燥后的混合物溶解于磷酸缓冲液中;
s2,将所述双靶向多肽溶解于磷酸缓冲液中制得双靶向多肽溶液,向步骤s1制得的混合物溶液中逐滴加入双靶向多肽溶液并混匀制得纳米颗粒溶液并孵育过夜;
s3,使用浓缩离心管浓缩孵育过夜后的纳米颗粒溶液制得纳米颗粒,使用纯化纳米颗粒获得最终产物。
本发明还公开了一种靶向肿瘤相关巨噬细胞的纳米颗粒的应用,所述纳米颗粒用于靶向肿瘤相关巨噬细胞运输药物,特异性剔除促进肿瘤生长的肿瘤相关巨噬细胞进而抑制肿瘤生长。
在上述技术方案的基础上,所述纳米颗粒通过sr-b1靶向基团及m2型巨噬细胞靶向基团的协同靶向作用靶向m2型巨噬细胞。
与现有技术相比,本发明的优点在于:
本发明公开了一种肿瘤相关巨噬细胞双靶向多肽,还公开了利用此双靶向多肽制备得到的纳米颗粒能够高效靶向肿瘤相关巨噬细胞运输药物,从而特异性地剔除肿瘤相关巨噬细胞进而抑制肿瘤生长。
本发明公开了靶向肿瘤相关巨噬细胞的纳米颗粒的制备方法,制备工艺简单,便于规模化生产;制备该纳米颗粒的原材料大多数都已用于临床或临床实验,且对小鼠的生理生化指标检测结果显示无毒副作用;制备的纳米颗粒具有良好的理化特性,纳米颗粒的粒径均一、分散性好,无聚集现象。
本发明公开了靶向肿瘤相关巨噬细胞的纳米颗粒的应用,将纳米颗粒用于靶向肿瘤相关巨噬细胞运输药物,可实现特异性剔除促进肿瘤生长的肿瘤相关巨噬细胞,达到抑制肿瘤生长的目的。
附图说明
图1为fplc系统纯化制备的肿瘤相关巨噬细胞靶向纳米颗粒时的双波段吸收-时间曲线图(280nm和700nm);
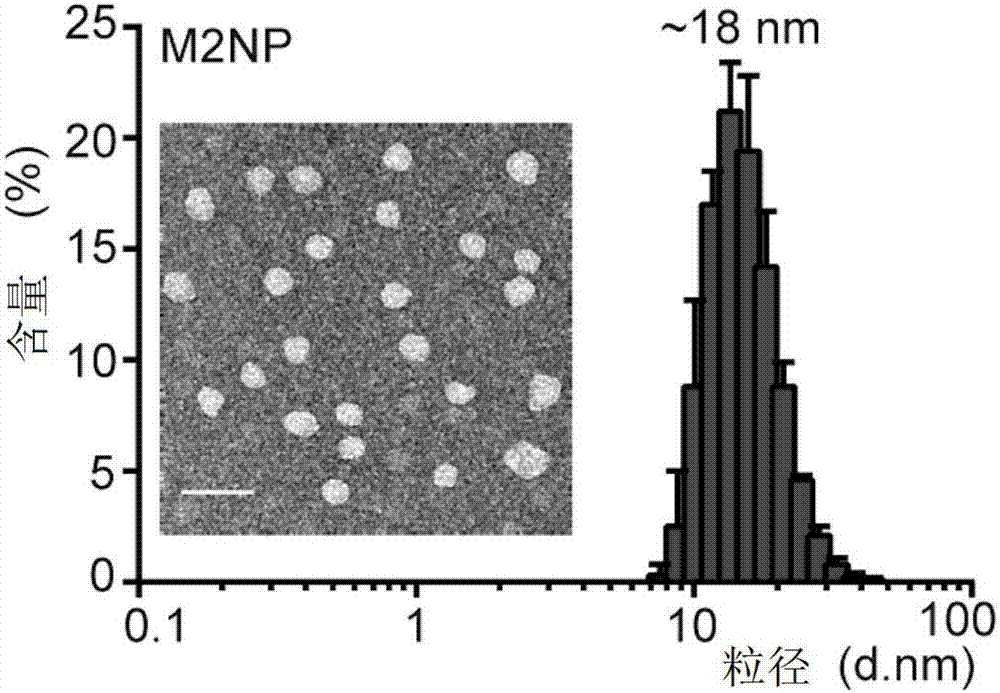
图2为动态光散射系统(dls)和透射电子显微镜(tem)对纳米颗粒的形态和粒径的检测结果示意图;
图3为使用流式细胞仪检测纳米颗粒靶向m2型巨噬细胞的能力的结果示意图;
图4为使用共聚焦显微镜检测注射了纳米颗粒后的肿瘤组织冰冻切片的结果示意图;
图5为纳米颗粒与chol-sicd115孵育并进行琼脂糖凝胶电泳后的荧光成像结果示意图;
图6为流式细胞仪检测装载sicd115的纳米颗粒剔除tam的能力的结果示意图;
图7为装载sicd115的纳米颗粒抑制肿瘤生长能力的检测结果曲线图;
图8为装载sicd115的纳米颗粒抑制肿瘤生长能力的检测结果示意图。
具体实施方式
以下结合附图及实施例对本发明作进一步详细说明。
实施例1:肿瘤相关巨噬细胞双靶向多肽
本发明实施例提供一种肿瘤相关巨噬细胞双靶向多肽,双靶向多肽由α螺旋多肽、连接序列和m2型巨噬细胞靶向肽以共价键的形式串连而成。α螺旋多肽的氨基酸序列为faekfkeavkdyfakfwd,α螺旋多肽的氨基酸序列为序列表中seqidno.1所示。连接序列的氨基酸序列为gsg。m2型巨噬细胞靶向肽的氨基酸序列为yeqdpwgvkwwy,m2型巨噬细胞靶向肽的氨基酸序列为序列表中seqidno.2所示。
实施例2:靶向肿瘤相关巨噬细胞的纳米颗粒
本发明实施例提供一种靶向肿瘤相关巨噬细胞的纳米颗粒,纳米颗粒由双靶向多肽和磷脂、胆固醇脂和脂溶性光学探针组成。磷脂为二肉豆蔻酰磷脂酰胆碱(dmpc)和二硬脂酰磷脂酰乙醇胺-聚乙二醇(dspe-peg2000)中一种或两种的组合。脂溶性光学探针为dir-boa。
实施例3:靶向肿瘤相关巨噬细胞的纳米颗粒的制备方法
本发明实施例提供一种靶向肿瘤相关巨噬细胞的纳米颗粒的制备方法,包括以下步骤:
s1,将3μmoldmpc,0.0114μmoldspe-peg2000,0.2μmoldir-boa和0.1μmolc.o(胆固醇酯)溶解于200μl氯仿中。混匀后,将混合物置于氮吹仪中,使用氮气吹干。将吹干后的混合物置于真空干燥器中,室温干燥1小时。使用2ml磷酸缓冲液溶解干燥后的混合物,并使用漩涡震荡仪混匀,然后使用超声仪在48℃下超声1小时。
s2,使用分析天枰称取0.4μmol双靶向多肽,并溶解于3ml磷酸缓冲液中。向水化后的磷脂,胆固醇混合物逐滴加入多肽溶液,并混匀。将多肽,磷脂,胆固醇混合物置于4℃下孵育过夜。
s3,使用30kd浓缩离心管于4℃,2500rpm下将孵育过夜后的纳米颗粒浓缩至1ml。使用凝胶过滤预装柱hiload16/60superdex200pg在fplc系统下获得纯化后的纳米颗粒,纯化结果参照图1所示,收集图中60-70min时间段内的纳米颗粒。dls和tem的结果显示,纳米颗粒成球形,分散性均一,粒径20nm左右,如图2所示。
实施例4:靶向肿瘤相关巨噬细胞的纳米颗粒的应用
本发明实施例提供一种靶向肿瘤相关巨噬细胞的纳米颗粒的应用:纳米颗粒用于靶向肿瘤相关巨噬细胞运输药物,特异性剔除促进肿瘤生长的肿瘤相关巨噬细胞进而抑制肿瘤生长。该纳米颗粒包括sr-b1靶向基团及m2型巨噬细胞靶向基团。该纳米颗粒通过sr-b1靶向基团及m2型巨噬细胞靶向基团的协同靶向作用靶向m2型巨噬细胞。
实施例5:纳米颗粒的tam靶向能力测试
实施例3中制备得到的纳米颗粒的tam靶向能力见图3和图4。由于tam趋向于m2型分化的巨噬细胞,因此先测试纳米颗粒靶向m2型巨噬细胞的能力,如图3所示,纳米颗粒可以高效靶向m2型巨噬细胞。当由荷瘤小鼠尾静脉注射纳米颗粒后,可以高效靶向tam,如图4所示。
实施例6:纳米颗粒装载剔除tam的药物能力测试
使用实施例3中的纳米颗粒装载剔除tam的药物,以sirna为例。使用胆固醇修饰具备tam剔除能力的sirna(sicd115)获得chol-sicd115,通过胆固醇chol-sicd115可以插入纳米颗粒的磷脂单分子层上。如图5所示,将chol-sicd115与纳米颗粒按照摩尔比10:1于室温下孵育1小时后进行琼脂糖凝胶电泳,可见chol-sicd115可以与纳米颗粒很好地结合。
实施例7:装载sirna的纳米颗粒剔除肿瘤中tam能力测试
实施例6中得到的装载sirna的纳米颗粒可以有效剔除肿瘤中的tam,如图6所示。经过多次给药后,荷瘤鼠肿瘤组织中的tam比例明显降低。
实施例8:装载sirna的纳米颗粒抑制肿瘤生长能力测试
实施例6中得到的装载sirna的纳米颗粒可以有效抑制小鼠黑色素瘤的生长。如图7和图8所示,经过多次给药后,小鼠黑色素瘤的生长得到显著抑制。
本发明不局限于上述实施方式,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围之内。本说明书中未作详细描述的内容属于本领域专业技术人员公知的现有技术。
序列表
<110>华中科技大学
<120>肿瘤相关巨噬细胞双靶向多肽、纳米颗粒、制备及应用
<160>2
<170>siposequencelisting1.0
<210>1
<211>18
<212>prt
<213>人工序列(artificialsequence)
<400>1
phealaglulysphelysglualavallysasptyrphealalysphe
151015
trpasp
<210>2
<211>12
<212>prt
<213>人工序列(artificialsequence)
<400>2
tyrgluglnaspprotrpglyvallystrptrptyr
1510
- 还没有人留言评论。精彩留言会获得点赞!