一种淫羊藿ISSR-PCR分子标记方法与流程
本发明属于分子标记技术领域,具体地说,涉及一种淫羊藿issr-pcr分子标记方法。
背景技术
淫羊藿属(epimediuml.)植物是小檗科(berberidaceae)多年生草本药用植物,具有补肾强身,强筋健骨、祛风湿等功效,是我国传统中药材之一。我国是淫羊藿最主要的分布区,淫羊藿属植物约占世界总数的80%,在甘肃、贵州、湖南、湖北等地均有分布。研究表明,不同产地淫羊藿的活性成分、形态、质量差异较大,且不同居群的淫羊藿生物学特征也存在明显差异,这表明淫羊藿资源生物多样性丰富。目前。关于淫羊藿的研究主要集中在其活性成分、分类、抗逆性、光合生理、物候特征等方面,而缺乏关于其遗传变异的研究。
分子标记技术能从dna水平上反映物种的遗传差异,是研究遗传多样性的有效方法。近年来,issr分子标记技术因其操作简单、多态性高、重复性好等优点被广泛应用于动植物的品种鉴定等。但issr标记是一种随机性标记方法,不同物种甚至同一物种不同条件下其试验参数均有差异,因此建立一个科学合理的issr-pcr反应体系,探寻最佳的pcr各组分的用量,可为后续开展淫羊藿的遗传多样性研究及良种选育等工作提供理论依据。
技术实现要素:
有鉴于此,本发明针对现有针对淫羊藿的研究缺乏关于其遗传变异研究的问题,提供了一种淫羊藿issr-pcr分子标记方法。
为了解决上述技术问题,本发明公开了一种淫羊藿issr-pcr分子标记方法,具体包括以下步骤:
步骤1,采集淫羊藿的嫩叶,提取植物组dna;
步骤2,采用1%琼脂糖凝胶电泳检测dna的完整性;
步骤3,采用引物及issr-pcr反应体系对步骤1提取的dna样品进行扩增。
进一步地,步骤3中issr-pcr反应体系为:20μl的反应体系中含有2×taqmastermix9.8μl,模板dna30ng,引物0.325μm。
进一步地,步骤3中issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,46.8~65℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
进一步地,步骤3中引物为:
ubc808,其核苷酸序列为:seqidno.1;
或ubc814,其核苷酸序列为:seqidno.2;
或ubc826,其核苷酸序列为:seqidno.3;
或ubc827,其核苷酸序列为:seqidno.4;
或ubc840,其核苷酸序列为:seqidno.5;
或ubc846,其核苷酸序列为:seqidno.6;
或ubc856,其核苷酸序列为:seqidno.7。
进一步地,步骤3中引物在issr-pcr扩增中优化后的退火温度,具体如下:ubc80860.3℃;ubc81446.8℃;ubc82660.3℃;ubc82765℃;ubc84052.4℃;ubc84654.3℃;ubc85654.3℃。
本发明还提供了一种引物,所述引物用于标记淫羊藿issr-pcr分子,所述引物为:
ubc808,其核苷酸序列为:seqidno.1;
或ubc814,其核苷酸序列为:seqidno.2;
或ubc826,其核苷酸序列为:seqidno.3;
或ubc827,其核苷酸序列为:seqidno.4;
或ubc840,其核苷酸序列为:seqidno.5;
或ubc846,其核苷酸序列为:seqidno.6;
或ubc856,其核苷酸序列为:seqidno.7。
进一步地,所述引物在issr-pcr扩增中优化后的退火温度,具体如下:ubc80860.3℃;ubc81446.8℃;ubc82660.3℃;ubc82765℃;ubc84052.4℃;ubc84654.3℃;ubc85654.3℃。
与现有技术相比,本发明可以获得包括以下技术效果:
1)本发明利用引物及优化后的issr-pcr反应体系对淫羊藿的dna进行issr-pcr扩增,该方法准确可靠、操作简单、节约时间和成本,扩增条带清晰稳定,多态性好,对淫羊藿的遗传多样性分析、鉴定及良种选育等方面具有较好的应用价值。
2)本发明提供一种淫羊藿的issr-pcr分子标记用引物,并在该引物的基础上建立并优化了淫羊藿的issr-pcr分子标记体系,根据结果显示,该体系扩增的条带清晰稳定,具有较好的多态性特点,操作步骤较少,易于快速分析检测。
当然,实施本发明的任一产品并不一定需要同时达到以上所述的所有技术效果。
附图说明
此处所说明的附图用来提供对本发明的进一步理解,构成本发明的一部分,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
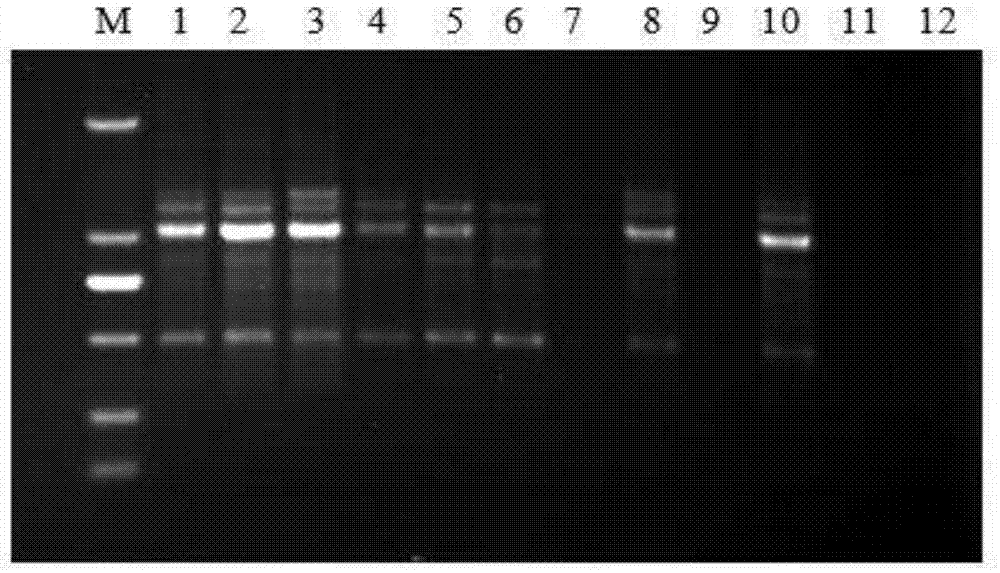
图1为本发明issr-pcr均匀设计试验的扩增结果;其中m表示:marker;引物为ubc840;1-12为表2的处理组合1-12;
图2为本发明2×taqmastermix作为单因素的issr-pcr扩增结果;m表示:marker;引物为ubc840;1-7为表3中的处理组合1-7;
图3为本发明2×taqmastermix微调的issr-pcr扩增结果;m表示:marker;引物为ubc840;1-12为表4中的处理组合1-12;
图4为本发明引物作为单因素的issr-pcr扩增结果;m表示:marker;引物为ubc840;1-7为表5中的处理组合1-7;
图5为本发明引物微调的issr-pcr扩增结果;m表示:marker;引物为ubc840;1-9为表6中的处理组合1-9;
图6为本发明dna作为单因素的issr-pcr扩增结果;m表示:marker;引物为ubc840;1-7为表7中的处理组合1-7;
图7为引物ubc840最佳退火温度的确定;m表示:marker;引物为ubc840;从左到右温度依次为:45℃、46.4℃、48.8℃、52.4℃、57.2℃、61.0℃、63.5℃、65℃;
图8为13个淫羊藿样本验证优化后反应体系的issr-pcr扩增结果;m表示:marker;引物为ubc840;1-13为13个淫羊藿样品issr-pcr产物的电泳条带。
具体实施方式
以下将配合实施例来详细说明本发明的实施方式,藉此对本发明如何应用技术手段来解决技术问题并达成技术功效的实现过程能充分理解并据以实施。
实施例1issr-pcr扩增体系的建立与优化
1、dna的提取
将研钵用清水洗净晾干,加入5ml的无水乙醇后点燃,待研钵晾凉后,取采集到的淫羊藿嫩芽500mg于研钵中,倒入适量液氮,以液氮没过样品2~3cm高度为宜,研磨3~5min,然后采用试剂盒法提取石斛基因组dna。
2、issr-pcr扩增体系的建立
1)issr-pcr反应体系的均匀设计试验方案
采用u12(43)均匀设计表,pcr扩增体系的因素水平见表1。以ubc840为引物,淫羊藿dna为模板,利用表2中的12个反应体系对issr-pcr进行优化筛选,反应体系为20μl,具体见表2。
所述的issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,52.4℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
表1因素水平表(单位:μl)
表2均匀设计试验表u12(43)/单位:μl
结果如图1所示,除7、9、11、12以外,其他处理均有扩增条带。其中处理1、2、3、8、10扩增条带明亮清晰,且条带数多,为较为理想的处理。在此基础上进行2×taqmastermix的单因素试验。
2)2×taqmastermix作为单因素的issr-pcr试验方案
根据均匀设计试验结果,以ubc840为引物,淫羊藿的基因组dna为模板,在20μl的反应体系中,设计2×taqmastermix的量分别为0μl、4μl、6μl、8μl、10μl、12μl、14μl进行issr-pcr,引物、dna及ddh2o的用量见表3。
所述的issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,52.4℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
表32×taqmastermix的单因素试验表(单位:μl)
2×taqmastermix的单因素试验结果见图2,处理4、5、6、7扩增条带清晰明亮,为较为理想的处理。考虑引物用量的经济性,在处理4的基础上进行引物的微调试验。
3)2×taqmastermix作为单因素的issr-pcr微调试验方案
根据均匀设计试验结果,以ubc840为引物,淫羊藿的基因组dna为模板,在20μl的反应体系中,设计2×taqmastermix的量分别为7.8μl、8μl、8.2μl、8.4μl、8.6μl、8.8μl、9μl、9.2μl、9.4μl、9.6μl、9.8μl、10μl进行issr-pcr,引物、dna及ddh2o的用量见表4。
所述的issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,52.4℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
表42×taqmastermix微调试验表(单位:μl)
2×taqmastermix微调试验结果见图3,所有处理均有扩增条带。处理11的扩增条带清晰明亮且无拖尾现象,为较为理想的扩增条件。
4)引物作为单因素的issr-pcr试验方案
以ubc840为引物,淫羊藿的基因组dna为模板,在20μl的反应体系中,设计引物的量分别为0μl、1μl、2μl、3μl、4μl、5μl进行issr-pcr,2×taqmastermix、dna及ddh2o的用量见表5。
所述的issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,52.4℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
表5引物的单因素试验表(单位:μl)
引物单因素试验结果见图4,处理3、4、5、6、7有扩增条带。处理4、5、6、7明亮清晰,为较为理想的扩增条件。考虑引物用量的经济性,在处理3的基础上进行引物的微调试验。
5)引物作为单因素的issr-pcr微调试验方案
以ubc840为引物,引物的基因组dna为模板,在20μl的反应体系中,设计引物的量分别为1.8μl、2μl、2.2μl、2.4μl、2.6μl、2.8μl、3μl、3.2μl、3.4μl进行issr-pcr,2×taqmastermix、dna及ddh2o的用量见表6。
所述的issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,52.4℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
表6引物微调试验表(单位:μl)
引物微调试验结果见图5,所有处理均有条带,且处理5、6、7条带较为清晰、稳定,为较理想的扩增条件。综合考虑引物的用量、清晰度,确定处理5是引物的最佳用量。
6)dna作为单因素的issr-pcr试验方案
以ubc840为引物,淫羊藿的基因组dna为模板,在20μl的反应体系中,设计dna的量分别为0μl、1μl、2μl、3μl、4μl、5μl、6μl进行issr-pcr,2×taqmastermix、dna及ddh2o的用量见表7。
所述的issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,52.4℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
表7dna的单因素试验表(单位:μl)
dna的单因素试验结果见图6,除处理1外,其余处理均有扩增条带。且处理4条带清晰明亮,为较为理想的扩增条件。
实施例2issr引物的筛选及最佳退火温度的确定
本发明所用的issr引物来自于加拿大哥伦比亚大学公布的引物序列,由上海英骏负责合成。
在均匀设计及单因素试验确定最优反应体系的基础上,在伯乐pcr仪上进行引物最佳退火温度的确定,梯度的设定以理论退火温度tm-5℃~tm+5℃进行设定,共设置8个温度梯度(图7)。筛出的引物及最佳退火温度见表8。
表8引物及退火温度
引物为:
ubc808,其核苷酸序列为:agagagagagagagagc,如seqidno.1所示;
ubc814,其核苷酸序列为:ctctctctctctctcta,如seqidno.2所示;
ubc826,其核苷酸序列为:acacacacacacacacc,如seqidno.3所示;
ubc827,其核苷酸序列为:acacacacacacacacg,如seqidno.4所示;
ubc840,其核苷酸序列为:gagagagagagagagayt,如seqidno.5所示;
ubc846,其核苷酸序列为:cacacacacacacacart,如seqidno.6所示;
ubc856,其核苷酸序列为:acacacacacacacacya,如seqidno.7所示。
引物ubc840的梯度pcr扩增结果见图7。由图7可知,温度过高时无扩增条带,温度过低时,有微弱扩增条带。当温度为52.4℃时,扩增条带明亮清晰,据此确定引物ubc840的最佳退火温度为52.4℃。其余引物的最佳退火温度依据此方法确定,具体见表8。
实施例3优化后的issr-pcr反应体系的验证
以ubc840为引物,采自湖南、贵州、湖北的13个淫羊藿样本的dna为模板,对优化后的反应体系进行issr-pcr验证。
所述的issr-pcr扩增体系为:20μl的反应体系中含有2×taqmastermix9.8μl,模板dna30ng,引物0.325μm。
所述的issr-pcr扩增程序为:94℃预变性4min,94℃变性1min,48.6~65℃退火40s,72℃延伸40s,循环40次,72℃再延伸5min,4℃保存。
结果表明,扩增条带清晰稳定(图8),说明该反应体系适合淫羊藿的issr分析。
上述说明示出并描述了发明的若干优选实施例,但如前所述,应当理解发明并非局限于本文所披露的形式,不应看作是对其他实施例的排除,而可用于各种其他组合、修改和环境,并能够在本文所述发明构想范围内,通过上述教导或相关领域的技术或知识进行改动。而本领域人员所进行的改动和变化不脱离发明的精神和范围,则都应在发明所附权利要求的保护范围内。
序列表
<110>湖北省农业科学院中药材研究所
<120>一种淫羊藿issr-pcr分子标记方法
<141>2018-09-07
<160>7
<170>siposequencelisting1.0
<210>1
<211>17
<212>dna
<213>人工序列(artificialsequence)
<400>1
agagagagagagagagc17
<210>2
<211>17
<212>dna
<213>人工序列(artificialsequence)
<400>2
ctctctctctctctcta17
<210>3
<211>17
<212>dna
<213>人工序列(artificialsequence)
<400>3
acacacacacacacacc17
<210>4
<211>17
<212>dna
<213>人工序列(artificialsequence)
<400>4
acacacacacacacacg17
<210>5
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>5
gagagagagagagagayt18
<210>6
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>6
cacacacacacacacart18
<210>7
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>7
acacacacacacacacya18
- 还没有人留言评论。精彩留言会获得点赞!