福寿螺金属硫蛋白基因cds及其克隆方法和表达方法与流程
本发明属于基因工程技术领域,涉及一种福寿螺金属抗性相关功能基因类金属硫蛋白基因cds的克隆方法,以及该基因编码的蛋白质在大肠杆菌bl21(de3)系统中的表达方法以及其表达验证方法。
背景技术:
福寿螺(pomaceacanaliculata)是腹足纲瓶螺科瓶螺属的软体动物,是全球100种恶性入侵物种之一,除严重破坏入侵地农业生产和水生生态系统造成外,也是广州管圆线虫等致病性寄生虫的重要媒介。
福寿螺对cu2+污染水体的耐受能力显著高于其他淡水螺群,其cu2+96hlc50为146ug/l,是其他淡水螺群的1.6~6.6倍[1-6]。福寿螺体内存在能贮存cu2+并使之解毒的分子机制,涉及重要功能基因包括抗氧化酶系的超氧化物歧化酶,谷胱甘肽过氧化酶和谷胱甘肽转移酶等,非酶类的热休克蛋白基因等[7,8]。除了上述蛋白以外,金属硫蛋白(metallothionein,mts)作为水生软体动物非酶效应金属应激保护物质的典型代表,已证明能够显著减少机体有害金属存在并修复金属引起的机体氧化损伤[9]。该类基因的表达,编码蛋白的合成和调控是福寿螺金属逆境适应的关键机制。
软体动物mts核酸和氨基酸序列具有多样性,生理功能也存在显著差异,但通常末端具有c-x-c-x(3)-c-t-g-x(3)-c-x-c-x(3)-c-x-c-k的特征结构域。基于序列相似性和系统发育关系,软体动的mts归类为金属硫蛋白家族2,并可细分为mo、mo1、mo2和mog四个亚家族。福寿螺作为一种世界性的外来入侵物种,有关福寿螺中金属硫蛋白家族尚无基因或蛋白的相关研究报道,通过本发明获得福寿螺金属硫蛋白基因(metallothionein-likeprotein,mtlp)的cds及应用大肠杆菌bl21(de3)表达的该蛋白,能为软体动物腹足纲中金属硫蛋白家族相关基因和蛋白的功能研究奠定基础,更可为有效控制福寿螺扩散危害提供理论依据和实践参考。
[1]yaopingl,huangp,liuz,etal.acutetoxicityeffectsoffourheavymetalionsonbellamyaquadrata[j].journaloflishuiuniversity,2014。
[2]薛明,柯才焕,周时强,etal.金属对波部东风螺早期发育的毒性及edta的解毒效果[j].热带海洋学报,2004,23(1):44-50。
[3]kamblesb,kamblena.behaviouralchangesinfreshwatersnailbellamyabengalensisduetoacutetoxicityofcoppersulphateandacaciasinuata[j].internationaljournalofscienceenvironment&technology,2014,3(3)。
[4]guptapk,khangarotbs,durvevs.thetemperaturedependenceoftheacutetoxicityofcoppertoafreshwaterpondsnail,viviparusbengalensisl[j].hydrobiologia,1981,83(3):461-464。
[5]vipaweed,phanwimolt,maleeyak,etal.histopathologicalchangesinsnail,pomaceacanaliculata,exposedtosub-lethalcoppersulfateconcentrations[j].ecotoxicology&environmentalsafety,2015,122(4):s15256。
[6]khangarotbs,mathurs,durvevs.comparativetoxicityofheavymetalsandinteractionofmetalsonafreshwaterpulmonatesnaillymnaeaacuminata(lamarck)[j].clean-soil,air,water,2010,10(4):367-375。
[8]khangarotbs,mathurs,durvevs.comparativetoxicityofheavymetalsandinteractionofmetalsonafreshwaterpulmonatesnaillymnaeaacuminata(lamarck)[j].clean-soil,air,water,2010,10(4):367-375。
[9]bigota,doyenp,vasseurp,etal.metallothioneincodingsequenceidentificationandseasonalmrnaexpressionofdetoxificationgenesinthebivalvecorbiculafluminea[j].ecotoxicology&environmentalsafety,2009,72(2):382-387。
[10]徐炳政,张东杰,王颖,etal.金属硫蛋白及其金属解毒功能研究进展[j].中国食品添加剂,2014(5):171-175。
技术实现要素:
本发明针对现有技术存在的不足,提供一种福寿螺金属抗性相关基因类金属硫蛋白基因(metallothionein-likeprotein,mtlp)的cds克隆的方法,以及该基因在大肠杆菌bl21(de3)中表达编码蛋白的方法。
本发明中的福寿螺金属硫蛋白基因cds,该基因的核苷酸序列为:
atgtcttcttccgaagcacatgctcaccatcacggtgggtgcgctaaagagtgcaagaagtcaaaggagagctgctgtgaaggtgcttgcactgatgaatgcaaaaagaccccatgcaactgtggtgataactgcaaatgttctgatggatgcagatgtcagtcttgttcagcgccctgcaagtgtgatggtacttgtcagtgtggaaagggctgcactggagccgacagctgcaagtgtgatcgcaagtgttcttgcaagtga。
本发明中的福寿螺金属硫蛋白基因cds的克隆方法,包括以下步骤:
(1)mtlp基因的cds的扩增与纯化
上游引物为5’-ccggaattcatgtcttcttccgaagcac-3’,引入ecori酶切位点和保护碱基ccg,下游引物为5’-cccaagctttcacttgcaagaacacttgc-3’,引入了hindiii酶切位点和保护碱基ccc;以福寿螺肝胰腺组织总rna的反转录获得的cdna为模板,进行pcr扩增。
优选的,在步骤(1)中,pcr扩增的条件为94℃预变性3分钟,94℃30s,58℃30s,72℃1min,35个循环,72℃7min,产物用柱式pcr产物纯化试剂盒纯化。
本发明的福寿螺金属硫蛋白在大肠杆菌bl21(de3)中的表达方法,包括以下步骤:
(1)puc19-mtlp克隆重组质粒的构建
使用ecorⅰ,hindⅲ内切酶双酶切puc19质粒和pcr纯化产物,将双酶切产物进行1%琼脂糖凝胶电泳检测,对目的条带进行切胶回收,并用t4dna连接酶重组连接后转化大肠杆菌dh5α感受态细胞,经氨苄青霉素和蓝白斑筛选,挑取白色菌落进行pcr和双酶切鉴定,将阳性克隆进行测序;
(2)表达载体pet28(+)-mtlp质粒的构建
使用ecorⅰ,hindⅲ内切酶双酶切puc19-mtlp重组质粒和pet28a(+)质粒,将双酶切产物进行1%琼脂糖凝胶电泳,对目的条带进行切胶回收,并用t4dna连接酶重组连接后转化大肠杆菌dh5α感受态细胞,双酶切和pcr筛选阳性克隆,提取质粒再转化大肠杆菌bl2(de3)感受态细胞,pcr和双酶切鉴定,将阳性克隆进行测序以确定连接方向和对码情况;
(3)目的基因mtlp的表达
获得的含有正确重组子的工程菌bl21(de3)接种含有50ug/ml卡那霉素的lb液体培养基摇床过夜培养;再以1%接种量接种到新的含有50ug/ml卡那霉素的lb液体培养基20℃摇床培养3h至od600为0.4-0.6,添加iptg至终浓度0.9mm,20℃继续诱导培养4h,12000rpm离心5min收集菌体沉淀,加2×sds凝胶加样缓冲液,混匀后沸水浴10min,sds—page电泳分析表达产物。
优选的,获得的福寿螺金属硫蛋白在大肠杆菌bl21(de3)中表达的蛋白分子大小为13kd。
本发明对福寿螺金属硫蛋白基因cds的表达验证方法,包括以下步骤:
(1)mtlp的cds扩增结果
从福寿螺肝胰腺组织总rna反转录获得的cdna中获得300bp左右的dna片段;
(2)puc19-mtlp克隆重组质粒的构建
菌液pcr扩增,获得300bp左右的dna片段;用ecorⅰ,hindⅲ双酶切鉴定,获得300bp和2700bp左右两条特异条带,去除puc19部分,m13通用引物测序显示mtlp基因的cds其核苷酸序列如下:
atgtcttcttccgaagcacatgctcaccatcacggtgggtgcgctaaagagtgcaagaagtcaaaggagagctgctgtgaaggtgcttgcactgatgaatgcaaaaagaccccatgcaactgtggtgataactgcaaatgttctgatggatgcagatgtcagtcttgttcagcgccctgcaagtgtgatggtacttgtcagtgtggaaagggctgcactggagccgacagctgcaagtgtgatcgcaagtgttcttgcaagtga;
(3)pet28a(+)-mtlp表达重组质粒的构建
菌液pcr扩增,获得300bp左右的dna片段;用ecorⅰ,hindⅲ酶切,获得300bp和5000bp左右两条特异条带,去除pet28a(+)部分,用t7通用引物测序结果同上述mtlp基因的cds测序结果相同,插入方向和对码均正确,表达出87个氨基酸,序列如下:
metserserserglualahisalahishishisglyglycysalalysglucyslyslysserlysglusercyscysgluglyalacysthraspglucyslyslysthrprocysasncysglyaspasncyslyscysseraspglycysargcysglnsercysseralaprocyslyscysaspglythrcysglncysglylysglycysthrglyalaaspsercyslyscysasparglyscyssercyslys***。
利用本发明涉及的各种方法,可以获得福寿螺金属硫蛋白基因完整的cds序列,并实现其编码蛋白质在大肠杆菌bl21(de3)系统中的表达,本发明有助于进一步研究该基因在软体动物腹足纲金属逆境适应中的作用,更有助于开发福寿螺金属硫蛋白基因表达抑制药物,通过降低福寿螺金属抗性增强以硫酸铜为主要成分农药的对其杀灭效果。
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例中所需要使用的附图作简单介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
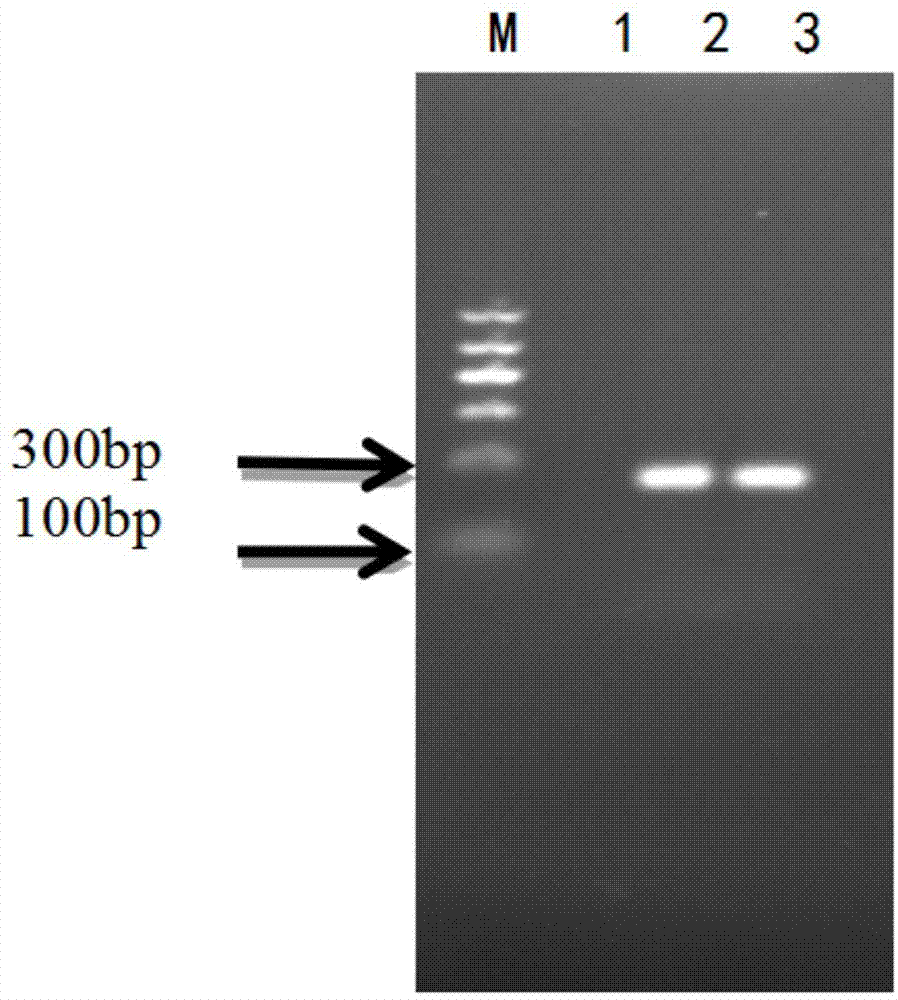
图1为扩增获得mtlp基因的cds片段的1.5%凝胶电泳检测图;
图2为puc19-mtlp质粒的双酶切鉴定结果图;
图3为福寿螺mtlp与其他软体动物mt家族成员遗传进化分析图;
图4为pet28a(+)-mtlp质粒的双酶切鉴定结果图;
图5为qrt-pcr测定相对福寿螺肝胰腺组织mtlp基因转录水平与cu2+胁迫浓度关系图。
图6为福寿螺mtlp在bl21(de3)表达情况sds-page电泳结果图
图1中,m为markerⅱ,1为阴性对照,2和3为pcr产物;
图2中,m1为markerⅳ,m2为markerⅱ,1、2、3、4为双酶切puc19-mtlp重组质粒,5为阴性对照;
图4中,m为markerⅳ123为双酶切pet28a(+)-mtlp质粒;
图6中,m为蛋白非预染markerⅰ,1为pet28a(+)-mtlp未诱导,2为pet28a(+)-mtlp诱导后。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
本发明列举了以下几个代表性实施,这些实施仅是示例性的,且不用于限制本发明的范围,这些实施例仅用于对本发明进行说明。且具体实施步骤以及所使用的试剂与仪器如下:
实例1
福寿螺肝胰腺组织总rna的提取和cdna第一条链的合成
福寿螺肝胰腺组织总rna的提取按照minibestuniversal总rna提取试剂盒操作指南进行,模板cdna第一条链合成按照primescriptrtreagentkitwithgdnaeraser试剂盒操作指南进行。肝胰腺组织置于-80℃保存,cdna置于-20℃保存。
实例2
mtlp基因的cds的扩增与纯化
利用clonemanager9分析目的片段及原核表达载体pet28a(+)的核酸序列后,用primerpremier6.0设计引物,上游引物为5’-ccggaattcatgtcttcttccgaagcac-3’,下游引物为5’-cccaagctttcacttgcaagaacacttgc-3’。pcr体系为2×tagmastermix12.5ul,ddh2o8.5ul,上下游引物各0.5ul(10um),cdna2ul。结束后按照柱式pcr产物纯化试剂盒操作指南对产物进行纯化,并进行1%琼脂糖凝胶电泳检测,参见图1。
实例3
puc19-mtlp克隆重组质粒的构建
酶切条件为37℃酶切4h后,65℃加热20分钟灭活限制性内切酶,连接条件为16℃连接6h后,于70℃加热10分钟灭活t4dna连接酶,酶切体系为:mtlp基因cdspcr产物70ul,灭菌水10ul,ecorⅰ5ul,hindⅲ5ul,10xbufferw10ul;puc19质粒25ul,灭菌水10ul,ecorⅰ5ul,hindⅲ5ul,10xbufferw5ul,连接体系为:puc19质粒回收片段2ul,mtlp基因cdspcr产物回收片段6ul,t4dnaligase1ul,10xligasebuffer1ul,成功构建的puc19-mtlp重组质粒双酶切鉴定结果,参见图2。
实例4
pet28(+)-mtlp表达重组质粒的构建
酶切条件puc19-mtlp质粒25ul,pet28a(+)-mtlp质粒25ul,灭菌水10ul,ecorⅰ5ul,hindⅲ5ul,10xbufferw5ul。连接体系为:pet28a(+)质粒dna4ul,mtlp基因cds4ult4dnaligase1ul,10xligasebuffer1ul。重组连接后先转化大肠杆菌dh5α感受态细胞,双酶切和pcr筛选阳性克隆,按照质粒提取试剂盒操作指南提取提取质粒再转化大肠杆菌bl21(de3)感受态细胞,挑选单个白色菌落进行pcr和双酶切鉴定,将阳性克隆进行测序以确定对码情况,成功构建的pet28(+)-mtlp重组质粒双酶切鉴定结果,参见图4。
实例5
不同浓度下胁迫7天,福寿螺目的基因mtlp的表达分析
0、50、100、150、200ug/l的cu2+胁迫下,福寿螺肝胰腺组织mtlp基因表达倍数值分别为:1.00±0,1.94±0.4,2.77±1.49,1.5±0.5,1.75±0.51(图5),以t检验分析每两组间产生的2-△△ct值,其中50,100,150和200ug/lcu2+实验组福寿螺肝胰腺组织中mtlp基因转录水平较0ug/l对照组存在显著差异(p<0.05),cu2+浓度由50ug/l升高到100ug/l对mtlp基因的转录未产生显著影响(p>0.05),而由100ug/l提高到150ug/l则影响显著(p<0.05),200ug/l和50ug/lcu2+浓度下mtlp基因的表达水平没有显著差异(p>0.05)。结果表明,mtlp基因可能与福寿螺铜离子解毒过程紧密相关,低浓度cu2+即可诱导福寿螺肝胰腺组织mtlp基因表达,并随浓度升高诱导作用进一步增强,当cu2+浓度>100ug/l时,诱导作用下降,提示该浓度可能接近福寿螺cu2+承受能力的极限,为诱导的阈值。
实例6
福寿螺mtlp与其他软体动物mt家族成员遗传进化分析:用mega7.0软件构建6种淡水软体动物mts的n-j遗传进化树,bootstrap进行检验,结果如图3所示,福寿螺同属不同种间mts亲缘关系最近,分支最短;与腹足纲的玉黍螺的亲缘关系较近,与三角帆蚌、近江牡蛎的亲缘关系较远,与珠蚌和贻贝的亲缘关系最远,该进化树显示了福寿螺mtlp和其他软体动物mts家族成员可能具有共同的进化根源。
实例7
含有重组子pet28a(+)-mtlp的bl21(de3)工程菌,经iptg诱导后,取处理的菌体沉淀进行sds—page电泳,由于mtlp结合sds的量会偏少,在sds-page电泳中迁移速度将比预期慢,结果如图6所示,经诱导的转化菌株在20kd处出现高浓度蛋白条带,其位置大于预期的13kd,而经未诱导的细菌相应位置蛋白条带较弱。
本发明所用材料如下:rna提取试剂盒,cdna第一条链合成试剂盒,荧光定量试剂盒为takara公司产品;琼脂糖凝胶dna回收试剂盒为axygen公司产品;质粒提取试剂盒购为omega公司产品;tagmastermix,markerⅰ、markerⅱ、markerⅳ为天根公司产品;pet28a(+),puc19质粒为中国疾病预防控制中心寄生虫病预防控制所重点实验室保存;柱式pcr产物纯化试剂盒,dh5α,bl21(de3)感受态细胞,iptg溶液,x-gal溶液,硫酸卡那霉素粉末,氨苄青霉素钠粉末,非预染蛋白markerⅰ,sds-page变性丙烯酰胺凝胶快速制备试剂盒,限制性内切酶ecorⅰ,hindⅲ为生工公司产品。
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!