新型肽的制作方法
本发明涉及一种新型肽,更具体地,涉及一种用于促进硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽、一种对上述肽进行编码的多核苷酸、一种包含上述多核苷酸的表达载体及包含上述肽的用于预防或治疗牙本质-牙髓疾病和/或牙周疾病的药学组合物、用于预防或改善牙本质-牙髓疾病和/或牙周疾病的医药外品组合物以及用于预防或改善的保健功能性食品组合物。
背景技术:
:牙髓作为存在于牙齿内部的填满牙髓腔的柔软的结缔组织,是指神经和血管分布得丰富,并且达到牙本质内表层的地方。在这种牙髓中发生的病变被称为牙髓疾病。牙髓疾病的原因有很多种,在大部分的情况下,通过基于龋齿的细菌感染以及牙齿的穿孔、断裂、龟裂、牙周袋,由向牙髓内部产生感染而发生。并且,外伤、磨耗、牙齿龟裂及治疗时在牙科用器具中产生的热和摩擦等也可诱发牙髓疾病。基于细菌感染的牙髓炎可发展为齿根端疾病和牙周疾病。当发生牙髓疾病时,按照牙髓充血、牙髓炎、牙髓坏死的顺序展开。在牙髓坏死的情况下,由于牙髓死亡,从而完全不能向牙髓供给血液,因此导致使整个牙周组织消失,最终可导致齿根端疾病或整个牙齿的异常。在牙髓、齿根端疾病的治疗中使用盖髓材料和牙根管填充材料,通常使用氢氧化钙、三氧化矿物凝聚体(mta,mineraltrioxideaggregate)、杜仲胶(gutta-percha)。在mta的情况下,具有密封力和生物相容性,从而在治疗中呈现效果,但是相对地,作为牙科治疗剂产生高费用、变色,从而产生审美性问题。在杜仲胶的情况下,费用经济且流动性好,但是是导致丧失牙髓活力的非生理性的治疗方法。就截至目前治疗牙本质-牙髓疾病的保守的治疗方法而言,使治疗的牙齿变弱或易碎,并且具有再感染的风险。牙周组织(periodontium)是由上皮组织、软组织性结缔组织及钙化的结缔组织构成的复合器官。作为牙周组织的结构有牙龈(gingiva)、牙周韧带(pdl:periodontalligament)、牙骨质(cementum)及牙槽骨(alveolarbone)。牙龈成纤维细胞(gingivalfibroblast)和牙周韧带成纤维细胞(periodontalligamentfibroblast)是牙龈软组织性结缔组织的主要细胞构成成分,执行形成细胞外基质(extracellularmatrix)并对其进行维持的作用。其中,已知牙龈成纤维细胞主要参与维持牙龈结缔组织,相反地,牙周韧带成纤维细胞因其特有的功能,不仅可以形成牙周韧带而且参与生物体内的邻接牙槽骨及牙骨质的修复和再生。若出现牙周疾病,则在临床上因牙龈出血和肿胀、牙周袋的形成及牙槽骨破坏等而使得失去牙齿。治疗牙周疾病的最终结果是复原损伤的结缔组织、牙骨质及牙槽骨,为此不仅需要使支撑牙槽骨的牙周韧带再生,而且需要可供牙周韧带附着的牙槽骨和牙骨质的再生。因此,为了开发出能够有效地治疗上述牙本质-牙髓疾病或牙周疾病的治疗剂,正活跃地进行着相关的研究。例如,在韩国公开专利第2012-0089547号中公开有一种包含成釉细胞、顶芽细胞或它们的培养液作为有效成分的硬组织形成及牙本质或牙髓组织再生用组合物,在韩国公开专利第2009-0033643号中公开有一种新型来源于牙滤泡的牙齿干细胞及其培养方法。而且,在韩国公开专利第2016-0105627号中公开了一种包含成釉细胞培养液的牙周疾病治疗用组合物。在这种背景下,本发明人为了开发出能够更有效地治疗诱发牙本质-牙髓疾病和/或牙槽骨和牙骨质损伤的牙周疾病的制剂,锐意研究,努力的结果开发出了用于促进包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生的细胞治疗及呈现牙本质-牙髓疾病和/或牙周疾病治疗效果的肽,并且完成了本发明。技术实现要素:解决的技术问题本发明的一目的在于,提供一种用于促进硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽。本发明的另一目的在于,提供对上述肽进行编码的多核苷酸。本发明的再一目的在于,提供一种包含上述多核苷酸的表达载体。本发明的还一目的在于,提供一种包含上述肽的牙本质-牙髓疾病和/或牙周疾病的预防或治疗用药学组合物。本发明的又一目的在于,提供一种包含上述肽的牙本质-牙髓疾病和/或牙周疾病的预防或改善用医药外品组合物。本发明的又一目的在于,提供一种包含上述肽的牙本质-牙髓疾病和/或牙周疾病的预防或改善用保健功能性食品组合物。本发明的又一目的在于,提供一种牙本质-牙髓疾病和/或牙周疾病的预防或治疗方法,其包括将包含上述肽的组合物给予到除了人之外的个体的步骤。本发明的又一目的在于,提供一种包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生促进方法,其包括将包含上述肽的组合物给予到除了人之外的个体的步骤。本发明的又一目的在于,提供一种上述肽的硬组织和/或牙髓组织的再生促进用途。本发明的又一目的在于,提供一种上述肽的牙本质-牙髓疾病或牙周疾病的预防或治疗用途。本发明的目的不限于以上提及的内容,本发明所属
技术领域:
的普通技术人员可以从以下记载明确理解未提及的其它目的。技术方案作为旨在达成如上所述目的的一种实施方式,本发明提供一种肽,上述肽包含以下通式1的氨基酸序列。k-y-r1-r2-r3-r4-r5(通式1)上述通式1中,r1及r2分别为精氨酸(r)、赖氨酸(k)、谷氨酰胺(q)或天冬酰胺酸(n);r3、r4及r5分别为精氨酸(r)或赖氨酸(k)。根据一实施方式,上述肽包含序列号1至128中的任意一种氨基酸序列,或可由序列号1至128中的任意一种氨基酸序列构成。根据一实施方式,上述肽包含序列号1至序列号24中的任意一种氨基酸序列,或可由序列号1至24中的任意一种氨基酸序列构成。根据一实施方式,在上述通式1中,r1可以为谷氨酰胺(q),r2可以为精氨酸(r)。根据一实施方式,在上述通式1中,r1可以为精氨酸(r)或赖氨酸(k),r2可以为谷氨酰胺(q)。根据一实施方式,上述肽包含序列号25至48中的任意一种氨基酸序列,或可由序列号25至48中的任意一种氨基酸序列构成。根据一实施方式,在上述通式1中,r1及r2分别可以为谷氨酰胺(q)。根据一实施方式,在上述通式1中,r1可以为精氨酸(r)或赖氨酸(k),r2可以为精氨酸(r)。根据一实施方式,上述肽包含序列号49至128中的任意一种氨基酸序列,或可由序列号49至128中的任意一种氨基酸序列构成。根据一实施方式,在上述通式1中,r1可以为谷氨酰胺(q)、精氨酸(r)或赖氨酸(k),r2可以为赖氨酸(k)。根据一实施方式,在上述通式1中,r1可以为精氨酸(r)、赖氨酸(k)、谷氨酰胺(q)或天冬酰胺酸(n),r2可以为精氨酸(r)、赖氨酸(k)、谷氨酰胺(q)或天冬酰胺酸(n),r1及r2中的至少一种可以为天冬酰胺酸(n)。根据一实施方式,通过n-末端或c-末端的乙酰化、酰胺化或甲基化;d-氨基酸导入;如同ch2-nh、ch2-s、ch2-s=o或ch2-ch2的肽键修饰主链修饰或者侧链修饰来形成上述肽。根据一实施方式,上述肽可用于硬组织和/或牙髓组织的再生促进及牙本质-牙髓疾病和/或牙周疾病的治疗。根据一实施方式,上述硬组织可包含牙本质、骨及牙骨质。上述牙本质-牙髓疾病可包括牙本质过敏症、牙髓充血、牙髓炎、牙髓变性和/或牙髓的坏死或坏疽症等。上述牙周疾病可包括牙龈炎、牙周炎、牙周袋和/或牙周脓肿。作为另一实施方式,本发明提供对上述肽进行编码的多核苷酸。作为再一实施方式,本发明提供包含上述多核苷酸的表达载体。作为又一实施方式,本发明提供包含上述肽的组合物。在一实施方式中,上述组合物可以为牙本质-牙髓疾病的预防或治疗用药学组合物。在一实施方式中,上述组合物可以为牙周疾病的预防或治疗用药学组合物。作为另一实施方式,本发明提供包含上述肽的牙本质-牙髓疾病和/或牙周疾病的预防或改善用医药外品组合物。作为再一实施方式,本发明提供包含上述肽的牙本质-牙髓疾病和/或牙周疾病的预防或改善用保健功能性食品组合物。作为还一实施方式,本发明提供牙本质-牙髓疾病的预防或治疗方法,其包括将包含上述肽的组合物给予到具有牙本质-牙髓疾病的个体的步骤。作为又一实施方式,本发明提供牙周疾病的预防或治疗方法,其包括将包含上述肽的组合物给予到具有牙周疾病的个体的步骤。作为又一实施方式,本发明提供包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生促进方法,其包括将包含上述肽的组合物给予到个体的步骤。上述个体可以为人,或为除了人之外的个体。作为又一实施方式,本发明提供上述肽的牙本质-牙髓疾病的预防或治疗用途。作为又一实施方式,本发明提供上述肽的牙周疾病的预防或治疗用途。作为又一实施方式,本发明提供包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生促进用途。发明效果本发明的用于促进硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽,呈现出硬组织和/或牙髓组织的优秀的再生促进效果,因此可广泛地应用于多种用于预防或治疗牙本质-牙髓疾病的制剂的开发,或可广泛地应用于用于预防或治疗诱发骨和/或牙骨质的损伤的牙周疾病的制剂的开发。附图说明图1a为表示在用本发明的新型肽处理的人牙髓细胞(hdpcs)中,对作为成牙本质细胞分化标志基因的牙本质涎磷蛋白(dspp(dentinsialophosphoprotein))的表达水平进行比较的结果的图表。图1b为表示在用本发明的新型肽处理的人牙髓细胞中,对作为成牙本质细胞分化标志基因的dspp的表达水平进行比较的结果的另一图表。图1c为表示在用本发明的肽处理的人牙髓细胞中,对作为成牙本质细胞分化标志基因的巢蛋白(nestin)基因的表达水平进行比较的结果的图表。图2a为表示在用本发明的新型肽处理的人类来源的骨髓间充质干细胞(hbmscs)中,对作为骨及牙骨质的分化标志基因的骨涎蛋白(bsp)基因的表达水平进行比较的结果的图表。图2b为表示在用本发明的新型肽处理的人类来源的骨髓间充质干细胞中,对作为骨及牙骨质的分化标志基因的bsp基因的表达水平进行比较的结果的另一图表。图3为表示对于在体内使用人牙髓细胞6周从而新形成的硬组织的量进行测定的结果。图4作为表示对在体内使用人牙髓细胞6周从而形成的硬组织进行组织形态学分析的显微镜照片,分别地,a至d示出将把人牙髓细胞及100mg的羟基磷灰石/磷酸三钙(ha/tcp)混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠6周的结果、e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠6周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。图5作为表示在体内使用人牙髓细胞6周而形成的硬组织中所包含的胶原蛋白的形成水平的显微镜照片,分别地,a至d示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠6周的结果、e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠6周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。图6作为表示对在体内使用人牙髓细胞6周而形成的硬组织,利用免疫染色法来分析作为成牙本质细胞分化标志的dsp的表达水平的免疫染色照片,分别地,a示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠6周的结果、b示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠6周的结果。a及b利用抗-dsp抗体来对所形成的硬组织进行免疫染色。c为仅用二抗处理的免疫组织化学性分析的阴性对照组。a及b的箭头表示在新形成的钙化的组织中的dsp的表达。比例尺为50μm。图7为表示对于在体内使用人牙髓细胞12周而新形成的硬组织的量进行测定的结果。图8作为表示对在体内使用人牙髓细胞12周而形成的硬组织进行组织形态学分析的显微镜照片,分别地,a至d示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果、e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。图9作为表示在生物体内使用人牙髓细胞12周而形成的硬组织中所包含的胶原蛋白的形成水平的显微镜照片,分别地,a至d示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果、e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。图10作为表示对在生物体内使用人牙髓细胞12周而形成的硬组织,利用免疫染色法来分析作为成牙本质细胞分化标志的dsp的表达水平的免疫染色照片,分别地,a示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果、b示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果。a及b利用抗-dsp抗体来对所形成的硬组织进行免疫染色。c为仅用二抗处理的免疫组织化学性分析的阴性对照组。a及b的箭头表示在新形成的钙化的组织中的dsp的表达。比例尺为50μm。图11作为表示对在生物体内使用人牙髓细胞12周而形成的硬组织,利用扫描电子显微镜(scanningelectronmicroscope:sem)来进行分析的sem照片,分别地,a示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果、b和c示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果。比例尺为10μm。图12为将以生理性牙本质对受损的牙本质的牙本质小管进行再生并封闭,利用扫描电子显微镜进行观察的结果。具体而言,图12的b、c、d分别为对图12的a进行放大的图片。而且图12的f、g、h分别为对图12的e进行放大的图片。(比例尺:a:1mm、b:50μm、c:20μm、d:10μm、e:1mm、f:50μm、g:20μm、h:10μm)图13为将借助生理性再矿化对露出于受损的牙本质的表面的牙本质小管进行封闭,利用扫描电子显微镜进行观察的结果。具体而言,图13的b、c、d分别为对图13的a进行放大的图片。而且图13的f、g、h分别为对图13的e进行放大的图片。(比例尺:a:1mm、b:50μm、c:20μm、d:10μm、e:1mm、f:50μm、g:20μm、h:10μm)具体实施方式本发明人为了开发能够更有效地治疗牙本质-牙髓疾病和/或牙周疾病的制剂,进行多种研究,结果开发了包含7个氨基酸或由7个氨基酸构成的新型肽。开发的上述新型肽作为取代可呈现牙本质-牙髓疾病和/或牙周疾病治疗效果的肽的氨基酸序列的一部分而制备出的肽,示出如下效果,即可增加作为成牙本质细胞分化标志基因的牙本质涎磷蛋白(dspp(dentinsialophosphoprotein))基因及巢蛋白基因的表达水平,从而既呈现促进牙本质再生的效果,同时可增加作为成骨细胞及成牙骨质细胞的分化标志基因的骨涎蛋白(bsp(bonesialoprotein))基因的表达水平,从而呈现出可促进骨和牙骨质再生的效果。而且,制备与人牙髓细胞一并包含上述肽的移植物,并将上述制备的移植物移植于免疫系统受损的小鼠的皮下组织,经过6周或12周之后,对所移植的组织进行分析,结果确认到,形成了与生物体内的牙本质-牙髓组织最类似的形态的牙本质-牙髓类似组织,并形成了与生物体内的骨组织最类似的形态的骨类似组织,胶原蛋白的形成水平得到增加,作为成牙本质细胞特异分化标志基因的dsp的表达水平增加。并且,通过扫描电子显微镜对上述移植的组织的形状进行分析,其结果确认到,沿着形成的硬组织观察到成牙本质细胞-类似细胞,且成牙本质细胞突起也向所形成的硬组织方向延伸。而且确认到呈现在所形成的硬组织的表面附着有立方形细胞的典型的成骨细胞和/或成牙骨质细胞的特征。因此,可知本发明的肽呈现促进硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的效果。到目前为止尚无报告可呈现这种效果的本发明的肽,并且由本发明人最初开发。作为一实施方式,本发明提供包含以下通式1的氨基酸序列的用于促进硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽。k-y-r1-r2-r3-r4-r5(通式1)在上述通式1中,r1及r2分别为精氨酸(r)、赖氨酸(k)、谷氨酰胺(q)或天冬酰胺酸(n);r3、r4及r5分别为精氨酸(r)或赖氨酸(k)。而且,在上述通式1中,k意指赖氨酸,y意指酪氨酸。本发明的术语"硬组织(hardtissue)"意指,包含骨(骨架)、透明软骨(hyalinecartilage)、以及纤维软骨的,相对坚硬的骨架组织。在根据本发明的一实施方式中,上述硬组织可包括牙本质、骨及牙骨质。本发明的术语"牙本质(dentine)"还被称为齿质,是指形成牙齿的大部分的、具有略显黄色的白色坚硬组织。上述牙本质在齿冠部中由牙釉质覆盖,在齿根部中由牙骨质覆盖,因此不露出于牙齿表面,但是随着年龄增加,若牙釉质磨损,则牙本质将暴露在牙冠的前端或咬合面。虽然上述牙本质是一种骨-类似组织,但是形成牙本质的细胞的本体位于牙髓内,并且仅有其突起向牙本质内延伸,在上述方面上和通常的骨组织不同。本发明的术语"牙骨质(cementum)"是指,覆盖哺乳动物的牙齿根部(齿根)和其他一部分的骨略微变形的形态的薄薄的膜。上述牙骨质由50%的无机质及50%的水分-有机质构成,呈黄色,具有比牙本质或牙釉质低的硬度。上述牙骨质包含使牙齿固定于牙槽骨的牙周韧带纤维质,若牙龈感染细菌,将引起包围牙齿的牙骨质的变性,而连接牙齿和牙槽骨的牙周韧带纤维质由于无法紧贴于变性的牙骨质,从而使牙齿松动。为了治疗这种牙骨质的变性,使用着去除变性的牙骨质并促进新的牙骨质的形成的方法。本发明中提供的肽,可以增加作为成牙本质细胞分化标志基因的dspp及巢蛋白基因,和作为成骨细胞及成牙骨质细胞分化标志基因的bsp基因的表达水平,与人牙髓细胞一并移植于生物体内时,可呈现出上述人牙髓细胞形成牙本质/牙髓组织-类似组织及骨类似组织的特征。就本发明中提供的肽,只要能呈现出包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生促进及牙本质-牙髓疾病和/或牙周疾病的治疗效果,具有与构成上述肽的氨基酸序列一个以上不同氨基酸残基的序列的突变体肽也包含于在本发明中提供的肽的范畴。通常,在整体上不改变分子的活性的蛋白质及多肽中的氨基酸的交换在本发明所属
技术领域:
中是公知的。最普遍地发生的交换为氨基酸残基ala/ser、val/ile、asp/glu、thr/ser、ala/gly、ala/thr、ser/asn、ala/val、ser/gly、thy/phe、ala/pro、lys/arg、asp/asn、leu/ile、leu/val、ala/glu、asp/gly之间的交换。并且,通过氨基酸序列上的突变或修饰可包含如下的肽,即包含与肽的热、ph等有关的结构性稳定性增加或包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生促进能力增加的肽。氨基酸突变基于氨基酸侧链取代物的相对相似性,例如,疏水性、亲水性、电荷、尺寸等而实现。构成本发明的肽的7个氨基酸均属于亲水性氨基酸,因此氨基酸侧链取代物的相对相似性高。因此,构成序列号1的肽的氨基酸即使以具有亲水性质的各种氨基酸进行取代,因其结构上的相似性,也能够照样显示出在本发明中提供的肽的效果。例如,本发明中提供的位于序列号1的肽的第3位的酸性氨基酸谷氨酰胺即使被酸性氨基酸天冬酰胺酸取代,或者被碱性氨基酸精氨酸或赖氨酸取代,也可照样显示出在本发明中提供的肽的效果;位于序列号1的肽的第4位的碱性氨基酸精氨酸即使被碱性氨基酸赖氨酸取代,或者被酸性氨基酸谷氨酰胺或天冬酰胺酸取代,也可照样显示出在本发明中提供的肽的效果;位于序列号1的肽的第5位的碱性氨基酸精氨酸即使被碱性氨基酸赖氨酸取代,也可照样显示出在本发明中提供的肽的效果;位于序列号1的肽的第6位或第7位的碱性氨基酸赖氨酸即使被碱性氨基酸精氨酸取代,也可照样显示出在本发明中提供的肽的效果。如此地,构成本发明的肽的酸性氨基酸或碱性氨基酸即使分别被与其不同的其他酸性氨基酸或碱性氨基酸取代,也可照样显示出在本发明中提供的肽的效果,因此具有与构成本发明的肽的氨基酸序列一个以上不同氨基酸残基的序列的突变体肽也包含于在本发明中提供的肽的范畴,这是显而易见的。并且,本发明的肽即使具有在它的n-末端或c-末端附加有任意氨基酸的形式,也可照样显示出在本发明中提供的肽的效果,因此包含于在本发明中提供的肽的范畴。例如,可以是在上述肽的n-末端或c-末端附加有1至300个的氨基酸的形式,再如,可以是在上述肽的n-末端或c-末端附加有1至100个氨基酸的形式,又如,可以是在上述肽的n-末端或c-末端附加有1至24个氨基酸的形式。为了从生物体内的蛋白质切割酶保护本发明的肽并增加稳定性,本发明的肽可以为在其n-末端和/或c-末端等进行化学修饰或以有机基团进行保护、或者在肽末端等添加氨基酸而修饰的形式。尤其,在化学合成的肽的情况下,因n-及c-末端带有电荷,为了去除这样的电荷,可对n-末端进行乙酰化(acetylation)、对n-末端进行甲基化(metylation)和/或对c-末端进行酰胺化(amidation),或可包括d-氨基酸导入、ch2-nh、ch2-s、ch2s=o、ch2-ch2之类的肽键修饰、主链修饰、侧链修饰,但并不限定于此。制备肽类化合物的方法作为在本发明
技术领域:
中公知的方法,例如可参照quantitativedrugdesign,c.a.ramsdengd.,choplinpergamonpress(1992)中记载的内容。本发明的术语“主链修饰”是指,构成肽的氨基酸的主要部分的链状或环状的骨架被称为主链(主链:backbone),并且将构成上述肽主链的氨基酸直接修饰为氨基酸类似物,将此称为主链修饰。氨基酸类似物是指氨基酸主链的氮或α-碳中,通过取代作用使氢原子进行修饰的氨基酸。本发明的术语“侧链修饰”是指,从构成肽的氨基酸的主要部分的链状或环状骨架,如同树枝分出的原子团被称为氨基酸的侧链(侧链:side-chains),利用化学物质对这些侧链进行修饰,将此称为侧链修饰。肽侧链修饰的实例包含如下的氨基的修饰:如还原烷基化反应;基于亚氨酰乙酸甲酯的酰胺化;基于乙酸酐的烷基化;基于氰酸酯的氨基的氨甲酰化;基于2,4,6-三硝基苯磺酸(tnbs)的氨基酸的三硝基苄基化;基于琥珀酐的氨基的烷基化;或吡哆醛-5-磷酸处理后用nabh4还原的如吡哆醛化(pyridoxylation)等。并且,本发明的肽可单独使用,并且可以与批准作为药剂的载体(cattier)(如有机溶剂)混合使用,为了增大稳定性及功效还可包含碳水化合物,如葡萄糖、蔗糖或葡聚糖等;抗氧化剂(antioxidants),如抗坏血酸(ascorbicacid)或谷胱甘肽(glutathione)等;螯合剂(chelatingagents);低分子蛋白质或其他稳定剂(stabilizers)等使用。根据本发明的一个实施方式,合成相当于在本发明中提供的通式1的128种肽,并检验上述合成的肽对作为成牙本质细胞分化标志基因的dspp基因的表达水平产生的影响。其结果确认到,与在未用本发明的肽处理的人牙髓细胞(对照组)中测定的作为成牙本质细胞分化标志的dspp基因的mrna水平相比,处理上述128种肽的人牙髓细胞中,上述dspp基因的mrna水平均呈现8倍以上的值,或6倍以上的值,或3倍以上的值,或至少约1.5倍以上的值(图1a、图1b及表18至表33)。根据当前为止的报告,已知,若dspp的mrna的表达水平增加,则促进成牙本质细胞分化及牙本质再生,因此可知如下:呈现增加上述dspp基因的mrna水平的效果的上述128种肽呈现促进成牙本质细胞分化及牙本质再生的效果(tadurusreenathetal.,thejournalofbiologicalchemistry,vol.278,no.27,issueofjμly4,pp.24874-24880,2003;williamt.butleretal,connectivetissueresearch,44(suppl.1):171178,2003)。而且,检验上述合成肽对作为成骨细胞/成牙骨质细胞分化标志基因的bsp基因的表达水平产生的影响。其结果确认到,与在未用本发明的肽处理的人牙髓细胞(对照组)中测定的作为成骨细胞/成牙骨质细胞分化标志的bsp基因的mrna水平相比,处理上述128种肽的人牙髓细胞中,上述bsp基因的mrna水平呈现13倍以上的值,或12倍以上的值,或9倍以上的值,或至少约3倍以上的值(图2a及图2b)。据此,由于已知若bsp的mrna表达水平增加,则促进成骨细胞/成牙骨质细胞分化及骨和牙骨质的再生,因此呈现出增加上述bsp基因的mrna水平的效果的上述128种肽可呈现出促进成骨细胞/成牙骨质细胞分化及骨和牙骨质的再生的效果。作为另一实施方式,本发明提供对上述肽进行编码的多核苷酸。就上述多核苷酸而言,一个以上的碱基可通过取代,缺失,插入或它们的组合而进行突变。在化学合成核苷酸序列而进行制备的情况下,可使用在本发明所属领域中公知的合成法,例如在文献(engelsanduhlmann,angewchemintedengl.,37:73-127,1988)中记载的方法,并且可利用三酯、亚磷酸盐亚磷酰胺以及h-磷酸盐方法、聚合酶链式反应(pcr)及其他自动引物方法、固体支撑物上的寡核苷酸合成法来合成。例如,对本发明的肽进行编码的多核苷酸可包含序列号4的碱基序列。作为另一实施方式,本发明提供包含上述多核苷酸的表达载体、包含上述表达载体的转化体及利用上述转化体来制备上述肽的方法。本发明的术语“表达载体”是指作为在目的宿主细胞中可表达目的肽的重组载体,意指包含可操作地连接以表达基因插入物的必需调节元件的基因构建体。上述表达载体包含起始密码子、终止密码子、启动子、操纵基因等的表达调节元件,上述起始密码子及终止密码子通常被视为对多肽进行编码的核苷酸序列的一部分,并且当给予基因构建体时必须在个体呈现作用,并且需与编码序列位于框架中(inframe)。载体的启动子可以为组成型或诱导型启动子。本发明的术语“可操作地连接(operablylinked)”是指为了执行通常的功能使核酸表达调节序列和对目的蛋白质或rna进行编码的核酸序列功能性地相连接(functionallinkage)的状态。例如,将启动子和对蛋白质或核糖核酸进行编码的核酸序列可操作地连接可对编码序列的表达产生影响。与表达载体的可操作地连接可利用在本发明所属
技术领域:
中公知的基因重组技术来制备,而位点-特异性dna切割及连接可使用本发明所属
技术领域:
中通常公知的酶等。并且,为了促进从细胞培养液的肽的分离,上述表达载体可包含用于排出上述肽的信号序列。在进行所插入的核酸序列的有效的翻译时也会需要特异性起始信号。这些信号包含atg起始密码子及相邻的序列。在有些情况下,需要提供可包含atg起始密码子的外源翻译调节信号。这种外源翻译调节信号及起始密码子可以为多种天然及合成来源。可通过引入适当的转录或翻译增强子来增加表达效率。并且,为了容易地检出上述肽,上述表达载体还可包含可使用内肽酶任选地去除的蛋白质标签。本发明的术语“标签(tag)”是指呈现可进行定量的活性或特性的分子,可以为包括化学荧光物质(fluoracer)(如荧光素)和多肽荧光物质(如荧光蛋白质(gfp)或相关蛋白质)的荧光分子;还可以为myc标签、flag标签、组氨酸标签、亮氨酸标签、igg标签、链霉亲和素标签等的表位标签。尤其,在使用表位标签的情况下,优选地可使用由6个以上的氨基酸残基构成的肽标签,更优选地可使用由8个至50个氨基酸残基构成的肽标签。在本发明中,上述表达载体可包含对上述本发明的肽进行编码的核苷酸序列,该肽为用于促进包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的的肽,此时所使用的载体优选地可以为质粒dna、噬菌体dna等,更优选地可以为商业上开发的质粒(puc18、pbad、pidtsamrt-amp等)、大肠杆菌(e.coli)来源的质粒(pyg601br322、pbr325、puc118、puc119等)、枯草芽孢杆菌(bacillussubtilis)来源质粒(pub110、ptp5等)、酵母-来源质粒(yep13、yep24、ycp50等)、噬菌体dna(charon4a、charon21a、embl3、embl4、λgt10、λgt11、λzap等)、动物病毒载体(逆转录病毒(retrovirus)、腺病毒(adenovirus)、牛痘病毒(vacciniavirus)等)、昆虫病毒载体(杆状病毒(baculovirus)等),但只要能够生产上述肽,则可不特别限制于此。上述表达载体根据宿主细胞呈现不同的蛋白质的表达量和修饰等,因此优选地选择使用最适合于目的的宿主细胞。可向宿主导入在本发明中提供的上述表达载体来进行转化,从而可制备本发明中提供的转化体,通过使包含于上述表达载体的多核苷酸表达,来用于上述肽的生产。可通过多种方法进行上述转化,可使用cacl2沉淀法、在cacl2沉淀法中使用被称为二甲基亚砜(dmso(dimethylsulfoxide))的还原物质来提高效率的hanahan方法、电穿孔法(electroporation)、磷酸钙沉淀法、原生质体融合法、使用碳化硅纤维的搅拌方法、土壤杆菌(agrobacterium)介导的转化法、利用聚乙二醇(peg)的转化法、硫酸葡聚糖-、脂质体-及干燥/抑制-介导的转化方法等,但只要能够生产上述肽,就并不特别限定于此。并且,制备上述转化体中使用的宿主也是只要能够生产上述肽,就并不特别限定于此,但是可以为细菌细胞,如大肠杆菌、链霉菌(streptomyces)、鼠伤寒沙门氏菌(salmonellatyphimurium)等;酵母细胞,如酿酒酵母(saccharomycescerevisiae)、粟酒裂殖酵母(schizosaccharomycespombe)等;菌类细胞,如毕赤酵母(pichiapastoris)等;昆虫细胞,如果蝇(drosophila)、斜纹夜蛾(spodoptera)sf9细胞;动物细胞,如cho细胞、cos细胞、nso细胞、293细胞、人黑色素瘤(bowesmelanoma)细胞等;或植物细胞。上述转化体还可使用于生产如下本发明的肽的方法,其中上述肽为用于促进包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽。具体地,生产本发明的用于促进包含有牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽的方法可包括:步骤(a):通过培养上述转化体来获得培养物;以及步骤(b),从上述培养物回收本发明的肽。本发明的术语“培养”是指在适当地人工调节的环境条件下使微生物生长发育的方法。在本发明中,培养上述转化体的方法可利用在本发明所属
技术领域:
中公知的方法来进行。具体地,就上述培养而言,在分批工艺或分批补料或重复分批补料工艺(fedbatchorrepeatedfedbatchproess)中,可进行连续式培养,但只要能通过表达本发明的用于促进包含有牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽来进行生产,则并不特别限定于此。使用于培养的培养基需要在包含适当的碳源、氮源、氨基酸、维生素等的通常的培养基中,在好氧性条件下,调节温度、ph等并且以适当的方式满足特定菌株的条件。作为可使用的碳源,将葡萄糖及木糖的混合糖用作主碳源,除此之外,包含:糖和碳水化物,如蔗糖、乳糖、果糖、麦芽糖、淀粉、纤维素;以及油和脂肪,如大豆油、葵花籽油、蓖麻油、椰子油等;以及脂肪酸,如棕榈酸、硬脂酸、亚油酸;以及醇,如甘油、乙醇;以及有机酸,如醋酸。这些物质可个别使用或作为混合物使用。作为可使用的氮源,可使用无机氮源,如氨、硫酸铵、氯化铵、乙酸铵、磷酸铵、碳酸铵及硝酸铵;氨基酸,如谷氨酸、蛋氨酸、谷氨酰胺;以及有机氮源,如蛋白胨、nz-胺、肉类提取物、酵母提取物、麦芽提取物、玉米浆、酪蛋白水解物、鱼类或其分解产物、脱脂大豆饼或其分解产物等。这些氮源可单独或组合使用。在上述培养基中,作为磷源,可包含磷酸一钾、磷酸二钾及相应的含钠盐。作为可使用的磷源包含磷酸二氢钾或磷酸氢二钾或相应的含钠盐。并且作为无机化合物,可使用氯化钠、氯化钙、氯化铁、硫酸镁、硫酸铁、硫酸锰及碳酸钙等。最后,在上述物质上可添加生长必需物质,如氨基酸及维生素来进行使用。并且,在培养基中可使用适当的前体。上述的原料在培养过程中可通过适当的方式以分批式、流加式或连续式添加于培养物,但并不特别限定于此。可通过以适当的方式使用碱性化合物,如氢氧化钠、氢氧化钾、氨等;酸性化合物,如磷酸或硫酸等来调节培养物的ph。并且,可通过使用诸如脂肪酸聚乙二醇酯的消泡剂来抑制气泡生成。为了维持好氧环境,向培养物内注入氧或含氧气体(例如,空气)。通常培养物的温度为27℃至37℃,优选为30℃至35℃。持续培养直至获得最大生成量的上述肽。这种目的通常在10小时至100小时内实现。并且,从培养物回收上述肽的步骤可通过本发明所属
技术领域:
中公知的方法执行。具体地,上述回收方法只要可适用于所生产的上述肽的回收,就不受特别限制,优选地,可使用离心分离、过滤、提取、喷雾、干燥、蒸发、沉淀、结晶化、电泳、分级溶解(例如,硫酸铵沉淀)、色谱(例如离子交换、亲和性、疏水性和尺寸排阻)等方法。作为另一实施方式,本发明提供包含上述肽的牙本质-牙髓疾病的预防或治疗用药学组合物。如上所述,包含本发明的用于促进牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽,在与人牙髓细胞一同移植于生物体内时,可促进上述人牙髓细胞形成牙本质/牙髓组织-类似组织,因此,可用作用于治疗因牙髓组织损伤而发生的牙本质-牙髓疾病的药学组合物的有效成分。包含于上述药学组合物的肽能够以肽的单独形式使用,也能够以由上述肽重复2次以上而连接的多肽形式使用,还能够以在上述肽的n-末端或c-末端结合的呈现牙本质-牙髓疾病治疗效果的药物的复合体形式使用。本发明的术语"牙本质-牙髓疾病"是指因上述牙髓组织损伤,而使牙髓组织和与其相结合的牙本质损伤从而发病的疾病。在本发明中,上述牙本质-牙髓疾病,例如可以为牙本质过敏症、牙髓充血、牙髓炎、牙髓变性、牙髓的坏死及坏疽症等,但只要是基于本发明的肽呈现治疗效果,就不特别限定于此。作为另一实施方式,本发明提供包含上述肽的牙周疾病的预防或治疗用药学组合物。如上所述,本发明的用于促进包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽,在与人牙髓细胞一同移植于生物体内时,可促进上述人牙髓细胞形成骨类似组织,因此,可用作用于治疗诱发骨和/或牙骨质的损伤的牙周疾病的药学组合物的有效成分。包含于上述药学组合物的肽还能够以肽的单独形式使用,也能够以由上述肽重复2次以上而连接的多肽的形式使用,还能够以在上述肽的n-末端或c-末端结合的呈现牙周疾病治疗效果的药物的复合体形式使用。本发明的术语"牙周疾病(periodontaldisease)"也称为风齿,意指因牙龈(牙床)和牙齿之间的缝隙被细菌感染而使得牙周韧带和邻近组织损伤的疾病,根据病症程度分为牙龈炎和牙周炎。上述牙周疾病在发病时,随着炎症发展而使得更多组织受损,并形成牙周袋(periodontalpocket),而众所周知牙周炎越严重牙周袋的深度越深,而随着牙周袋变深,使牙周韧带发生炎症,最终会诱发骨质流失。在本发明中,上述牙周疾病例如可以为牙龈炎(gingivitis)、牙周炎(periodontitis)、牙周袋(periodontalpocket)或牙周脓肿(periodontalabscess)等,但只要是基于本发明的肽呈现治疗效果,就不特别限定于此。本发明的术语“预防”是指通过给予包含本发明的肽的用于预防或治疗牙本质-牙髓疾病的药学组合物,来抑制或延迟牙本质-牙髓疾病的发生的全部行为,或者意指通过给予包含本发明的肽的用于预防或治疗牙周疾病的药学组合物,来抑制或延迟牙周疾病的发生的全部行为。本发明的术语“治疗”是指将包含本发明的肽作为有效成分的药学组合物给予需要治疗牙本质-牙髓疾病的个体,来促进牙本质或牙髓组织的再生,从而进行牙髓疾病的治疗的全部行为,或者意指将包含本发明的肽作为有效成分的药学组合物给予需要治疗牙周疾病的个体,来促进骨和/或牙骨质的再生,从而进行牙周疾病的治疗的全部行为。本发明的药学组合物可制备成用于治疗牙本质-牙髓疾病和/或牙周疾病的药学组合物的形式,药学组合物除了上述肽外,还包含在药学组合物的制备中通常所使用的适当的载体(天然的或非天然的载体)、赋形剂或稀释剂。具体地,上述药学组合物可分别按通常的方法以灭菌注射液的形式配制使用,该灭菌注射液可给予到诱发牙本质-牙髓疾病和/或牙周疾病的部位。在本发明中,作为可包含于上述药学组合物的载体、赋形剂及稀释剂可例举乳糖、右旋糖、蔗糖、山梨醇、甘露醇、木糖醇、赤藓糖醇、麦芽糖醇、淀粉、阿拉伯橡胶、藻酸盐、明胶、磷酸钙、硅酸钙、纤维素、甲基纤维素、微晶纤维素、聚乙烯吡咯烷酮、水、羟基苯甲酸甲酯、羟基苯甲酸丙酯、滑石、硬脂酸镁、矿物油、胶原蛋白等。在制剂化的情况下,可使用通常使用的填充剂、增量剂、结合剂、润湿剂、崩解剂、表面活性剂等稀释剂或赋形剂来制备。尤其是,灭菌水溶液、非水性溶剂、悬浮剂、乳剂、冷冻干燥剂、栓剂、软膏剂(例如,牙髓衬底材料等)。作为非水性溶剂、悬浮剂可使用植物性油,如丙二醇(propyleneglycol)、聚乙二醇、橄榄油等;能够注射的酯,如油酸乙酯等。作为栓剂的基质可使用合成脂肪酸酯(witepsol)、聚乙二醇、吐温(tween)61、可可脂、月桂酸甘油酯脂肪甘油明胶等。包含于本发明的药学组合物的上述肽的含量,基于最终组合物总重量,可包含0.0001至50wt%,更优选地可包含0.01至20wt%,但并不特别局限于此。上述本发明的药学组合物能够以药剂学上有效的量给予,本发明的术语“药剂学上有效的量”是指以可适用于医学治疗或预防的合理的受益/风险比率,对于疾病的治疗或者预防充分的量,可根据包括疾病的严重程度、药物的活性、患者的年龄、体重、健康、性别、患者对药物的敏感度、所使用的本发明组合物的给药时间、给药途径及排出比率、疗程、与所使用的本发明的组合物配合或同时使用的药物的要素及其他在医药领域中公知的要素来确定有效用量水平。本发明的药学组合物可单独给予或可与公知的用于治疗牙本质-牙髓疾病和/或牙周疾病的药学组合物组合给予。最重要的是考虑全部上述要素,在无副作用的情况下以最少的量获得最大效果的量进行给药。本发明所属
技术领域:
的普通技术人员可考虑使用目的、疾病中毒程度患者的年龄、体重、性别、病史或作为有效成分使用的物质的种类等来确定本发明的药学组合物的给药量。例如,本发明的药学组合物可以每一名成人给予约0.1ng至约100mg/kg,优选地,给予1ng至约10mg/kg,,本发明的组合物的给药频率可以为1天给予一次或分剂量1天给予几次,但并不特别限定于此。上述给药量在任意方面都不限定本发明的范围。作为再一实施方式,本发明提供牙本质-牙髓疾病治疗方法,上述牙本质-牙髓疾病治疗方法包括以药剂学上有效的量,将上述药学组合物给予到患有牙本质-牙髓疾病的人或除了人以外的个体的步骤。作为又一实施方式,提供牙周疾病的治疗方法,上述牙周疾病的治疗方法包括以药剂学上有效的量,将上述药学组合物给予患有牙周疾病的人或除了人以外的个体的步骤。本发明的术语“个体”是指可无限制地包括,包括需要治疗牙本质-牙髓疾病和/或牙周疾病的人或除了人以外的小鼠、家畜等的哺乳动物。本发明的牙本质-牙髓疾病和/或牙周疾病治疗用药学组合物的给药途径只要是可达到目的组织,则可通过任意通常的途径来给药。本发明的药学组合物可根据目的通过口腔内给予或口腔内注射等的途径来给予,但不特别限定于此。作为另一实施方式,本发明提供包含上述肽的用于预防或改善牙本质-牙髓疾病的医药外品组合物,或者提供包含上述肽的用于预防或改善牙周疾病的医药外品组合物。本发明的术语“改善”是指至少减少与所治疗的状态相关的参数(例如,症状的程度)的全部行为。在本发明中,上述改善可作如下解释:将包含本发明的肽作为有效成分的药学组合物给予到需要治疗牙本质-牙髓疾病的个体,来促进牙本质或牙髓组织的再生,从而使牙本质-牙髓疾病的症状好转或得到有利改变的全部行为,或者将包含本发明的肽作为有效成分的药学组合物给予到需要治疗牙周疾病的个体,来促进骨和/或牙骨质的再生,从而使牙周疾病的症状好转或得到有利改变的全部行为。本发明的术语“医药外品”是指在以对人或动物的疾病进行诊断、治疗、改善、减轻、处置或预防的目的使用的物品中,与医药品相比作用轻微的物品,例如根据药事法,医药外品是指除了作为医药品的用途使用的物品以外的物品,包括用于治疗或预防人/动物的疾病的纤维/橡胶产品、对人体的作用轻微或不直接作用的物品(并非器具或机械)和与此类似的物品、用于防止传染病的杀菌/杀虫剂等。在本发明中,并不特别限定包含上述肽的医药外品组合物的种类或剂型例如,可以为口腔用消毒清洁剂、口腔清洁用品、牙膏、牙线、口腔用软膏剂等。作为另一实施方式,本发明提供包含上述肽的用于预防或改善牙本质-牙髓疾病和/或牙周疾病的保健功能性食品组合物。本发明的术语“食品”有肉类、香肠、面包、巧克力、糖果类、快餐类、饼干类、比萨、方便面、其他面类、口香糖类、包括冰淇淋类的奶制品、各种汤、饮料、茶、补液、酒精饮料、维生素复合剂、保健功能食品及保健食品等,包括常规意义上的所有食品。上述保健功能(性)食品(functionalfood)作为和特定保健用食品(foodforspecialhealthuse,foshu)相同的术语,是指使之除了供给营养之外,还可以有效地呈现生物体调节功能而加工的医学、医疗效果高的食品。其中,所谓“功能(性)”是指调节营养素(对人体的结构及功能)或在保健用途(如生理学作用等)中取得有用的效果。可通过本发明所属
技术领域:
中通常所使用的方法制备本发明的食品,进行上述制备时可添加通常所添加的原料及成分来制备。并且,作为上述食品的剂型而言,只要是认定为食品的剂型,就可无限制地进行制备。本发明的食品用组合物具有如下优点:能够制备成多种形式的剂型,与普通药品不同,可将食品作为原料,从而没有长期服用药品时可能发生的副作用等,并且便携性优秀,因此本发明的食品可作为用于增进牙本质-牙髓疾病和/或牙周疾病的预防或改善的效果的辅助剂来摄取。上述保健食品(healthfood)是指与普通食品相比,具有积极的维持健康或增进健康的效果的食品,保健辅助食品(healthsupplementfood)是指健康辅助目的的食品。根据情况,可混用保健功能食品、保健食品、保健辅助食品的术语。具体地,上述保健功能食品是指将本发明的肽添加于饮料,茶类,香辛料、口香糖类、饼干类等食品材料或作为利用胶囊化、粉末化、悬浮液等制备的食品,在摄取上述食品的情况下,在健康方面带来特定的效果,但是与普通药品不同,将食品作为原料,具有在长期服用药品时不会产生副作用的优点。本发明的食品组合物可日常摄取,因此可期望对于预防或改善牙本质-牙髓疾病和/或牙周疾病的良好效果,由此可非常有用地使用。上述食品组合物还可包含在生理学上可接受的载体,载体的种类并不受特别限制,只要是在本发明所属
技术领域:
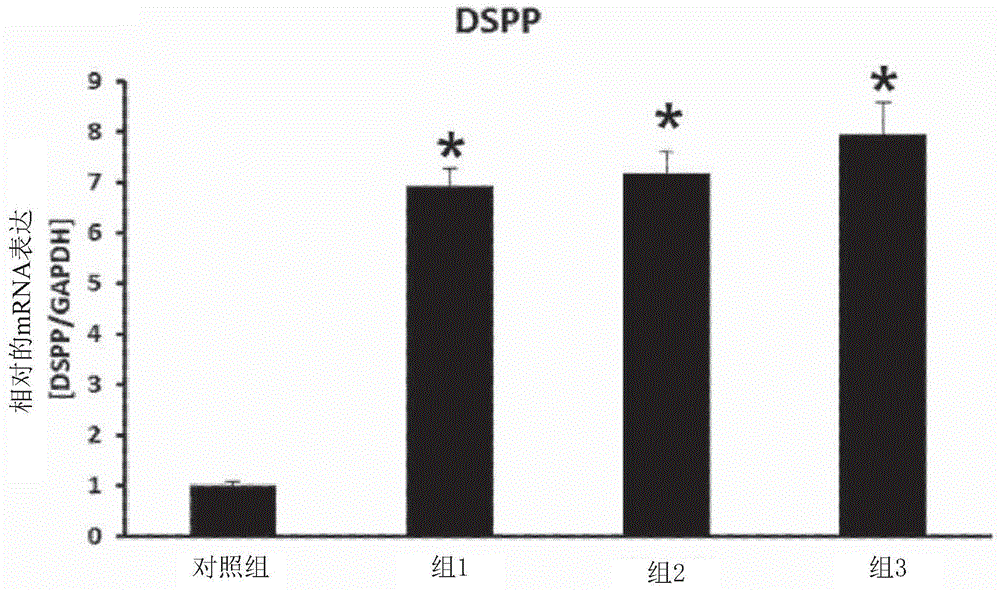
中通常所使用的载体,就都可任意使用。并且,上述食品组合物可包含可通常用于食品组合物以提高气味、味道、视觉等的添加成分。例如,可包含维生素a、c、d、e、b1、b2、b6、b12、烟酸(niacin)、生物素(biotin)、叶酸(folate)、泛酸(pantothenicacid)等。并且,可包含矿物质,如锌(zn)、铁(fe)、钙(ca)、铬(cr)、镁(mg)、锰(mn)、铜(cu)、铬(cr)等。并且,可包含氨基酸,如赖氨酸、色氨酸、半胱氨酸、缬氨酸等。并且,上述食品组合物可包含食品添加剂(foodadditives),如防腐剂(山梨酸钾、苯甲酸钠、水杨酸、脱氢醋酸钠等)、杀菌剂(漂白粉与高效漂白粉、次氯酸钠等)、抗氧化剂(丁基羟基苯甲醚(bha)、丁基羟基甲苯(bht)等)、着色剂(焦油色素等)、显色剂(亚硝酸钠、亚醋酸钠等)、漂白剂(亚硫酸钠)、调料(msg谷氨酸钠等)、甜味剂(甘素、环己胺磺酸盐、糖精、钠等)、香料(香草醛、内酯类等)、膨胀剂(明矾、d-酒石酸氢钾等)、强化剂、乳化剂、增稠剂(糊料)、被膜剂、胶基础剂、泡沫抑制剂、溶剂、改良剂等。可根据食品的种类筛选并使用适当的量的上述添加物。本发明的肽可直接添加或与其他食品或食品成分一同使用,并可按照通常方法适当地使用。可根据其使用目的(预防、健康或治疗性处理)适当地确定有效成分的混合量。通常,当制备食品或饮料时,相对于食品或饮料,本发明的食品组合物可添加50重量份以下,具体地,20重量份以下的量。但是,在以健康及卫生为目的长时间摄取的情况下,可包含上述范围以下的量,由于在安全性方面无任何问题,作为有效成分还可使用上述范围以上的量。作为本发明的食品组合物的一例,可用作保健饮料组合物使用,在上述情况下,可与一般的饮料相同,含有多种香味剂或天然碳水化物等作为添加成分。上述天然碳水化合物可以为单糖,如葡萄糖、果糖;二糖,如麦芽糖、蔗糖;多糖,如糊精、环糊精;糖醇,如木糖醇、山梨醇、赤藓糖醇等。甜味剂可使用天然甜味剂,如奇异果甜蛋白、甜叶菊提取物;合成甜味剂,如糖精、阿斯巴甜,等。上述天然碳水化合物的比率在每100ml的本发明的保健饮料组合物中通常可以为约0.01g至0.04g,具体地可以为约0.02g至0.03g。除了上述之外,保健饮料组合物可包含多种营养剂、维生素、电解质、风味剂、着色剂、果胶酸、果胶酸盐、褐藻酸、褐藻酸盐、有机酸、保护性胶体增稠剂、ph调节剂、稳定剂、防腐剂、甘油、乙醇或碳酸化剂等。除此之外,还可包含用于制备天然果汁、果汁饮料或蔬菜饮料的果肉。这种成分可独立使用或混合使用。虽然这种添加剂的比率并不特别重要,但是通常每100重量份的本发明的保健饮料组合物中,在0.01至0.1重量份的范围内进行选择。若本发明的食品组合物可呈现预防或改善牙本质-牙髓疾病和/或牙周疾病的效果,则可以多种重量百分比包含本发明的肽,具体地,基于食品组合物的总重量,可包含0.00001至100wt%或0.01至80wt%的本发明的肽,但是并不限定于此。作为本发明的另一实施方式,提供包括将包含上述肽的组合物给予到个体的步骤的牙本质-牙髓疾病的预防或治疗方法和/或牙周疾病的预防或治疗方法。作为再一实施方式,本发明提供包括将包含上述肽的组合物给予到个体的步骤的促进牙本质或牙髓组织再生的方法和/或促进骨或牙骨质再生的方法。作为本发明的又一实施方式,提供包括包含以下通式1的氨基酸序列的肽或上述肽的组合物在促进包括牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生中的用途,及预防或治疗牙本质-牙髓疾病或牙周疾病的用途。k-y-r1-r2-r3-r4-r5(通式1)在上述通式1中,r1及r2分别为精氨酸(r)、赖氨酸(k)、谷氨酰胺(q)或天冬酰胺酸(n);r3、r4及r5分别为精氨酸(r)或赖氨酸(k)。作为另一实施方式,本发明提供包括包含序列号1至128中的任意一种氨基酸序列的肽或上述肽的组合物促进包括牙本质、骨及牙骨质的硬组织和/或牙髓组织再生的用途,及预防或治疗牙本质-牙髓疾病和/或牙周疾病的用途。以下通过实施例对本发明进行更详细的说明。但是这些实施例只用于示例性地说明本发明,而不是以这些实施例限定本发明的范围。实施例1:实验方法及材料实施例1-1.用于促进包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生及治疗牙本质-牙髓疾病和/或牙周疾病的肽的合成本发明人通过9-芴甲氧羰基(9-fluorenylmethyloxycarbonyl,fmoc)方法合成呈现促进包含牙本质、骨及牙骨质的硬组织和/或牙髓组织的再生的效果的肽(序列号1),并且将合成的上述肽的氨基酸取代以合成了代表性组的肽(表1至表16)。n-kyqrrkk-c(序列号1)首先,组1的肽为序列号1的肽,或以赖氨酸或精氨酸取代上述序列号1的肽的第5至7位的氨基酸而合成的(表1)。【表1】组1的肽序列号氨基酸序列(n-c)1kyqrrkk2kyqrrkr3kyqrrrk4kyqrrrr5kyqrkkk6kyqrkrk7kyqrkkr8kyqrkrr然后,以精氨酸取代序列号1的肽的第3位的氨基酸,并以谷氨酰胺取代第4位的氨基酸,以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组2的肽(表2)。【表2】组2的肽序列号氨基酸序列(n-c)9kyrqrkk10kyrqrkr11kyrqrrk12kyrqrrr13kyrqkkk14kyrqkrk15kyrqkkr16kyrqkrr然后,以赖氨酸取代序列号1的肽的第3位的氨基酸,并以谷氨酰胺取代第4位的氨基酸,以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组3的肽(表3)。【表3】组3的肽序列号氨基酸序列(n-c)17kykqrkk18kykqrkr19kykqrrk20kykqrrr21kykqkkk22kykqkrk23kykqkkr24kykqkrr然后,以谷氨酰胺取代序列号1的肽的第4位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组4的肽(表4)。【表4】组4的肽序列号氨基酸序列(n-c)25kyqqrkk26kyqqrkr27kyqqrrk28kyqqrrr29kyqqkkk30kyqqkrk31kyqqkkr32kyqqkrr然后,以精氨酸取代序列号1的肽的第3位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组5的肽(表5)。【表5】组5的肽序列号氨基酸序列(n-c)33kyrrrkk34kyrrrkr35kyrrrrk36kyrrrrr37kyrrkkk38kyrrkrk39kyrrkkr40kyrrkrr然后,以赖氨酸取代序列号1的肽的第3位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组6的肽(表6)。【表6】组6的肽序列号氨基酸序列(n-c)41kykrrkk42kykrrkr43kykrrrk44kykrrrr45kykrkkk46kykrkrk47kykrkkr48kykrkrr然后,以赖氨酸取代序列号1的肽的第4位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组7的肽(表7)。【表7】组7的肽序列号氨基酸序列(n-c)49kyqkrkk50kyqkrkr51kyqkrrk52kyqkrrr53kyqkkkk54kyqkkrk55kyqkkkr56kyqkkrr然后,以天冬酰胺酸取代序列号1的肽的第3位的氨基酸,并以赖氨酸取代第4位的氨基酸,以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组8的肽(表8)。【表8】组8的肽序列号氨基酸序列(n-c)57kynkrkk58kynkrkr59kynkrrk60kynkrrr61kynkkkk62kynkkrk63kynkkkr64kynkkrr然后,以天冬酰胺酸取代序列号1的肽的第3位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组9的肽(表9)。【表9】组9的肽然后,以精氨酸取代序列号1的肽的第3位的氨基酸,并以天冬酰胺酸取代第4位的氨基酸,以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组10的肽(表10)。【表10】组10的肽序列号氨基酸序列(n-c)73kyrnrkk74kyrnrkr75kyrnrrk76kyrnrrr77kyrnkkk78kyrnkrk79kyrnkkr80kyrnkrr然后,以赖氨酸取代序列号1的肽的第3位的氨基酸,并以天冬酰胺酸取代第4位的氨基酸,以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组11的肽(表11)。【表11】组11的肽然后,以天冬酰胺酸取代序列号1的肽的第4位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组12的肽(表12)。【表12】组12的肽序列号氨基酸序列(n-c)89kyqnrkk90kyqnrkr91kyqnrrk92kyqnrrr93kyqnkkk94kyqnkrk95kyqnkkr96kyqnkrr然后,以天冬酰胺酸取代序列号1的肽的第3位的氨基酸,并以谷氨酰胺取代第4位的氨基酸,以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组13的肽(表13)。【表13】组13的肽然后,以天冬酰胺酸取代序列号1的肽的第3位的氨基酸和第4位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组14的肽(表14)。【表14】组14的肽序列号氨基酸序列(n-c)105kynnrkk106kynnrkr107kynnrrk108kynnrrr109kynnkkk110kynnkrk111kynnkkr112kynnkrr然后,以精氨酸取代序列号1的肽的第3位的氨基酸,并以赖氨酸取代第4位的氨基酸,以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组15的肽(表15)。【表15】组15的肽最后,以赖氨酸取代序列号1的肽的第3位的氨基酸和第4位的氨基酸,并以赖氨酸或精氨酸取代第5至7位的氨基酸,从而合成了组16的肽(表16)。【表16】组16的肽序列号氨基酸序列(n-c)121kykkrkk122kykkrkr123kykkrrk124kykkrrr125kykkkkk126kykkkrk127kykkkkr128kykkkrr实施例1-2.细胞培养在包含5%的co2的湿润的空气中,在37℃的条件下进行培养,并使用于实验。人骨髓间充质干细胞(humanbonemarrowmesenchymalstemcell;hbmscs)从龙沙(lonza,瑞士)购买并使用。在添加有10%热灭活的牛血清的α-最低必需培养基(α-mem,英杰公司(invitrogen))的培养液中培养了hbmscs。实施例1-3.人类来源的牙髓细胞分离及培养就人牙髓细胞(即,人类来源的牙髓细胞)而言,在首尔大学牙科医院,从10名成人(18-22岁)的智齿中分离了人牙髓细胞。具体地,全部实验在得到临床研究评审委员会(hospital’sinstitutionalreviewboard)的认可后,并在获得患者的同意的情况下进行了实验,根据junghs等人(jmolhistol.(2011))的方法切割智齿来使牙髓露出,并利用镊子分离了牙髓。利用剃须刀刀片细切分离的牙髓,并放入60mm平皿,利用盖玻片覆盖之后,在达尔伯克氏改良伊格尔氏培养基(dmem)中进行培养。而众所周知,人牙髓细胞在各种的条件下可分化为成牙本质细胞、成骨细胞、成牙骨质细胞及牙周韧带细胞(tissueengparta.2014apr;20(7-8):1342-51).实施例1-4.逆转录-聚合酶链式反应(rt-pcr)及实时pcr分析利用trizol试剂分离出人牙髓细胞与人骨髓间充质干细胞的总(total)rna。利用2μg的总rna和1μl的逆转录酶及0.5μg的寡核苷酸(oligo;dt)合成了cdna。将合成的cdna利用于实时聚合酶链式反应。利用sybrgreenpcrmastermix(takara,日本),在abiprism7500序列检测系统(sequencedetectionsystem,appliedbiosystems)中进行了实时聚合酶链式反应。以在94℃下,1分钟;在95℃下,15秒钟;在60℃下,34秒钟的方式重复40个循环(cycles)的条件下进行了实时聚合酶链式反应。作为结果分析,利用比较循环阈值(comparativecyclethreshold;ct)方法进行了评价,引物的碱基序列记载如下表17。【表17】<人实时pcr引物一览表(completelistsofhumanrealtimepcrprimers)>实施例1-5.生物体内移植及组织学分析分离人牙髓细胞(hdpcs)并将其使用于生物体内移植实验。将hdpcs(2x106细胞)单独与100mg的羟基磷灰石(hydroxyapatite)/磷酸三钙(tricalciumphosphate)(ha/tcp)陶瓷粉(美国捷迈公司(zimmer,usa)),或与本发明的肽(10μg)一并,分别与0.5%的纤维蛋白凝胶一起混合之后,移植于免疫系统受损的小鼠(nih-bg-nu-xid;harlanlaboratories,indianapolis,in)6周和12周。之后,收获样品并将其固定于4%的多聚甲醛,且在10%的乙二胺四乙酸(edta)(ph7.4)中进行脱钙,包埋(embedding)于石蜡,以苏木精-伊红(h-e)(vectorlabs)进行染色或进行免疫组织化学性分析。为了执行免疫组织化学性分析,用以1:150稀释的抗-dsp抗体作为一级抗原,并且与作为二级抗原的用生物素标记的山羊抗兔免疫球蛋白g(igg)(vectorlabs)一起,检测了蛋白质。胶原蛋白染色(masson'strichromestain)是利用polysciences公司的马松三色染色试剂盒(masson’strichromestainkit)(cat.25088-100)依照所提供的实验方法而实施的。新形成的硬组织的定量分析使用lsstarter程序(olympussoftimagingsolution,muster,德国)来进行分析。新形成的硬组织的比率按照在总面积中新形成的硬组织的面积的百分比来进行计算。实施例1-6.扫描电子显微镜分析(scanningelectronmicroscopeanalysis)将样品组织在2.5%的戊二醛(glutaraldehyde)/0.1m二甲胂酸缓冲液(cacodylatebuffer)中固定30分钟,并在0.1m二甲胂酸缓冲液中包含有1%的四氧化锇(osmiumtetroxide)的溶液中反应1小时。然后,利用乙醇对样品进行快速脱水及干燥之后,利用金来涂敷试料,并用扫描式电子显微镜(日本东京日立s-4700(s-4700,hitachi,tokyo,japan))进行观察。实施例1-7.统计分析使用studentt检验来执行统计分析。使用spss19.0版软件执行所有的统计分析。实施例2:实验结果实施例2-1.用于促进牙本质或牙髓组织的再生及治疗牙本质-牙髓疾病的肽对于作为成牙本质细胞分化标志基因的dspp基因的表达水平产生的影响众所周知,dspp基因被使用作为成牙本质细胞分化标志,对于牙本质的钙化而言是重要基因。因此,确认了本发明的肽是否具有使作为成牙本质细胞分化标志基因的dspp基因的表达增加,从而促进成牙本质细胞的分化和牙本质形成的效果。将上述实施例1-1中合成的各个组的肽以10/浓度处理通过执行上述实施例1-3的方法培养的人牙髓细胞,并培养48小时之后,测定在上述人牙髓细胞中表达的作为成牙本质细胞分化标志基因的dspp基因的mrna水平,并且将上述测定的各个dspp基因的mrna水平换算为对于对照组中测定的dspp基因的mrna水平的相对比率(表18至33)。而且,按各组,比较了根据上述表1至表3的各组的肽测定的dspp基因的mrna水平的平均值(图1a)。具体地,将氨基酸碱基序列的取代或部分序列缺失的本发明的新型肽分组如表1至表3,作为示出各组的新型肽在人牙髓细胞中对于作为成牙本质细胞分化标志基因的dspp的表达产生的影响的结果,在图1a中示出呈现出利用定量实时pcr来测定人牙髓细胞中dsppmrna的水平的各组的平均值的图表。此时,作为对照组使用了未用本发明的肽处理的人牙髓细胞。而且,按各组,比较了根据上述表4至表16的各组的肽测定的dspp基因的mrna水平的平均值(图1b)。具体地,将氨基酸碱基序列的取代或部分序列缺失的本发明的新型肽分组如表4至表16,作为示出各组的新型肽在人牙髓细胞中对于作为成牙本质细胞分化标志基因的dspp的表达产生的影响的结果,在图1b中示出呈现出利用定量实时pcr来测定人牙髓细胞中dsppmrna的水平的各组的平均值的图表。此时,作为对照组使用了未用本发明的肽处理的人牙髓细胞。上述dspp基因的表达水平通过在上述实施例1-4中说明的rt-pcr及实时pcr分析来测定。此时作为内部对照组,使用了gapdh基因,测定值则在执行3次重复实验之后,使用其平均值及标准偏差值。引物的碱基序列记载于上述表17。【表18】组1的肽对dspp基因的mrna水平产生的效果【表19】组2的肽对dspp基因的mrna水平产生的效果【表20】组3的肽对dspp基因的mrna水平产生的效果【表21】组4的肽对dspp基因的mrna水平产生的效果【表22】组5的肽对dspp基因的mrna水平产生的效果【表23】组6的肽对dspp基因的mrna水平产生的效果【表24】组7的肽对dspp基因的mrna水平产生的效果【表25】组8的肽对dspp基因的mrna水平产生的效果【表26】组9的肽对dspp基因的mrna水平产生的效果【表27】组10的肽对dspp基因的mrna水平产生的效果【表28】组11的肽对dspp基因的mrna水平产生的效果【表29】组12的肽对dspp基因的mrna水平产生的效果【表30】组13的肽对dspp基因的mrna水平产生的效果【表31】组14的肽对dspp基因的mrna水平产生的效果【表32】组15的肽对dspp基因的mrna水平产生的效果【表33】组16的肽对dspp基因的mrna水平产生的效果图1a为表示在用本发明的肽处理的人牙髓细胞中对作为成牙本质细胞分化标志的dspp基因的表达水平进行比较的结果的图表。参考图1a及表18至表20可以确认,与在未用本发明的肽处理的人牙髓细胞(对照组,control)中测定的作为成牙本质细胞分化标志的dspp基因的mrna水平相比,在用本发明的肽处理时,dspp基因的mrna水平均增加6倍至8倍以上。尤其以组3的肽进行处理时,表现出最高的dsppmrna表达值。图1b为表示在用本发明的肽处理的人牙髓细胞中,对作为成牙本质细胞分化标志的dspp基因的表达水平进行比较的结果。参考图1b及表21至表33可以确认,与在未用本发明的肽处理的人牙髓细胞(对照组,control)中测定的作为成牙本质细胞分化标志的dspp基因的mrna水平相比,在用本发明的肽处理时,dspp基因的mrna水平均增加了约1.5倍至3倍以上。实施例2-2.用于促进牙本质或牙髓组织的再生及治疗牙本质-牙髓疾病的肽对作为成牙本质细胞分化标志基因的巢蛋白基因的表达水平产生的影响从上述实施例2-1的结果可确认,本发明的肽可增加dspp基因的mrna水平,例如,所有组的肽可使dspp基因的mrna水平增加1.5倍以上,进而可增加至3倍以上,尤其组1至组3的肽可使dspp基因的mrna水平增加6倍以上。据此,确认了上述组1至3的肽是否也能增加其他作为成牙本质细胞分化标志基因的巢蛋白基因的mrna水平。大致上,除了使用不同引物之外,执行与上述实施例2-1相同、类似的方法,测定本发明的肽对巢蛋白基因的表达水平产生的效果,并比较了按各组算出的平均水平(图1c)。此时,作为对照组,使用了未用本发明的肽处理的人牙髓细胞。图1c为表示在用本发明的肽处理的人牙髓细胞中,对作为成牙本质细胞分化标志基因的巢蛋白基因的表达水平进行比较的结果的图表。如图1c中所示,可确认,与对照组(control)相比,用本发明的肽处理的组(组1、2、3)中,作为成牙本质细胞分化标志基因的巢蛋白基因的表达水平均增加5倍以上。众所周知,上述dspp及巢蛋白基因被使用作为成牙本质细胞分化标志,并且是参与牙本质的钙化过程的基因,因此分析出在本发明中提供的肽呈现出促进牙本质再生的效果。实施例2-3.用于促进骨和/或牙骨质的再生及治疗牙周疾病的肽对作为成骨细胞及成牙骨质细胞分化标志基因的bsp基因的表达水平产生的影响众所周知,bsp基因被使用作为成骨细胞及成牙骨质细胞分化标志,对于骨和牙骨质的钙化而言,是重要的基因。因此,为了确认本发明的新型肽对作为成骨细胞和成牙骨质细胞分化标志基因的bsp基因的表达产生的效果,用各个组的肽处理了执行上述实施例1-2的方法来培养的人类来源的间充质干细胞(即,人骨髓间充质干细胞,hbmscs)之后,利用实时pcr确认bsp基因的表达。大致上,除了使用不同引物之外,执行与上述实施例2-1相同、类似的方法,测定本发明的肽对bsp基因的表达水平产生的效果,并比较了按组算出的平均水平(图2a、图2b)。具体地,在如表1至表3分组的本发明的新型肽中,作为显示出在各组的新型肽在人类来源的骨髓间充质干细胞(hbmscs)中,对作为骨和牙骨质分化标志基因的骨涎蛋白(bsp(bonesialoprotein))的表达产生的影响的结果,将利用定量实时pcr测定人类来源的骨髓间充质干细胞中的bspmrna的水平的结果的图表示出于图2a。而且,如表4至表16分组的本发明的新型肽中,作为示出各个组的新型肽在人类来源的骨髓间充质干细胞中,对于作为骨和牙骨质分化标志基因的bsp的表达产生的影响的结果,将利用定量实时pcr测定人类来源的骨髓间充质干细胞中的bspmrna的水平的结果的图表示出于图2b。此时,以10μg/ml的浓度的肽进行了处理。而且作为对照组,使用了未用本发明的肽处理的人骨髓间充质干细胞。图2a为表示在用本发明的肽处理的人类来源的骨髓间充质干细胞中,对作为骨及牙骨质的分化标志基因的bsp基因的表达水平进行比较的结果的图表。如图2a所示,可确认,在用本发明的肽处理的组(组1、2、3)中,与对照组(control)相比,bsp基因表达增加约9倍至13倍以上。尤其以组3的肽处理时,示出了最高的bspmrna表达值。图2b为表示在用本发明的肽处理的人类来源的骨髓间充质干细胞中,对于作为骨及牙骨质的分化标志基因的bsp基因的表达水平进行比较的结果的图表。如图2b所示,可确认,在用本发明的肽处理的组(组4至组16)中,与对照组(control)相比,bsp基因表达增加约3倍至9倍以上,进而增加12倍以上。尤其以组11的肽进行处理时,表现出最高的bspmrna表达值。众所周知,上述bsp基因被使用作为成骨细胞和成牙骨质细胞分化标志,并且是参与骨和牙骨质的钙化过程的基因,因此分析出在本发明中提供的肽会示出促进骨和牙骨质的再生的效果。实施例2-4.6周间在生物体内借助于新型肽的人牙髓细胞(hdpcs)的硬组织的形成(1)组织形态学分析为了根据显示于图1a、图1b、图1c、图2a及图2b中的体外实验结果,测定本发明的肽对于体内硬组织形成的效果,如在上述实施例1-5中进行的说明,将人牙髓细胞及100mg的羟基磷灰石/磷酸三钙(ha/tcp)与10μg的组3的肽(例如,序列号24)一并,分别与0.5%的纤维蛋白凝胶进行混合而制备移植物。将上述移植物移植于免疫系统受损的小鼠的皮下组织。此时,作为对照组,使用了不包含本发明的肽的移植物进行移植。在进行移植6周后,如在上述实施例1-5中进行的说明,在提取样品之后,利用lsstarter程序定量分析新形成的硬组织,并将其结果示出于图3。图3表示对在体内使用人牙髓细胞6周而新形成的硬组织量进行测定的结果。如图3所示,作为进行移植6周后的硬组织形成比率,相比于对照组(control,13.5%),用新型肽处理的组(组3,29.6%)增加约2倍以上。图4作为表示对在体内使用人牙髓细胞6周而形成的硬组织,以组织形态学进行分析的显微镜照片,分别地,a至d示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠6周的结果,e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠6周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。所形成的硬组织利用苏木精-伊红(h-e)进行染色。如图4所示,通过苏木精-伊红染色的组织形态学分析结果,在不包含本发明的肽的对照组(图4的a-d)及包含本发明的肽的组(图4的e-h)中均观察到,在ha/tcp粒子的周围的钙化的组织的基质中形成了陷入有细胞的骨类似组织和牙本质-牙髓类似组织。(2)胶原蛋白染色分析胶原蛋白为在牙本质、骨及牙骨质中最为丰富地存在的有机基质(organicmatrix),执行收容沉着的无机质的作用。因此,为了确认在上述组织形态学分析的各实验组中形成的钙化的组织中的胶原蛋白的蛋白质积累,实施了胶原蛋白染色。图5作为表示在体内使用人牙髓细胞6周而形成的硬组织中所包含的胶原蛋白的形成水平的显微镜照片,分别地,a至d示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠6周的结果,e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠6周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。所形成的硬组织利用胶原蛋白染色(masson'strichromestain)方法进行染色。如图5所示,确认了相比于对照组(图5的a-d),在包含本发明的肽的组(图5的e-h)中,胶原蛋白的形成水平增加。(3)免疫组织化学性分析通过免疫组织化学性分析确认了作为成牙本质细胞特异性分化标志基因的dsp的表达。图6作为表示对在体内使用人牙髓细胞6周而形成的硬组织,利用免疫染色法分析作为成牙本质细胞分化标志的dsp的表达水平的免疫染色照片,分别地,a示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠6周的结果,b示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠6周的结果。a及b利用抗-dsp抗体对所形成的硬组织进行免疫染色。c为仅用二抗处理的免疫组织化学性分析的阴性对照组。a及b的箭头表示在新形成的钙化的组织中dsp的表达。比例尺为50μm。如图6所示,在对照组(图6的a)中,在新形成的牙本质-牙髓类似组织中dsp表达弱,但在包含本发明的肽的组(图6的b)中,在新形成的钙化的组织中dsp表达是强的。图6的c示出在免疫组织化学性分析中,以仅用二抗处理的阴性对照组是无法实现dsp染色的。实施例2-5.12周间在生物体内借助于新型肽的人牙髓细胞的硬组织的形成(1)组织形态学分析除了饲育12周移植有移植物的小鼠之外,执行上述实施例2-4的方法,对人牙髓细胞的硬组织形成进行了分析。图7表示对于在体内使用人牙髓细胞12周而新形成的硬组织的量进行测定的结果。如图7所示,作为进行移植12周后的硬组织形成比率,相比于对照组(control,23.7%),用新型肽处理的组(组3,39.5%)增加约1.6倍以上。图8作为表示对在体内使用人牙髓细胞12周而形成的硬组织,以组织形态学进行分析的显微镜照片,分别地,a至d示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果,e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。所形成的硬组织利用苏木精-伊红(h-e)进行染色。如图8所示,通过苏木精-伊红染色的组织形态学分析结果,在不包含本发明的肽的对照组(图8的a-d)及包含本发明的肽的组(图8的e-h)中均观察到,与图4的情况(移植6周)类似地,在ha/tcp粒子的周围的钙化的组织的基质中形成了陷入有细胞的骨类似组织和牙本质-牙髓类似组织。(2)胶原蛋白染色分析为了确认在上述实施例2-5的组织形态学分析的各实验组中形成的钙化的组织中的胶原蛋白的蛋白质积累,实施了胶原蛋白染色。图9作为表示在体内使用人牙髓细胞12周而形成的硬组织中所包含的胶原蛋白的形成水平的显微镜照片,分别地,a至d示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果,e至h示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果(比例尺:a、e为500μm,b、f为200μm,c、g为100μm,d、h为50μm)。所形成的硬组织利用胶原蛋白染色(masson'strichromestain)方法进行染色。如图9所示,确认了相比于对照组(图9的a-d),在包含本发明的肽的组(图9的e-h)中,胶原蛋白的形成水平增加。(3)免疫组织化学性分析通过免疫组织化学性分析确认了作为成牙本质细胞特异性分化标志基因的dsp的表达。图10作为表示对在体内使用人牙髓细胞12周而形成的硬组织,利用免疫染色法分析作为成牙本质细胞分化标志的dsp的表达水平的免疫染色照片,分别地,a示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果,b示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果。a及b利用抗-dsp抗体对所形成的硬组织进行免疫染色。c为仅用二抗处理的免疫组织化学性分析的阴性对照组。a及b的箭头表示在新形成的钙化的组织中的dsp的表达。比例尺为50μm。如图10所示,在对照组(图6的a)中,在新形成的牙本质-牙髓类似组织中dsp表达弱,但在包含本发明的肽的组(图6的b)中,在新形成的钙化的组织中dsp表达是强的。图10的c示出在免疫组织化学性分析中,以仅用二抗处理的阴性对照组是无法实现dsp染色的。综合上述实施例2-4及2-5的结果可知,本发明的新型肽呈现出能够促进牙本质/牙髓组织复合物及骨/牙骨质类似组织的再生的效果。实施例2-6.移植组织的利用扫描电子显微镜的细胞分析为了在移植12周后的对照组和处理新型肽的实验组中,确认人牙髓细胞向成牙本质细胞或成骨细胞/成牙骨质细胞的分化,以上述实施例1-6的方法执行扫描电子显微镜分析。图11作为表示对在体内使用人牙髓细胞12周而形成的硬组织,利用扫描电子显微镜(scanningelectronmicroscope:sem)来进行分析的sem照片,分别地,a示出将把hdpcs及100mg的ha/tcp混合于0.5%的纤维蛋白凝胶而制备的对照组的移植物,移植于免疫系统弱化的小鼠12周的结果,b和c示出将把hdpcs及100mg的ha/tcp与10μg的组3的肽一并混合于0.5%的纤维蛋白凝胶而制备的移植物,移植于免疫系统弱化的小鼠12周的结果。比例尺为10μm。所形成的硬组织利用扫描电子显微镜来对细胞进行观察。如图11所示,在hdpcs-单独处理的对照组中所形成的硬组织周围,观察到不完全地形成的成牙本质细胞突起的部分成牙本质细胞-类似细胞(图11的a)。在用本发明的肽处理(例如,组3的肽)的组中,沿着所形成的硬组织观察到成牙本质细胞-类似细胞,成牙本质细胞突起也向所形成的硬组织方向扩大(图11的b)。而且,确认了在用本发明的肽处理的组中,呈现出所形成的硬组织的表面附着有立方形细胞的典型的成骨细胞/成牙骨质细胞特征(图11的c)。因此,可知本发明的肽可更有效地形成成牙本质细胞及成骨细胞/成牙骨质细胞。实施例2-7.在体内牙本质小管的封闭能力实验利用牙科用牙钻(bur)在出生12个月的成犬的小臼齿中去除牙颈部的牙釉质,从而使牙本质露出。对于露出牙本质的成犬的小臼齿,为了完全去除在涡动形成时产生的牙釉质-牙本质碎片而充分清洗,然后去除了水分。在露出的牙本质部位的牙本质小管入口涂敷1.5μg的根据本发明的肽(序列号24)(组3),在3周之后对成犬进行安乐死,并拔出牙齿。然后利用钻石锯(diamondsaw)制作出所拔出的牙齿的样品而且为了确认根据本发明的新型肽对于受损的牙本质的露出的牙本质小管封闭产生的影响,通过扫描电子显微镜对牙本质小管封闭能力进行评价,并将其结果表示于图12。具体地,如图12a及图12e,在切割牙本质损伤部位的下面部分之后,观察切割面下面(框部分)。根据扫描电子显微镜的观察结果,确认了在未做任何处理的对照组中,受损的牙本质的下面部分露出有牙本质小管(图12a至图12d)。相反地,在用肽处理的实验组中可确认露出的牙本质小管借助于生理性再矿化而实现封闭(图12e至图12h)。实施例2-8.体内的牙本质损伤部位表面的观察利用如实施例2-7的方法制备拔出的成犬牙齿的样品。而且为了确认在受损的牙本质的表面,根据本发明的新型肽对于牙本质小管封闭产生的影响,通过扫描电子显微镜评价表面部位的牙本质小管封闭能力,并将其结果示出于图13。根据扫描电子显微镜观察结果,可确认在未做任何处理的对照组的受损的牙本质表面,露出有牙本质小管(图13a至图13d)。相反地,在用肽处理的实验组中露出的牙本质小管大部分被封闭(图13e至图13h)。此研究为基于2017年度韩国产业通商资源部及产业技术评价管理院(keit)研究费支援的研究(10078369,"利用诱导牙齿牙本质的再生的功能性肽治疗敏感性牙齿的原创技术开发")。以上,参考所附附图对本发明的实施例进行了说明,但本发明所属
技术领域:
的普通技术人员将理解,本发明在不变更其技术思想或必要特征的情况下,可以以其他具体形式进行实施。因此应理解在上面中记述的实施例在所有方面是示例性的而非限定性的。<110>海森斯柏奥公司<120>新型肽<130>lp171007krpri<160>128<170>kopatentin3.0<210>1<211>7<212>prt<213>人工序列<220><223>新型肽<400>1lystyrglnargarglyslys15<210>2<211>7<212>prt<213>人工序列<220><223>新型肽<400>2lystyrglnargarglysarg15<210>3<211>7<212>prt<213>人工序列<220><223>新型肽<400>3lystyrglnargargarglys15<210>4<211>7<212>prt<213>人工序列<220><223>新型肽<400>4lystyrglnargargargarg15<210>5<211>7<212>prt<213>人工序列<220><223>新型肽<400>5lystyrglnarglyslyslys15<210>6<211>7<212>prt<213>人工序列<220><223>新型肽<400>6lystyrglnarglysarglys15<210>7<211>7<212>prt<213>人工序列<220><223>新型肽<400>7lystyrglnarglyslysarg15<210>8<211>7<212>prt<213>人工序列<220><223>新型肽<400>8lystyrglnarglysargarg15<210>9<211>7<212>prt<213>人工序列<220><223>新型肽<400>9lystyrargglnarglyslys15<210>10<211>7<212>prt<213>人工序列<220><223>新型肽<400>10lystyrargglnarglysarg15<210>11<211>7<212>prt<213>人工序列<220><223>新型肽<400>11lystyrargglnargarglys15<210>12<211>7<212>prt<213>人工序列<220><223>新型肽<400>12lystyrargglnargargarg15<210>13<211>7<212>prt<213>人工序列<220><223>新型肽<400>13lystyrargglnlyslyslys15<210>14<211>7<212>prt<213>人工序列<220><223>新型肽<400>14lystyrargglnlysarglys15<210>15<211>7<212>prt<213>人工序列<220><223>新型肽<400>15lystyrargglnlyslysarg15<210>16<211>7<212>prt<213>人工序列<220><223>新型肽<400>16lystyrargglnlysargarg15<210>17<211>7<212>prt<213>人工序列<220><223>新型肽<400>17lystyrlysglnarglyslys15<210>18<211>7<212>prt<213>人工序列<220><223>新型肽<400>18lystyrlysglnarglysarg15<210>19<211>7<212>prt<213>人工序列<220><223>新型肽<400>19lystyrlysglnargarglys15<210>20<211>7<212>prt<213>人工序列<220><223>新型肽<400>20lystyrlysglnargargarg15<210>21<211>7<212>prt<213>人工序列<220><223>新型肽<400>21lystyrlysglnlyslyslys15<210>22<211>7<212>prt<213>人工序列<220><223>新型肽<400>22lystyrlysglnlysarglys15<210>23<211>7<212>prt<213>人工序列<220><223>新型肽<400>23lystyrlysglnlyslysarg15<210>24<211>7<212>prt<213>人工序列<220><223>新型肽<400>24lystyrlysglnlysargarg15<210>25<211>7<212>prt<213>人工序列<220><223>新型肽<400>25lystyrglnglnarglyslys15<210>26<211>7<212>prt<213>人工序列<220><223>新型肽<400>26lystyrglnglnarglysarg15<210>27<211>7<212>prt<213>人工序列<220><223>新型肽<400>27lystyrglnglnargarglys15<210>28<211>7<212>prt<213>人工序列<220><223>新型肽<400>28lystyrglnglnargargarg15<210>29<211>7<212>prt<213>人工序列<220><223>新型肽<400>29lystyrglnglnlyslyslys15<210>30<211>7<212>prt<213>人工序列<220><223>新型肽<400>30lystyrglnglnlysarglys15<210>31<211>7<212>prt<213>人工序列<220><223>新型肽<400>31lystyrglnglnlyslysarg15<210>32<211>7<212>prt<213>人工序列<220><223>新型肽<400>32lystyrglnglnlysargarg15<210>33<211>7<212>prt<213>人工序列<220><223>新型肽<400>33lystyrargargarglyslys15<210>34<211>7<212>prt<213>人工序列<220><223>新型肽<400>34lystyrargargarglysarg15<210>35<211>7<212>prt<213>人工序列<220><223>新型肽<400>35lystyrargargargarglys15<210>36<211>7<212>prt<213>人工序列<220><223>新型肽<400>36lystyrargargargargarg15<210>37<211>7<212>prt<213>人工序列<220><223>新型肽<400>37lystyrargarglyslyslys15<210>38<211>7<212>prt<213>人工序列<220><223>新型肽<400>38lystyrargarglysarglys15<210>39<211>7<212>prt<213>人工序列<220><223>新型肽<400>39lystyrargarglyslysarg15<210>40<211>7<212>prt<213>人工序列<220><223>新型肽<400>40lystyrargarglysargarg15<210>41<211>7<212>prt<213>人工序列<220><223>新型肽<400>41lystyrlysargarglyslys15<210>42<211>7<212>prt<213>人工序列<220><223>新型肽<400>42lystyrlysargarglysarg15<210>43<211>7<212>prt<213>人工序列<220><223>新型肽<400>43lystyrlysargargarglys15<210>44<211>7<212>prt<213>人工序列<220><223>新型肽<400>44lystyrlysargargargarg15<210>45<211>7<212>prt<213>人工序列<220><223>新型肽<400>45lystyrlysarglyslyslys15<210>46<211>7<212>prt<213>人工序列<220><223>新型肽<400>46lystyrlysarglysarglys15<210>47<211>7<212>prt<213>人工序列<220><223>新型肽<400>47lystyrlysarglyslysarg15<210>48<211>7<212>prt<213>人工序列<220><223>新型肽<400>48lystyrlysarglysargarg15<210>49<211>7<212>prt<213>人工序列<220><223>新型肽<400>49lystyrglnlysarglyslys15<210>50<211>7<212>prt<213>人工序列<220><223>新型肽<400>50lystyrglnlysarglysarg15<210>51<211>7<212>prt<213>人工序列<220><223>新型肽<400>51lystyrglnlysargarglys15<210>52<211>7<212>prt<213>人工序列<220><223>新型肽<400>52lystyrglnlysargargarg15<210>53<211>7<212>prt<213>人工序列<220><223>新型肽<400>53lystyrglnlyslyslyslys15<210>54<211>7<212>prt<213>人工序列<220><223>新型肽<400>54lystyrglnlyslysarglys15<210>55<211>7<212>prt<213>人工序列<220><223>新型肽<400>55lystyrglnlyslyslysarg15<210>56<211>7<212>prt<213>人工序列<220><223>新型肽<400>56lystyrglnlyslysargarg15<210>57<211>7<212>prt<213>人工序列<220><223>新型肽<400>57lystyrasnlysarglyslys15<210>58<211>7<212>prt<213>人工序列<220><223>新型肽<400>58lystyrasnlysarglysarg15<210>59<211>7<212>prt<213>人工序列<220><223>新型肽<400>59lystyrasnlysargarglys15<210>60<211>7<212>prt<213>人工序列<220><223>新型肽<400>60lystyrasnlysargargarg15<210>61<211>7<212>prt<213>人工序列<220><223>新型肽<400>61lystyrasnlyslyslyslys15<210>62<211>7<212>prt<213>人工序列<220><223>新型肽<400>62lystyrasnlyslysarglys15<210>63<211>7<212>prt<213>人工序列<220><223>新型肽<400>63lystyrasnlyslyslysarg15<210>64<211>7<212>prt<213>人工序列<220><223>新型肽<400>64lystyrasnlyslysargarg15<210>65<211>7<212>prt<213>人工序列<220><223>新型肽<400>65lystyrasnargarglyslys15<210>66<211>7<212>prt<213>人工序列<220><223>新型肽<400>66lystyrasnargarglysarg15<210>67<211>7<212>prt<213>人工序列<220><223>新型肽<400>67lystyrasnargargarglys15<210>68<211>7<212>prt<213>人工序列<220><223>新型肽<400>68lystyrasnargargargarg15<210>69<211>7<212>prt<213>人工序列<220><223>新型肽<400>69lystyrasnarglyslyslys15<210>70<211>7<212>prt<213>人工序列<220><223>新型肽<400>70lystyrasnarglysarglys15<210>71<211>7<212>prt<213>人工序列<220><223>新型肽<400>71lystyrasnarglyslysarg15<210>72<211>7<212>prt<213>人工序列<220><223>新型肽<400>72lystyrasnarglysargarg15<210>73<211>7<212>prt<213>人工序列<220><223>新型肽<400>73lystyrargasnarglyslys15<210>74<211>7<212>prt<213>人工序列<220><223>新型肽<400>74lystyrargasnarglysarg15<210>75<211>7<212>prt<213>人工序列<220><223>新型肽<400>75lystyrargasnargarglys15<210>76<211>7<212>prt<213>人工序列<220><223>新型肽<400>76lystyrargasnargargarg15<210>77<211>7<212>prt<213>人工序列<220><223>新型肽<400>77lystyrargasnlyslyslys15<210>78<211>7<212>prt<213>人工序列<220><223>新型肽<400>78lystyrargasnlysarglys15<210>79<211>7<212>prt<213>人工序列<220><223>新型肽<400>79lystyrargasnlyslysarg15<210>80<211>7<212>prt<213>人工序列<220><223>新型肽<400>80lystyrargasnlysargarg15<210>81<211>7<212>prt<213>人工序列<220><223>新型肽<400>81lystyrlysasnarglyslys15<210>82<211>7<212>prt<213>人工序列<220><223>新型肽<400>82lystyrlysasnarglysarg15<210>83<211>7<212>prt<213>人工序列<220><223>新型肽<400>83lystyrlysasnargarglys15<210>84<211>7<212>prt<213>人工序列<220><223>新型肽<400>84lystyrlysasnargargarg15<210>85<211>7<212>prt<213>人工序列<220><223>新型肽<400>85lystyrlysasnlyslyslys15<210>86<211>7<212>prt<213>人工序列<220><223>新型肽<400>86lystyrlysasnlysarglys15<210>87<211>7<212>prt<213>人工序列<220><223>新型肽<400>87lystyrlysasnlyslysarg15<210>88<211>7<212>prt<213>人工序列<220><223>新型肽<400>88lystyrlysasnlysargarg15<210>89<211>7<212>prt<213>人工序列<220><223>新型肽<400>89lystyrglnasnarglyslys15<210>90<211>7<212>prt<213>人工序列<220><223>新型肽<400>90lystyrglnasnarglysarg15<210>91<211>7<212>prt<213>人工序列<220><223>新型肽<400>91lystyrglnasnargarglys15<210>92<211>7<212>prt<213>人工序列<220><223>新型肽<400>92lystyrglnasnargargarg15<210>93<211>7<212>prt<213>人工序列<220><223>新型肽<400>93lystyrglnasnlyslyslys15<210>94<211>7<212>prt<213>人工序列<220><223>新型肽<400>94lystyrglnasnlysarglys15<210>95<211>7<212>prt<213>人工序列<220><223>新型肽<400>95lystyrglnasnlyslysarg15<210>96<211>7<212>prt<213>人工序列<220><223>新型肽<400>96lystyrglnasnlysargarg15<210>97<211>7<212>prt<213>人工序列<220><223>新型肽<400>97lystyrasnglnarglyslys15<210>98<211>7<212>prt<213>人工序列<220><223>新型肽<400>98lystyrasnglnarglysarg15<210>99<211>7<212>prt<213>人工序列<220><223>新型肽<400>99lystyrasnglnargarglys15<210>100<211>7<212>prt<213>人工序列<220><223>新型肽<400>100lystyrasnglnargargarg15<210>101<211>7<212>prt<213>人工序列<220><223>新型肽<400>101lystyrasnglnlyslyslys15<210>102<211>7<212>prt<213>人工序列<220><223>新型肽<400>102lystyrasnglnlysarglys15<210>103<211>7<212>prt<213>人工序列<220><223>新型肽<400>103lystyrasnglnlyslysarg15<210>104<211>7<212>prt<213>人工序列<220><223>新型肽<400>104lystyrasnglnlysargarg15<210>105<211>7<212>prt<213>人工序列<220><223>新型肽<400>105lystyrasnasnarglyslys15<210>106<211>7<212>prt<213>人工序列<220><223>新型肽<400>106lystyrasnasnarglysarg15<210>107<211>7<212>prt<213>人工序列<220><223>新型肽<400>107lystyrasnasnargarglys15<210>108<211>7<212>prt<213>人工序列<220><223>新型肽<400>108lystyrasnasnargargarg15<210>109<211>7<212>prt<213>人工序列<220><223>新型肽<400>109lystyrasnasnlyslyslys15<210>110<211>7<212>prt<213>人工序列<220><223>新型肽<400>110lystyrasnasnlysarglys15<210>111<211>7<212>prt<213>人工序列<220><223>新型肽<400>111lystyrasnasnlyslysarg15<210>112<211>7<212>prt<213>人工序列<220><223>新型肽<400>112lystyrasnasnlysargarg15<210>113<211>7<212>prt<213>人工序列<220><223>新型肽<400>113lystyrarglysarglyslys15<210>114<211>7<212>prt<213>人工序列<220><223>新型肽<400>114lystyrarglysarglysarg15<210>115<211>7<212>prt<213>人工序列<220><223>新型肽<400>115lystyrarglysargarglys15<210>116<211>7<212>prt<213>人工序列<220><223>新型肽<400>116lystyrarglysargargarg15<210>117<211>7<212>prt<213>人工序列<220><223>新型肽<400>117lystyrarglyslyslyslys15<210>118<211>7<212>prt<213>人工序列<220><223>新型肽<400>118lystyrarglyslysarglys15<210>119<211>7<212>prt<213>人工序列<220><223>新型肽<400>119lystyrargasnlyslysarg15<210>120<211>7<212>prt<213>人工序列<220><223>新型肽<400>120lystyrargasnlysargarg15<210>121<211>7<212>prt<213>人工序列<220><223>新型肽<400>121lystyrlyslysarglyslys15<210>122<211>7<212>prt<213>人工序列<220><223>新型肽<400>122lystyrlyslysarglysarg15<210>123<211>7<212>prt<213>人工序列<220><223>新型肽<400>123lystyrlyslysargarglys15<210>124<211>7<212>prt<213>人工序列<220><223>新型肽<400>124lystyrlyslysargargarg15<210>125<211>7<212>prt<213>人工序列<220><223>新型肽<400>125lystyrlyslyslyslyslys15<210>126<211>7<212>prt<213>人工序列<220><223>新型肽<400>126lystyrlyslyslysarglys15<210>127<211>7<212>prt<213>人工序列<220><223>新型肽<400>127lystyrlyslyslyslysarg15<210>128<211>7<212>prt<213>人工序列<220><223>新型肽<400>128lystyrlyslyslysargarg15当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1