鉴定vcgE基因型创伤弧菌的方法及专用引物与流程
本发明属于生物技术领域,尤其涉及一种鉴定vcge基因型创伤弧菌的方法及专用引物。
背景技术:
创伤弧菌(vibriovulnificue)是一种重要的致病菌,1964年首次由美国cdc从腹泻患者粪便中分离,1970年首次报道引起小腿坏疽和内毒素休克。其广泛存在于海水和海产品中。创伤弧菌可通过食源性和伤口感染,人们通常由于生吃或食用未煮熟的海产品,处理海产品时受伤或者有伤口时接触被污染的海产品或海水而引起感染。食源性感染会导致胃肠炎,进一步可发展为脓毒症,致死率高达50%;伤口感染会导致蜂窝织炎,坏死性筋膜炎等,严重者有截肢风险,致死率高达25%。该菌一旦感染,起病急,病死快。创伤弧菌属于条件致病菌,慢性肝病、糖尿病以及由此产生的血清铁浓度升高患者或免疫力低下人群容易导致感染。流行病学调查数据分析显示,只有部分创伤弧菌可引发感染。在对创伤弧菌基因分型的研究中发现,根据vcg毒力相关基因的序列可将创伤弧菌分为vcgc型(临床型)和vcge型(环境型)两种,vcgc型有潜在的致病性,vcge型通常不致病。有效鉴定这两种型别的创伤弧菌有助于临床治疗和环境中创伤弧菌的种群分析。因此,对创伤弧菌vcgc型和vcge型的鉴定具有重要的意义。目前鉴定vcge型创伤弧菌的方法主要采用普通pcr方法,该方法耗时较长,且灵敏度低。
技术实现要素:
为了更好且准确的鉴定vcge型创伤弧菌,本发明提供了如下技术方案:
本发明提供了一种检测vcge基因型创伤弧菌的成套试剂,包括引物和探针,
所述引物为能扩增靶序列的引物对;
所述靶序列为如下1)或2):
1)序列表的序列4第29-180所示的单链dna分子;
2)将序列4第29-180经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列3具有相同功能的dna分子;
所述探针为结合所述靶序列的探针。
上述引物和探针中,所述引物对由引物f和引物r组成;
所述引物f为如下a1)或a2):
a1)序列表中序列1所示的单链dna分子;
a2)将序列1经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列1具有相同功能的单链dna分子;
所述引物r为如下b1)或b2):
b1)序列表中序列2所示的单链dna分子;
b2)将序列2经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列2具有相同功能的单链dna分子;
所述探针的核苷酸序列如下c1)或c2):
c1)序列表中序列3;
c2)将序列3经过一个或几个核苷酸的取代和/或缺失和/或添加且与序列3具有相同功能的单链dna分子的序列。
所述探针核苷酸序列第8和18个碱基均为锁核酸修饰。
上述成套试剂中,所述引物f、所述引物r和所述探针的摩尔比为2:2:1;
和/或,所述探针的两端分别标记荧光基团fam和淬灭基团bhq1。
含有上述成套试剂的荧光定量pcr试剂也是本发明保护的范围。
上述荧光定量pcr试剂中,所述引物f和所述引物r在所述pcr试剂中的浓度均为0.5μmol/l;
所述探针在所述pcr试剂中的浓度为0.25μmol/l。
含有上述成套试剂或上述pcr试剂的试剂盒也是本发明保护的范围。
上述成套试剂或上述的pcr试剂或上述试剂盒在检测待测样本中是否含有vcge基因型创伤弧菌中的应用也是本发明保护的范围;
或,上述成套试剂或上述的pcr试剂或上述试剂盒在制备检测待测样本中是否含有vcge基因型创伤弧菌产品中的应用也是本发明保护的范围。
或,上述成套试剂或上述的pcr试剂或上述试剂盒在筛选vcge型创伤弧菌的创伤弧菌中的应用也是本发明保护的范围;
或,上述成套试剂或上述的pcr试剂或上述试剂盒在制备筛选vcge型创伤弧菌产品中的应用也是本发明保护的范围。
或,上述成套试剂或上述的pcr试剂或上述试剂盒在检测待测创伤弧菌是否为vcge基因型创伤弧菌中的应用也是本发明保护的范围;
或,上述成套试剂或上述的pcr试剂或上述试剂盒在制备检测待测创伤弧菌是否为vcge基因型创伤弧菌产品中的应用也是本发明保护的范围。
本发明另一个目的是提供一种检测待测样本是否含有vcge基因型创伤弧菌的方法。
本发明提供的方法,包括如下步骤:
用上述成套试剂针对待测创伤弧菌进行荧光定量pcr扩增,检测扩增产物;
若所述扩增产物的探针检测通道无ct值,且无扩增曲线,则所述待测样本不含有或候选不含有vcge基因型创伤弧菌;
若所述扩增产物的探针检测通道ct值≤35,且出现典型的扩增曲线,则所述待测样本中含有或候选含有vcge基因型创伤弧菌。
本发明的实验证明,本发明提供了一组检测vcge基因型创伤弧菌的引物和探针,可用于鉴定或检测待测样本中是否感染或含有vcge型创伤弧菌,为创伤弧菌vcge型的鉴定提供了新的检测方法,具有重要的意义。
附图说明
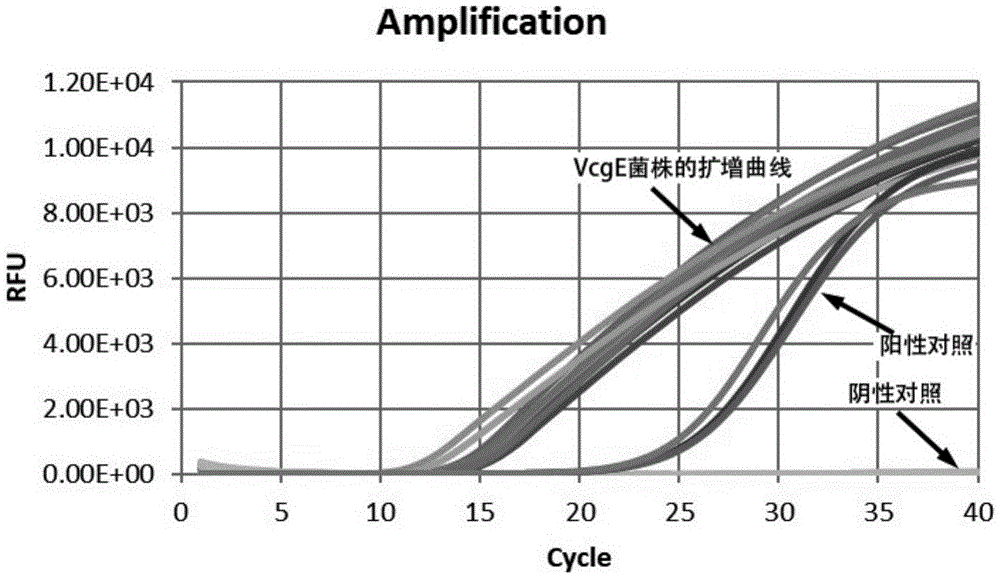
图1为扩增vcge型创伤弧菌结果。
图2为扩增非vcge型创伤弧菌结果。
图3为检测灵敏度的结果。
具体实施方式
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
下述实施例中所用的部分试剂如下:
心浸液肉汤培养基(hi,heartinfusion):称取25g心浸液培养基(bactotmheartinfusionbroth,bd公司,货号238400)和25gnacl溶于800ml去离子水中,待培养基充分溶解后用去离子水定容至1l,121℃高压15分钟灭菌。
哥伦比亚血琼脂(cba,columbiabloodagarbase)平板:称取39g哥伦比亚血琼脂培养基(columbiabloodagarbase,oxoid,货号cm0331)溶于800ml去离子水中,待培养基充分溶解后用去离子水定容至1l,121℃高压15min灭菌,待温度降至90℃时放入50℃水浴锅中平衡30分钟,加入5%无菌脱纤维养血,震荡混匀,倒平板时平板厚度为培养皿深度一半。
上游和下游引物(生工生物工程(上海)股份有限公司合成)。
细菌基因组dna提取试剂盒:天根生化科技(北京)有限公司(货号dp302-02)。
premixextaqtm(probeqpcr)预混液:日本takara公司(货号rr390a)。
下述实施例中所用的部分仪器如下:
生物安全柜:美国nuaire公司
电热恒温培养箱:天津市中环实验电炉有限公司(dhp-500)
恒温振荡培养箱:苏州培英实验设备有限公司(hzq-x100)
实时定量pcr仪:美国bio-rad公司(cfxconnect)
实施例1、创伤弧菌vcge基因型荧光定量pcr检测方法的建立及专用引物探针的设计
一、引物探针合成
根据vcg毒力基因vcge(序列4)设计如下上游引物、下游引物和探针:
上游引物vcge-f:agtgatgagatcattgtcaat(序列1)
下游引物vcge-r:ttgtcagtgtcgcacttat(序列2)
探针vcge-lna-p:fam-agccttt/lna_c/tgagaccaa/lna_g/tttgt-bhq1(序列3)(lna_c表示该位点c碱基为锁核酸;lna_g表示该位点g碱基为锁核酸)
在基因合成公司合成上述引物序列(本例中为生工生物工程(上海)股份有限公司合成)。
二、创伤弧菌vcge基因型荧光定量pcr检测方法的建立
1、创伤弧菌基因组的提取
按照细菌基因组dna提取试剂盒说明书标准操作流程提取待测创伤弧菌基因组dna。提取后的基因组dna放置在-20℃冰箱中储存备用。
2、荧光定量pcr反应
将上述提取的基因组dna加入表1所示的荧光定量pcr反应体系中,进行荧光定量pcr反应。
表1、荧光定量pcr反应体系
上述反应再荧光定量pcr仪上进行,反应条件为95℃预变性5min,95℃变性15s,60℃退火40s,68℃延伸20s,45个循环。探针检测通道设置为fam。
以包含靶序列的基因片段为阳性对照,以ddh2o为模板作为空白对照。
观察检测结果,
若探针检测通道(fam通道)无ct值,且无扩增曲线,则待测样本不含有或候选不含有vcge基因型创伤弧菌;
若探针检测通道(fam通道)15≤ct值≤35,且出现典型的扩增曲线(s形曲线),则待测样本含有或候选含有vcge基因型创伤弧菌;
若探针检测通道(fam通道)ct值>35或<15的样本建议重做。
vcge基因型创伤弧菌为vcg毒力基因是vcge的创伤弧菌。
实施例2、创伤弧菌vcge基因型荧光定量pcr检测
一、待测菌株
47株非vcge基因型创伤弧菌(已经测序验证过基因型),6株vcge基因型创伤弧菌(已经测序验证过基因型)(roschetmetal.arapidandsimplepcranalysisindicatestherearetwosubgroupsofvibriovulnificuswhichcorrelatewithclinicalorenvironmentalisolation.microbiolimmunol.2005;49(4):381-9.)。
取上述各个创伤弧菌甘油菌种,1μl接种环蘸取微量菌液四区划线接种于cba平板,37℃电热恒温培养箱中培养形成单菌落,1μl接种环挑取单菌落接种于hi肉汤,37℃,200r/min条件下置于恒温振荡培养箱中过夜培养,得到各个创伤弧菌培养物。
二、荧光定量pcr特异检测vcge基因型创伤弧菌
1、创伤弧菌基因组的提取
按照细菌基因组dna提取试剂盒说明书标准操作流程提取上述各个创伤弧菌培养物,得到各个创伤弧菌基因组dna。
2、荧光定量pcr反应
按照实施例1的方法对上述各个创伤弧菌基因组dna进行荧光定量pcr反应。
若探针检测通道(fam通道)无ct值,且无扩增曲线,则待测样本不含有或候选不含有vcge基因型创伤弧菌;
若探针检测通道(fam通道)15≤ct值≤35,且出现典型的扩增曲线(s形曲线),则待测样本含有或候选含有vcge基因型创伤弧菌;
若探针检测通道(fam通道)ct值>35或<15的样本建议重做。
6株vcge基因型创伤弧菌的检测结果如图1所示,本方法扩增6株vcge型创伤弧菌时,均出现典型扩增曲线,且ct值均≤35,空白对照无扩增;说明本发明方法检测率为100%。
47株非vcge基因型创伤弧菌的检测结果如图2所示,本方法扩增非vcge型创伤弧菌时,阳性对照有典型扩增曲线,空白对照和非vcge型创伤弧菌均未出现典型扩增曲线。
依据上述方法鉴定待测菌株的结果如下:从6株vcge基因型创伤弧菌菌株中鉴定出6株vcge基因型创伤弧菌,从47株非vcge基因型创伤弧菌菌株中鉴定出0株vcge基因型创伤弧菌,该方法的灵敏度为6/6×100%=100.0%,特异性为47/47×100%=100.0%,具体见表2。
表2、荧光定量pcr鉴定vcge基因型创伤弧菌的结果
上述结果表明,此方法可用于特异鉴定vcge型创伤弧菌。
三、荧光定量pcr检测vcge基因型创伤弧菌的灵敏度
将vcge基因(序列4)导入到质粒(peasy-t1克隆载体,北京全式金生物技术有限公司,产品目录号:ct101)中构建标准质粒。
根据标准质粒浓度分别稀释至106、105、104、103、102、101、100个拷贝数/μl作为模板,按照实施例1的方法对各个模板进行荧光定量pcr检测。
结果如图3所示,可以看出,该方法检测的灵敏度为100个拷贝/μl。
sequencelisting
<110>中国人民解放军军事科学院军事医学研究院
<120>鉴定vcge基因型创伤弧菌的方法及专用引物
<160>4
<170>patentinversion3.5
<210>1
<211>21
<212>dna
<213>人工序列
<400>1
agtgatgagatcattgtcaat21
<210>2
<211>19
<212>dna
<213>人工序列
<400>2
ttgtcagtgtcgcacttat19
<210>3
<211>23
<212>dna
<213>人工序列
<400>3
agcctttctgagaccaagtttgt23
<210>4
<211>544
<212>dna
<213>人工序列
<400>4
atgtacaagaaaatcgctatcgccgcctttgtcagtgtcgcacttatggggtgtcaaacg60
acatcgaaacaagctcaaacaggtacagaaagtggttatggcgaaatggctaacgccgcg120
ctgatgagcgcagtacaaacttggtctcagaaaggctcaattgacaatgatctcatcact180
actatccaaagtagcgccaacattttgtcagaacaggcggtcggcggagtgggatcactc240
cttgcgctcgcgaaaaactcattgagcaataacgaaagcaccgagttagcagggcttatg300
cctgggtttgattcactacaatcaagcggccttacagcgttaatcagcaataacgacacg360
gttaagagcgccttttcggcattgggattagatccagctcttatttctacctttacaccg420
atcatcctaagcgcactacaaaatcagggcgcaagctcaggtttgctagatagtctttct480
tctatctggaaataagcgagaagcgagaagcgagaagcgagaagcgagaagcgagaagcg540
agaa544
- 还没有人留言评论。精彩留言会获得点赞!