一种CAR-T毒性指示细胞的快速构建方法与流程
本发明涉及细胞免疫治疗技术领域,具体说是一种car-t毒性指示细胞的快速构建方法。
背景技术:
嵌合抗原受体t细胞疗法car-t在肿瘤治疗领域具有极大地应用前景和价值,car-t以其治疗高度精确性、确定的临床疗效和良好的安全性成为肿瘤治疗领域极具前景的研究方向。
在医学研究和临床应用中,对car-t细胞毒性的测定是一个不可避免的重要问题,car-t细胞毒性也是衡量car-t产品质量的重要标准之一。目前常用的体外检测细胞毒性的方法步骤是将car-t细胞与靶细胞混合后,经过一段时间的培养期后,采用流式抗体标记后利用流式细胞法测定。此法面临着检测时间长、操作繁琐、误差较大等问题。
荧光素酶法是一种新兴的测定car-t细胞毒性的方法,具体为:改造指示细胞,使其稳定表达荧光素酶,指示细胞数目和荧光素酶活力值存在定量关系,指示细胞表达肿瘤相关细胞膜靶抗原,car-t细胞特异性识别并结合这些肿瘤相关靶抗原,发挥杀伤作用并裂解指示细胞,荧光素酶随之释放,离心可使未裂解细胞位于沉淀中,因此通过检测上清和沉淀中的荧光素酶活力值,即可推算出裂解和未裂解细胞的数目,从而计算裂解细胞比例,表征car-t细胞毒性。
指示细胞是荧光素酶法的关键,目前指示细胞的构建主要方法是利用携带荧光素酶基因的慢病毒去感染目的细胞(表达肿瘤细胞膜靶抗原),经过筛选后最终获取稳定表达荧光素酶的细胞株(即指示细胞);另外,如果无法获取表达肿瘤特异性抗原的细胞株,那么利用慢病毒感染常见细胞系,使其同时稳定表达荧光素酶和肿瘤细胞膜靶抗原也是car-t细胞毒性检测中常用的策略。
但是无论哪种方法,首先都必须经过制备慢病毒、感染细胞并筛选稳转细胞株等一系列繁琐步骤;其次针对不同的car-t细胞,必然需要制备与之相应的一系列的指示细胞,整个指示细胞构建过程存在耗时较长、工作量巨大、成功率较低等问题;最后多靶点car-t细胞毒性的检测,要求指示细胞同时表达多个肿瘤抗原,这也意味着指示细胞构建难度随之攀升。因此,设计一种耗时短,工作量小,成功率高,步骤简便易行,甚至可以同时表达多个肿瘤抗原的car-t毒性指示细胞的构建方法成为亟待解决的问题。
技术实现要素:
为解决上述问题,本发明的目的是提供一种car-t毒性指示细胞的快速构建方法。
本发明为实现上述目的,通过以下技术方案实现:
一种car-t毒性指示细胞的快速构建方法,包括以下步骤:
①构建序列为seqno:1的慢病毒质粒,该慢病毒质粒携带以下外源基因片段:igkleader、avidin、cd28跨膜区、t2a序列及luciferase;
②慢病毒质粒大提,病毒包装制备得到慢病毒;
③慢病毒感染常用细胞x,通过嘌呤霉素筛选获取稳定表达荧光素酶luciferase和
抗生物素蛋白avidin的通用细胞u;
其中常用细胞x为工具细胞、悬浮细胞或贴壁肿瘤细胞;所述工具细胞为293ft细胞或jurkat细胞;所述悬浮细胞为u266细胞、rpmi8226细胞、raji细胞或k562细胞;贴壁肿瘤细胞为mcf-7细胞或mda-mb-231细胞;
④将一种或几种生物素化处理的蛋白a加入到通用细胞u中,与u细胞膜上的avidin紧密结合,得到car-t毒性指示细胞;生物素化处理的蛋白a为以下细胞的细胞膜靶抗原胞外域部分:cd19、cd20、cd38、cs1、cd30、pdl1、gpc3或her2肿瘤细胞。
优选的,生物素化处理的蛋白a的种类为两种或三种。
优选的,常用细胞x为293ft细胞或k562细胞。
优选的,生物素化处理的蛋白a为cd19、cd20和cd30的细胞膜靶抗原胞外域部分。
优选的一种car-t毒性指示细胞的快速构建方法,步骤①中构建序列为seqno:1的慢病毒质粒包括以下步骤:
⑴全基因合成序列为seqno:1的基因片段,设计上下游酶切位点分别为xhoi和bamhi;
⑵用xhoi和bamhi双酶切上述基因片段,及plvx-ires-puro质粒,切胶回收后连接;
⑶将连接产物转化stbl3感受态细胞,涂布含有氨苄青霉素抗性的lb培养基平板;
⑷挑取单克隆至含有氨苄青霉素抗性的lb培养基培养8~12小时;
⑸小提质粒,xhoi和bamhi双酶切结合凝胶电泳验证,质粒测序验证其正确性后保存。
本发明相比现有技术具有以下优点:
本发明的car-t毒性指示细胞的快速构建方法,通过添加不同的生物素化处理的蛋白a(肿瘤靶抗原胞外域部分)或其组合,能够快速的将含有luciferase基因片段的细胞u转变为多种适用于car-t毒性检测的指示细胞,大大省略了繁琐的制备步骤,节省了制备时间,降低了成本;由于car-t毒性检测的指示细胞能同时具有荧光素酶和一种或多种肿瘤靶抗原,因此能作为一种抗原的指示细胞或多种抗原的指示细胞,能够满足单靶点或多靶点car-t细胞毒性的检测。
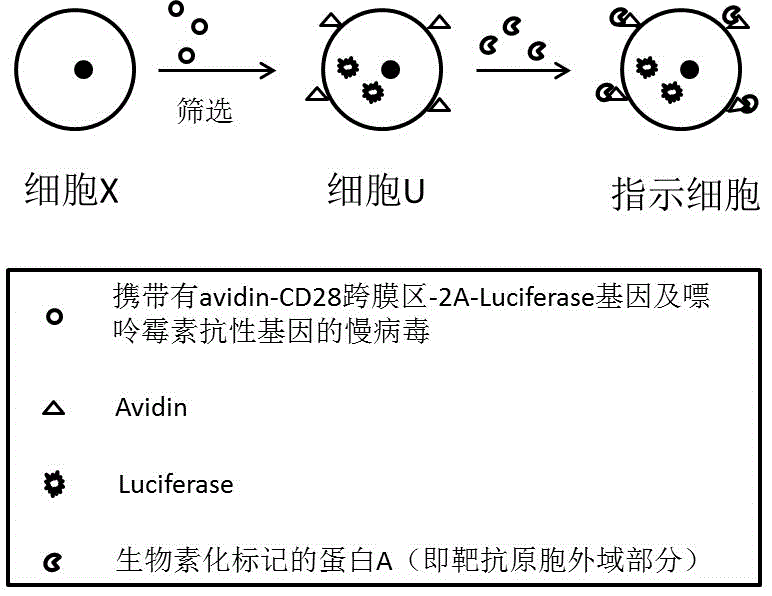
图1为car-t毒性指示细胞的快速构建方法的原理示意图;
图2为慢病毒质粒携带的外源基因片段示意图;
图3为luciferase活力(发光强度)与细胞数目的关系示意图;
图4为cd19car-t的杀伤效应示意图。
具体实施方式
本发明的目的是提供一种car-t毒性指示细胞的快速构建方法,通过以下技术方案实现:
一种car-t毒性指示细胞的快速构建方法,原理如图1所示,包括以下步骤:
①构建序列为seqno:1的慢病毒质粒,该慢病毒质粒携带以下外源基因片段:igkleader(免疫球蛋白k的信号肽)、avidin(抗生物素蛋白)、cd28跨膜区、t2a序列及luciferase(荧光素酶),如图2所示;
②慢病毒质粒大提,病毒包装制备得到慢病毒;
③慢病毒感染常用细胞x,通过嘌呤霉素筛选获取稳定表达荧光素酶luciferase和抗生物素蛋白avidin的通用细胞u;
其中常用细胞x为工具细胞、悬浮细胞或贴壁肿瘤细胞;所述工具细胞为293ft细胞或jurkat细胞;所述悬浮细胞为u266细胞、rpmi8226细胞、raji细胞或k562细胞;贴壁肿瘤细胞为mcf-7细胞或mda-mb-231细胞;
④将生物素化处理的蛋白a加入到通用细胞u中,与u细胞膜上的avidin紧密结合,得到单抗原car-t毒性指示细胞;生物素化处理的蛋白a为以下细胞的细胞膜靶抗原胞外域部分:cd19、cd20、cd38、cs1、cd30、pdl1、gpc3或her2肿瘤细胞;
将几种不同生物素化处理的蛋白a加入到通用细胞u中,与u细胞膜上的avidin紧密结合,得到多抗原car-t毒性指示细胞;生物素化处理的蛋白a为以下细胞的细胞膜靶抗原胞外域部分:cd19、cd20、cd38、cs1、cd30、pdl1、gpc3或her2肿瘤细胞。
优选的,生物素化处理的蛋白a的种类为两种或三种。
优选的,常用细胞x为293ft细胞或k562细胞。
优选的,生物素化处理的蛋白a为cd19、cd20和cd30细胞的细胞膜靶抗原胞外域部分。
优选的一种car-t毒性指示细胞的快速构建方法,步骤①中构建序列为seqno:1的慢病毒质粒包括以下步骤:
⑴全基因合成序列为seqno:1的基因片段,设计上下游酶切位点分别为xhoi和bamhi;
⑵用xhoi和bamhi双酶切上述基因片段,及plvx-ires-puro质粒,切胶回收后连接;
⑶将连接产物转化stbl3感受态细胞,涂布含有氨苄青霉素抗性的lb培养基平板;
⑷挑取单克隆至含有氨苄青霉素抗性的lb培养基培养8~12小时;
⑸小提质粒,xhoi和bamhi双酶切结合凝胶电泳验证,质粒测序验证其正确性后保存。
本发明实施例中质粒大提所用的试剂盒为天根质粒大提试剂盒。生物素化处理的cd19、cd20和cd30胞外域蛋白均由acrobiosystems公司提供;
以下结合具体实施例来对本发明作进一步的描述。
实施例1
一、构建慢病毒质粒
1、全基因合成图1所示基因片段,序列为sedno:1,该片段中含有igkleader、avidin、cd28跨膜区、t2a序列及firefly来源的luciferase,同时设计上下游酶切位点分别为xhoi和bamhi;
2、用xhoi和bamhi双酶切上述基因片段和plvx-ires-puro质粒;切胶回收,常规分子生物学方法连接;
3、将连接产物转化stbl3感受态细胞,涂布lb培养基平板(氨苄青霉素抗性)
4、挑取单克隆至lb培养基培养8~12小时;
5、小提质粒,xhoi和bamhi双酶切,结合凝胶电泳验证条带大小是否正确,利用通用引物进一步质粒测序验证正确性;通用引物由生工生物工程(上海)股份有限公司提供;
6、将质粒保存于-20℃,命名为plvx-avidin-luc-ires-puro。
二、制备慢病毒
1、质粒大提
将plvx-avidin-luc-ires-puro质粒常规转化stbl3感受态,挑取单克隆至500ml锥形瓶(内含100mllb培养基),过夜培养,利用质粒提取盒提取质粒,ddh2o洗脱质粒,nanadrop测得质粒浓度大于1μg/μl;
2、病毒包装
(1)制备a液:取1.5mlep管,加入opti-mem1.2ml,加入各质粒如下,涡旋振荡5~10秒混匀,加入质粒质量比为:
pspax27.5μg
pmd2.g2.5μg
plvx-avidin-luc-ires-puro10μg
(2)制备b液:取15ml离心管,加入opti-mem1.5ml,lipo200060μl,涡旋振荡5~10秒;
(3)将a液加入b液中,涡旋振荡5~10秒,20~30℃放置20分钟;
(4)准备293t细胞:将293t细胞铺10cm板中,至293t细胞融合度达到80%;
(5)将a、b混合液均匀滴在上述10cm板中,静置3~5分钟,轻轻摇匀,37℃培养箱培养60小时;
(6)2000rpm离心10分钟,去除细胞碎片,0.45μm滤膜过滤;
(7)收集上清液,分装置于-80℃保存。
三、慢病毒感染k562细胞
1、取2×105个k562细胞,加入0.5mlimdm完全培养基(含10%fbs)重悬,置于12孔板中,加入polybrene至6μg/ml、0.5ml病毒上清液,充分混匀,3000rpm室温离心4小时;
2、4小时后加入等体积新鲜培养基以稀释polybrene;继续培养3~4天,隔天换液;
3、按照常规嘌呤霉素筛选方法,多次传代,获取嘌呤霉素抗性细胞k562-avidin-luc;
4、常规方法提取第3步嘌呤霉素抗性细胞k562-avidin-luc,利用常规荧光定量pcr方法,检测seqno:1基因表达情况,利用fireflyluciferase检测试剂盒检测luciferase活力,证明k562-avidin-luc细胞中已经稳定表达avidin和luciferase。
四、慢病毒感染293ft细胞
1、取5×105个293ft细胞,加入0.5mlimdm完全培养基(含10%fbs)重悬,置于12孔板中,加入polybrene至4μg/ml和0.5ml病毒上清液,充分混匀,3000rpm室温离心4小时;
2、4小时后加入等体积新鲜培养基以稀释polybrene;继续培养3~4天,隔天换液;
3、按照常规嘌呤霉素筛选方法,多次传代,获取嘌呤霉素抗性细胞293ft-avidin-luc;
4、常规方法提取第3步嘌呤霉素抗性细胞293ft-avidin-luc,利用常规荧光定量pcr方法,检测seqno:1基因表达情况,利用fireflyluciferase检测试剂盒检测luciferase活力,证明293ft-avidin-luc细胞中已经稳定表达avidin和luciferase。
步骤三和步骤四中的k562细胞和293ft细胞可以用其它常用细胞系替换,包括但不限于jurkat等工具细胞以及其他肿瘤细胞系,例如u266、rpmi8226、raji等悬浮细胞及mcf-7、mda-mb-231等贴壁肿瘤细胞系。
实施例2
构建携带cd19抗原的k562细胞
1、在12孔板中培养步骤三构建的k562-avidin-luc细胞,使其处于对数生长期;
2、cd19抗原蛋白胞外域氨基酸序列见seqno:2,可以将此序列委托公司外源表达,为易于纯化,在序列末端加入组氨酸标签。蛋白纯化后,委托公司进行生物素化处理。或者,生物素化处理的cd19胞外域蛋白已经商品化,可以通过购买获取,如acrobiosystems公司可以提供。
3、取1×106个k562-avidin-luc细胞,加入上述获取的生物素化处理的cd19抗原胞外域蛋白至终浓度10μg/ml,4℃孵育30分钟;
4、离心去除上清液,用imdm完全培养基(含10%fbs)重悬,重复本步骤1次,得到携带cd19抗原的k562细胞。
得到的携带cd19抗原的k562细胞在稳定表达luciferase的基础上,又结合了cd19抗原胞外域,可以作为检测cd19car-t细胞毒性的指示细胞。利用fireflyluciferase测定试剂盒所述方法,分析在一定细胞数目范围内,luciferase活力(发光强度)与细胞数目呈现线性关系,如图3所示。
实施例3构建携带cd19和cd30抗原的k562细胞
1、在12孔板中培养步骤三构建的k562-avidin-luc细胞,使其处于对数生长期;
2、准备生物素化处理的cd19和cd30胞外域蛋白;
3、取1×106个k562-avidin-luc细胞,同时加入上述生物素化处理的cd19和cd30胞外域蛋白至终浓度为10μg/ml,4℃孵育60分钟;
4、离心去除上清液,用imdm完全培养基(含10%fbs)重悬,重复本步骤1次,得到携带cd19和cd30抗原的k562细胞。
得到携带cd19和cd30抗原的k562细胞在稳定表达luciferase的基础上,又结合了cd19和cd30抗原胞外域,可以作为检测同时靶向cd19和cd30的car-t细胞毒性的指示细胞。
实施例4
构建同时携带cd19、cd20和cd30抗原的k562细胞
1、在12孔板中培养步骤三构建的k562-avidin-luc细胞,使其处于对数生长期;
2、准备生物素化处理的cd19、cd20和cd30胞外域蛋白;
3、取1×106个k562-avidin-luc细胞,同时加入上述生物素化处理的cd19、cd20和cd30胞外域蛋白至终浓度为10μg/ml,4℃孵育60分钟;
4、离心去除上清液,用imdm完全培养基(含10%fbs)重悬,重复本步骤1次,得到携带cd19、cd20和cd30抗原的k562细胞。
得到携带cd19、cd20和cd30抗原的k562细胞在稳定表达luciferase的基础上,又结合了cd19、cd20和cd30抗原胞外域,可以作为检测同时靶向cd19、cd20和cd30的car-t细胞毒性的指示细胞。
实施例5
携带cd19抗原的k562细胞作为cd19car-t细胞毒性指示细胞的应用
1、将步骤五构建的携带cd19抗原的k562细胞用imdm完全培养基(含10%fbs)悬浮至1×107/ml,取10μl/孔加入到96孔板中;
2、cd19car-t细胞制备过程如文献(oncotargetsther.2018,11:1767-1776)所示;
3、用imdm完全培养基(含10%fbs)将cd19car-t细胞悬浮至1×107/ml,取相应体积加入到上述孔中,使cd19car-t细胞的数目和指示细胞的数目之比分别为0:1(对照组)、1:1(实验组)、2:1(实验组)、5:1(实验组)、10:1(实验组),且每个比例至少3个重复孔;
3、用imdm完全培养基(含10%fbs)补足每孔150μl;
4、co2培养箱中培养24h;
5、300g离心5min去掉培养基上清;
6、按照fireflyluciferase测定试剂盒(promegae1501)所述方法,加入裂解液至细胞沉淀中,测定裂解产物中luciferase活力;
7、计算cd19car-t的杀伤效应killingeffect(%)=(对照组生物发光强度-实验组生物发光强度)/对照组生物发光强度*100;如图4所示,经过计算cd19car-t具有明显的细胞毒性,可以得出采用本申请的制备方法得到的携带cd19抗原的k562细胞作为cd19car-t细胞毒性指示细胞。
序列表
<110>山东昂科诺生物科技有限公司
<120>一种car-t毒性指示细胞的快速构建方法
<141>2019-05-06
<160>2
<170>siposequencelisting1.0
<210>1
<211>2505
<212>dna
<213>人工序列(artificialsequence)
<400>1
ctcgagatggagacagacacactcctgctatgggtactgctgctctgggttccaggttcc60
actggtgactatccatatgatgttccagattatgctggggcccagccggccagatctatg120
gcggaagcgggtatcaccggcacgtggtacaaccagtctggttctaccttcaccgttacc180
gcgggtgcggacggtaacctgaccggtcagtacgaaaaccgtgcgcagggcactggttgc240
cagaactctccgtacaccctgaccggtcgttacaacggtaccaaactggaatggcgtgtt300
gaatggaacaactctaccgaaaactgccactctcgtaccgaatggcgtggtcagtaccag360
ggtggtgcggaagcgcgtatcaacacccagtggaacctgacctacgaaggtggttctggt420
ccggcgaccgaacagggtcaggacaccttcaccaaagttaaaccgtctgcggcgtctgac480
tacaaggacgatgacgacaagggcgcgccggaattcattgaagttatgtatcctcctcct540
tacctagacaatgagaagagcaatggaaccattatccatgtgaaagggaaacacctttgt600
ccaagtcccctatttcccggaccttctaagcccttttgggtgctggtggtggttggtgga660
gtcctggcttgctatagcttgctagtaacagtggcctttattattttctgggtgaggagt720
aagaggagcaggctcctgcacagtgactacatgaacatgactccccgccgccccgggccc780
acccgcaagcatgaaggtagaggtagtctcctcacatgtggcgatgtagaagagaaccct840
ggtccgatggaagatgccaaaaacattaagaaaggcccagcgccattctacccactcgaa900
gacgggaccgctggcgagcagctgcataaagccatgaagcgctacgccctggtgcccggc960
accatcgcctttaccgacgcacatatcgaggtggacattacctacgccgagtacttcgag1020
atgagcgttcggctggcagaagctatgaagcgctatgggctgaatacaaaccatcggatc1080
gtggtgtgtagcgagaatagcttgcagttcttcatgcccgtgttgggtgccctgttcatc1140
ggtgtggctgtggccccagctaacgacatctacaacgagcgcgagctgctgaacagcatg1200
ggcatcagccagcccaccgtcgtattcgtgagcaagaaagggctgcaaaagatcctcaac1260
gtgcaaaagaagctaccgatcatacaaaagatcatcatcatggatagcaagaccgactac1320
cagggcttccaaagcatgtacaccttcgtgacttcccatttgccacccggcttcaacgag1380
tacgacttcgtgcccgagagcttcgaccgggacaaaaccatcgccctgatcatgaacagt1440
agtggcagtaccggattgcccaagggcgtagccctaccgcaccgcaccgcttgtgtccga1500
ttcagtcatgcccgcgaccccatcttcggcaaccagatcatccccgacaccgctatcctg1560
agcgtggtgccatttcaccacggcttcggcatgttcaccacgctgggctacttgatctgc1620
ggctttcgggtcgtgctcatgtaccgcttcgaggaagagctattcttgcgcagcttgcaa1680
gactataagattcaatctgccctgctggtgcccacactatttagcttcttcgctaagagc1740
actctcatcgacaagtacgacctaagcaacttgcacgagatcgccagcggcggggcgccg1800
ctcagcaaggaggtaggtgaggccgtggccaaacgcttccacctaccaggcatccgccag1860
ggctacggcctgacagaaacaaccagcgccattctgatcacccccgaaggggacgacaag1920
cctggcgcagtaggcaaggtggtgcccttcttcgaggctaaggtggtggacttggacacc1980
ggtaagacactgggtgtgaaccagcgcggcgagctgtgcgtccgtggccccatgatcatg2040
agcggctacgttaacaaccccgaggctacaaacgctctcatcgacaaggacggctggctg2100
catagcggcgacatcgcctactgggacgaggacgagcacttcttcatcgtggaccggctg2160
aagagcctgatcaaatacaagggctaccaggtagccccagccgaactggagagcatcctg2220
ctgcaacaccccaacatcttcgacgccggggtcgccggcctgcccgacgacgatgccggc2280
gagctgcccgccgcagtcgtcgtgctggaacacggtaaaaccatgaccgagaaggagatc2340
gtggactatgtggccagccaggttacaaccgccaagaagctgcgcggtggtgttgtgttc2400
gtggacgaggtgcctaaaggactgaccggcaagttggacgcccgcaagatccgcgagatt2460
ctcattaaggccaagaagggcggcaagatcgccgtctagggatcc2505
<210>2
<211>538
<212>prt
<213>人工序列(artificialsequence)
<400>2
proglugluproleuvalvallysvalglugluglyaspasnalaval
151015
leuglncysleulysglythrseraspglyprothrglnglnleuthr
202530
trpserarggluserproleulyspropheleulysleuserleugly
354045
leuproglyleuglyilehismetargproleualailetrpleuphe
505560
ilepheasnvalserglnglnmetglyglyphetyrleucysglnpro
65707580
glyproproserglulysalatrpglnproglytrpthrvalasnval
859095
gluglyserglygluleupheargtrpasnvalseraspleuglygly
100105110
leuglycysglyleulysasnargsersergluglyproserserpro
115120125
serglylysleumetserprolysleutyrvaltrpalalysasparg
130135140
progluiletrpgluglygluproprocysleuproproargaspser
145150155160
leuasnglnserleuserglnaspleuthrmetalaproglyserthr
165170175
leutrpleusercysglyvalproproaspservalserargglypro
180185190
leusertrpthrhisvalhisprolysglyprolysserleuleuser
195200205
leugluleulysaspaspargproalaargaspmettrpvalmetglu
210215220
thrglyleuleuleuproargalathralaglnaspalaglylystyr
225230235240
tyrcyshisargglyasnleuthrmetserphehisleugluilethr
245250255
alaargprovalleutrphistrpleuleuargthrglyglytrplys
260265270
valseralavalthrleualatyrleuilephecysleucysserleu
275280285
valglyileleuhisleuglnargalaleuvalleuargarglysarg
290295300
lysargmetthraspprothrargargphephelysvalthrpropro
305310315320
proglyserglyproglnasnglntyrglyasnvalleuserleupro
325330335
thrprothrserglyleuglyargalaglnargtrpalaalaglyleu
340345350
glyglythralaprosertyrglyasnproserseraspvalglnala
355360365
aspglyalaleuglyserargserproproglyvalglyprogluglu
370375380
glugluglygluglytyrglugluproaspserglugluaspserglu
385390395400
phetyrgluasnaspserasnleuglyglnaspglnleuserglnasp
405410415
glyserglytyrgluasnprogluaspgluproleuglyprogluasp
420425430
gluaspserpheserasnalaglusertyrgluasngluaspgluglu
435440445
leuthrglnprovalalaargthrmetasppheleuserprohisgly
450455460
seralatrpaspproserargglualathrserleualaglysergln
465470475480
sertyrgluaspmetargglyileleutyralaalaproglnleuarg
485490495
serileargglyglnproglyproasnhisglugluaspalaaspser
500505510
tyrgluasnmetaspasnproaspglyproaspproalatrpglygly
515520525
glyglyargmetglythrtrpserthrarg
530535
- 还没有人留言评论。精彩留言会获得点赞!