毒黄素半抗原、人工抗原、抗体及其合成方法和应用与流程
本发明涉及了免疫化学分析
技术领域:
,特别是涉及了毒黄素半抗原、人工抗原、抗体及其合成方法和应用。
背景技术:
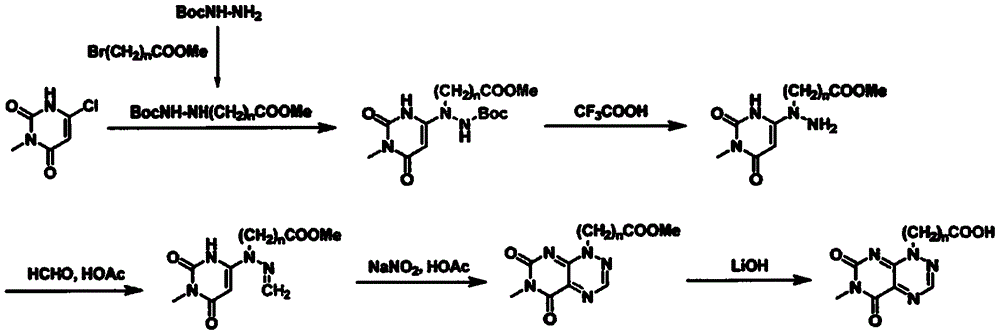
:酵米面中毒是我国广大农村致死率极高的一种细菌性食物中毒。椰毒假单胞菌酵米面亚种是引起酵米面食物中毒和变质银耳中毒的原因,研究证明该菌的致病物质是其在生长繁殖过程中产生的两种毒素:米酵菌酸(bongkrekicacid,ba)和毒黄素(toxoflavin,tf)。两种毒素均为脂肪酸类的小分子物质,具有剧毒、耐热、毒性强,不能被一般的烹调方法所破坏,故食品被污染后极易引起中毒,目前尚无特效解毒药物,且米酵菌酸的产量远高于毒黄素。目前用于检测米酵菌酸的方法主要有传统的检测方法,如分光光度法、高效液相色谱法及其联用技术等,以上方法虽然可以精确定量,但由于设备仪器昂贵,检测时间长,且需专业人员操作,因此无法实现真正意义上的现场检测。而免疫学检测分析技术以其高灵敏、特异性高、快速、操作简便等优点在药物残留检测领域已被广泛应用,比起仪器等检验方法有很多优势。所以免疫分析为米酵菌酸残留研究提供了一条新的分析检测方法。在建立免疫学检测方法并应用该检测方法检测米酵菌酸残留量时,关键技术在于能够获取到特异性强、灵敏度高的抗体,而要实现这一目标,前提条件就是得合成、制备出合适的米酵菌酸半抗原。但是米酵菌酸为链状结构,免疫动物难以获得高质量的抗体。而毒黄素则是由两个并环组成的立体状的分子,相对于米酵菌酸,免疫动物更容易获得高灵敏、高特异的抗体。通过免疫检测毒黄素可以间接检测米酵菌酸,对米酵菌酸的中毒检测提供一种简便可靠的检测方案。但是,目前,国内还没有针对毒黄素半抗原的相关报道。技术实现要素:为了弥补已有技术的缺陷,本发明提供毒黄素半抗原、人工抗原、抗体及其合成方法和应用。本发明所要解决的技术问题通过以下技术方案予以实现:毒黄素半抗原,其具有如下结构式:其中,n为-ch2基团数目,n为2-8的整数。本发明还提供上述毒黄素半抗原的合成方法,包括如下步骤:s1.6-氯-3-甲基嘧啶与化合物1进行反应,得到化合物2,所述化合物1的分子式为:bocnh-nh(ch2)ncoome,其中,n为-ch2基团数目,n为2-8的整数;所述化合物2具有结构式其中,n为-ch2基团数目,n为2-8的整数;s2.所述化合物2与三氟乙酸进行反应,得到化合物3,所述化合物3具有结构式其中,n为-ch2基团数目,n为2-8的整数;s3.在酸性条件下,所述化合物3与甲醛进行反应,得到化合物4,所述化合物4具有结构式其中,n为-ch2基团数目,n为2-8的整数;s4.在亚硝酸钠和乙酸存在下,所述化合物4进行反应,得到化合物5,所述化合物5具有结构式其中,n为-ch2基团数目,n为2-8的整数;s5.所述化合物5进行水解反应,得到所述毒黄素半抗原。进一步地,所述化合物1的合成方法为:(1)提供中间体1,所述中间体1的分子式为:br(ch2)ncoome,其中,n为-ch2基团数目,n为2-8的整数;(2)所述中间体1与肼基甲酸叔丁酯进行反应,得到所述化合物1。本发明还提供毒黄素人工抗原,所述毒黄素人工抗原包括毒黄素免疫抗原和毒黄素包被抗原,其是由上述毒黄素半抗原与载体蛋白偶联得到的。进一步地,所述载体蛋白为牛血清白蛋白(bsa),卵清蛋白(ova),人血清白蛋白(has)或血蓝蛋白(klh)中的任意一种。进一步地,制备毒黄素免疫抗原时,所述毒黄素半抗原结构中,3≤n≤8;制备毒黄素包被抗原时,所述毒黄素半抗原结构中,2≤n≤5。进一步地,制备毒黄素免疫抗原时,所述毒黄素半抗原结构中,n为5或6;制备毒黄素包被抗原时,所述毒黄素半抗原结构中,n为3。本发明还提供毒黄素人工抗原的合成方法,其是采用混合酸酐法将所述毒黄素半抗原与载体蛋白偶联制备得到。本发明还提供一种毒黄素抗体,它是由上述毒黄素免疫抗原经动物免疫得到。一种检测毒黄素的免疫学方法,其采用上述毒黄素抗体。进一步地,待测样品经甲醇和盐酸羟胺处理,其中,所述盐酸羟胺的浓度为0.2m-0.8m。进一步地,所述免疫学方法为免疫层析法、酶联免疫吸附试验、时间分辨荧光免疫分析、化学发光免疫分析在内的任意一种免疫学分析方法。本发明具有如下有益效果:特别说明,本申请文件中化学结构式中et为乙基;ac为乙酰基;me为甲基。本发明中,在毒黄素1位上的氮原子上衍生脂肪链连接臂,衍生的脂肪链连接臂末段带有羧基,本发明的毒黄素半抗原最大程度保留了毒黄素的特征结构,能更好地暴露半抗原的抗原决定簇,使得毒黄素半抗原的免疫原性明显增强,又具有可以与载体蛋白发生偶联的羧基;该毒黄素半抗原与载体蛋白偶联后得到的毒黄素免疫抗原去免疫动物,更有利于刺激动物免疫应答产生特异性更强、灵敏度更高的抗体,采用该抗体的免疫学方法可以检测出0.02ng/ml的毒黄素污染,为米酵菌酸中毒提供了简便快捷的解决方案,整个检测流程只需要十多分钟,完全能够满足实际检测需求。本发明中毒黄素半抗原的合成方法,使用的原料易得,反应操作较为简单,反应条件易于控制。本发明的毒黄素半抗原合成方法,合成路线简单,毒黄素半抗原的纯度和收率高,整体的合成成本更具优势。附图说明图1为本发明毒黄素半抗原的合成路线。具体实施方式第一方面,本发明提供毒黄素半抗原,其具有如下结构式:其中,n为-ch2基团数目,n为2-8的整数。人工抗原的合成是免疫检测中抗体制备和建立免疫分析方法最关键的步骤,半抗原的合成是人工抗原合成的关键。毒黄素因分子量小而不具有免疫原性(分子量小于1000),不能在动物体内产生抗体,必须与大分子载体蛋白偶联制备人工抗原,才能诱导特异性抗体的产生。由于毒黄素分子上没有可以直接与载体蛋白偶联的活性基团,因此需先通过衍生过程在毒黄素小分子上适当的位置引入合适的连接臂和与载体蛋白偶联的活性基团。不同结构的连接臂、不同的偶联方法或连接臂的引入位置,都影响后续建立的免疫学方法检测的灵敏度和特异性。目前,以毒黄素衍生物为半抗原制备合成抗体和人工抗原进行检测毒黄素的免疫学方法鲜有报道。本发明中,在毒黄素1位上的氮原子上衍生脂肪链连接臂,衍生的脂肪链连接臂末段带有羧基,本发明的毒黄素半抗原最大程度保留了毒黄素的特征结构,能更好地暴露半抗原的抗原决定簇,使得毒黄素半抗原的免疫原性明显增强,又具有可以与载体蛋白发生偶联的羧基;该毒黄素半抗原与载体蛋白偶联后得到的毒黄素免疫抗原去免疫动物,更有利于刺激动物免疫应答产生特异性更强、灵敏度更高的抗体,采用该抗体的免疫学方法可以检测出0.02ng/ml的毒黄素污染,为米酵菌酸中毒提供了简便快捷的解决方案,整个检测流程只需要十多分钟,完全能够满足实际检测需求。本发明的毒黄素半抗原,不仅合成方法简便、纯度较高,而且能应用于合成适于动物免疫的抗原体系,弥补了国内毒黄素免疫学方法
技术领域:
的空白,为毒黄素免疫检测方法的进一步发展奠定了基础。第二方面,本发明提供上述毒黄素半抗原的合成方法。具体地,上述结构的毒黄素半抗原的合成方法包括如下步骤:s1.6-氯-3-甲基嘧啶与化合物1进行反应,得到化合物2,所述化合物1的分子式为:bocnh-nh(ch2)ncoome,其中,n为-ch2基团数目,n为2-8的整数;所述化合物2具有结构式其中,n为-ch2基团数目,n为2-8的整数;此步骤中,6-氯-3-甲基嘧啶与化合物1进行取代反应,其原理都为本技术人员均可通过技术手册得知或通过常规实验方法获知,本发明对反应的具体操作不作具体限定,本领域技术人员可以根据实际需要进行常规调整。所述化合物1的合成方法为:(1)提供中间体1,所述中间体1的分子式为:br(ch2)ncoome,其中,n为-ch2基团数目,n为2-8的整数;(2)所述中间体1与肼基甲酸叔丁酯进行反应,得到所述化合物1。s2.所述化合物2与三氟乙酸进行反应,得到化合物3,所述化合物3具有结构式其中,n为-ch2基团数目,n为2-8的整数;此步骤中,化合物2与三氟乙酸反应,脱去boc(叔丁氧羰基)基团,脱boc基团的反应原理都为本技术人员均可通过技术手册得知或通过常规实验方法获知,本发明对反应的具体操作不作具体限定,本领域技术人员可以根据实际需要进行常规调整。s3.在酸性条件下,所述化合物3与甲醛进行反应,得到化合物4,所述化合物4具有结构式其中,n为-ch2基团数目,n为2-8的整数;此步骤中,化合物3和甲醛在酸性条件下进行羰胺缩合反应,形成碳氮双键。羰胺缩合反应的反应原理都为本技术人员均可通过技术手册得知或通过常规实验方法获知,本发明对反应的具体操作不作具体限定,本领域技术人员可以根据实际需要进行常规调整。s4.在亚硝酸钠和乙酸存在下,所述化合物4进行反应,得到化合物5,所述化合物5具有结构式其中,n为-ch2基团数目,n为2-8的整数;此步骤中,化合物4进行成环反应,反应原理都为本技术人员均可通过技术手册得知或通过常规实验方法获知,本发明对反应的具体操作不作具体限定,本领域技术人员可以根据实际需要进行常规调整。s5.所述化合物5进行水解反应,得到所述毒黄素半抗原。此步骤中,化合物5进行水解反应,反应原理都为本技术人员均可通过技术手册得知或通过常规实验方法获知,本发明对反应的具体操作不作具体限定,本领域技术人员可以根据实际需要进行常规调整。可以理解,步骤s1中化合物1的n值确定后,后续步骤中各化合物的n值也确定了。本发明根据毒黄素的结构特点,合理设计毒黄素半抗原的合成方法,以6-氯-3-甲基嘧啶与化合物1为起始原料,先后进行取代反应、脱boc、羰胺缩合反应、成环反应和水解反应,合成路线简单,使用的原料易得,反应操作较为简单,反应条件易于控制。本发明的毒黄素半抗原合成方法,毒黄素半抗原的纯度和收率高,整体的合成成本更具优势。第三方面,本发明提供毒黄素人工抗原,所述毒黄素人工抗原包括毒黄素免疫抗原和毒黄素包被抗原,其是由上述毒黄素半抗原与载体蛋白偶联得到的。所述载体蛋白为牛血清白蛋白(bsa),卵清蛋白(ova),人血清白蛋白(has)或血蓝蛋白(klh)中的任意一种,但不限于前面所列举的几种材料,也可以是其他未列举在本实施例中的但被本领域技术人员所熟知的其他材料。其中,制备毒黄素免疫抗原时,所述毒黄素半抗原结构中,3≤n≤8;制备毒黄素包被抗原时,所述毒黄素半抗原结构中,2≤n≤5。更优选地,制备毒黄素免疫抗原时,所述毒黄素半抗原结构中,n为5或6;制备毒黄素包被抗原时,所述毒黄素半抗原结构中,n为3。发明人发现,采用混合酸酐法合成毒黄素包被抗原,当毒黄素包被抗原中,n为3,而毒黄素免疫抗原中n为5或6时,所建立的免疫学方法具有更高的灵敏度,较之edc法合成毒黄素包被抗原和其它组合,检测下限提高了一个数量级,取得了预料不到的技术效果。第四方面,本发明提供毒黄素人工抗原的合成方法,其是采用混合酸酐法将所述毒黄素半抗原与载体蛋白偶联制备得到,步骤如下:称取5mg毒黄素半抗原,溶于1mldmf中,置于4℃下10min,加入8.5μl三乙胺,再加入6.3ul氯甲酸异丁酯,4℃搅拌反应30min,得甲液;取20mgova溶于1.8ml50%dmf中,预冷至4℃,置于冰浴不断搅拌,用1mnaoh调节ph至8.0,得毒黄素人工抗原。发明人发现,采用混合酸酐法合成毒黄素包被抗原,相较于edc法合成毒黄素包被抗原,所建立的免疫学方法具有更高的灵敏度。第五方面,本发明还提供一种毒黄素抗体,它是由上述毒黄素免疫抗原经动物免疫得到。第六方面,本发明提供一种检测毒黄素的免疫学方法,其采用上述毒黄素抗体和毒黄素包被抗原。所述免疫学方法为免疫层析法、酶联免疫吸附试验、时间分辨荧光免疫分析、化学发光免疫分析在内的任意一种免疫学分析方法。检测毒黄素的免疫学方法中,需要采用处理液对待测样品进行处理。发明人在实践中发现,处理液为甲醇和盐酸羟胺,其中,所述盐酸羟胺的浓度为0.2m-0.8m时,可以提高检测的灵敏性。下面结合实施例对本发明进行详细的说明,实施例仅是本发明的优选实施方式,不是对本发明的限定。实施例1:毒黄素半抗原的合成s1.6-氯-3-甲基嘧啶与化合物1进行反应,得到化合物2,所述化合物1的分子式为:bocnh-nh(ch2)ncoome,其中,n为-ch2基团数目,n为2-8的整数;所述化合物2具有结构式其中,n为-ch2基团数目,n为2-8的整数;所述化合物1的合成方法为:(1)提供中间体1,所述中间体1的分子式为:br(ch2)ncoome,其中,n为-ch2基团数目,n为2-8的整数;(2)所述中间体1与肼基甲酸叔丁酯进行反应,得到所述化合物1。s2.所述化合物2与三氟乙酸进行反应,得到化合物3,所述化合物3具有结构式其中,n为-ch2基团数目,n为2-8的整数;s3.在酸性条件下,所述化合物3与甲醛进行反应,得到化合物4,所述化合物4具有结构式其中,n为-ch2基团数目,n为2-8的整数;s4.在亚硝酸钠和乙酸存在下,所述化合物4进行反应,得到化合物5,所述化合物5具有结构式其中,n为-ch2基团数目,n为2-8的整数;s5.所述化合物5进行水解反应,得到所述毒黄素半抗原。实施例2:毒黄素免疫抗原的合成取载体蛋白(牛血清白蛋白,bsa)20mg溶于4ml磷酸盐缓冲液(ph7.4)中,加入5mg毒黄素半抗原,混匀,加入10mgedc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐),室温(25℃)反应2小时,透析除去未结合到载体蛋白上的小分子,收集透析后的蛋白质即为毒黄素免疫抗原。实施例3:毒黄素包被抗原的合成(混合酸酐法)称取5mg毒黄素半抗原,溶于1mldmf中,置于4℃下10min,加入8.5μl三乙胺,再加入6.3ul氯甲酸异丁酯,4℃搅拌反应30min,得甲液;取20mgova溶于1.8ml50%dmf中,预冷至4℃,置于冰浴不断搅拌,用1mnaoh调节ph至8.0,得毒黄素包被抗原。实施例4:毒黄素抗体将实施例2合成的毒黄素免疫抗原与等体积弗氏佐剂(首次用弗氏完全佐剂,第二、三、四次用弗氏不完全佐剂)混合、乳化,免疫balb/c鼠,采用elisa评价不同毒黄素免疫抗原的免疫效果,并制备毒黄素单克隆抗体。表1为n值不同的毒黄素免疫抗原免疫血清评价情况。其中,毒黄素单克隆抗体的制备流程为:(1)融合前3天,用50μg抗原经腹腔加强免疫一次;(2)融合前一天,制备饲养细胞,按照100μl/孔铺到96孔板中;(3)摘眼球取血,脱颈处死,于75%酒精中浸泡5min;(4)取出脾脏,于纱网上碾磨,显微镜下计数;(5)1200rpm,5min,弃掉上清;(6)按照1个骨髓瘤细胞对应5个脾细胞的比例加入骨髓瘤细胞,补加1640培养基至30ml,充分混匀;(7)1200rpm,10min,弃上清;(8)轻弹管底,充分重悬细胞;(9)于37℃下,1min内沿管壁加入50%peg14501ml;(10)缓慢加入25ml1640培养基;(11)900rpm,7min,弃上清;(12)120mlhat培养液重悬细胞,按照100μl/孔铺到准备好的饲养细胞板中;于37℃5%二氧化碳培养箱中培养;(13)第8天用ht培养基换液;(14)第10天elisa检测;(15)用完全培养基稀释elisa检测呈强阳性的孔中的细胞,使细胞浓度为5cells/ml;(16)将细胞悬液按照200μl/孔分装到96孔板中,置于37℃5%二氧化碳培养箱中培养;(17)待微孔中的细胞长到约100cells/孔时,进行elisa检测;(18)再次进行克隆筛选,直至所有有细胞的孔均呈阳性反应;(19)随后转入24孔细胞培养板进行培养,随后用细胞培养瓶进行培养;(20)按照100万个细胞/只小鼠的剂量腹腔注射balb/c小鼠;(21)收集腹水,纯化其中的抗体。表1为n值不同的毒黄素免疫抗原免疫血清评价情况实施例5:检测毒黄素的免疫学方法,1.纳米颗粒标记毒黄素抗体的制备:按照frens法(1973)制备40nm胶体金颗粒;按照每毫升胶体金颗粒加入3μl0.2m碳酸钾的量调节ph;按照每毫升胶体金颗粒加入3μg毒黄素单克隆抗体,室温反应15min;加入牛血清白蛋白(bsa),使其终浓度为1%,室温静置15min;10000rpm离心10min;弃掉上清,加入1/10胶体金体积的重悬液(10mmtris(ph8.0),0.5%tween20、0.4%酪蛋白、2%蔗糖)重悬颗粒;2.结合垫的制备:按照5μl/cm喷纳米颗粒标记毒黄素抗体于奥斯龙8964玻璃纤维素膜上,置于37℃烘干,裁成0.4cm宽,备用;3.层析膜的制备:按照1μl/cm喷涂浓度为1mg/ml的毒黄素包被抗原于硝酸纤维素膜(millipore135)上,作为检测线;按照1μl/cm喷涂浓度为0.2mg/ml的羊抗鼠igg作为质控线,置于室温晾干,备用;4.样品垫的制备:用[100mmtris(ph8.0),0.5%tween20]浸泡聚酯纤维素膜,置于37℃烘干,裁成1.2cm宽,备用;5.试纸条的组装:将样品垫、结合垫、层析膜、吸水垫依次搭接粘贴到pvc底板上,裁成3.5mm宽的试纸条,干燥保存,备用;6.试纸条的使用:(1)样品处理:取样品(木耳、病人呕吐物、发酵米面制品等)10g,加入20ml样品处理液,振摇1min;10000rpm离心1min,取上清检测;(2)检测样品:将试纸条样品垫一端插入待检上清中,注意结合垫应在页面上方,静置10min,判读结果。当检测线不显色时,结果为阳性;当检测线出线时,结果为阴性。表2为不同处理液处理样品时,试纸条的检测下限比对结果。从结果来看,联合应用甲醇和盐酸羟胺可以提高检测的灵敏性,其中盐酸羟胺的浓度在0.2m-0.8m之间时,检测下限最佳。而单独应用盐酸羟胺(0.4m),则不能改善检测的灵敏性。表2处理液对于检测检测下限的影响处理液配方检测下限(lod)120%甲醇25ng/ml220%甲醇,0.1m盐酸羟胺15ng/ml320%甲醇,0.2m盐酸羟胺5ng/ml420%甲醇,0.4m盐酸羟胺0.25ng/ml620%甲醇,0.6m盐酸羟胺1.25ng/ml720%甲醇,0.8m盐酸羟胺15ng/ml820%甲醇,1m盐酸羟胺15ng/ml90.4m盐酸羟胺30ng/ml注:lod是检测下限实施例6:采用混合酸酐法和edc法合成毒黄素包被抗原的影响采用实施例3中的混合酸酐法制备不同的毒黄素包被抗原,按照实施例5的方法建立检测毒黄素的免疫学方法,采用混合酸酐法制备的不同的毒黄素包被抗原的免疫学方法的检测下限参见表4。采用edc法制备不同的毒黄素包被抗原:取载体蛋白(卵清蛋白,ova)20mg溶于4ml磷酸盐缓冲液(ph7.4)中,加入5mg毒黄素半抗原,混匀,加入10mgedc(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐),室温(25℃)反应2小时,透析除去未结合到载体蛋白上的小分子,收集透析后的蛋白质即为毒黄素包被抗原;按照实施例5的方法建立检测毒黄素的免疫学方法,采用edc法制备的不同的毒黄素包被抗原的免疫学方法的检测下限参见表3。我们发现,采用混合酸酐法制备的包被抗原与某些抗体组合可以建立更为灵敏的免疫层析法,与表3结果相比,当包被抗原(n=3)、免疫抗原(n=5或6)时,所建立的方法具有很高的灵敏性,检测下限整整较edc法偶联抗原提高了一个数量级。表3包被抗原、抗体对于检测检测下限(lod)的影响(单位:ng/ml)表4混合酸酐法制备的包被抗原与不同抗体组合的免疫学方法检测下限(lod)(单位:ng/ml)实施例7:特异性评价采用实施例3中的混合酸酐法制备毒黄素包被抗原(n为3),采用实施例4的方法合成毒黄素抗体(n为5),按照实施例5的方法建立检测毒黄素的免疫学方法检测阴样本,评价该方法的特异性,一共检测了98份样本(其中病人呕吐物37份、木耳样品13份、发酵米面制品48份),没有假阳性结果出现,说明该方法具有良好的特异性。以上所述实施例仅表达了本发明的实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制,但凡采用等同替换或等效变换的形式所获得的技术方案,均应落在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1