一种大豆GmEF1B基因突变体植株及其制备方法及应用与流程
本发明属于植物生物技术领域,具体涉及一种大豆gmef1b基因突变体植株及其制备方法及应用。
背景技术:
大豆菌核病是由核盘菌(sclerotiniasclerotiorum(lib.)debary)引起的真菌性病害,是一种危害严重的世界性病害,直接影响大豆的品质及产量,病情严重时发病率高达50%~90%,甚至绝产。由于传统育种方法的局限性,利用分子手段筛选及鉴定有效的抗病基因,对抗病品种的选育便显得尤为重要,然而目前抗病品种培育的基因资源稀少,制约了新品种选育的效率以及准确性。
技术实现要素:
为了明确大豆抗核盘菌相关基因的抗病功能,加快大豆抗菌核病品种选育的进程,本发明提供了一种大豆gmef1b基因突变体植株,所述突变体植株含有突变的大豆gmef1b基因,所述突变是指gmef1b基因编码区中5’-gcttccccggcaatgctcaa-3’核苷酸序列发生碱基取代或缺失,使其编码的氨基酸序列发生改变;所述大豆gmef1b基因核苷酸序列如seqidno:1所示。
进一步地限定,所述突变的大豆gmef1b基因的核苷酸序列如seqidno:10所示。
本发明还提供了上述大豆gmef1b基因突变体植株的制备方法,包括如下步骤:
1)根据大豆gmef1b基因设计grna单靶点引物;
2)制备grna单靶点引物二聚体;
3)将引物二聚体插入到cas9/grna载体中,构建大豆gmef1b基因敲除载体;
4)将步骤3)构建的gmef1b基因敲除载体转化大豆,经筛选获得大豆gmef1b基因突变体植株。
进一步地限定,步骤1)所述大豆gmef1bgrna单靶点引物的正向引物为gmef1b-1-s,其核苷酸序列如seqidno:2所示,反向引物为gmef1b-1-a,其核苷酸序列seqidno:3所示。
进一步地限定,步骤2)所述制备grna单靶点引物二聚体,是指每20ul合成体系中正向引物5μl,正向引物5μl和h2o15μl,反应条件为95℃3min,冷却后静置。
进一步地限定,步骤3)所述构建gmef1b基因敲除载体,是指每10ul反应体系中,引物二聚体1-7μl,cas9/grnavector,1μl,solution11μl,solution21μl,h2o0-6μl,16℃反应5-10h。
进一步地限定,步骤4)所述大豆为大豆品种maplearrow;所述农杆菌为农杆菌eha105。
进一步地限定,步骤4)所述筛选所用正向引物为mutv-s,其核苷酸序列如seqidno:4所示,反向引物为mutv-a,其核苷酸序列如seqidno:5所示,用于筛选阳性突变体植株。
进一步地限定,步骤4)所述筛选所用正向引物为gmef1b-target1-s,其核苷酸序列如seqidno:6所示,反向引物序列为gmef1b-target1-a,其核苷酸序列如seqidno:7所示,上述两条引物作为单靶点突变检测引物,用于检测利用引物gmef1b-1-s和gmef1b-1-a构建获得的大豆gmef1b基因突变体植株。
本发明所述的大豆gmef1b基因突变体植株可用于gmef1b基因功能研究或抗大豆菌核病品种选育。
名词及缩写:卡那霉素:kan;链霉素:str;利福平:rif。
有益效果
本发明利用crispr/cas9技术对大豆gmef1b基因编码区进行靶向突变,获得了大豆突变体植株,通过与野生型表型鉴定及gmef1b基因表达量分析对比可看出,gmef1b基因突变后,其对大豆菌核病的抵抗力削弱,确定了gmef1b能够参与到抗大豆菌核病的抗性反应中,本发明为大豆抗菌核病相关基因功能的研究提供了理论依据。
附图说明
图1gmef1b基因敲除载体转化大肠杆菌后菌落pcr鉴定结果,m:dl2000marker;1-5:5个阳性菌落;
图2t1代gmef1b基因突变体植株的pcr检测结果,m:dl2000maker;1:阳性对照,2:阴性对照,3:空白对照组(水),4-6:t1代突变体植株的pcr产物;
图3t1代gmef1b基因突变体植株的pcr产物测序结果;
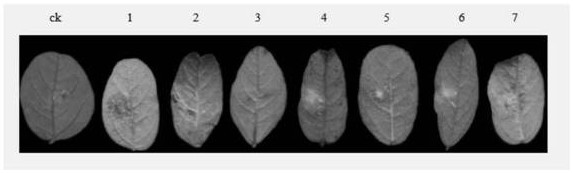
图4t1代gmef1b基因突变体及野生型植株叶片接种核盘菌后表现,ck:maplearrow叶片;1-7:突变体植株叶片。
具体实施方式
大豆品种maplearrow,记载在吕春梅,赵月,赵雪,etal.大豆品种maplearrow耐菌核病生化机制[j].中国油料作物学报,2014,36(5):630.,公众可通过东北农业大学获得。
核盘菌记载在吕春梅,赵月,赵雪,etal.大豆品种maplearrow耐菌核病生化机制[j].中国油料作物学报,2014,36(5):630.,公众可通过东北农业大学获得。
所使用的crispr/cas9试剂盒购买自北京唯尚立德生物科技有限公司,货号vk005-15。
所用的lb培养基的配制方法为:配制每升培养基,在950ml去离子水中加入:胰蛋白胨10g,酵母提取物5g,nacl10g,摇动容器直至溶质溶解。用5mol/lnaoh调ph至7.0,用去离子水定容至1l。在温度121℃、15psi高压下蒸汽灭菌21min。
yep液体培养基:配制每升培养基,在950ml去离子水中加入:胰蛋白胨10g,酵母提取物5g,nacl5g,摇动容器直至溶质溶解。用5mol/lnaoh调ph至7.0,用去离子水定容至1l。在温度121℃、15psi高压下蒸汽灭菌21min。
ms0培养基:称取4.43gms粉末,30g蔗糖,加600-800ml蒸馏水溶解,玻璃棒搅拌充分溶解后,调节ph值至5.8,定容至1l,加入6g琼脂粉末,在温度121℃、15psi高压下蒸汽灭菌21min。
其他涉及的试剂、仪器、设备等如无特殊说明,均为本领域常用的试剂、仪器或设备,均可通过商业化途径购买获得。
下述实施方式中所涉及的分子生物学实验如反转录、pcr扩增,胶回收等各实验步骤如无特殊说明,均参照相应的产品说明书或按照标准的分子克隆技术进行。
实施例1.大豆gmef1b基因突变体植株。
本实施例所述的大豆gmef1b基因突变体植株,所述突变体植株含有突变的大豆gmef1b基因,所述突变是指gmef1b基因编码区中5’-gcttccccggcaatgctcaa-3’核苷酸序列发生碱基取代或缺失,使其编码的氨基酸序列发生改变;所述大豆gmef1b基因核苷酸序列如seqidno:1所示。
实施例2.大豆gmef1b基因突变体植株的制备方法。
下面举例描述本发明所述的大豆gmef1b基因突变体植株的制备方法:
本实施例所述的突变体植株中,所述的突变的gmef1b基因是指在gmef1b基因编码区中5’-gcttccccggcaatgctcaa-3’核苷酸序列发生碱基取代或缺失,使其编码的氨基酸序列发生改变;即靶点核苷酸序列为:5’gcttccccggcaatgctcaa3’位于gmef1b编码区第203位至第222位碱基处。制备步骤如下:
1)根据大豆gmef1b基因设计grna单靶点引物。
首先扩增获得大豆gmef1b基因,以大豆品种maplearrow为材料,待长出第一组三出复叶时,取材,提取总rna并反转录合成cdna第一链。根据phytozome上gmef1b基因序列,利用primer5软件设计基因克隆引物,其核苷酸序列如下:
引物1-s:5’-atggccgttaccttctcaaat-3’(seqidno:8所示);
引物1-a:5’-ttagattttgttgaatgcaac-3’(seqidno:9所示)。
以cdna为模板进行rt-pcr反应,反应体系如下,反应程序:94℃5min;38个循环:94℃30s,60℃30s,72℃30s;72℃10min,4℃保存。反应后取pcr产物进行1%琼脂糖凝胶电泳检测并进行胶回收纯化目的片段。rt-pcr反应体系如下:
按照tiangen公司的pgm-t克隆试剂盒的步骤,将上述得到的胶回收产物与克隆载体进行连接,获得带有目的基因的克隆质粒pgm-t-gmef1b,转化top10大肠感受态细胞,挑取单克隆并进行pcr及测序验证。最终得到目的片段大小为675bp的gmef1b基因,如seqidno:1所示。
根据获得的gmef1b基因序列,设计grna单靶点引物。正向引物为gmef1b-1-s,5’-ttggcttccccggcaatgctcaa-3’(seqidno:2所示),反向引物为gmef1b-1-a,5’-aacttgagcattgccggggaagc-3’(seqidno:3所示),上述引物经引物合成公司合成获得。
2)制备grna单靶点引物二聚体。
将上述正、反向引物按如下比例混合形成二聚体:gmef1b-1-s/a(10μm)各5μl,h2o15μl混合后,进行如下处理:95℃3min;95℃到25℃缓慢冷却;16℃5min。
3)将引物二聚体插入到crispr/cas9试剂盒中cas9/grna载体中,构建gmef1b基因敲除载体。
反应体系如下(10μl体系):16℃过夜反应。
4)将步骤3)构建的gmef1b基因敲除载体转化农杆菌,侵染大豆,经鉴定获得大豆gmef1b基因突变体植株。
a转化:取上述产物10μl加入到刚解冻的50μltop10感受态中,轻弹混匀,冰浴30min,42℃热激90s,冰上静置2min,再加入500μl无抗lb培养基中,置于37℃恒温摇床中,170转,复苏1h后,涂kana抗性的固体平板,37℃过夜培养,挑取3-5个单斑摇菌,进行菌液pcr及测序,如图1所示。所述菌液pcr检测引物为:
mutv-s:5’-aaaagtcccacatcgcttag-3’(seqidno:4所示)
mutv-a:5’-tgtgcaaggtaagaagatgg-3’(seqidno:5所示),目的片段为435bp,将测序结果与载体序列进行比对,保存阳性菌液于-80℃备用。
b.根癌农杆菌介导法转化大豆茎尖。
将gmef1b基因敲除载体转入农杆菌eha105中,采用本实验保存的质粒,冻融法转化农杆菌的方法,该方法可参考:王涛.大豆mirna172及靶基因参与开花诱导和逆境响应的功能分析.博士学位论文.东北农业大学.2016中所述农杆菌转化方法。
通过农杆菌介导法将ggmef1b-cas9基因敲除载体转化耐病大豆品种maplearrow中,具体方法如下:
(1)菌液制备:取制备好的菌液分别在yep固体平板(50mg/mlstr,50mg/mlkan,25mg/mlrif,所述各抗生素浓度均为在培养基中的终浓度,下同)上划线28℃培养,挑取单菌落接种于yep液体培养基(50mg/mlstr,50mg/mlkan,25mg/mlrif)中,28℃200rpm震荡培养1-2天,取1-2ml菌液接种于50ml新鲜的yep液体培养基中震荡培养至od600为0.6-0.8。
(2)种子灭菌:选取饱满、无菌斑种子于培养皿中,采用氯气灭菌法,将种子放入通风厨的干燥器内,在干燥器的三角瓶中倒入96ml次氯酸钠,再快速加入6ml浓盐酸后迅速盖紧封盖。灭菌16h后置于超净工作台内吹走残留的氯气,大约30min左右,密封待用。
(3)种子萌发:将灭菌后的种子种脐向下种于ms0培养基中,每瓶种10粒,在23℃、16h光照/8h黑暗条件下萌发5-6天。
(4)茎尖外植体的制备:种子萌发至子叶即将冲破种皮时,用镊子和解剖刀去掉种皮,将两半子叶中的一半切掉,用解剖刀轻轻刮掉子叶和生长点之间的腋芽,并在子叶节处轻轻划3-5道伤口,剩余的部分作为外植体用于侵染。
(5)侵染与共培养:将制备好的外植体放入侵染液中进行抽真空处理,抽真空条件为0.6pa,10min。真空侵染后的外植体用灭菌蒸馏水清洗三次,用无菌纸将外植体表面的侵染液吸干,插入ms0培养基中共培养3天,观察复活情况,根据外植体返青的情况确定移栽时间,移栽至土壤中后,置于25℃,16h光照/8h黑暗条件下的培养箱中培养。
c.突变体植株鉴定:取经敲除gmef1b基因的大豆植株的t1代叶片以及对照(maplearrow)叶片,提取其dna,进行pcr鉴定,引物为:
mutv-s:5’-aaaagtcccacatcgcttag-3’(seqidno:4所示);
mutv-a:5’-tgtgcaaggtaagaagatgg-3’(seqidno:5所示),目的片段为435bp,鉴定出转gmef1b基因敲除载体的转基因植株。收取t1代中鉴定为转基因植株的大豆种子并种下,提取叶片dna,用单靶点突变检测引物进行pcr检测,正向引物为:gmef1b-target1-s:5'-ttttcccaatgctgccaagt-3'(seqidno:6);反向引物:gmef1b-target1-a:5'-gccctgtaaccataggtcacatc-3'(seqidno:7)。扩增出目的片段641bp(图2)并将产物进行测序,如图3所示,测序结果发现有1个阳性植株在靶点处发生了突变,较野生型发生1个碱基缺失,突变的gmef1b基因序列如seqidno:10所示。收取t1代中鉴定为转基因植株的大豆种子并种下,在第一轮三出复叶完全展开取叶片接种核盘菌,接种一天后观察发现(图4):maplearrow对照大豆叶片初期叶面产生暗绿色水渍状斑纹,后扩展为不规则状病斑,病斑处中心为深褐色,病斑四周颜色为浅褐色,处理后期叶片泛黄,病斑扩展终止;gmef1b突变体植株大豆叶片初期叶面产生较大的暗绿色水渍状斑纹,后期病斑扩展速度加快,最后几乎布满整个叶片。证明敲除gmef1b基因后的抗病品种maplearrow植株对大豆菌核病的抗性减弱,说明了gmef1b基因在所述的靶点区(核苷酸序列为5’-gcttccccggcaatgctcaa-3’)发生上述的碱基缺失,使得功能氨基酸发生了变化,从而导致抗病品种maplearrow对核盘菌的抗性被削弱。
核苷酸序列表
<110>东北农业大学
<120>一种大豆gmef1b基因突变体植株及其制备方法及应用
<130>
<160>10
<170>patentinversion3.5
<210>1
<211>675
<212>dna
<213>大豆gmef1b基因
<400>1
atggccgttaccttctcaaatctccacacagaatcaggtctcaagtccctcgacgacttc60
ctctctgggaaggtctacgtttctggggatcagttcacaaaggacgacatcaaagtgtat120
ggtgctgttttggagaagccaggtgactcttttcccaatgctgccaagtggtacgaggtt180
gtctcatctcagcttgctgcaagcttccccggcaatgctcaaggggtgagattcagtggc240
aaagcttctgctccagcggaggctgctcctgcgaaaccggatgcttctgctgctgaagat300
gatgatgaccttgatctctttggcgatgagactgaggaagacaaaaaggcagcagaggaa360
agggaggctgctaagaagtctaccaagaagaaagagagtggcaaatcttctgttctgctt420
gacgttaagccttgggatgatgaaacagacatgaagaagctggaagaggctgttcgcagt480
gttgagatgcctggtctattgtggggagcatccaaactggttcctgttggttatgggatc540
aagaagttgcagatcatgttaactattgtcgatgaccttgtatctgtggacacccttgtt600
gaggagactctcacagttgagcccatcaatgagtatgtccaaagctgtgacattgttgca660
ttcaacaaaatctaa675
<210>2
<211>23
<212>dna
<213>正向引物gmef1b-1-s
<400>2
ttgcgacgacttcctctctggga23
<210>3
<211>23
<212>dna
<213>反向引物gmef1b-1-a
<400>3
aactcccagagaggaagtcgtcg23
<210>4
<211>20
<212>dna
<213>正向引物mutv-s
<400>4
aaaagtcccacatcgcttag20
<210>5
<211>20
<212>dna
<213>反向引物mutv-a
<400>5
tgtgcaaggtaagaagatgg20
<210>6
<211>20
<212>dna
<213>正向引物gmef1b-target1-s
<400>6
ttttcccaatgctgccaagt20
<210>7
<211>23
<212>dna
<213>反向引物序列gmef1b-target1-a
<400>7
gccctgtaaccataggtcacatc23
<210>8
<211>21
<212>dna
<213>引物1-s
<400>8
atggccgttaccttctcaaat21
<210>9
<211>21
<212>dna
<213>引物1-a
<400>9
ttagattttgttgaatgcaac21
<210>10
<211>674
<212>dna
<213>突变的大豆gmef1b基因
<400>10
atggccgttaccttctcaaatctccacacagaatcaggtctcaagtccctcgacgacttc60
ctctctgggaggtctacgtttctggggatcagttcacaaaggacgacatcaaagtgtatg120
gtgctgttttggagaagccaggtgactcttttcccaatgctgccaagtggtacgaggttg180
tctcatctcagcttgctgcaagcttccccggcaatgctcaaggggtgagattcagtggca240
aagcttctgctccagcggaggctgctcctgcgaaaccggatgcttctgctgctgaagatg300
atgatgaccttgatctctttggcgatgagactgaggaagacaaaaaggcagcagaggaaa360
gggaggctgctaagaagtctaccaagaagaaagagagtggcaaatcttctgttctgcttg420
acgttaagccttgggatgatgaaacagacatgaagaagctggaagaggctgttcgcagtg480
ttgagatgcctggtctattgtggggagcatccaaactggttcctgttggttatgggatca540
agaagttgcagatcatgttaactattgtcgatgaccttgtatctgtggacacccttgttg600
aggagactctcacagttgagcccatcaatgagtatgtccaaagctgtgacattgttgcat660
tcaacaaaatctaa674
- 还没有人留言评论。精彩留言会获得点赞!