新颖化合物及包含其的有机发光器件的制作方法
本发明涉及新颖化合物及包含其的有机发光器件。
背景技术:
:在有机发光二极管中,用作有机物层的材料可根据功能大致分类为发光材料、空穴注入材料、空穴输送材料、电子输送材料、电子注入材料等。并且,上述发光材料可根据分子量分类为高分子和低分子,可根据发光机理分类为来源于电子的单态激发状态的荧光材料和来源于电子的三重态激发状态的磷光材料,发光材料可根据发光色分类为蓝色、绿色、红色发光材料和体现更好的天然色所需的黄色及橙色发光材料。并且,为了增加色纯度,并通过能量转移增加发光效率,可将主体/掺杂剂类用作发光物质。其原理为若将与主要构成发光层的主体相比,能带隙小且发光效率优秀的掺杂剂少量混合于辅助层中,则在主体中产生的激子向掺杂剂输送,从而发出效率高的光。此时,主体的波长向掺杂剂的波长带移动,因而可根据利用的掺杂剂和主体的种类得到所需的波长的光。至今,作为使用于这种有机发光器件的物质,众所周知的有多种化合物,但在利用至今众所周知的物质的有机发光器件的情况下,由于高的驱动电压、低的效率及短寿命,持续要求开发新的材料。因此,持续努力利用具有优秀的特性的物质来开发具有低电压驱动、高亮度及长寿命的有机发光器件。技术实现要素:技术问题本发明提供新颖有机化合物及包含其的有机发光器件。但是,本发明所要解决的问题不局限于以上描述的问题,本发明所属
技术领域:
的普通技术人员可根据以下的记载内容明确地理解未描述的其他问题。技术方案本发明的第一实施方式提供由以下化学式1表示的化合物:化学式1在上述化学式1中,x为o、s或crr`,y及z各自独立地为o或s,ar1为包含成环碳原子数为c6~c13的取代或未取代的芳基的取代或未取代的c6~c50的芳基、或者包含成环碳原子数为c6~c13的取代或未取代的芳基的取代或未取代的c6~c50的杂芳基,r、r`、r1至r6各自独立地为氢、重氢、卤素、硝基、腈基、取代或未取代的c1~c30的烷基、取代或未取代的c2~c30的烯基、取代或未取代的c1~c30的烷氧基、取代或未取代的c1~c30的硫醚基、取代或未取代的c6~c30的芳基、或者取代或未取代的c5~c30的杂芳基,相邻的r与r’能够形成环或者不形成环,l1至l3各自独立地为直接键合、取代或未取代的c6~c30的亚芳基、或者取代或未取代的c5~c30的杂亚芳基,l及q各自独立地为0或1至4的整数,m、n、o及p各自独立地为0或1至3的整数,上述l、m或n、o、p或q为2以上时,r1至r6能够各自相同或者不同。本发明的第二实施方式提供在第一电极与第二电极之间包括含有本发明的化合物的有机物层的有机发光器件。发明的效果根据本发明的一实例的化合物,将线性连接的2个三环稠环基(二苯并呋喃、二苯并噻吩或芴和二苯并呋喃或二苯并噻吩)连接在芳基胺的氮,形成适合于空穴输送层或发光辅助层的深的homo能级,可形成高的lumo,由此可实现高效率的有机发光器件。并且,根据本发明的一实例的化合物,在芳基胺的一侧导入线性连接的2个三环稠环基,并在另一侧导入二苯并呋喃或二苯并噻吩,具有快速的空穴迁移率(holemobility),在形成薄膜时可使分子的排列变得优秀。由此通过实现低电压及抑制滚降现象可实现长寿命的有机发光器件。并且,根据本发明的一实例的化合物,在芳基胺的另一侧导入电子耐性优秀的二苯并呋喃或二苯并噻吩,维持高的lumo的同时从发光层中阻断电子时可更加提高化合物的耐久性。由此可实现高效率及长寿命的有机发光器件。并且,根据本发明的一实例的化合物,在芳基胺的一侧导入成环碳原子数为6至13个的三重态能量高的取代基,可维持高的t1。由此通过使发光层内的激子束缚效果极大化,可实现高效率的有机发光器件。并且,根据本发明的一实例的化合物,包含3个以上的三环稠环基结构,形成高tg,可防止薄膜重结晶化,由此可确保有机发光器件的驱动稳定性。附图说明图1表示本发明一实例的有机发光器件的简图。具体实施方式以下,参照附图,详细说明本发明的实例及实施例,使得本发明所属
技术领域:
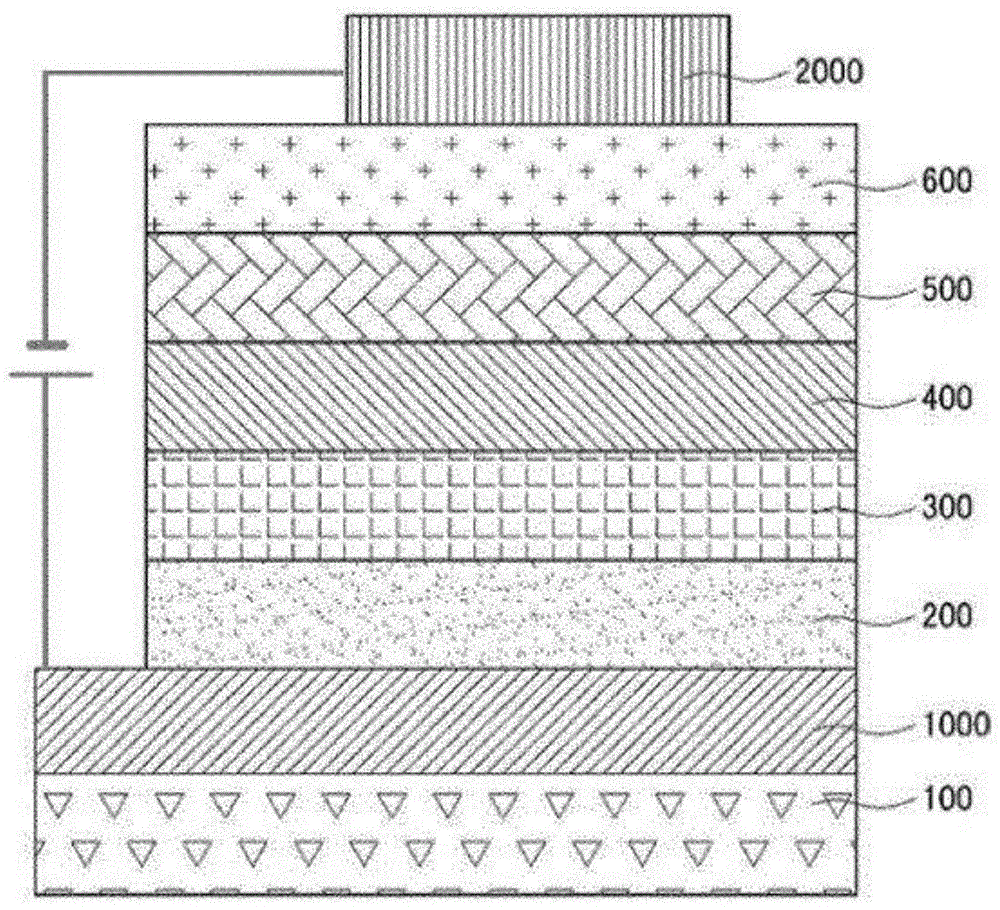
的普通技术人员可容易实施。但是,本发明能够以多种不同的形态实现,且不局限于在此说明的实例及实施例。并且,在图中,为了明确说明本发明,省略了与说明无关的部分,在说明书全文中,对于类似的部分,标注了类似的附图标记。在本发明说明书全文中,当一个部件位于另一部件“上”时,不仅包括一个部件与另一部件相接触的情况,还包括在两个部件之间存在其他部件的情况。在本发明说明书全文中,当一个部分“包括”一个结构要素时,除非有特别相反的记载,则意味着还可包括其他结构要素,而不是排除其他结构要素。在本发明说明书全文中使用的术语“约”、“实质上”等在所提及的含义上提示固有的制备及物质容差时以其数值或接近于其数值的含义使用,以防止昧良心的侵权人不当地利用为了帮助理解本发明而提及准确或绝对的数值的公开内容。在本发明说明书全文中使用的术语“~(的)步骤”或“~的步骤”不意味着“用于~的步骤”。在本发明说明书全文中,马库什(markush)形式的表现中所含的“它们的组合”这一术语意味着选自由马库什形式的表现中所记载的多个结构要素组成的组中的一种以上的混合或组合,意味着包括选自由上述多个结构要素组成的组中的一种以上。在本发明说明书全文中,“a和/或b”这一记载意味着“a或b,或者a及b”。在本发明说明书全文中,术语“芳基”意味着包含c5-30的芳香族烃环基,例如,苯基、苄基、萘基、联苯基、三联苯基、芴、菲基、三苯基烯基、苯基烯基、基、荧蒽基、苯并芴基、苯并三苯基烯基、苯并基、蒽基、均二苯乙烯基、芘基等芳香族环,“杂芳基”作为包含至少一个杂元素的c3-30的芳香族环,例如,意味着包含吡咯啉基、吡嗪基、吡啶基、吲哚基、异吲哚基、呋喃基、苯并呋喃基、异苯并呋喃基、二苯并呋喃基、苯并噻吩基、二苯并噻吩基、喹啉基、异喹啉基、喹喔啉基、咔唑基、菲基唳基、吖啶基、菲咯啉基、噻吩基及由吡啶环、吡嗪环、嘧啶环、哒嗪环、三嗪环、吲哚环、喹啉环、吖啶环、吡咯烷环、二烷环、哌啶环、吗啉环、哌嗪环、咔唑环、呋喃环、噻吩环、唑环、二唑环、苯并唑环、噻唑环、噻重氮环、苯并噻唑环、三唑环、咪唑环、苯并咪唑环、吡喃环、二苯并呋喃环、二苯并噻吩环形成的杂环基。在本发明说明书全文中,术语“取代或未取代”可意味着以选自由重氢、卤素、氨基、腈基、硝基或c1~c20的烷基、c2~c20的烯基、c1~c20的烷氧基、c3~c20的环烷基、c3~c20的杂环烷基、c6~c30的芳基及c3~c30的杂芳基组成的组中的一种以上的基团取代或未取代。并且,本发明说明书全文中,相同的附图标记只要没有特殊提及的内容就可以具有相同意思。在本发明的说明书全文中,术语“芴”可包含与第9位碳相结合的氢被取代或未取代的c1-20的烷基、取代或未取代的c5-30的芳基、或者取代或未取代的c3-30的杂芳基取代的情况。本发明的第一实施方式提供由以下化学式1表示的化合物。化学式1在上述化学式1中,x为o、s或crr`,y及z各自独立地为o或s,ar1为包含成环碳原子数为c6~c13的取代或未取代的芳基的取代或未取代的c6~c50的芳基、或者包含成环碳原子数为c6~c13的取代或未取代的芳基的取代或未取代的c6~c50的杂芳基,r、r`、r1至r6各自独立地为氢、重氢、卤素、硝基、腈基、取代或未取代的c1~c30的烷基、取代或未取代的c2~c30的烯基、取代或未取代的c1~c30的烷氧基、取代或未取代的c1~c30的硫醚基、取代或未取代的c6~c30的芳基、或者取代或未取代的c5~c30的杂芳基,相邻的r与r’能够形成环或者不形成环,l1至l3各自独立地为直接键合、取代或未取代的c6~c30的亚芳基、或者取代或未取代的c5~c30的杂亚芳基,l及q各自独立地为0或1至4的整数,m、n、o及p各自独立地为0或1至3的整数,上述l、m或n、o、p或q为2以上时,r1至r6能够各自相同或者不同。根据本发明的一实例的化合物,将线性连接的2个三环稠环基(二苯并呋喃、二苯并噻吩或芴和二苯并呋喃或二苯并噻吩)连接在芳基胺的氮,形成适合于空穴输送层或发光辅助层的深的homo能级,可形成高的lumo,由此可实现高效率的有机发光器件。根据本发明的一实例的化合物可形成深的homo能级,由此可更适合于发光辅助层。并且,根据本发明的一实例的化合物,在芳基胺的一侧导入线性连接的2个三环稠环基,并在另一侧导入二苯并呋喃或二苯并噻吩,具有快速的空穴迁移率(holemobility),在形成薄膜时可使分子的排列变得优秀。由此通过实现低电压及抑制滚降现象可实现长寿命的有机发光器件。并且,根据本发明的一实例的化合物,在芳基胺的另一侧导入电子耐性优秀的二苯并呋喃或二苯并噻吩,维持高的lumo的同时从发光层中阻断电子时可更加提高化合物的耐久性。由此可实现高效率及长寿命的有机发光器件。并且,根据本发明的一实例的化合物,在芳基胺的一侧导入成环碳原子数为6至13个的三重态能量高的取代基,可维持高的t1。由此通过使发光层内的激子束缚效果极大化,可实现高效率的有机发光器件。并且,根据本发明的一实例的化合物,包含3个以上的三环稠环基结构,形成高tg,可防止薄膜重结晶化,由此可确保有机发光器件的驱动稳定性。根据本发明的一实例,在上述化学式1中,ar1可以为包含成环碳原子数为c6~c13的取代或未取代的芳基的取代或未取代的c6~c50的芳基、或者包含成环碳原子数为c6~c13的取代或未取代的芳基的取代或未取代的c6~c50的杂芳基。ar1可包含成环碳原子数为c6~c13的芳基,上述芳基可以是取代或未取代的。包含这种芳基在内,ar1的整个碳原子数可以为c6~c50。在本发明的一实例中,上述化合物可由以下化学式2或化学式3表示。化学式2化学式3在上述化学式2及化学式3中,x、y、z、ar1、r、r`、r1至r6、l1、l2、l3、l、m、n、o、p及q如上述化学式1中所定义。由上述化学式2表示的化合物为上述化学式1中的l1为直接键合的情况,是芳基胺一侧的2个三环稠环(包含x的三环稠环和包含y的三环稠环)在无连接基的情况下直接键合的结构。这种情况下,使连接基最小化,由此可维持高的t1以及形成容易适用于发光辅助层的深的homo,可有效改善发光效率。由上述化学式3表示的化合物为上述化学式1中的l2为直接键合的情况,是包含y的三环稠环直接键合在氮的结构。这种情况下,使连接基最小化,通过维持高的t1以及与芳基胺的氮直接键合,具有快速的空穴迁移率,由此可有利于低电压驱动。在本发明的一实例中,上述化合物可由以下化学式4或化学式5表示。化学式4化学式5在上述化学式4及化学式5中,x、y、z、ar1、r、r`、r1至r6、l2、l3、l、m、n、o、p及q如上述化学式1中所定义。由上述化学式4或化学式5表示的化合物是将上述化学式1中包含y的三环稠环的第2位或第4位用作与l2的结合位置的结构。这种情况下,可形成深的homo的同时维持高的lumo,由此可改善发光效率,并可有效阻断电子从发光层流入到空穴输送层。并且,上述三环稠环化合物的连接位置编号可如下所示。在本发明的一实例中,上述化合物可由以下化学式6或化学式7表示。化学式6化学式7在上述化学式6及化学式7中,x、y、z、ar1、r、r`、r1至r6、l3、l、m、n、o、p及q如上述化学式1中所定义。由上述化学式6或化学式7表示的化合物为上述化学式1中的l1及l2为直接键合的情况,是包含y的三环稠环与氮直接键合且包含y的三环稠环的第2位或第4位用作结合位置的结构。这种情况下,可维持快速的空穴迁移率的同时维持高的lumo,由此可有效地实现低电压驱动以及阻断电子从发光层流入空穴输送层。根据本发明的一实例,在上述化学式1至化学式7中,上述r1至r6可各自独立地为氢、重氢或苯基。具体地,r1至r6均可以为氢。并且,根据本发明的一实例,在上述化学式1至化学式7中,上述x可以为o或s。并且,根据本发明的一实例,在上述化学式1至化学式7中,上述x、y及z均可以为o。并且,根据本发明的一实例,在上述化学式1至化学式7中,上述x及y均可以为s,包含y的三环稠环将第2位或第4位用作结合位置可连接在芳基胺的氮侧。并且,根据本发明的一实例,在上述化学式1至化学式7中,上述l1至l3可各自独立地选自由直接键合、亚苯基、亚联苯基及它们的组合组成的组中。并且,根据本发明的一实例,在上述化学式1至化学式7中,上述l1至l3中的至少一个可以为取代或未取代的c6~c30的亚芳基、或者取代或未取代的c5~c30的杂亚芳基,具体地,可选自由亚苯基、亚联苯基及它们的组合组成的组中。并且,根据本发明的一实例,在上述化学式1至化学式7中,上述ar1可选自由苯基、联苯基、三联苯基、芴、二烷基芴、二苯并呋喃、二苯并噻吩及它们的组合组成的组中。根据本发明的一实例,由上述化学式1表示的化合物可以为以下化合物中的一种,可不局限于此:本发明的第二实施方式提供包含由上述化学式1表示的化合物的有机发光器件。上述有机发光器件可在第一电极与第二电极之间包括含有本发明的化合物的一层以上的有机物层。在本发明的一实例中,上述有机物层可以为空穴注入层、空穴输送层及发光辅助层,但可不局限于此。并且,当形成有机层时,本发明的化合物可单独使用或与公知的化合物一同使用。对于本发明的一实例而言,上述有机发光器件可包含含有空穴输送物质的有机物层及包含由上述化学式1表示的化合物的有机物层,但不限于此。上述有机发光器件可在阳极(anode)与阴极(cathode)之间包括一层以上的空穴注入层(hil)、空穴输送层(htl)、发光层(eml)、电子输送层(etl)、电子注入层(eil)等有机物层。例如,上述有机发光器件可根据图1中所记载的结构来制备而成。有机发光器件可自下而上依次层叠阳极(空穴注入电极1000)/空穴注入层200/空穴输送层300/发光层400/电子输送层500/电子注入层600/阴极(电子注入电极2000)。在图1中,基板100可使用用于有机发光器件的基板,尤其,可以为机械强度、热稳定性、透明性、表面平滑性、处理容易性及防水性优秀的透明的玻璃基板或可弯曲的塑料基板。空穴注入电极1000用作用于注入有机发光器件的空穴的阳极。为了可注入空穴,利用具有低的功函数的物质,可由氧化铟锡(ito)、氧化铟锌(izo)、石墨烯(graphene)之类的透明的材质形成。通过真空沉积法、旋涂法、铸造法、lb(langmuir-blodgett)法等方法在上述阳极电极上部沉积空穴注入层物质,由此可形成空穴注入层200。在通过上述真空沉积法来形成空穴注入层的情况下,其沉积条件因用作空穴注入层200的材料的化合物、所需空穴注入层的结构及热特性等而不同,但通常可在50-500℃的沉积温度、10-8至10-3torr(托)的真空度、0.01至的沉积速度、至5μm的层厚度范围内适当地进行选择。接着,通过真空沉积法、旋涂法、铸造法、lb法等方法在上述空穴注入层200上部沉积空穴输送层物质,由此可形成空穴输送层300。在通过上述真空沉积法来形成空穴输送层的情况下,其沉积条件因使用的化合物而不同,但通常,优选地,在与空穴注入层的形成几乎相同的条件范围内进行选择。上述空穴输送层300可使用本发明的化合物,如上所述,可单独使用或者与公知的化合物一起使用本发明的化合物。并且,根据本发明的一实例,空穴输送层300可以为一层以上,可一同包含仅由公知的物质形成的空穴输送层。并且,根据本发明的一实例,在上述空穴输送层300上可形成发光辅助层。通过真空沉积法、旋涂法、铸造法、lb法等方法,在上述空穴输送层300或发光辅助层上部沉积发光层物质,由此可形成发光层400。在通过上述真空沉积法来形成发光层的情况下,其沉积条件因使用的化合物而不同,但通常,优选地,在与空穴注入层的形成几乎相同的条件范围内进行选择。并且,上述发光层材料可将公知的化合物用作主体或掺杂剂。并且,在发光层中,与磷光掺杂剂一同使用的情况下,为了防止三重态激子或空穴向电子输送层扩散的现象,通过真空沉积法或旋涂法还可层叠空穴抑制材料(hbl)。此时可使用的空穴抑制物质不受特别的限制,但可从用作空穴抑制材料的公知的物质中选择任意物质来利用。例如,可例举二唑衍生物或三唑衍生物、菲咯啉衍生物或日本特开平11-329734(a1)中所记载的空穴抑制材料等,代表性地,可使用balq(双(8-羟基-2-甲基喹啉)-铝联苯酚盐)、菲咯啉(phenanthrolines)类化合物(如通用显示器(udc)公司的bcp(bathocuproine,浴铜灵)等。在如上形成的发光层400上部形成有电子输送层500,此时,上述电子输送层可通过真空沉积法、旋涂法、铸造法等方法来形成。并且,上述电子输送层的沉积条件因使用的化合物而不同,但通常,优选地,在与空穴注入层的形成几乎相同的条件范围内进行选择。之后,可在上述电子输送层500上部沉积电子注入层物质来形成电子注入层600,此时,上述电子输送层可通过真空沉积法、旋涂法、铸造法等方法来形成常规的电子注入层物质。上述有机发光器件的空穴注入层200、空穴输送层300、发光层400、电子输送层500可使用本发明的化合物或如下的物质,或者,可一同使用本发明的化合物和公知的物质。通过真空沉积法或溅射法等方法来在电子注入层600上形成用于注入电子的阴极2000。作为阴极,可使用多种金属。具体例有铝、金、银等物质。本发明的有机发光器件不仅可以采用阳极、空穴注入层、空穴输送层、发光层、电子输送层、电子注入层、阴极结构的有机发光器件,还可采用多种结构的有机发光器件的结构,根据需要,还可形成一层或两层的中间层。如上所述,根据本发明形成的各个有机物层的厚度可根据所需的程度来进行调节,具体为1至1000nm,更具体为5至200nm。并且,在本发明中,包含由上述化学式1表示的化合物的有机物层可将有机物层的厚度调节为分子单位,因而具有表面均匀且形态稳定性突出的优点。针对本实施方式的有机化合物,均可适用对于本发明的第一实施方式记载的内容,但可不局限于此。以下,通过本发明的实施例进行更具体的说明,本发明的范围不局限于本实施例。[实施例]由化学式1表示的化合物的合成由化学式1表示的化合物可通过如下反应进行合成,而不局限于此。中间体im的合成为了合成目标化合物,中间体im可通过如下反应进行合成,而不局限于此。中间体im1的合成中间体im1以如下的方法进行合成。在圆底烧瓶中,将20.0g的二苯并[b,d]呋喃-4-基硼酸(dibenzo[b,d]furan-4-ylboronicacid)、33.8g的2,8-二溴二苯并[b,d]呋喃(2,8-dibromodibenzo[b,d]furan)溶解于800ml的1,4-二烷(1,4-dioxan)之后,放入140ml的k2co3(2m)和3.3g的pd(pph3)4之后进行回流搅拌。利用薄层色谱法(tlc)来确认反应,添加水之后,结束反应。利用二氯甲烷(mc)来提取有机层,并进行减压过滤之后进行重结晶,从而得到中间体26.1g的im1(收率67%)。中间体im2至im3的合成如下列表1,改变起始物质来以与上述im1相同的方法合成im2至im3。[表1]中间体im4的合成中间体im4通过如下方法进行合成。在圆底烧瓶中,将20.0g的二苯并[b,d]呋喃-4-基硼酸(dibenzo[b,d]furan-4-ylboronicacid)、33.8g的4,6-二溴二苯并[b,d]呋喃(4,6-dibromodibenzo[b,d]furan)溶解于800ml的1,4-二烷(1,4-dioxan)之后,放入140ml的k2co3(2m)和3.3g的pd(pph3)4之后进行回流搅拌。利用薄层色谱法(tlc)来确认反应,添加水之后,结束反应。利用二氯甲烷(mc)来提取有机层,并进行减压过滤之后进行重结晶,从而得到25.3g的中间体im4-1(收率65%)。在圆底烧瓶中,将25.0g的上述im4-1、20g的双(频哪醇合)二硼(bis(pinacolato)diboron)溶解于450ml的1,4-二烷(1,4-dioxan)之后,放入17.0g的koac和0.2g的pd(dppf)cl2之后进行回流搅拌。利用薄层色谱法(tlc)来确认反应,添加水之后,结束反应。利用二氯甲烷(mc)来提取有机层,并进行减压过滤之后进行重结晶,从而得到22.3g的中间体im4-2(收率80%)。在圆底烧瓶中,将22.0g的上述im4-2、14.9g的1-溴-4-碘苯(1-bromo-4-iodobenzene)溶解于550ml的1,4-二烷(1,4-dioxan)之后,放入70ml的k2co3(2m)和1.7g的pd(pph3)4之后进行回流搅拌。利用薄层色谱法(tlc)来确认反应,添加水之后,结束反应。利用二氯甲烷(mc)来提取有机层,并进行减压过滤之后进行重结晶,从而得到14.0g的中间体im4(收率60%)。中间体im5至im13的合成如下列表2,改变起始物质来以与上述im4相同的方法合成im5至im13。[表2]中间体op的合成中间体op1通过如下方法进行合成。在圆底烧瓶中,将30.0g的上述2-溴二苯并[b,d]呋喃(2-bromodibenzo[b,d]furan)、7.8g的[1,1'-联苯]-4-胺([1,1'-biphenyl]-4-amine)、10.9g的t-buona、2.8g的pd2(dba)3、3.4ml的(t-bu)3p溶解于570ml的甲苯之后,进行回流搅拌。利用薄层色谱法来确认反应,添加水之后,结束反应。利用二氯甲烷来提取有机层,并进行减压过滤之后进行重结晶,从而得到21g的op1(收率68%)。中间体op2至op5的合成如下列表3所示,使用不同的起始物质,通过与上述op1相同的方法合成以下op2至op5。[表3]化合物的合成使用上述中间体im1至im13及op1至op5,合成目标化合物1至15。化合物1的合成在圆底烧瓶中,将3.0g的im1、2.7g的op1、1.1g的t-buona、0.3g的pd2(dba)3、0.3ml的(t-bu)3p溶解于100ml的甲苯之后,进行回流搅拌。利用薄层色谱法来确认反应,添加水之后,结束反应。利用二氯甲烷来提取有机层,并进行减压过滤之后进行柱纯化及重结晶,从而得到3.0g的化合物1(收率67%)。m/z:667.21(100.0%)、668.22(52.4%)、669.22(14.2%)、670.22(2.6%)化合物2的合成利用im2及op2来代替im1及op1,以与化合物1相同的方法,合成化合物2(收率63%)。m/z:699.17(100.0%)、700.17(53.9%)、701.18(13.4%)、701.16(9.0%)、702.17(4.8%)、702.18(2.6%)、703.17(1.3%)、701.17(1.2%)化合物3的合成利用im3及op2来代替im1及op1,以与化合物1相同的方法,合成化合物3(收率60%)。m/z:715.15(100.0%)、716.15(54.7%)、717.15(14.6%)、717.14(13.6%)、718.15(7.5%)、718.16(2.2%)、719.15(1.8%)化合物4的合成利用op3来代替op1,以与化合物1相同的方法,合成化合物4(收率65%)。m/z:667.21(100.0%)、668.22(52.4%)、669.22(14.2%)、670.22(2.6%)化合物5的合成利用im4及op4来代替im1及op1,以与化合物1相同的方法,合成化合物5(收率71%)。m/z:819.28(100.0%)、820.28(65.4%)、821.28(21.6%)、822.29(4.4%)化合物6的合成利用im4及op5来代替im1及op1,以与化合物1相同的方法,合成化合物6(收率67%)。m/z:819.28(100.0%)、820.28(65.4%)、821.28(21.6%)、822.29(4.4%)化合物7的合成利用im5及op4来代替im1及op1,以与化合物1相同的方法,合成化合物7(收率65%)。m/z:819.28(100.0%)、820.28(65.4%)、821.28(21.6%)、822.29(4.4%)化合物8的合成利用im6及op4来代替im1及op1,以与化合物1相同的方法,合成化合物8(收率67%)。m/z:819.28(100.0%)、820.28(65.4%)、821.28(21.6%)、822.29(4.4%)化合物9的合成利用im7及op4来代替im1及op1,以与化合物1相同的方法,合成化合物9(收率63%)。m/z:819.28(100.0%)、820.28(65.4%)、821.28(21.6%)、822.29(4.4%)化合物10的合成利用im8及op4来代替im1及op1,以与化合物1相同的方法,合成化合物10(收率66%)。m/z:835.25(100.0%)、836.26(65.4%)、837.26(22.0%)、838.26(4.9%)、837.25(4.8%)、838.25(3.0%)、836.25(1.2%)、839.26(1.0%)化合物11的合成利用im9及op4来代替im1及op1,以与化合物1相同的方法,合成化合物11(收率65%)。m/z:835.25(100.0%)、836.26(65.4%)、837.26(22.0%)、838.26(4.9%)、837.25(4.8%)、838.25(3.0%)、836.25(1.2%)、839.26(1.0%)化合物12的合成利用im10及op4来代替im1及op1,以与化合物1相同的方法,合成化合物12(收率60%)。m/z:835.25(100.0%)、836.26(65.4%)、837.26(22.0%)、838.26(4.9%)、837.25(4.8%)、838.25(3.0%)、836.25(1.2%)、839.26(1.0%)化合物13的合成利用im11及op4来代替im1及op1,以与化合物1相同的方法,合成化合物13(收率62%)。m/z:851.23(100.0%)、852.24(65.4%)、853.24(21.2%)、853.23(10.3%)、854.23(6.0%)、854.24(5.0%)、855.23(2.0%)、852.23(2.0%)化合物14的合成利用im12及op4来代替im1及op1,以与化合物1相同的方法,合成化合物14(收率60%)。m/z:835.25(100.0%)、836.26(65.4%)、837.26(22.0%)、838.26(4.9%)、837.25(4.8%)、838.25(3.0%)、836.25(1.2%)、839.26(1.0%)化合物15的合成利用im13及op4来代替im1及op1,以与化合物1相同的方法,合成化合物15(收率65%)。m/z:845.33(100.0%)、846.33(68.6%)、847.34(23.2%)、848.34(5.4%)有机发光器件的制备实施例1通过蒸馏水超声波对以的厚度将氧化铟锡(ito)涂敷成薄膜的玻璃基板进行了洗涤。若蒸馏水洗涤结束,则利用异丙醇、丙酮、甲醇等溶剂来进行超声波洗涤,并进行干燥之后,移送至等离子清洗机,然后利用氧等离子来将上述基板清洗5分钟之后,在氧化铟锡基板上部利用热真空沉积器(thermalevaporator),作为空穴注入层将的hi01进行制膜,将的hatcn进行制膜,作为空穴输送层将的ht01进行制膜,作为发光辅助层将的化合物1进行制膜之后,作为上述发光层掺杂3%的bh01:bd01,以进行制膜。接着,作为电子输送层将的et01:liq(1:1)进行制膜之后,将的lif、的铝(al)进行制膜,并将该器件在手套箱中进行密封(encapsulation),从而制备了有机发光器件。实施例2至实施例15以与实施例1相同的方法制备通过使用化合物2至15来代替化合物1而制膜的有机发光器件。比较例1至比较例7以与实施例1相同的方法制备通过使用ref.1至ref.7来代替化合物1而制膜的有机发光器件。有机发光器件的性能评价利用吉时利2400源测量单元(kiethley2400sourcemeasurementunit)施加电压来注入电子及空穴,利用柯尼卡美能达(konicaminolta)分光辐射计(cs-2000)来测定发光时的亮度,由此在大气压条件下,测定对于施加电压的电流密度及亮度,从而评价实施例及比较例的有机发光器件的性能,并将其结果示于下列表4中。[表4]op.vma/cm2cd/aqe(%)ciexcieylt95实施例13.7107.66.60.1400.109150实施例23.7107.76.60.1390.110153实施例33.7107.76.60.1400.110150实施例43.7107.76.70.1400.110155实施例53.8108.17.20.1420.109190实施例63.8108.27.20.1400.109185实施例73.8108.07.10.1410.109187实施例83.8108.17.00.1400.110182实施例93.8108.17.00.1410.110180实施例103.8108.07.10.1400.109176实施例113.8108.07.00.1390.109176实施例123.9108.37.40.1400.110172实施例133.9108.47.40.1410.110170实施例143.9108.37.30.1400.111170实施例153.8107.97.00.1400.110165比较例14.2107.16.10.1400.110105比较例24.1107.06.00.1410.110113比较例34.2107.36.30.1400.110125比较例44.2107.26.30.1420.110120比较例54.4106.75.90.1400.111110比较例64.6106.65.90.1410.112100比较例74.7107.06.10.1400.11292如上述表4所示可确认,作为空穴输送层使用本发明的化合物的实施例1至15相比于比较例1至比较例7,效率及寿命上升。更具体地,相比于比较例1,实施例1至15在芳基胺的一侧可具有连接2个三环稠环的取代基的快速的空穴迁移率(holemobility),因此更加有利于低电压驱动。并且,相比于比较例2、3,实施例1至15在芳基胺的一侧具有连接2个三环稠环的取代基,在另一侧还包含三环稠环,在形成薄膜时,分子排列优秀,空穴迁移率得到改善,由此抑制滚降现象并改善了寿命。并且,相比于比较例4、5,实施例1至15的芳基胺的氮除了2个三环稠环以外结合在另外二苯并呋喃或二苯并噻吩,维持深的homo并形成高的lumo,由此可实现优秀的效率及长寿命的特性。并且,相比于比较例6、7,实施例1至15的芳基胺为ar1具有三重态能量高的碳原子数为13个以下的芳基,维持高的t1,可使发光层内激子束缚效果极大化,并具有低的驱动电压,由此可实现效率及寿命大大改善的有机发光器件。上述本发明的说明是用于例示性的,本发明所属
技术领域:
的普通技术人员可以理解在不变更本发明的技术思想或必要特征的情况下,能够以其他具体形态容易变形。因此,应理解以上描述的多个实施例在所有方面是例示性的,而不是限定性的。例如,以单一方式说明的各个结构要素可分散地实施,同样,说明为分散的多个结构要素也能够以结合的形态实施。本发明的范围由所附的权利要求书表示,而不是上述详细说明,权利要求书的含义及范围以及由其等同概念导出的所有变更或变形的形态应当被解释为包括在本发明的范围中。附图标记的说明100:基板200:空穴注入层300:空穴输送层400:发光层500:电子输送层600:电子注入层1000:阳极2000:阴极。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1