一种甲基胺的制备方法与流程
本发明涉及制备甲基胺的技术领域,具体涉及一种甲基胺的制备方法。
背景技术:
甲基胺是重一种要的中间体,广泛应用于染料、天然产物和精细化学品的制备等。传统上,甲基胺通常以甲醛、碘化甲酯或硫酸二甲酯为甲基化剂,由胺制备而成。然而,与甲基化剂相关的毒性和有限的底物范围是这些现有方法的重大缺点。在这方面,从可持续化学的角度来看,一种使用co2作为c1组成单元的合成方法成为了胺中甲基胺的替代品,并且很有前景。二氧化碳是一种丰富的可再生的c1合成子,广泛用于合成有附加值的化学物质。二氧化碳转化领域已经付出了很多努力,得到了一系列有价值的化学物质,例如碳酸盐,醇,尿素衍生物,羧基酸,n-取代化合物等。
在已开发的方法中,金属基催化剂包括zn、ru、cu、ni、cs已被广泛使用。以h2为还原剂,在金属基催化剂的催化下,co2与胺反应得到酰胺和甲基胺。然而,反应中通常需要高温(>100℃)和/或高压(>5mpa)。将co2与胺温和地转化成n取代化合物,在学术界和工业界都具有很高的吸引力。另外,近年来,有机催化体系如原氮磷膦超碱基、n-杂环卡宾、b(c6f5)3以及四丁基氟化铵等也被开发为绿色替代品,但是这些有机催化剂不稳定,往往需要无水无氧的反应条件。因此,尽管在这一领域取得了进展,但在温和的反应条件下使用简单、易于处理和廉价的催化剂仍是人们所需要的,但尚未得到满足。
技术实现要素:
针对现有技术存在的技术问题,本发明提供一种甲基胺的制备方法,以克服现有技术中催化co2制备甲基胺反应的金属催化剂存在价格昂贵、毒性高,有机催化剂不稳定,反应条件苛刻,导致甲基胺的生产环节复杂以及制造成本高的缺陷。
本发明提供的一种甲基胺的制备方法,所述制备方法为利用胺甲基化反应制备甲基胺;所述胺甲基化反应中,催化剂为十二烷基二甲基胺己内酯。
优选地,所述制备方法包括下述具体步骤:在十二烷基二甲基胺己内酯的催化下,芳香胺与co2发生胺甲基化反应生成甲基胺。
优选地,所述制备方法包括下述具体步骤:在十二烷基二甲基胺己内酯(catalyst)的催化下,式(i)所示的芳香胺与co2以及还原剂聚甲基聚硅氧烷(pmhs)发生胺甲基化反应,生成式(ii)所示的甲基胺;所述胺甲基化反应的反应路线如下:
其中,r1选自h、未取代的或取代的c1-c6的烷基、未取代的或取代的c6-c30的芳基、或者
优选地,所述r1选自h、甲基、乙基、异丙基、正丁基、苯甲基、苯基、
优选地,所述胺甲基化反应的反应温度为50-100℃,反应时间为6-18h。
优选地,所述芳香胺与所述聚甲基聚硅氧烷的摩尔比为1:1-4。
优选地,所述十二烷基二甲基胺己内酯的加入量是所述芳香胺摩尔质量的10-50%。
优选地,所述胺甲基化反应中,反应溶剂选自乙腈、二甲基亚砜、二甲基甲酰胺、n,n-二乙基甲酰胺、二乙二醇二甲醚和1,4-二氧六环中的至少一种。
优选地,所述制备方法还包括以下步骤:将反应完成后得到的混合溶液冷却至室温,淬灭反应,收集有机相液体,将所述有机相液体纯化后,得到甲基胺。
优选地,使用ch2cl2萃取所述混合溶液;使用硅胶柱层析纯化所述有机相液体。
与现有技术相比,本发明具有以下有益效果:
1、本发明中将十二烷基二甲基胺己内酯作为胺甲基化反应的催化剂,为合成甲基胺提供了一种新型的反应催化剂。以十二烷基二甲基胺己内酯作为催化剂催化芳香胺与co2反应,不需要使用金属配体,有效减少了反应所需添加物,有利于简化反应结束的后处理过程。
十二烷基二甲基胺己内酯属于非金属化合物,因此制备十二烷基二甲基胺己内酯催化剂的原料来源丰富、且价格低廉,能够有效降低合成甲基胺化合物的合成成本。此外,以十二烷基二甲基胺己内酯代替传统毒性高的过渡金属作为催化剂,使甲基化反应的环境友好性显著提高、减轻对环境和人体的危害,适于在制药等对安全性要求高的领域应用、推广,并且能够避免在光电领域由于过渡金属离子残留造成的器件性能降低。此外,十二烷基二甲基胺己内酯中的氧原子带有负电荷,具有强路易斯碱性,其亲硅性强,作为催化剂具有高的催化活性,能够显著提高制备甲基胺的产率。
2、本发明是在十二烷基二甲基胺己内酯的催化下,芳香胺中n-h键发生甲基化反应。在利用十二烷基二甲基胺己内酯作为催化剂时,甲基化反应唯一地发生在芳香胺中n-h键,使芳香胺中n-h键官能化形成c-n键。此外,在以十二烷基二甲基胺己内酯作为催化剂时,对原料物质芳香胺中高活性的分子键(例如,c-cl键)具有高的兼容性,在催化芳香胺中n-h键甲基化的过程中,能够避免破坏芳香胺中高活性的分子键,有利于通过高活性的分子键进一步进行后续的合成反应。
3、本发明由式(i)所示的芳香胺与co2,在十二烷基二甲基胺己内酯的催化下,生成式(ii)所示的甲基化芳香胺。由于催化剂具有高的选择性,唯一性地催化芳香胺中n-h键甲基化,并能保留原料分子中高活性的分子键,因此,以十二烷基二甲基胺己内酯作为催化剂,允许多取代基选择的不同结构的芳香胺进行反应,得到具有多结构类型选择的甲基化芳香胺,扩大了合成的甲基化芳香胺的范围。
4、本发明中甲基化的碳源为co2,实现了co2的增值利用,有利于解决人类每年排放大量co2,造成的温室效应等环境问题。
5、本发明中,所述胺甲基化反应的反应温度为50-100℃,反应时间为6-18h。以十二烷基二甲基胺己内酯作为甲基化反应的催化剂,反应条件温和,反应步骤简单、易于实现,有利于大规模的工业生产。
通过进一步调节芳香胺与pmhs的质量比,以及十二烷基二甲基胺己内酯的加入量,使其处于适宜的范围内,能够进一步提高十二烷基二甲基胺己内酯催化的甲基化反应的催化效率,使得到的甲基化芳香胺的产率达到85%以上。
6、本发明具有多种可选择的反应溶剂,在所述胺甲基化反应的反应溶剂选自乙腈、二甲基亚砜、二甲基甲酰胺、n,n-二乙基甲酰胺、二乙二醇二甲醚和1,4-二氧六环等有机溶剂内均可实现十二烷基二甲基胺己内酯高选择性和高催化活性,得到唯一位置的n-h键甲基化的芳香胺。
7、本发明将反应完成后得到的混合溶液稀释,浓缩有机相液体,然后进行纯化处理,进一步提高反应制备的甲基化芳香胺的纯度。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
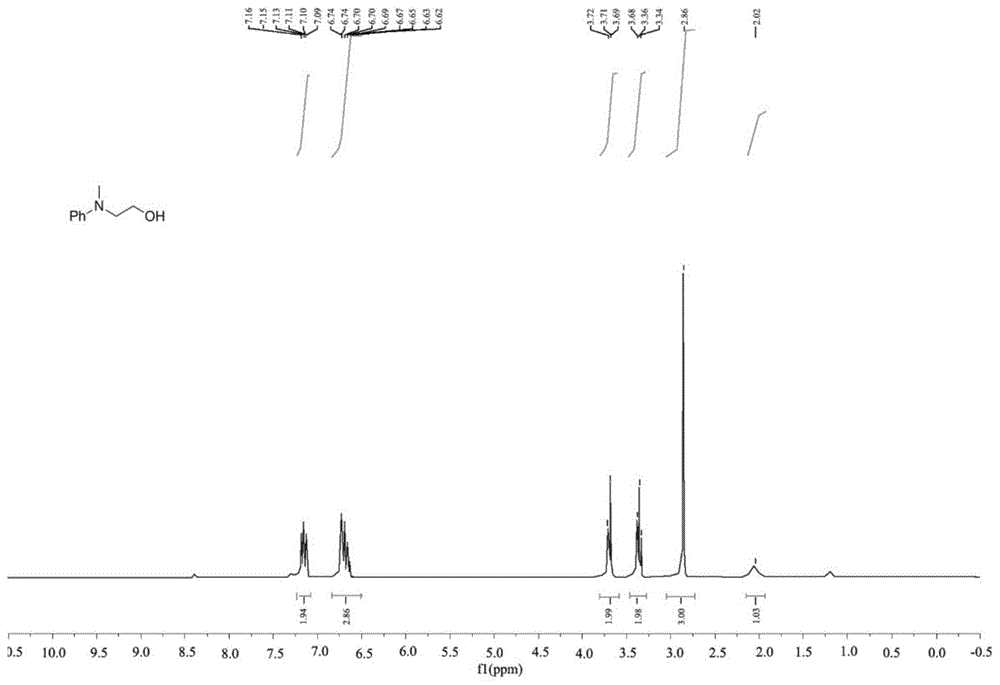
图1是本发明实施例1中制备的2-(甲基(苯基)氨基)乙醇的氢核磁谱图。
图2是本发明实施例1中制备的2-(甲基(苯基)氨基)乙醇的碳核磁谱图。
图3是本发明实施例2中制备的n-苄基-n-甲基苯胺的氢核磁谱图。
图4是本发明实施例2中制备的n-苄基-n-甲基苯胺的碳核磁谱图。
图5是本发明实施例3中制备的n,n-二甲基-[1,1′-二苯基]-2-胺的氢核磁谱图。
图6是本发明实施例3中制备的n,n-二甲基-[1,1′-二苯基]-2-胺的碳核磁谱图。
图7是本发明实施例4中制备的1-甲基吲哚啉的氢核磁谱图。
图8是本发明实施例4中制备的1-甲基吲哚啉的碳核磁谱图。
图9是本发明实施例5中制备的4-甲氧基-n,n-二甲基苯胺的氢核磁谱图。
图10是本发明实施例5中制备的4-甲氧基-n,n-二甲基苯胺的碳核磁谱图。
具体实施方式
提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。
实施例1
本实施例提供一种甲基胺的制备方法,其中,所用催化剂为十二烷基二甲基胺己内酯,甲基胺为2-(甲基(苯基)氨基)乙醇,制备甲基胺的反应路线如下所示:
2-(甲基(苯基)氨基)乙醇的制备方法包括以下步骤:
取一只严格干燥的史莱克反应管(schlenk管),将一个装满二氧化碳的气球通过侧管连接到schlenk管,并清洗3次,依次加入十二烷基二甲基胺己内酯(5mol%相对于胺)、2-(苯基氨基)乙醇(0.25mmol)、聚甲基聚硅氧烷pmhs(1mmol)和ch3cn(2ml),schlenk管在70℃加热12h,冷却到室温,释放气球中的co2,在混合液中加入etoac(10ml),淬灭还原性反应,用ch2cl2萃取三次,浓缩的有机层在无水na2so4上干燥,在真空下蒸发,用石油醚/乙酸乙酯进行硅胶色谱柱纯化,得到相应的产物。
其中,反应的产率为85.5%,利用核磁共振对产物进行分析,确定其为2-(甲基(苯基)氨基)乙醇,2-(甲基(苯基)氨基)乙醇的氢核磁谱图如图1所示,碳核磁谱图如图2所示;核磁数据如下所示:
1hnmr(300mhz,chloroform-d)δ7.15(td,j=7.2,2.2hz,2h),6.83-6.51(m,3h),3.68(t,j=5.7hz,2h),3.35(t,j=5.7hz,2h),2.85(s,3h),2.04(br,1h);13cnmr(75mhz,cdcl3)δ149.9,129.1,117.0,112.9,59.9,55.3,38.6。
实施例2
本实施例提供一种甲基胺的制备方法,其中,所用催化剂为十二烷基二甲基胺己内酯,甲基胺为n-苄基-n-甲基苯胺,制备甲基胺的反应路线如下所示:
n-苄基-n-甲基苯胺的制备方法包括以下步骤:
取一只严格干燥的史莱克反应管(schlenk管),将一个装满二氧化碳的气球通过侧管连接到schlenk管,并清洗3次,依次加入十二烷基二甲基胺己内酯(5mol%相对于胺)、n-苄基苯胺(0.25mmol)、聚甲基聚硅氧烷pmhs(1mmol)和ch3cn(2ml),schlenk管在50℃加热10h,冷却到室温,释放气球中的co2,在混合液中加入etoac(10ml),淬灭还原性反应,用ch2cl2萃取三次,浓缩的有机层在无水na2so4上干燥,在真空下蒸发,用石油醚/乙酸乙酯进行硅胶色谱柱纯化,得到相应的产物。
反应的产率为90.2%,利用核磁共振对产物进行分析,确定其为n-苄基-n-甲基苯胺,n-苄基-n-甲基苯胺的氢核磁谱图如图3所示,碳核磁谱图如图4所示;核磁数据如下所示:
1hnmr(300mhz,chloroform-d)δ7.38-7.02(m,7h),6.85-6.48(m,3h),4.45(s,2h),2.93(s,3h);13cnmr(75mhz,cdcl3)δ153.1,149.7,130.3,129.1,128.5,128.5,127.3,126.8,126.7,126.6,124.3,117.9,116.5,112.3,112.3,107.4,56.6,56.1,38.4,36.3,28.7。
实施例3
本实施例提供一种甲基胺的制备方法,其中,所用催化剂为十二烷基二甲基胺己内酯,甲基胺为n,n-二甲基-[1,1'-二苯基]-2-胺,制备甲基胺的反应路线如下所示:
n,n-二甲基-[1,1'-二苯基]-2-胺的制备方法包括以下步骤:
取一只严格干燥的史莱克反应管(schlenk管),将一个装满二氧化碳的气球通过侧管连接到schlenk管,并清洗3次,依次加入十二烷基二甲基胺己内酯(5mol%相对于胺)、n-甲基-[1,1'-二苯基]-2-胺(0.25mmol)、聚甲基聚硅氧烷pmhs(1.2mmol)和ch3cn(2ml),schlenk管在60℃加热6h,冷却到室温,释放气球中的co2,在混合液中加入etoac(10ml),淬灭还原性反应,用ch2cl2萃取三次,浓缩的有机层在无水na2so4上干燥,在真空下蒸发,用石油醚/乙酸乙酯进行硅胶色谱柱纯化,得到相应的产物。
反应的产率为92.3%,利用核磁共振对产物进行分析,确定其为n,n-二甲基-[1,1'-二苯基]-2-胺,n,n-二甲基-[1,1'-二苯基]-2-胺的氢核磁谱图如图5所示,碳核磁谱图如图6所示;核磁数据如下所示:
1hnmr(300mhz,chloroform-d)δ7.58-7.43(m,2h),7.35-7.27(m,2h),7.24-7.11(m,3h),7.01-6.83(m,2h),2.46(s,6h);13cnmr(75mhz,cdcl3)δ153.1,151.1,141.9,134.1,134.6,128.6,128.2,128.0,127.3,126.4,124.2,121.4,117.5,107.4,56.1,43.3,36.3,28.7。
实施例4
本实施例提供一种甲基胺的制备方法,其中,所用催化剂为十二烷基二甲基胺己内酯,甲基胺为1-甲基吲哚啉,制备甲基胺的反应路线如下所示:
1-甲基吲哚啉的制备方法包括以下步骤:
取一只严格干燥的史莱克反应管(schlenk管),将一个装满二氧化碳的气球通过侧管连接到schlenk管,并清洗3次,依次加入十二烷基二甲基胺己内酯(5mol%相对于胺)、吲哚(0.25mmol)、聚甲基聚硅氧烷pmhs(1.5mmol)和ch3cn(2ml),schlenk管在100℃加热18h,冷却到室温,释放气球中的co2,在混合液中加入etoac(10ml),淬灭还原性反应,用ch2cl2萃取三次,浓缩的有机层在无水na2so4上干燥,在真空下蒸发,用石油醚/乙酸乙酯进行硅胶色谱柱纯化,得到相应的产物。
反应的产率为82.6%,利用核磁共振对产物进行分析,确定其为1-甲基吲哚啉,1-甲基吲哚啉的氢核磁谱图如图7所示,碳核磁谱图如图8所示;核磁数据如下所示:
1hnmr(300mhz,chloroform-d)δ7.10-6.90(m,2h),6.61(t,j=7.8hz,1h),6.43(d,j=8.1hz,1h),3.22(t,j=8.2hz,2h),2.87(t,j=8.1hz,2h),2.68(s,3h);13cnmr(75mhz,cdcl3)δ153.1,130.3,127.3,124.2,117.9,107.4,56.1,36.3,28.7。
实施例5
本实施例提供一种甲基胺的制备方法,其中,所用催化剂为十二烷基二甲基胺己内酯,甲基胺为4-甲氧基-n,n-二甲基苯胺,制备甲基胺的反应路线如下所示:
4-甲氧基-n,n-二甲基苯胺的制备方法包括以下步骤:
取一只严格干燥的史莱克反应管(schlenk管),将一个装满二氧化碳的气球通过侧管连接到schlenk管,并清洗3次,依次加入十二烷基二甲基胺己内酯(5mol%相对于胺)、4-甲氧基-n-甲基苯胺(0.25mmol)、聚甲基聚硅氧烷pmhs(1mmol)和ch3cn(2ml),schlenk管在70℃加热12h,冷却到室温,释放气球中的co2,在混合液中加入etoac(10ml),淬灭还原性反应,用ch2cl2萃取三次,浓缩的有机层在无水na2so4上干燥,在真空下蒸发,用石油醚/乙酸乙酯进行硅胶色谱柱纯化,得到相应的产物。
反应的产率为91.2%,利用核磁共振对产物进行分析,确定其为4-甲氧基-n,n-二甲基苯胺,4-甲氧基-n,n-二甲基苯胺的氢核磁谱图如图9所示,碳核磁谱图如图10所示;核磁数据如下所示:
1hnmr(300mhz,chloroform-d)δ7.00-6.34(m,4h),3.69(s,3h),2.79(s,6h);13cnmr(75mhz,cdcl3)δ153.1,152.1,145.6,130.3,127.3,124.2,117.9,115.1,114.6,107.4,56.1,55.7,41.9,36.3,28.7。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!