寨卡病毒丝氨酸蛋白酶在去除重组蛋白亲合标签中的应用的制作方法
本发明属于生物技术领域,具体涉及寨卡病毒丝氨酸蛋白酶在去除重组蛋白亲合标签中的应用。
背景技术:
蛋白质纯化是一种将目标蛋白与其它蛋白分离开的技术,在生物学研究中起到重要作用。所要纯化的目标蛋白可以从生物体中直接分离出来,但是这样的操作效率极低。基因工程技术的发展促进了多种蛋白表达系统的发展。通过将目标蛋白的基因克隆出来,再构建到表达载体中,从而目标蛋白可在一些宿主细胞中进行高效表达。重组蛋白被广泛应用于科学研究以及工业生产过程中,大部分不同来源的目标蛋白都可以采取重组蛋白的方法进行分离纯化。但是,仍然有一些目标蛋白很难通过此种方法分离纯化,这主要是由于其表达水平较低、较低溶解度和对宿主细胞有毒性所致。因此,采用亲和标签的方法可以有效的提高此类目标蛋白的产量。许多亲合标签如谷胱甘肽-s-转移酶(gst)和多聚组氨酸标签等被广泛应用于重组蛋白的纯化中,这类亲合标签的加入,极大地增加了蛋白纯化的效率,可以提高目标蛋白的产量和纯度。由于所加入的亲合标签不属于目标蛋白,这类标签可能会影响蛋白的功能,因此,在重组蛋白的构建过程中,将人为引入蛋白酶酶切位点,再通过蛋白酶酶切的方法去除重组蛋白中的亲合标签,以达到纯化目标蛋白的目的。
技术实现要素:
本发明的目的是针对现有技术中的上述不足,提供寨卡病毒丝氨酸蛋白酶在去除重组蛋白亲合标签中的应用。
目前有不同来源的多种蛋白酶用于重组蛋白与亲合标签的分离。但来源于寨卡病毒的蛋白酶所能够识别的酶切位点是由含正电荷的氨基酸如赖氨酸和精氨酸组成,因此,寨卡病毒的蛋白酶特别适用于切割蛋白序列中不含有其酶切位点的目标蛋白。而且,寨卡病毒的蛋白酶位于细胞膜表面,膜系统对其酶活性的影响不大,因此,此类蛋白酶适合切除目标膜蛋白两端的亲合标签。通过在目标蛋白和亲合标签之间加入天冬酰胺-赖氨酸-精氨酸-精氨酸-甘氨酸-丝氨酸(nkrrgs)序列,使得寨卡病毒丝氨酸蛋白酶可用于去除此种重组蛋白中的亲合标签。
本发明的第一目的是提供寨卡病毒丝氨酸蛋白酶在去除重组蛋白亲合标签中的应用,所述的寨卡病毒丝氨酸蛋白酶,其氨基酸序列如seqidno.1所示,其酶切位点为氨基酸序列nkrrgs,所述的重组蛋白的目标蛋白中不含有氨基酸序列nkrrgs。
本发明的第二目的是提供一种亲合标签的去除方法,包括以下步骤:
在重组蛋白表达载体的构建过程中,将表达天冬酰胺-赖氨酸-精氨酸-精氨酸-甘氨酸-丝氨酸(nkrrgs)的基因序列插入到表达亲合标签的基因序列和表达目标蛋白的基因序列之间,构建得到重组蛋白表达载体;然后将表达载体转入到宿主细胞中进行重组蛋白表达,纯化重组蛋白,然后加入寨卡病毒丝氨酸蛋白酶并混合,进行酶切反应,纯化后得到去除了亲和标签的目标蛋白;
所述的寨卡病毒丝氨酸蛋白酶,其氨基酸序列如seqidno.1所示,所述的目标蛋白中不含有氨基酸序列nkrrgs。
优选,所述的表达载体为pet29b载体、pet载体或pgex载体。
优选,所述的亲合标签为谷胱甘肽-s-转移酶(gst)标签或多聚组氨酸标签。
根据所选择的表达宿主,选择相应的表达载体。常用的表达宿主为大肠杆菌(bl21de3)。
优选,所述的纯化重组蛋白利用亲合层析法进行,所述的酶切反应后的纯化是经分子筛层析柱纯化得到目标蛋白。
与现有技术相比,本发明具有以下有益效果:
1.本发明表明了寨卡病毒丝氨酸蛋白酶可以用于亲合标签的切除。只要目标蛋白中不含有此酶的酶切位点,就可使用此酶进行亲合标签的去除。
2.寨卡病毒丝氨酸蛋白酶可以广泛应用于可溶性蛋白和膜蛋白的制备、分离纯化过程中,具有广泛的应用前景。
附图说明
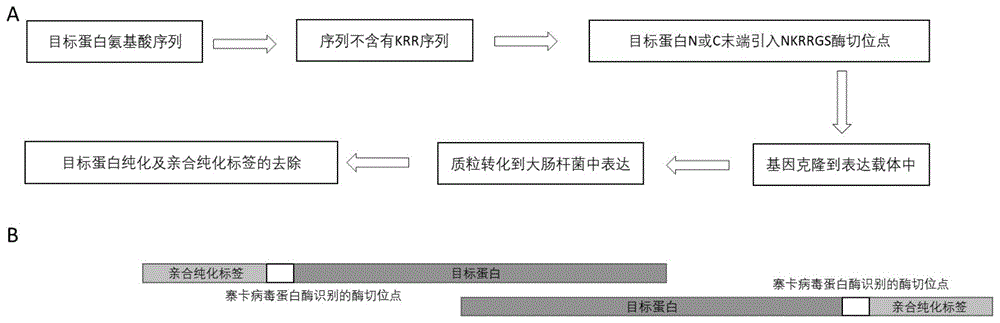
图1是本发明方法的总体实施路线图;a:将寨卡病毒丝氨酸蛋白酶的酶切位点引入至目标蛋白的n或c末端,b:将亲合纯化标签如多聚组氨酸或gst亲合纯化标签引入至目标蛋白的n或c末端,目标蛋白纯化后,可利用寨卡病毒丝氨酸蛋白酶将亲合标签去除。
图2目标蛋白1的sds-page电泳分析图;m,分子量标准;1,纯化的重组蛋白;2-5,酶切后从凝胶柱中洗脱下的组分,含有纯化的目标蛋白;6,经酶切、缓冲液清洗后仍然留在凝胶上的组分,这些组分包括没有被切开的重组蛋白,gst标签以及其它杂蛋白。
具体实施方式
以下实施例是对本发明的进一步说明,而不是对本发明的限制。
本发明方法的总体实施路线如图1所示。
在重组蛋白表达载体的构建过程中,将表达天冬酰胺-赖氨酸-精氨酸-精氨酸-甘氨酸-丝氨酸(nkrrgs)的基因序列引入到表达亲合标签的基因序列和表达目标蛋白的基因序列之间(即表达的nkrrgs酶切位点和亲和标签可引入在目标蛋白的n或c端),以构建表达载体。然后将此表达载体转入到宿主细胞中表达,再依次进行重组蛋白表达、重组蛋白纯化,然后加入寨卡病毒丝氨酸蛋白酶(其氨基酸序列如seqidno.1所示)与纯化的重组蛋白混合,从nkrrgs酶切位点切除亲合标签,洗脱纯化目标蛋白。
实施例1
实施目标蛋白1(分子量为31kda)的纯化过程中谷胱甘肽-s-转移酶(gst)标签的去除。步骤如下:
1.目标蛋白1表达载体的构建:将天冬酰胺-赖氨酸-精氨酸-精氨酸-甘氨酸-丝氨酸
(nkrrgs)序列基因和目标蛋白1的基因合成后,克隆至含gst的细菌表达载体pgex系统质粒中。所得到的重组表达载体可以表达重组蛋白:含有gst标签、寨卡病毒丝氨酸蛋白酶酶切位点和目标蛋白。
2.重组蛋白的表达:重组表达载体转化至大肠杆菌(bl21de3)中,在含相应抗生素的lb平板上培养,挑取一个单菌落,接种于lb培养基中,置于37℃,过夜(12小时)振荡培养后,转至1升的含相应抗生素的lb培养基中37℃振荡培养。当在600nm处的吸光度达到1.0时,加入iptg至1mm诱导重组蛋白的表达,菌体细胞继续在20℃摇床上培养12小时后,于8000×g离心收集菌体。
3.重组蛋白的纯化:每4g菌体细胞悬浮于40ml缓冲液(20mm磷酸钠,ph7.8,300mm氯化钠)中,置于冰浴中用超声波破碎仪破碎15min,于4℃,18000×g离心20分钟后,取上清液与4ml谷胱甘肽-琼脂糖凝胶4b混合后,用40ml缓冲液(20mm磷酸钠,ph7.8,100mm氯化钠)清洗凝胶。
4.酶切去除gst标签:将0.5mg寨卡病毒丝氨酸蛋白酶(其氨基酸序列如seqidno.1所示)加入到2ml的缓冲液(20mm磷酸钠,ph7.8,100mm氯化钠)中与4ml谷胱甘肽-琼脂糖凝胶4b混合,置于16℃条件下振荡12小时,然后将混合液转移至层析柱中,收集流出的溶液。再用4ml的缓冲液(20mm磷酸钠,ph7.8,100mm氯化钠)清洗凝胶2-5次。gst标签和没有被切除的重组蛋白将会留在凝胶上,而目标蛋白则被洗脱下来。
5.纯化效果检测:将收集到的各种组分用sds-page进行分析,从而可以检测目标蛋白的纯度。
结果如图2所示:其中1表示的是纯化的重组蛋白(含有gst标签、寨卡病毒丝氨酸蛋白酶酶切位点和目标蛋白),2-5表示的是用寨卡病毒丝氨酸蛋白酶酶切后从凝胶柱中洗脱下的组分,含有纯化的目标蛋白,大小均约为31kda,与目标蛋白分子量吻合;6表示经酶切、缓冲液清洗后仍然留在凝胶上的组分,这些组分包括没有被切开的重组蛋白、gst标签以及其它杂蛋白。以上结果说明,寨卡病毒丝氨酸蛋白酶能够准确的对蛋白上的nkrrgs位点进行酶切从而切除亲和标签。
序列表
<110>广东省科学院生物工程研究所
<120>寨卡病毒丝氨酸蛋白酶在去除重组蛋白亲合标签中的应用
<160>1
<170>siposequencelisting1.0
<210>1
<211>231
<212>prt
<213>寨卡病毒(zikavirus)
<400>1
glyserglyalaleutrpaspvalproalaprolysgluvallyslys
151015
glygluthrthraspglyvaltyrargvalmetthrargargleuleu
202530
glyserthrglnvalglyvalglyvalmetglngluglyvalphehis
354045
thrmettrphisvalthrlysglyalaalaleuargserglyglugly
505560
argleuaspprotyrtrpglyaspvallysglnaspleuvalsertyr
65707580
cysglyprotrplysleuaspalaalatrpaspglyleusergluval
859095
glnleuleualavalproproglygluargalalysasnileglnthr
100105110
leuproglyilephelysthrlysaspglyaspileglyalavalala
115120125
leuasptyrproalaglythrserglyserproileleuasplyscys
130135140
glyargvalileglyleutyrglyasnglyvalvalilelysasngly
145150155160
sertyrvalseralailethrglnglylysarggluglugluthrpro
165170175
valglumetthrglylysservalaspmettyrilegluargalagly
180185190
aspilethrtrpglulysaspalagluvalthrglyasnserproarg
195200205
leuaspvalalaleuaspgluserglyasppheserleuvalgluglu
210215220
aspglyproprometargglu
225230
- 还没有人留言评论。精彩留言会获得点赞!
- 丝氨酸蛋白酶、特别是hcv ns3-ns4a蛋白酶的抑制剂的制作方法
- 丝氨酸蛋白酶、特别是丙型肝炎病毒ns3-ns4蛋白酶的抑制剂的制作方法
- 某些作为丝氨酸蛋白酶xa因子抑制剂的1-(d-环丙基甘氨酰基)-4-(哌啶-4-基)哌 ...的制作方法
- 丝氨酸蛋白酶、特别是丙型肝炎病毒ns3蛋白酶的抑制剂的制作方法
- 丝氨酸蛋白酶和外用类视色素组合物的制作方法
- 一种新的多肽——人蛋白丝氨酸-苏氨酸磷酸酶14.30和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——丝氨酸蛋白酶11和编码这种多肽的多核苷酸的制作方法
- 丙型肝炎病毒ns3/ns4a丝氨酸蛋白酶的抑制剂的制作方法
- 一种多肽——丝氨酸蛋白酶-10.12和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——丝氨酸蛋白酶12.32和编码这种多肽的多核苷酸的制作方法