抗突变的KRAS的T细胞受体的制作方法
抗突变的kras的t细胞受体
1.相关申请的交叉引用
2.本专利申请要求于2014年11月26日提交的美国临时专利申请第62/084,654号以及于2015年6月5日提交的美国临时专利申请第62/171,321号的权益,其各自通过引用整体并入本文。
3.关于联邦政府资助研究与开发的声明
4.本发明是由美国国立卫生研究院国家癌症研究所在政府支持下完成的,项目编号为z01bc011337-04。政府拥有本发明的某些权利。
5.通过引用并入电子提交的材料
6.通过引用整体并入本文的是,随本文同时提交的并且如下确定的计算机可读的核苷酸/氨基酸序列表:名称为“722261_st25.txt”,日期为2015年11月20日的一份231,164字节的ascii(文本)文件。
7.发明背景
8.一些癌症可能具有非常有限的治疗选择,特别是当癌症转移且不可切除时。尽管在例如手术、化学疗法和放射疗法的治疗方面取得进展,但许多癌症,例如胰癌、结直肠癌、肺癌、子宫内膜癌、卵巢癌和前列腺癌的预后可能较差。因此,对癌症的其他治疗需求尚未满足。
9.发明概述
10.本发明的实施方案提供了对突变的表位具有抗原特异性的分离的或纯化的t细胞受体(tcr),所述突变的表位(a)包含vvvgadgvgk(seq id no:2),或者(b)由vvvgavgvgk(seq id no:33)或vvgavgvgk(seq id no:35)组成。
11.本发明还提供了相关的多肽和蛋白,以及相关的核酸、重组表达载体、宿主细胞、细胞群和与本发明的tcr有关的药物组合物。
12.本发明还提供了检测哺乳动物中癌症的存在的方法和治疗或预防哺乳动物中的癌症的方法。
13.发明详述
14.kirsten大鼠肉瘤病毒致癌基因同源物(kras)也称为gtp酶kras,v-ki-ras2 kirsten大鼠肉瘤病毒致癌基因或kras2,是小gtp酶超家族的成员。kras有两种转录本变体:kras变体a和kras变体b。除非另有说明,下文提及“kras”(突变的或未突变的)是指变体a和变体b。不受特定理论或机制的束缚,据认为当突变时,kras可能参与多种人类癌症的肿瘤发生早期的信号转导。单个氨基酸置换可能激活该突变。当激活时,突变的kras与鸟苷-5'-三磷酸(gtp)结合,并将gtp转变为鸟苷5
′‑
二磷酸(gdp)。突变的kras蛋白产物可被组成型激活。突变的kras蛋白可在众多人类癌症的任何一种中表达,例如,胰癌(pancreatic cancer)(例如,胰腺癌(pancreatic carcinoma))、结直肠癌、肺癌(例如,肺腺癌)、子宫内膜癌、卵巢癌(例如,上皮性卵巢癌)和前列腺癌。
15.本发明的实施方案提供了分离的或纯化的tcr,其对突变的人kras(下文称“突变的kras”)具有抗原特异性。除非另有说明,下文提及“tcr”也指tcr的功能部分和功能变体。
本发明的tcr可对任何突变的kras蛋白、多肽或肽具有抗原特异性。在本发明的实施方案中,所述tcr对突变的kras蛋白具有抗原特异性,所述突变的kras蛋白包含seq id no:1、32、122或123的氨基酸序列或由seq id no:1、32、122或123的氨基酸序列组成。seq id no:1和32各自的突变的kras变体a蛋白氨基酸序列大体对应于seq id no:29的未突变的、野生型(wt)kras蛋白变体a氨基酸序列的第1-189位,不同之处在于:在seq id no:1和32中,第12位的甘氨酸分别由天冬氨酸或缬氨酸置换。seq id no:122和123各自的突变的kras变体b蛋白氨基酸序列大体对应于seq id no:121的未突变的、wt kras蛋白变体b氨基酸序列的第1-188位,不同之处在于:在seq id no:122和123中,第12位的甘氨酸分别由天冬氨酸或缬氨酸置换。在本发明的优选实施方案中,所述tcr对突变的kras
7-16
肽具有抗原特异性,所述突变的kras
7-16
肽包含vvvgadgvgk(seq id no:2)或vvvgavgvgk(seq id no:33)的氨基酸序列或由vvvgadgvgk(seq id no:2)、或vvvgavgvgk(seq id no:33)的氨基酸序列组成。seq id no:2和33的突变的kras肽氨基酸序列大体对应于seq id no:30的未突变的、wt kras
7-16
肽氨基酸序列的第1-10位,不同之处在于:在seq id no:2和33中,第6位的甘氨酸分别由天冬氨酸或缬氨酸置换。在本发明的实施方案中,所述tcr对突变的kras
8-16
肽具有抗原特异性,所述突变的kras
8-16
肽包含vvgadgvgk(seq id no:34)或vvgavgvgk(seq id no:35)的氨基酸序列或由vvgadgvgk(seq id no:34)或vvgavgvgk(seq id no:35)的氨基酸序列组成。seq id no:34和35的突变的kras肽氨基酸序列大体对应于seq id no:31的未突变的、wt kras
8-16
肽氨基酸序列的第1-9位,不同之处在于:在seq id no:34和35中,第5位的甘氨酸分别由天冬氨酸或缬氨酸置换。在优选的实施方案中,所述tcr对突变的kras表位具有抗原特异性,所述突变的kras表位(a)包含vvvgadgvgk(seq id no:2),或者(b)由vvvgavgvgk(seq id no:33)或vvgavgvgk(seq id no:35)组成。在特别优选的实施方案中,所述tcr对突变的kras表位具有抗原特异性,所述突变的kras表位包含vvvgadgvgk(seq id no:2)。在另一个优选实施方案中,所述tcr对突变的kras表位具有抗原特异性,所述突变的kras表位由vvvgavgvgk(seq id no:33)或vvgavgvgk(seq id no:35)组成。突变的kras氨基酸序列vvvgavgvgk(seq id no:33)和vvgavgvgk(seq id no:35)在本文也称为“kras g12v”。突变的kras氨基酸序列vvvgadgvgk(seq id no:2)和vvgadgvgk(seq id no:34)在本文也称为“kras g12d”。
16.本文所述的突变的kras表位氨基酸序列也存在于人癌症的两个其他突变的致癌基因,即神经母细胞ras病毒(v-ras)致癌基因同源物(nras)和harvey大鼠肉瘤病毒致癌基因同源物(hras)中。突变的人nras和突变的人hras的氨基酸序列含有本文所述的突变的人kras表位序列。因此,在本发明的实施方案中,本发明的tcr还对突变的人nras和hras具有抗原特异性。突变的人kras、突变的人nras和突变的人hras在本文总称为“突变的靶标”。
17.在本发明的实施方案中,本发明的tcr能够以主要组织相容性复合体(mhc)i类-依赖性的方式识别突变的靶标如突变的kras。如本文所用,“mhc i类-依赖性的方式”是指所述tcr在结合mhc i类分子背景下的突变的靶标如突变的kras时引发免疫应答。所述mhc i类分子可以为本领域已知的任何mhc i类分子,例如hla-a分子。在本发明的优选实施方案中,所述tcr对在hla-a11分子的背景下所呈递的突变的表位具有抗原特异性。
18.本发明的tcr提供许多优势,包括当由用于过继性细胞转移的细胞表达时。突变的kras、突变的nras和突变的hras由癌细胞表达而不由正常的非癌性细胞表达。不受特定理
论或机制的束缚,认为本发明的tcr有利地靶向破坏癌细胞,同时最小化或消除对正常的非癌性细胞的破坏,从而例如通过最小化或消除来降低毒性。而且,本发明的tcr可有利地成功治疗或预防突变的kras-阳性癌症、突变的nras-阳性癌症和突变的hras-阳性癌症(其不响应于诸如化疗、手术或放射的其他类型的治疗)中的一种或多种。此外,本发明的tcr可提供对突变的kras、突变的nras和突变的hras中的一种或多种的高度亲合的识别,其可提供识别未经处理的肿瘤细胞(例如,没有用干扰素(ifn)-γ处理、用编码突变的kras和hla-a11之一或的载体转染、用突变的kras
7-16
或kras
8-16
肽脉冲或以上的组合的肿瘤细胞)的能力。
19.如本文所用,短语“抗原特异性”是指tcr能以高亲合力特异性结合并免疫识别突变的靶标如突变的kras。例如,当与以下细胞共培养时,如果表达tcr的t细胞分泌至少约200pg/ml或更多(例如,200pg/ml或更多,300pg/ml或更多,400pg/ml或更多,500pg/ml或更多,600pg/ml或更多,700pg/ml或更多,1000pg/ml或更多,5,000pg/ml或更多,7,000pg/ml或更多,10,000pg/ml或更多,20,000pg/ml或更多,或由上述数值中任意两个所限定的范围)的ifn-γ,则该tcr可被认为对突变的靶标具有“抗原特异性”:(a)用低浓度的突变的靶肽(例如,约0.05ng/ml至约5ng/ml、0.05ng/ml、0.1ng/ml、0.5ng/ml、1ng/ml、5ng/ml,或由上述数值中任意两个所限定的范围)脉冲的抗原阴性的hla-a11
+
靶细胞,或者(b)已向其中引入编码突变的靶标的核苷酸序列的抗原阴性的hla-a11
+
靶细胞,从而使靶细胞表达突变的靶标。当与用较高浓度的突变的靶肽脉冲的抗原阴性的hla-a11
+
靶细胞共培养时,表达本发明的tcr的细胞也可分泌ifn-γ。
20.可选地或此外,当与以下细胞共培养时,如果相比阴性对照所表达的ifn-γ的量,表达tcr的t细胞分泌至少两倍的ifn-γ,则该tcr可被认为对突变的靶标具有“抗原特异性”:(a)用低浓度的突变的靶肽脉冲的抗原阴性的hla-a11
+
靶细胞,或者(b)已向其中引入编码突变的靶标的核苷酸序列的抗原阴性的hla-a11
+
靶细胞,从而使靶细胞表达突变的靶标。阴性对照可为例如,(i)与以下细胞共培养的表达所述tcr的t细胞:(a)用相同浓度的不相关肽(例如,具有与突变的靶肽不同的序列的某个其他肽)脉冲的抗原阴性的hla-a11
+
靶细胞,或(b)已向其中引入编码不相关肽的核苷酸序列的抗原阴性的hla-a11
+
靶细胞,从而使所述靶细胞表达该不相关肽;或者(ii)与以下细胞共培养的未转导的t细胞(例如源自pbmc,其不表达所述tcr):(a)用相同浓度的突变的靶肽脉冲的抗原阴性的hla-a11
+
靶细胞,或(b)已向其中引入编码突变的靶标的核苷酸序列的抗原阴性的hla-a11
+
靶细胞,从而使靶细胞表达所述突变的靶标。可通过本领域熟知的方法例如,酶联免疫吸附测定(elisa)来测量ifn-γ的分泌。
21.可选地或此外,当与以下细胞共培养时,如果相比分泌ifn-γ的阴性对照t细胞的数量,至少两倍数量的表达tcr的t细胞分泌ifn-γ,则所述tcr可被认为对突变的靶标具有“抗原特异性”:(a)用低浓度的突变的靶肽脉冲的抗原阴性的hla-a11
+
靶细胞,或者(b)已向其中引入编码突变的靶标的核苷酸序列的抗原阴性的hla-a11
+
靶细胞,从而使靶细胞表达突变的靶标。肽和阴性对照的浓度可以如针对本发明其他方面所描述的。可通过本领域熟知的方法例如elispo来测量分泌ifn-γ的细胞数量。
22.本发明提供了包含两种多肽(即多肽链)的tcr,所述多肽为如tcr的α链、tcr的β链、tcr的γ链、tcr的δ链或其组合。本发明tcr的多肽可包含任何氨基酸序列,条件是所述
tcr对突变的靶标如突变的kras具有抗原特异性。
23.在本发明的实施方案中,所述tcr包含两条多肽链,其各自包含可变区,所述可变区包含tcr的互补决定区(cdr)1、cdr2和cdr3。在本发明的实施方案中,所述tcr包含:(a)第一多肽链,其包含:包含seq id no:3的氨基酸序列的cdr1(抗-kras g12d tcr的α链的cdr1),包含seq id no:4的氨基酸序列的cdr2(抗-kras g12d tcr的α链的cdr2),和包含seq id no:5的氨基酸序列的cdr3(抗-kras g12dtcr的α链的cdr3);以及第二多肽链,其包含:包含seq id no:6的氨基酸序列的cdr1(抗-kras g12d tcr的β链的cdr1),包含seq id no:7的氨基酸序列的cdr2(抗-kras g12d tcr的β链的cdr2),和包含seq id no:8的氨基酸序列的cdr3(抗-kras g12d tcr的β链的cdr3);(b)第一多肽链,其包含:包含seq id no:125的氨基酸序列的抗-kras g12v tcrα链cdr1,包含seq id no:126的氨基酸序列的抗-kras g12v tcrα链cdr2,和包含seq id no:127的氨基酸序列的抗-kras g12v tcrα链cdr3;以及第二多肽链,其包含:包含seq id no:128的氨基酸序列的抗-kras g12v tcrβ链cdr1,包含seq id no:129的氨基酸序列的抗-kras g12v tcrβ链cdr2,和包含seq id no:130的氨基酸序列的抗-kras g12v tcrβ链cdr3;(c)第一多肽链,其包含:包含seq id no:137的氨基酸序列的抗-kras g12vtcrα链cdr1,包含seq id no:138的氨基酸序列的抗-kras g12vtcrα链cdr2,和包含seq id no:139的氨基酸序列的抗-kras g12vtcrα链cdr3;以及第二多肽链,其包含:包含seq id no:140的氨基酸序列的抗-kras g12v tcrβ链cdr1,包含seq id no:141的氨基酸序列的抗-kras g12v tcrβ链cdr2,和包含seq id no:142的氨基酸序列的抗-kras g12v tcrβ链cdr3;或者(d)第一多肽链,其包含:包含seq id no:149的氨基酸序列的抗-kras g12d tcrα链cdr1,包含seq id no:150的氨基酸序列的抗-kras g12d tcrα链cdr2,和包含seq id no:151的氨基酸序列的抗-kras g12d tcrα链cdr3;以及第二多肽链,其包含:包含seq id no:152的氨基酸序列的抗-kras g12d tcrβ链cdr1,包含seq id no:153的氨基酸序列的抗-kras g12d tcrβ链cdr2,和包含seq id no:154的氨基酸序列的抗-kras g12d tcrβ链cdr3。在这方面,本发明的tcr可包含选自seq id no:3-8;125-130;137-142;和149-154的氨基酸序列的任意一个或多个。优选地,所述tcr包含以下的氨基酸序列:seq id no:3-5;seq id no:6-8;seq id no:125-127;seq id no:128-130;seq id no:137-139;seq id no:140-142;seq id no:149-151;或seq id no:152-154。在特别优选的实施方案中,所述tcr包含以下的氨基酸序列:(a)seq id no:3-8的全部;(b)seq id no:125-130的全部;(c)seq id no:137-142的全部;(d)seq id no:149-154的全部。
24.在本发明的实施方案中,所述tcr包含含有上述cdrs的tcr的可变区的氨基酸序列。在这方面,所述tcr可包含以下的氨基酸序列:seq id no:9(抗-kras g12d tcrα链的可变区);seq id no:10(抗-kras g12d tcrβ链的可变区);seq id no:9和10;seq id no:131(抗-kras g12v tcrα链的可变区);seq id no:132(抗-kras g12v tcrβ链的可变区);seq id no:131和132;seq id no:143(抗-kras g12v tcrα链的可变区);seq id no:144(抗-kras g12v tcrβ链的可变区);seq id no:143和144;seq id no:155(抗-kras g12d tcrα链的可变区);seq id no:156(抗-kras g12d tcrβ链的可变区);或seq id no:155和156。优选地,本发明的tcr包含以下的氨基酸序列:seq id no:9和10;seq id no:131和132;seq id no:143和144;或seq id no:155和156。
id no:146(抗-kras g12v tcrβ链)、或seq id no:158(抗-kras g12d tcrβ链)。本发明的tcr因此可包含以下的氨基酸序列:seq id no:11、seq id no:12、seq id no:133、seq id no:134、seq id no:145、seq id no:146、seq id no:157、seq id no:158、seq id no:11和12、seq id no:133和134、seq id no:145和146、或seq id no:157和158。优选地,本发明的tcr包含以下的氨基酸序列:seq id no:11和12、seq id no:133和134、seq id no:145和146、或seq id no:157和158。
29.在本发明的实施方案中,在(i)存在cd4且不存在cd8,或(ii)存在cd8且不存在cd4的条件下,本发明的tcr识别突变的靶标如突变的kras。在优选的实施方案中,在(i)存在cd4且不存在cd8,或(ii)存在cd8且不存在cd4的条件下,包含(i)seq id no:125-130;(ii)seq id no:131-132;或(iii)seq id no:133和134的氨基酸序列的tcr识别突变的靶标如突变的kras。因此,当由cd4+或cd8+细胞表达时,这些本发明的tcr可有利地识别突变的靶标如突变的kras。
30.在本发明的实施方案中,所述tcr是鼠tcr。如本文所用,术语“鼠”在提及本文所述的tcr或tcr的任意组分(例如,互补决定区(cdr)、可变区、恒定区、α链和/或β链)时,是指来自小鼠的tcr(或其组分),即来自小鼠t细胞或曾经由小鼠t细胞表达的tcr(或其组分)。在本发明的实施方案中,包含以下序列的tcr是鼠tcr:(i)seq id no:3-8的全部;(ii)seq id no:9和10;(iii)seq id no:11和12;(iv)seq id no:3-8和13-14的全部;(v)所有的seq id no:9、10、13和14的全部;(vi)seq id no:125-130的全部;(vii)seq id no:131和132;(viii)seq id no:133和134;(ix)seq id no:125-130和135-136的全部;(x)seq id no:131、132、135和136的全部;(xi)seq id no:137-142的全部;(xii)seq id no:143和144;(xiii)seq id no:145和146;(xiv)seq id no:137-142和147-148的全部;(xv)seq id no:143、144、147和148的全部;(xvi)seq id no:149-154的全部;(xvii)seq id no:155和156;(xviii)seq id no:157和158;(xix)seq id no:149-154和159-160的全部;或(xx)seq id no:155、156、159和160的全部。
31.本发明的范围包括本文所述的本发明tcr的功能变体。如本文所用,术语“功能变体”是指与母体tcr、多肽或蛋白具有大量或显著序列一致性或相似性的tcr、多肽或蛋白,所述功能变体保留了该变体所来源的tcr、多肽或蛋白的生物功能。功能变体涵盖例如,本文所述的tcr、多肽或蛋白(母体tcr、多肽或蛋白)的那些变体,所述变体保留了以与母体tcr、多肽或蛋白类似的程度、相同的程度或比母体tcr、多肽或蛋白更高的程度特异性结合突变的靶标如突变的kras的能力,所述母体tcr对所述突变的靶标如突变的kras具有抗原特异性或者所述母体多肽或蛋白能特异性结合所述突变的靶标如突变的kras。相对于母体tcr、多肽或蛋白,所述功能变体可与母体tcr、多肽或蛋白的氨基酸序列例如具有至少约30%、50%、75%、80%、90%、95%、96%、97%、98%、99%或更多的一致性。
32.所述功能变体可例如包含具有至少一个保守氨基酸置换的母体tcr、多肽或蛋白的氨基酸序列。保守氨基酸置换为本领域熟知,且包括这样的氨基酸置换,其中具有某种物理和/或化学特性的一个氨基酸被替换为具有相同物理或化学特性的另一个氨基酸。例如,所述保守氨基酸置换可为酸性氨基酸置换另一酸性氨基酸(例如,asp或glu),具有非极性侧链的氨基酸置换具有非极性侧链的另一氨基酸(例如,ala、gly、val、ile、leu、met、phe、pro、trp、val等),碱性氨基酸置换另一碱性氨基酸(lys、arg等),具有极性侧链的氨基酸置
换具有极性侧链的另一氨基酸(asn、cys、gln、ser、thr、tyr等)等。
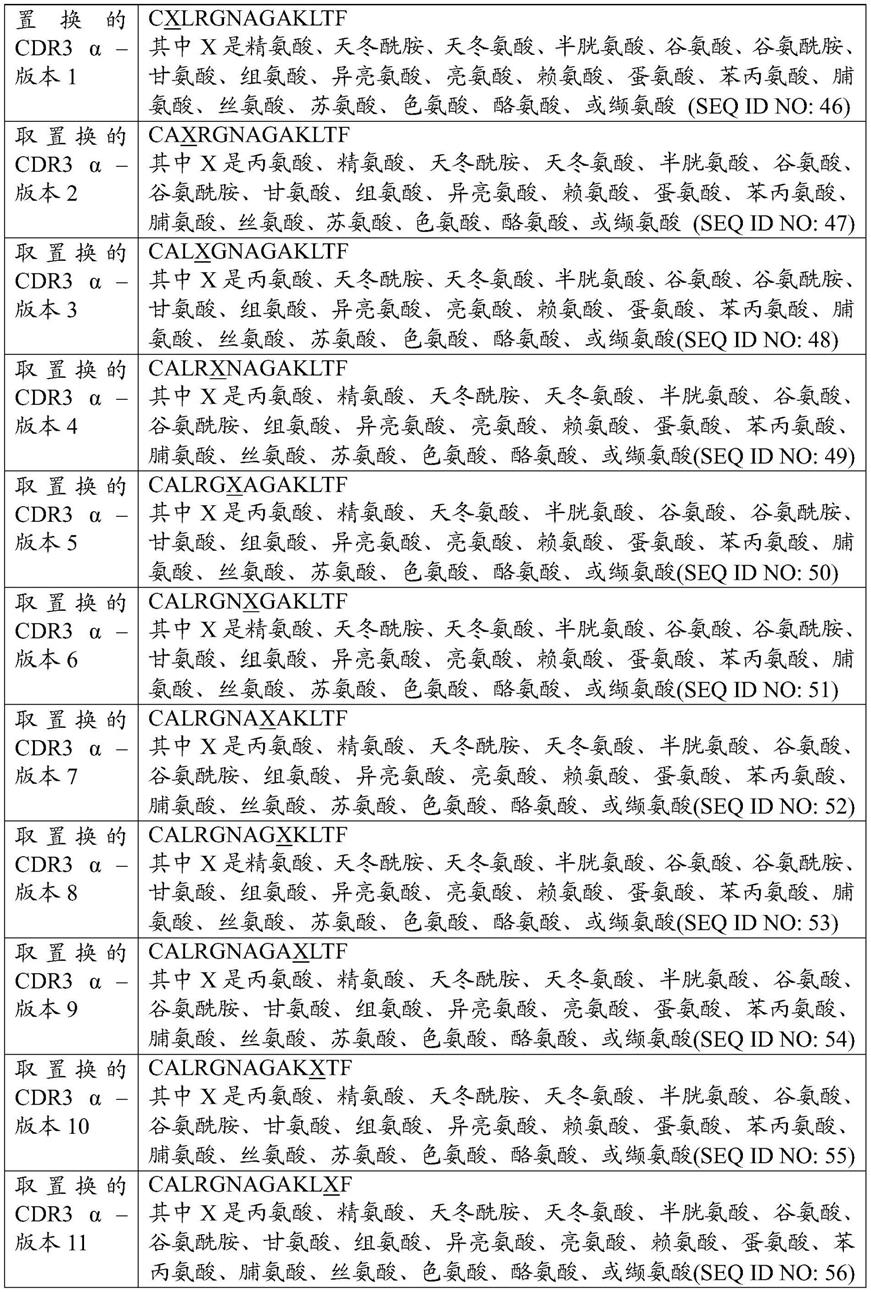
33.可选地或此外,所述功能变体可包含具有至少一个非保守氨基酸置换的母体tcr、多肽或蛋白的氨基酸序列。在此情况下,优选所述非保守氨基酸置换不干扰或抑制所述功能变体的生物活性。优选地,所述非保守氨基酸置换增强所述功能变体的生物活性,使得相比母体tcr、多肽或蛋白,所述功能变体的生物活性增加。在本发明的实施方案中,所述功能变体是置换的tcr、多肽或蛋白,其包含:(i)分别置换的cdr3α、α链的可变区,或seq id no:46-56和207、70-80和208、以及94-104和209中任一个的全长α链氨基酸序列;(ii)分别置换的cdr3β、β链的可变区、或seq id no:57-69、81-93和105-117中任一个的全长β链氨基酸序列;或(iii)(i)的氨基酸序列中的任一个与(ii)的氨基酸序列中的任一个组合的一对。
34.例如,在本发明的实施方案中,置换的tcr、多肽或蛋白可包含以下的一个或两个:(a)seq id no:46-56和207(表i)中的任一个的置换的cdr3α氨基酸序列,和(b)seq id no:57-69(表ii)中的任一个的置换的cdr3β氨基酸序列。本发明的实施方案提供了tcr、多肽或蛋白,其具有本文针对本发明其他方面所描述的天然的、未置换的cdr1α、cdr2α、cdr1β、cdr2β和cdr3β氨基酸序列中的任一个或多个,并组合有seq id no:46-56和207的置换的cdr3α氨基酸序列中的任一个。在这方面,本发明的实施方案提供了置换的tcr,其包含seq id no:149-150、207和152-154的全部的氨基酸序列。本发明的另一实施方案提供了tcr、多肽或蛋白,其具有本文针对本发明其他方面所描述的天然的、未置换的cdr1α、cdr2α、cdr3α、cdr1β和cdr2β氨基酸序列中的任一个或多个,并组合有seq id no:57-69的置换的cdr3β氨基酸序列中的任一个。
35.表i
36.[0037][0038]
表ii
[0039]
[0040][0041]
在本发明的实施方案中,seq id no:46-56的各个置换的cdr3α氨基酸序列不包含seq id no:5的天然的、未置换的cdr3α氨基酸序列。在本发明的实施方案中,seq id no:207的置换的cdr3α氨基酸序列不包含seq id no:151的天然的、未置换的cdr3α氨基酸序列。类似地,在本发明的实施方案中,seq id no:57-69的各个置换的cdr3β氨基酸序列不包含seq id no:8的天然的、未置换的cdr3β氨基酸序列。
[0042]
本发明的实施方案提供了置换的tcr、多肽或蛋白,其包含以下的一个或两个:(i)
包含seq id no:70-80和208(表iii)中的任一个的氨基酸序列的置换的α链可变区,和(ii)包含seq id no:81-93(表iv)中的任一个的氨基酸序列的置换的β链可变区。本发明的实施方案提供了tcr、多肽或蛋白,其具有本文针对本发明其他方面所描述的天然的、未置换的β链可变区中的任一个,并组合有seq id no:70-80和208的置换的α链可变区氨基酸序列的任一个。本发明的另一实施方案提供了tcr、多肽或蛋白,其具有本文针对本发明其他方面所描述的天然的、未置换的α链可变区中的任一个,并组合有seq id no:81-93的置换的β链可变区氨基酸序列的任一个。
[0043]
表iii
[0044]
[0045][0046]
表iv
[0047]
[0048][0049]
[0050]
在本发明的实施方案中,seq id no:70-80的各个置换的α链可变区氨基酸序列不包含seq id no:9的天然的、未置换的α链可变区氨基酸序列。在本发明的实施方案中,seq id no:208的置换的α链可变区氨基酸序列不包含seq id no:155的天然的、未置换的α链可变区氨基酸序列。类似地,在本发明的实施方案中,seq id no:81-93的各个置换的β链可变区氨基酸序列不包含seq id no:10的天然的、未置换的β链可变区氨基酸序列。
[0051]
本发明的实施方案提供了置换的tcr、多肽或蛋白,其包含以下的一个或两个:(i)包含seq id no:94-104和209(表v)中的任一个的氨基酸序列的置换的全长α链,和(ii)包含seq id no:105-117(表vi)中的任一个的氨基酸序列的置换的全长β链。本发明的实施方案提供了tcr、多肽或蛋白,其具有本文针对本发明其他方面所描述的天然的、未置换的全长β链序列中的任一个,并组合有94-104和209的置换的全长α链氨基酸序列中的任一个。本发明的另一实施方案提供了tcr、多肽或蛋白,其具有本文针对本发明其他方面所描述的天然的、未置换的全长α链中的任一个,并组合有105-117的置换的全长β链序列中的任一个。
[0052]
表v
[0053]
[0054][0055]
表vi
[0056]
[0057]
[0058][0059]
在本发明的实施方案中,seq id no:94-104的各个置换的全长α链氨基酸序列不包含seq id no:11的天然的、未置换的全长α链氨基酸序列。在本发明的实施方案中,seq id no:209的置换的全长α链氨基酸序列不包含seq id no:157的天然的、未置换的全长α链氨基酸序列。类似地,在本发明的实施方案中,seq id no:105-117的各个置换的全长β链氨基酸序列不包含seq id no:12的天然的、未置换的全长β链氨基酸序列。
[0060]
所述tcr、多肽或蛋白可基本上由本文所述的指定的一个或多个氨基酸序列组成,使得所述tcr、多肽或蛋白的其他组分如其他氨基酸,不会实质上改变所述tcr、多肽或蛋白的生物活性。在这方面,本发明的tcr、多肽或蛋白可以例如基本上由于以下的氨基酸序列组成:seq id no:11、seq id no:12、seq id no:133、seq id no:134、seq id no:145、seq id no:146、seq id no:157、seq id no:158、seq id no:209、seq id no:11和12、seq id no:133和134、seq id no:145和146、seq id no:157和158、或seq id no:158和209。同样,例如本发明的tcr、多肽或蛋白可以基本上由于以下的氨基酸序列组成:seq id no:9、seq id no:10、seq id no:131、seq id no:132、seq id no:143、seq id no:144、seq id no:155、seq id no:156、seq id no:208、seq id no:9和10、seq id no:131和132、seq id no:143和144、seq id no:155和156、或seq id no:156和208。而且,本发明的tcr、多肽或蛋白可以基本上由于以下的氨基酸序列组成:(a)seq id no:3(α链的cdr1)、seq id no:4(α链的cdr2)、seq id no:5(α链的cdr3)、seq id no:6(β链的cdr1)、seq id no:7(β链的cdr2)、seq id no:8(β链的cdr3)、或其任意组合,例如seq id no:3-5;6-8;或3-8;(b)seq id no:125(α链的cdr1)、seq id no:126(α链的cdr2)、seq id no:127(α链的cdr3)、seq id no:128(β链的cdr1)、seq id no:129(β链的cdr2)、seq id no:130(β链的cdr3)、或其任意组合,例如seq id no:125-127;128-130;或125-130;(c)seq id no:137(α链的cdr1)、seq id no:138(α链的cdr2)、seq id no:139(α链的cdr3)、seq id no:140(β链的cdr1)、seq id no:141(β链的cdr2)、seq id no:142(β链的cdr3)、或其任意组合,例如seq id no:137-139;140-142;或137-142;(d)seq id no:149(α链的cdr1)、seq id no:150(α链的cdr2)、seq id no:151(α链的cdr3)、seq id no:152(β链的cdr1)、seq id no:153(β链的cdr2)、seq id no:154(β链的cdr3)、或其任意组合,例如seq id no:149-151;152-154;或149-154;或(e)seq id no:149(α链的cdr1)、seq id no:150(α链的cdr2)、seq id no:207(置换
的α链的cdr3)、seq id no:152(β链的cdr1)、seq id no:153(β链的cdr2)、seq id no:154(β链的cdr3)、或其任意组合,例如seq id no:149-150和207;152-154;或149-150、207和152-154。
[0061]
本发明还提供了包含任何本文所述的tcr的功能部分的多肽。如本文所用,术语“多肽”包括寡肽并且是指由一个或多肽键连接的氨基酸的单链。
[0062]
对于本发明的多肽,所述功能部分可为包含其作为部分的tcr的连续氨基酸的任何部分,条件是所述功能部分能特异性结合突变的靶标如突变的kras。术语“功能部分”当提及tcr使用时是指本发明的tcr的任何部分或片段,所述部分或片段保留了所述部分或片段所来源的tcr(母体tcr)的生物活性。功能部分涵盖,例如tcr的那些部分,所述部分保留了以与母体tcr类似的程度、相同的程度或比母体tcr更高的程度特异性结合突变的靶标如突变的kras(例如,以hla-a11-依赖性方式)或检测、治疗或预防癌症的能力。相对于母体tcr,所述功能部分可包含例如母体tcr的约10%、25%、30%、50%、68%、80%、90%、95%或更多。
[0063]
所述功能部分可在该部分的氨基端或羧基端或两端包含另外的氨基酸,所述另外的氨基酸不存在于母体tcr的氨基酸序列中。可取的是,所述另外的氨基酸不干扰所述功能部分的生物功能,例如,特异性结合突变的靶标如突变的kras;和/或具有检测癌症,治疗或预防癌症的能力等。更可取的是,与母体tcr或其功能变体的生物活性相比,所述另外的氨基酸增强了生物活性。
[0064]
所述多肽可包含本发明的tcr的α和β链的任一个或两个的功能部分,如包含本发明tcr的α链和/或β链可变区的cdr1、cdr2和cdr3中的一个或多个的功能部分。在本发明的实施方案中,所述多肽可包含含有以下的氨基酸序列的功能部分:(a)seq id no:3(α链的cdr1)、4(α链的cdr2)、5(α链的cdr3)、6(β链的cdr1)、7(β链的cdr2)、8(β链的cdr3)、或其组合;(b)seq id no:125(α链的cdr1)、126(α链的cdr2)、127(α链的cdr3)、128(β链的cdr1)、129(β链的cdr2)、130(β链的cdr3)、或其组合;(c)seq id no:137(α链的cdr1)、138(α链的cdr2)、139(α链的cdr3)、140(β链的cdr1)、141(β链的cdr2)、142(β链的cdr3)、或其组合;(d)seq id no:149(α链的cdr1)、150(α链的cdr2)、151(α链的cdr3)、152(β链的cdr1)、153(β链的cdr2)、154(β链的cdr3)、或其组合;或(e)seq id no:149(α链的cdr1)、150(α链的cdr2)、207(置换的α链的cdr3)、152(β链的cdr1)、153(β链的cdr2)、154(β链的cdr3)、或其组合。优选地,本发明的多肽包含含有以下的氨基酸序列的功能部分:seq id no:3-5;6-8;125-127;128-130;137-139;140-142;149-151;152-154;seq id no:3-8的全部;seq id no:125-130的全部;seq id no:137-142的全部;seq id no:149-154的全部;或seq id no:149-150、207和152-154的全部。更优选地,所述多肽包含含有以下的氨基酸序列的功能部分:seq id no:3-8的全部;seq id no:125-130的全部;seq id no:137-142的全部;seq id no:149-154的全部;或seq id no:149-150、207和152-154的全部。
[0065]
在本发明的实施方案中,本发明的多肽可包含例如本发明的tcr或其功能变体的可变区,所述可变区包含以上所列的cdr区的组合。在这方面,所述多肽可包含以下的氨基酸序列:seq id no:9(α链的可变区)、seq id no:10(β链的可变区)、seq id no:131(α链的可变区)、seq id no:132(β链的可变区)、seq id no:143(α链的可变区)、seq id no:144(β链的可变区)、seq id no:155(α链的可变区)、seq id no:156(β链的可变区)、seq id no:
208(置换的α链的可变区)、seq id no:9和10、seq id no:131和132、seq id no:143和144、seq id no:155和156、或seq id no:208和156。优选地,所述多肽包含以下的氨基酸序列:seq id no:9和10、seq id no:131和132、seq id no:143和144、seq id no:155和156、或seq id no:208和156。
[0066]
在本发明的实施方案中,本发明的多肽还可包含以上所列的本发明的tcr或其功能变体的恒定区。在这方面,所述多肽可包含以下的氨基酸序列:seq id no:13(α链的恒定区)、seq id no:14(β链的恒定区)、seq id no:135(α链的恒定区)、seq id no:136(β链的恒定区)、seq id no:147(α链的恒定区)、seq id no:148(β链的恒定区)、seq id no:159(α链的恒定区)、seq id no:160(β链的恒定区)、seq id no:13和14、seq id no:135和136、seq id no:147和148、或seq id no:159和160。优选地,所述多肽包含以下的氨基酸序列:seq id no:13和14、seq id no:135和136、seq id no:147和148、或seq id no:159和160。
[0067]
在本发明的实施方案中,本发明的多肽可包含本发明的tcr或其功能变体的可变区和恒定区的组合。在这方面,所述多肽可包含:(a)以下的氨基酸序列:seq id no:9(α链的可变区)和seq id no:13(α链的恒定区)、seq id no:10(β链的可变区)和seq id no:14(β链的恒定区)、或seq id no:9、10、13和14的全部;(b)以下的氨基酸序列:seq id no:131(α链的可变区)和seq id no:135(α链的恒定区)、seq id no:132(β链的可变区)和seq id no:136(β链的恒定区)、或seq id no:131、132、135和136的全部;(c)以下的氨基酸序列:seq id no:143(α链的可变区)和seq id no:147(α链的恒定区)、seq id no:144(β链的可变区)和seq id no:148(β链的恒定区)、或seq id no:143、144、147和148的全部;(d)以下的氨基酸序列:seq id no:155(α链的可变区)和seq id no:159(α链的恒定区)、seq id no:156(β链的可变区)和seq id no:160(β链的恒定区)、或seq id no:155、156、159和160的全部;或(e)以下的氨基酸序列:seq id no:208(置换的α链的可变区)和seq id no:159(α链的恒定区)、seq id no:156(β链的可变区)和seq id no:160(β链的恒定区)、或seq id no:208、156、159和160的全部。优选地,所述多肽包含以下的氨基酸序列:seq id no:9、10、13和14的全部;seq id no:131、132、135和136的全部;seq id no:143、144、147和148的全部;seq id no:155、156、159和160的全部;或seq id no:208、156、159和160的全部。
[0068]
在本发明的实施方案中,本发明的多肽可包含任何本文所述的cdr区和本发明的tcr的恒定区的组合。在这方面,所述多肽可包含以下的氨基酸序列:seq id no:3-5和13的全部,seq id no:6-8和14的全部,seq id no:3-8和13-14的全部;seq id no:125-127和135的全部,seq id no:128-130和136的全部,seq id no:125-130和135-136的全部,seq id no:137-139和147的全部,seq id no:140-142和148的全部,seq id no:137-142和147-148的全部,seq id no:149-151和159的全部,seq id no:149-150、207和159的全部,seq id no:152-154和160的全部,seq id no:149-154和159-160的全部,或seq id no:149-150、207、152-154和159-160的全部。优选地,所述多肽包含以下的氨基酸序列:seq id no:3-8和13-14的全部,seq id no:125-130和135-136的全部,seq id no:137-142和147-148的全部,seq id no:149-154和159-160的全部,或seq id no:149-150、207、152-154和159-160的全部。
[0069]
在本发明的实施方案中,本发明的多肽可包含本文所述的tcr的α或β链全长。在这方面,本发明的多肽可包含以下的氨基酸序列:seq id no:11、seq id no:12、seq id no:
133、seq id no:134、seq id no:145、seq id no:146、seq id no:157、seq id no:209、seq id no:158、seq id no:11和12、seq id no:133和134、seq id no:145和146、seq id no:157和158、或seq id no:209和158。优选地,所述多肽包含以下的氨基酸序列:seq id no:11和12、seq id no:133和134、seq id no:145和146、seq id no:157和158、或seq id no:209和158。
[0070]
本发明还提供了包含至少一条本文所述的多肽的蛋白。“蛋白”是指包含一条或多条多肽链的分子。
[0071]
在实施方案中,本发明的蛋白可包含:包含seq id no:3-5的氨基酸序列的第一多肽链和包含seq id no:6-8的氨基酸序列的第二多肽链;包含seq id no:125-127的氨基酸序列的第一多肽链和包含seq id no:128-130的氨基酸序列的第二多肽链;包含seq id no:137-139的氨基酸序列的第一多肽链和包含seq id no:140-142的氨基酸序列的第二多肽链;包含seq id no:149-151的氨基酸序列的第一多肽链和包含seq id no:152-154的氨基酸序列的第二多肽链;或包含seq id no:149-150和207的氨基酸序列的第一多肽链和包含seq id no:152-154的氨基酸序列的第二多肽链。可选地或此外,本发明的蛋白可包含:包含seq id no:9的氨基酸序列的第一多肽链和包含seq id no:10的氨基酸序列的第二多肽链;包含seq id no:131的氨基酸序列的第一多肽链和包含seq id no:132的氨基酸序列的第二多肽链;包含seq id no:143的氨基酸序列的第一多肽链和包含seq id no:144的氨基酸序列的第二多肽链;包含seq id no:155的氨基酸序列的第一多肽链和包含seq id no:156的氨基酸序列的第二多肽链;或包含seq id no:208的氨基酸序列的第一多肽链和包含seq id no:156的氨基酸序列的第二多肽链。所述蛋白例如可包含:(a)包含seq id no:9和13两者或seq id no:3-5和13的全部的氨基酸序列的第一多肽链和包含seq id no:10和14两者或seq id no:6-8和14的全部的氨基酸序列的第二多肽链;(b)包含seq id no:131和135两者或seq id no:125-127和135的全部的氨基酸序列的第一多肽链和包含seq id no:132和136两者或seq id no:128-130和136的全部的氨基酸序列的第二多肽链;(c)包含seq id no:143和147两者或seq id no:137-139和147的全部的氨基酸序列的第一多肽链和包含seq id no:144和148两者或seq id no:140-142和148的全部的氨基酸序列的第二多肽链;(d)包含seq id no:155和159两者或seq id no:149-151和159的全部的氨基酸序列的第一多肽链和包含seq id no:156和160两者或seq id no:152-154和160的全部的氨基酸序列的第二多肽链;或(e)包含seq id no:208和159两者或seq id no:149-150、207和159的全部的氨基酸序列的第一多肽链和包含seq id no:156和160两者或seq id no:152-154和160的全部的氨基酸序列的第二多肽链。可选地或此外,本发明的蛋白可包含:(a)包含seq id no:11的氨基酸序列的第一多肽链和包含seq id no:12的氨基酸序列的第二多肽链;(b)包含seq id no:133的氨基酸序列的第一多肽链和包含seq id no:134的氨基酸序列的第二多肽链;(c)包含seq id no:145的氨基酸序列的第一多肽链和包含seq id no:146的氨基酸序列的第二多肽链;(d)包含seq id no:157的氨基酸序列的第一多肽链和包含seq id no:158的氨基酸序列的第二多肽链;或(e)包含seq id no:209的氨基酸序列的第一多肽链和包含seq id no:158的氨基酸序列的第二多肽链。在此情况下,本发明的蛋白可为tcr。可选地,如果例如所述蛋白包含含有以下的氨基酸序列的单条多肽链:seq id no:11和12、seq id no:133和134、seq id no:145和146、seq id no:157和158、
或seq id no:209和158,或者如果所述蛋白的第一和/或第二多肽链还包含其它氨基酸序列,例如编码免疫球蛋白或其部分的氨基酸序列,则本发明的蛋白可以为融合蛋白。在这方面,本发明还提供了包含至少一种本文所述的本发明多肽以及至少一种其它多肽的融合蛋白。其它多肽可以作为融合蛋白的单独的多肽存在,或可以以这样的多肽存在:其与本文所述的本发明多肽之一在框内(串联)表达。其它多肽可以编码任何肽分子或蛋白分子或其部分,包括但不限于:免疫球蛋白、cd3、cd4、cd8、mhc分子、cd1分子,例如cd1a、cd1b、cd1c、cd1d等。
[0072]
融合蛋白可以包含一个或多个拷贝的本发明多肽和/或一个或多个拷贝的其它多肽。例如,融合蛋白可以包含1、2、3、4、5或更多拷贝的本发明的多肽和/或其它多肽。制备融合蛋白的合适的方法为本领域已知,并且包括例如重组方法。
[0073]
在本发明的一些实施方案中,本发明的tcr、多肽和蛋白可被表达为含有连接α链和β链的接头肽的单个蛋白。在这方面,包含以下的本发明的tcr、多肽和蛋白还可包含接头肽:seq id no:11和12,seq id no:133和134,seq id no:145和146,seq id no:157和158,seq id no:209和158,seq id no:9和10,seq id no:131和132,seq id no:143和144,seq id no:155和156,seq id no:208和156,seq id no:3-8的全部,seq id no:125-130的全部,seq id no:137-142的全部,seq id no:149-154的全部,seq id no:9、10、13和14的全部,seq id no:131、132、135和136的全部,seq id no:143、144、147和148的全部,seq id no:155、156、159和160的全部,seq id no:208、156、159和160的全部,seq id no:3-8和13-14的全部,seq id no:125-130和135-136的全部,seq id no:137-142和147-148的全部,seq id no:149-154和159-160的全部,或seq id no:149-150、207、152-154和159-160的全部。所述接头肽可有利地促进宿主细胞中重组tcr、多肽和/或蛋白的表达。所述接头肽可包含任何合适的氨基酸序列。在本发明的实施方案中,所述tcr、多肽或蛋白包含自切割的病毒接头肽。例如,所述接头肽可包含seq id no:28。当由宿主细胞来表达包含所述接头肽的构建体时,所述接头肽可被切割而产生分离的α和β链。在本发明的实施方案中,所述tcr、多肽或蛋白可包含这样的氨基酸序列,其包含全长α链、全长β链和位于α和β链之间的接头肽(例如,seq id no:45(抗-kras g12d tcr)、seq id no:162(抗-kras g12d tcr)、seq id no:201(抗-kras g12v tcr)、或seq id no:203(抗-kras g12v tcr)的氨基酸序列)。
[0074]
本发明的蛋白可以为包含至少一种本文所述的本发明多肽的重组抗体。如本文所用,“重组抗体”是指包含至少一种本发明的多肽和抗体或其部分的多肽链的重组(例如,基因工程改造的)蛋白。抗体或其部分的多肽可以是抗体的重链、轻链、重链或轻链的可变区或恒定区、单链可变片段(scfv)或fc、fab或f(ab)2'片段等。抗体或其部分的多肽链可以作为重组抗体的单独的多肽存在。可选地,抗体或其部分的多肽链可以以这样的多肽存在:其与本发明的多肽在框内(串联)表达。抗体或其部分的多肽可以为任何抗体或任何抗体片段(包括本文所述的任何抗体和抗体片段)的多肽。
[0075]
本发明的tcr、多肽和蛋白(包括其功能变体)可以为任何长度,即可以包含任何数目的氨基酸,前提是所述tcr、多肽或蛋白(或其功能变体)保留它们的生物活性,例如,特异性结合突变的靶标如突变的kras、检测哺乳动物中的癌症、或治疗或预防哺乳动物中的癌症等的能力。例如,多肽可以为约50至约5000个氨基酸的长度,如50、70、75、100、125、150、175、200、300、400、500、600、700、800、900、1000或更多个氨基酸的长度。在这方面,本发明
的多肽也包括寡肽。
[0076]
本发明的tcr、多肽和蛋白可以包含代替一个或多个天然存在的氨基酸的合成氨基酸。此类合成氨基酸为本领域已知的,并且包括例如氨基环己烷羧酸、正亮氨酸、α-氨基正癸酸、高丝氨酸、s-乙酰基氨甲基-半胱氨酸、反式-3-羟脯氨酸和反式-4-羟脯氨酸、4-氨基苯丙氨酸、4-硝基苯丙氨酸、4-氯苯丙氨酸、4-羧基苯丙氨酸、β-苯基丝氨酸β-羟基苯丙氨酸、苯甘氨酸、α-萘基丙氨酸、环己基丙氨酸、环己基甘氨酸、二氢吲哚-2-羧酸、1,2,3,4-四氢异喹啉-3-羧酸、氨基丙二酸、氨基丙二酸单酰胺、n
’‑
苄基-n
’‑
甲基-赖氨酸、n’,n
’‑
二苄基-赖氨酸、6-羟赖氨酸、鸟氨酸、α-氨基环戊烷羧酸、α-氨基环己烷羧酸、α-氨基环庚烷羧酸、α-(2-氨基-2-降莰烷)-羧酸、α,γ-二氨基丁酸、α,β-二氨基丙酸、高苯丙氨酸和α-叔丁基甘氨酸。
[0077]
本发明的tcr、多肽和蛋白(包括其功能变体)可以被糖基化、酰胺化、羧化、磷酸化、酯化、n-酰化、经由例如二硫桥而环化、或被转化成酸加成盐和/或任选地二聚化或聚合或缀合。
[0078]
本发明的tcr、多肽和/或蛋白可以通过本领域已知的方法获得如从头合成。另外,多肽和蛋白可以利用标准的重组方法使用本文所述的核酸重组产生。参见,例如,green和sambrook,molecular cloning:a laboratory manual,4
th ed.,cold spring harbor press,cold spring harbor,ny(2012)。可选地,本文所述的tcr、多肽和/或蛋白(包括其功能变体)可以通过诸如synpep(dublin,ca)、peptide technologies corp.(gaithersburg,md)和multiple peptide systems(san diego,ca)的公司商业合成。在这方面,本发明的tcr、多肽和蛋白可以为合成的、重组的、分离的和/或纯化的。
[0079]
包括在本发明范围内的是缀合物,例如,包含本发明的tcr、多肽或蛋白、核酸、重组表达载体、宿主细胞、宿主细胞群和抗体或其抗原结合部分中任一种的生物缀合物。缀合物以及合成缀合物的方法通常为本领域已知的。
[0080]
本发明的实施方案提供了包含编码本文所述的tcr、多肽或蛋白中的任一种的核苷酸序列的核酸。如本文所用,“核酸”包括“多核苷酸”“寡核苷酸”和“核酸分子”,并且通常意指dna或rna的聚合物,其可为单链或双链的,合成的或由天然来源获得的(例如分离的和/或纯化的),其可以含有天然的、非天然的或改变的核苷酸,且其可以含有天然的、非天然的或改变的核苷酸间连键,如氨基磷酸酯键或硫代磷酸酯键替代未修饰的寡核苷酸的核苷酸之间存在的磷酸二酯。在实施方案中,所述核酸包括互补的dna(cdna)。通常优选的是不包含任何插入、缺失、倒置和/或置换的核酸。然而,在一些情况下,如本文所讨论的,包含一个或多个插入、缺失、倒置和/或置换的核酸可能是合适的。
[0081]
优选地,本发明的核酸为重组体。如本文所用,术语“重组体”是指:(i)通过将天然或合成的核酸片段与可以在活细胞中复制的核酸分子连接而在活细胞外构建的分子,或(ii)由以上(i)中所述的那些分子进行复制所产生的分子。为了本文的目的,所述复制可为体外复制或体内复制。
[0082]
可以使用本领域已知的程序,基于化学合成和/或酶促连接反应构建所述核酸。参见,例如,green和sambrook et al.,同上。例如,核酸可以使用天然存在的核苷酸或为增加分子的生物稳定性或增加杂交后形成的双链体的物理稳定性而设计的不同修饰的核苷酸(如,硫代磷酸酯衍生物和吖啶置换的核苷酸),进行化学合成。可以用于生成核酸的修饰的
核苷酸的实例包括但不限于:5-氟尿嘧啶、5-溴尿嘧啶、5-氯尿嘧啶、5-碘尿嘧啶、次黄嘌呤、黄嘌呤、4-乙酰胞嘧啶、5-(羧基羟甲基)尿嘧啶、5-羧甲基氨甲基-2-硫尿苷、5-羧甲基氨甲基尿嘧啶、二氢尿嘧啶、β-d-半乳糖基辫苷(queosine)、肌苷、n
6-异戊烯基腺嘌呤、1-甲基鸟嘌呤、1-甲基肌苷、2,2-二甲基鸟嘌呤、2-甲基腺嘌呤、2-甲基鸟嘌呤、3-甲基胞嘧啶、5-甲基胞嘧啶、n
6-置换的腺嘌呤、7-甲基鸟嘌呤、5-甲基氨甲基尿嘧啶、5-甲氧基氨甲基-2-硫尿嘧啶、β-d-甘露糖基辫苷、5'-甲氧基羧甲基尿嘧啶、5-甲氧基尿嘧啶、2-甲基硫基-n
6-异戊烯基腺嘌呤、尿嘧啶-5-氧基乙酸(v)、怀丁苷(wybutoxosine)、假尿嘧啶、辫苷、2-硫胞嘧啶、5-甲基-2-硫尿嘧啶、2-硫尿嘧啶、4-硫尿嘧啶、5-甲基尿嘧啶、尿嘧啶-5-氧基乙酸甲酯、3-(3-氨基-3-n-2-羧基丙基)尿嘧啶和2,6-二氨基嘌呤。可选地,本发明的一种或多种核酸可以购自诸如macromolecular resources(fort collins,co)和synthegen(houston,tx)的公司。
[0083]
所述核酸可以包含编码本文所述的tcr、多肽或蛋白中的任一种的任何核苷酸序列。在本发明的实施方案中,所述核酸可包含以下的核苷酸序列:(a)seq id no:22(抗-kras g12d tcrα链的cdr1);seq id no:23(抗-kras g12d tcrα链的cdr2)的核苷酸序列;seq id no:24(抗-kras g12d tcrα链的cdr3)的核苷酸序列;seq id no:25(抗-kras g12d tcrβ链的cdr1)的核苷酸序列;seq id no:26(抗-kras g12d tcrβ链的cdr2)的核苷酸序列;或seq id no:27(抗-kras g12d tcrβ链的cdr3)的核苷酸序列;(b)seq id no:164(抗-kras g12d tcrα链的cdr1);seq id no:165(抗-kras g12d tcrα链的cdr2)的核苷酸序列;seq id no:166(抗-kras g12d tcrα链的cdr3)的核苷酸序列;seq id no:167(抗-kras g12d tcrβ链的cdr1)的核苷酸序列;seq id no:168(抗-kras g12d tcrβ链的cdr2)的核苷酸序列;或seq id no:169(抗-kras g12d tcrβ链的cdr3)的核苷酸序列;(c)seq id no:177(抗-kras g12v tcrα链的cdr1);seq id no:178(抗-kras g12v tcrα链的cdr2)的核苷酸序列;seq id no:179(抗-kras g12v tcrα链的cdr3)的核苷酸序列;seq id no:180(抗-kras g12v tcrβ链的cdr1)核苷酸序列;seq id no:181(抗-kras g12v tcrβ链的cdr2)的核苷酸序列;或seq id no:182(抗-kras g12v tcrβ链的cdr3)的核苷酸序列;或(d)seq id no:189(抗-kras g12v tcrα链的cdr1);seq id no:190(抗-kras g12v tcrα链的cdr2)的核苷酸序列;seq id no:191(抗-kras g12v tcrα链的cdr3)的核苷酸序列;seq id no:192(抗-kras g12v tcrβ链的cdr1)的核苷酸序列;seq id no:193(抗-kras g12v tcrβ链的cdr2)的核苷酸序列;或seq id no:194(抗-kras g12v tcrβ链的cdr3)核苷酸序列。优选地,所述核酸包含以下的核苷酸序列:seq id no:22-24的全部;seq id no:25-27的全部;seq id no:22-27的全部;seq id no:164-166的全部;seq id no:167-169的全部;seq id no:164-169的全部;seq id no:177-179的全部;seq id no:180-182的全部;seq id no:177-182的全部;seq id no:189-191的全部;seq id no:192-194的全部;seq id no:189-194的全部。在特别优选的实施方案中,所述核酸包含以下的核苷酸序列:seq id no:22-27的全部;seq id no:164-169的全部;seq id no:177-182的全部;或seq id no:189-194的全部。在本发明的实施方案中,所述核酸可包含以下的核苷酸序列:(a)seq id no:15(抗-kras g12d tcrα链的可变区);seq id no:16(抗-kras g12d tcrβ链的可变区);或seq id no:15和16;(b)seq id no:170(抗-kras g12d tcrα链的可变区);seq id no:171(抗-kras g12d tcrβ链的可变区);或seq id no:170和171;(c)seq id no:183(抗-kras g12v tcrα
链的可变区);seq id no:184(抗-kras g12v tcrβ链的可变区);或seq id no:183和184;(d)seq id no:195(抗-kras g12vtcrα链的可变区);seq id no:196(抗-kras g12v tcrβ链的可变区);或seq id no:195和196。优选地,所述核酸包含以下的核苷酸序列:seq id no:15和16;seq id no:170和171;seq id no:183和184;或seq id no:195和196。在本发明的另一实施方案中,所述核酸可包含以下的核苷酸序列:(a)seq id no:17(全长抗-kras g12d tcrα链);seq id no:18(全长抗-kras g12d tcrβ链);或seq id no:17和18;(b)seq id no:172(全长抗-kras g12d tcrα链);seq id no:173(全长抗-kras g12d tcrβ链);或seq id no:172和173;(c)seq id no:185(全长抗-kras g12v tcr α链);seq id no:186(全长抗-kras g12v tcrβ链);或seq id no:185和186;或(d)seq id no:197(全长抗-kras g12v tcrα链);seq id no:198(全长抗-kras g12v tcrβ链);或seq id no:197和198。优选地,所述核酸包含以下的核苷酸序列:seq id no:17和18;seq id no:172和173;seq id no:185和186;或seq id no:197和198。
[0084]
在本发明的实施方案中,所述核酸还包含编码tcrα或β链的恒定区的核苷酸序列。在这方面,本文描述的核酸中的任意核酸还可包含以下的核苷酸序列:(a)seq id no:19(抗-kras g12d tcrα链的恒定区);seq id no:20(抗-kras g12d tcrβ链的恒定区);或seq id no:19和20;(b)seq id no:174(抗-kras g12d tcrα链的恒定区);seq id no:175(抗-kras g12d tcrβ链的恒定区);或seq id no:174和175;(c)seq id no:187(抗-kras g12v tcrα链的恒定区);seq id no:188(抗-kras g12v tcrβ链的恒定区);或seq id no:187和188;或(d)seq id no:199(抗-kras g12v tcrα链的恒定区);seq id no:200(抗-kras g12v tcrβ链的恒定区);或seq id no:199和200。优选地,所述核酸包含以下的核苷酸序列:seq id no:15和19;seq id no:16和20;seq id no:15-16和19-20的全部;seq id no:22-24和19的全部;seq id no:25-27和20的全部;seq id no:22-27和19-20的全部;seq id no:170和174;seq id no:171和175;seq id no:170-171和174-175的全部;seq id no:164-166和174的全部;seq id no:167-169和175的全部;seq id no:164-169和174-175的全部;seq id no:183和187;seq id no:184和188;seq id no:183-184和187-188的全部;seq id no:177-179和187;seq id no:180-182和188的全部;seq id no:177-182和187-188的全部;seq id no:195和199;seq id no:196和200;seq id no:195-196和199-200的全部;seq id no:189-191和199的全部;seq id no:192-194和200的全部;或seq id no:189-194和199-200的全部。在特别优选的实施方案中,所述核酸包含以下的核苷酸序列:seq id no:15-16和19-20的全部;seq id no:22-27和19-20的全部;seq id no:170-171和174-175的全部;seq id no:164-169和174-175的全部;seq id no:183-184和187-188的全部;seq id no:177-182和187-188的全部;seq id no:195-196和199-200的全部;或seq id no:189-194和199-200的全部。
[0085]
本文描述的任何核酸还可包含编码接头肽的核苷酸序列。编码接头肽的核苷酸序列可包含任何合适的核苷酸序列。例如,编码接头肽的核苷酸序列可包含seq id no:44的核苷酸序列。
[0086]
在本发明的实施方案中,包含以下的核苷酸序列的核酸编码鼠tcr:seq id no:22-24的全部;seq id no:25-27的全部;seq id no:22-27的全部;seq id no:15和16;seq id no:17和18;seq id no:15和19;seq id no:16和20;seq id no:15-16和19-20的全部;
seq id no:22-24和19的全部;seq id no:25-27和20的全部;seq id no:22-27和19-20的全部;seq id no:164-169的全部;seq id no:170和171;seq id no:172和173;seq id no:164-169和174-175的全部;seq id no:170-171和174-175的全部;seq id no:177-182的全部;seq id no:183-184;seq id no:185-186;seq id no:177-182和187-188的全部;seq id no:183-184和187-188的全部;seq id no:189-194的全部;seq id no:195-196;seq id no:197-198;seq id no:189-194和199-200的全部;或seq id no:195-196和199-200的全部。
[0087]
本发明还提供了核酸,其包含与本文所述的任何核酸的核苷酸序列互补的核苷酸序列,或包含在严紧条件下与本文所述的任何核酸的核苷酸序列杂交的核苷酸序列。
[0088]
在严紧条件下杂交的核苷酸序列优选在高严紧条件下杂交。“高严紧条件”意指核苷酸序列以可检测地强于非特异性杂交的量与靶序列(本文所述的任何核酸的核苷酸序列)特异性杂交。高严紧条件包括这样的条件:其可区分具有精确互补序列的多核苷酸,或仅含有少数分散错配的多核苷酸,所述分散错配来自碰巧具有匹配该核苷酸序列的一些小区域(例如,3-10个碱基)的随机序列。相比14-17个或更多个碱基的全长互补物,此类小的互补区域更容易熔解,并且高严紧杂交使得它们易于被区分。相对高的严紧条件将包括,例如,低盐和/或高温条件,如约50-70℃温度下通过约0.02-0.1m nacl或等同物提供的条件。此类高严紧条件容许该核苷酸序列与模板或靶链之间很少(如果有的话)的错配,并且特别适于检测任何本发明tcr的表达。通常认为,可以通过加入增加量的甲酰胺使条件更严紧。
[0089]
本发明还提供包含与本文所述的任何核酸具有至少约70%或更多,例如约80%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%或约99%一致性的核苷酸序列的核酸。在这方面,所述核酸可基本上由本文所述的任何核酸序列组成。
[0090]
本发明的核酸可以掺入至重组表达载体中。在这方面,本发明提供了包含本发明的任何核酸的重组表达载体。在本发明的实施方案中,所述重组表达载体包含编码α链、β链和接头肽的核苷酸序列。例如,在实施方案中,所述重组表达载体包含以下核苷酸序列:seq id no:21(编码α和β链seq id no:11和12以及位于它们之间的接头);seq id no:163(编码α和β链seq id no:157和158以及位于它们之间的接头);seq id no:202(编码α和β链seq id no:145和146以及位于它们之间的接头);或seq id no:176(编码α和β链seq id no:133和134以及位于它们之间的接头)。
[0091]
为了本文的目的,术语“重组表达载体”意指基因修饰的寡核苷酸或多核苷酸构建体,当该构建体包含编码mrna、蛋白、多肽或肽的核苷酸序列,并且在足以使得在宿主细胞内表达mrna、蛋白、多肽或肽的条件下将载体与宿主细胞接触时,所述构建体允许该宿主细胞表达mrna、蛋白、多肽或肽。本发明的载体并非整个是天然存在的。然而,载体的部分可以为天然存在的。本发明的重组表达载体可以包含任何类型的核苷酸,包括但不限于dna和rna,其可为单链或双链的、合成的或部分由天然来源获得,并且可以含有天然的、非天然的或改变的核苷酸。所述重组表达载体可以包含天然存在的、非天然存在的核苷酸间连键,或这两种类型的连键。优选地,所述非天然存在的或改变的核苷酸或核苷酸间连键不会阻碍载体的转录或复制。
[0092]
本发明的重组表达载体可以为任何合适的重组表达载体,并且可被用于转化或转染任何合适的宿主细胞。合适的载体包括设计用于繁殖和扩增或用于表达或这两者的那些
载体,如质粒和病毒。载体可以选自:puc系列(fermentas life sciences)、pbluescript系列(stratagene,lajolla,ca)、pet系列(novagen,madison,wi)、pgex系列(pharmacia biotech,uppsala,sweden)和pex系列(clontech,palo alto,ca)。也可使用噬菌体载体,如λgt10、λgt11、λzapii(stratagene)、λembl4和λnm1149。植物表达载体的实例包括pbi01、pbi101.2、pbi101.3、pbi121和pbin19(clontech)。动物表达载体的实例包括peuk-cl、pmam和pmamneo(clontech)。优选地,所述重组表达载体为病毒载体,例如,逆转录病毒载体。在特别优选的实施方案中,所述重组表达载体为msgv1载体。
[0093]
本发明的重组表达载体可以使用在例如green和sambrook et al.(同上)中描述的标准重组dna技术进行制备。可以将表达载体的构建体(其为环状或线性的)制备成含有在原核或真核宿主细胞中有功能的复制系统。复制系统可以来源于,例如colel、2μ质粒、λ、sv40、牛乳头瘤病毒等。
[0094]
可取的是,重组表达载体包含调控序列,如转录和翻译起始密码子和终止密码子,视情况而定并且考虑该载体是基于dna还是rna的,其对待引入该载体的宿主细胞类型(例如细菌、真菌、植物或动物)具有特异性。
[0095]
所述重组表达载体可以包含一个或多个标记基因,所述标记基因允许对转化或转染的宿主细胞进行选择。标记基因包括杀菌剂抗性,例如对抗生素、重金属等的抗性,与营养缺陷型宿主细胞互补以提供原养型等。本发明表达载体的合适标记基因包括,例如新霉素/g418抗性基因、潮霉素抗性基因、组氨醇抗性基因、四环素抗性基因和氨苄青霉素抗性基因。
[0096]
所述重组表达载体可以包含天然或非天然的启动子,该启动子可操作地连接至编码tcr、多肽或蛋白的核苷酸序列或可操作地连接至与编码tcr、多肽或蛋白的核苷酸序列互补或杂交的核苷酸序列。对启动子的选择,例如强、弱、可诱导的、组织特异的和发育特异的,在本领域普通技术人员的能力内。类似地,核苷酸序列与启动子的组合也在本领域技术人员的能力内。启动子可以为非病毒启动子或病毒启动子,例如巨细胞病毒(cmv)启动子、sv40启动子、rsv启动子或存在于鼠干细胞病毒的长末端重复序列中的启动子。
[0097]
本发明的重组表达载体可以被设计用于瞬时表达、用于稳定表达、或用于这两者。另外,可以制备用于组成型表达或用于诱导型表达的重组表达载体。
[0098]
此外,可以制备包含自杀基因的重组表达载体。如本文所用,术语“自杀基因”是指导致表达自杀基因的细胞死亡的基因。自杀基因可以为赋予表达该基因的细胞对药剂如药物的敏感性,并且当该细胞与所述药剂接触或暴露于所述药剂时引起该细胞死亡的基因。自杀基因为本领域已知的,并且包括例如,单纯性疱疹病毒(hsv)胸苷激酶(tk)基因、胞嘧啶脱氨酶基因、嘌呤核苷磷酸化酶基因和硝基还原酶基因。
[0099]
本发明的另一实施方案还提供了包含本文所述的任何重组表达载体的宿主细胞。如本文所用,术语“宿主细胞”是指可以含有本发明的重组表达载体的任何类型的细胞。所述宿主细胞可以为真核细胞,例如,植物、动物、真菌或藻类,或可以为原核细胞,例如,细菌或原生动物。宿主细胞可以为培养的细胞或原代细胞,即从生物体,例如人直接分离的细胞。宿主细胞可以为贴壁细胞或悬浮细胞,即悬浮生长的细胞。合适的宿主细胞为本领域已知的并且包括,例如,dh5α大肠杆菌细胞、中国仓鼠卵巢细胞、猴vero细胞、cos细胞、hek293细胞等。为了扩增或复制重组表达载体的目的,所述宿主细胞优选为原核细胞,例如,dh5α
细胞。为了产生重组的tcr、多肽或蛋白的目的,所述宿主细胞优选为哺乳动物细胞。最优选地,所述宿主细胞为人细胞。虽然所述宿主细胞可以为任何细胞类型的细胞,可以源于任何类型的组织,并且可以为任何发育阶段的细胞,但宿主细胞优选为外周血淋巴细胞(pbl)或外周血单核细胞(pbmc)。更优选地,所述宿主细胞为t细胞。
[0100]
为了本文的目的,t细胞可为任何t细胞,如培养的t细胞,例如原代t细胞或来自培养的t细胞系如jurkat、suptl等的t细胞,或从哺乳动物获得的t细胞。如果从哺乳动物获得,则t细胞可从许多来源获得,包括但不限于血液、骨髓、淋巴结、胸腺或其它组织或液体。t细胞也可被富集或纯化。优选地,t细胞为人t细胞。t细胞可以为任何类型的t细胞并且可以为任何发育阶段的t细胞,包括但不限于:cd4
+
/cd8
+
双阳性t细胞、cd4
+
辅助性t细胞,例如th1和th2细胞、cd4
+
t细胞、cd8
+
t细胞(例如,细胞毒性t细胞)、肿瘤浸润性淋巴细胞(til)、记忆性t细胞(例如,中心记忆性t细胞和效应记忆性t细胞)、初始t细胞等。
[0101]
本发明还提供了包含至少一种本文所述的宿主细胞的细胞群。所述细胞群可以为异质群体,其除了包含至少一种不包含任何重组表达载体的其它细胞例如宿主细胞(例如t细胞),或t细胞之外的细胞例如b细胞、巨噬细胞、中性粒细胞、红细胞、肝细胞、内皮细胞、上皮细胞、肌肉细胞、脑细胞等之外,还包含含有所述的任何重组表达载体的宿主细胞。可选地,所述细胞群可为大体上同质的群体,其中所述群体主要包含含有所述重组表达载体的宿主细胞(例如,基本上由其组成)。所述群体也可为克隆细胞群,其中该群体的所有细胞为包含重组表达载体的单个宿主细胞的克隆,以使得群体的所有细胞包含所述重组表达载体。在本发明的一实施方案中,所述细胞群为包含含有本文所述重组表达载体的宿主细胞的克隆群体。
[0102]
在本发明的实施方案中,所述群体中细胞的数目可以快速地扩增。t细胞数目的扩增可以通过以下文献中所述的本领域已知的许多方法中的任一种来实现,例如,美国专利8,034,334;美国专利8,383,099;美国专利申请公开号2012/0244133;dudley et al.,j.immunother.,26:332-42(2003);以及riddell et al.,j.immunol.methods,128:189-201(1990)。在实施方案中,通过将t细胞与okt3抗体、il-2和饲养层pbmc(例如,经辐照的同种异体pbmc)培养,来进行t细胞数量的扩增。
[0103]
本发明还提供了抗体或其抗原结合部分,其能特异性结合本文所述的任何tcr的功能部分。优选地,所述功能部分能特异性结合癌症抗原,例如,所述功能部分包含以下氨基酸序列:seq id no:3、125、137或149(α链的cdr1);seq id no:4、126、138或150(α链的cdr2);seq id no:5、127、139、151或207(α链的cdr3);seq id no:6、128、140或152(β链的cdr1);seq id no:7、129、141或153(β链的cdr2);seq id no:8、130、142或154(β链的cdr3);seq id no:9、131、143、155或208(α链的可变区);seq id no:10、132、144或156(β链的可变区);或它们的组合,例如seq id no:3-5;seq id no:6-8;seq id no:3-8;seq id no:9;seq id no:10;seq id no:9-10;seq id no:125-127;seq id no:128-130;seq id no:125-130;seq id no:137-139;seq id no:140-142;seq id no:137-142;seq id no:149-151;seq id no:149-150和207;seq id no:152-154;seq id no:149-154;seq id no:149-150、207和152-154;seq id no:131-132;seq id no:143-144;seq id no:155-156;seq id no:208;或seq id no:208和156。更优选地,所述功能部分包含以下的氨基酸序列:seq id no:3-8、seq id no:9和10、seq id no:125-130、seq id no:137-142、seq id no:
149-154、seq id no:149-150、207和152-154、seq id no:131-132、seq id no:143-144、seq id no:155-156、或seq id no:208和156。在优选的实施方案中,抗体或其抗原结合部分能结合由全部6个cdr(α链的cdr1-3和β链的cdr1-3)形成的表位。所述抗体可以为本领域已知的任何类型的免疫球蛋白。例如,所述抗体可以为任何同种型的抗体,例如,iga、igd、ige、igg、igm等。所述抗体可以为单克隆或多克隆的。所述抗体可以为天然存在的抗体,例如,分离和/或纯化自哺乳动物(例如小鼠、兔、山羊、马、鸡、仓鼠、人等)的抗体。可选地,所述抗体可以为基因工程改造的抗体,例如人源化抗体或嵌合抗体。所述抗体可以为单体形式或聚合形式。另外,所述抗体可以对本发明tcr的功能部分具有任何水平的亲和力或亲合力。可取的是,所述抗体对本发明的tcr的功能部分具有特异性,使得与其它肽或蛋白存在最小的交叉反应。
[0104]
测试抗体结合本发明tcr的任何功能部分或功能变体的能力的方法为本领域已知的,并且包括任何抗体-抗原结合测定,例如放射性免疫测定(ria)、elisa、蛋白质印迹、免疫沉淀和竞争性抑制测定。
[0105]
制备抗体的合适的方法为本领域已知的。例如,标准杂交瘤方法描述在,例如,c.a.janeway et al.(eds.),immunobiology,8
th ed.,garland publishing,new york,ny(2011))中。可选地,其它方法,如ebv-杂交瘤方法、在非人动物中产生抗体的方法和噬菌体载体表达系统为本领域已知的。
[0106]
噬菌体展示也可用于生成本发明的抗体。在这方面,编码抗体的抗原结合可变(v)结构域的噬菌体文库可以使用标准的分子生物学和重组dna技术来生成(参见,例如,green和sambrook et al.(eds.),molecular cloning,a laboratory manual,4
th edition,cold spring harbor laboratory press,new york(2012))。选择能特异性结合期望的抗原的编码具有期望的特异性的可变区的噬菌体,并重建包含所选的可变结构域的完整或部分抗体。将编码该重建的抗体的核酸序列引入合适的细胞系,如用于产生杂交瘤的骨髓瘤细胞,使得所述细胞分泌具有单克隆抗体特性的抗体(参见例如,janeway et al.,同上)。
[0107]
产生人源化抗体的方法是本领域熟知的。抗体也可以通过针对特定的重链和轻链免疫球蛋白基因进行转基因的转基因小鼠产生。此类方法为本领域已知的,并且描述在例如janeway et al.,同上中。
[0108]
本发明还提供了本文所述的任何抗体的抗原结合部分。所述抗原结合部分可以为具有至少一个抗原结合位点的任何部分,如fab、f(ab')2、dsfv、sfv、双链抗体和三链抗体。
[0109]
可以使用常规的重组dna技术方法(参见,如,janeway et al.,同上)生成单链可变区片段(sfv)抗体片段,其由截短的fab片段组成,所述截短的fab片段包含经由合成肽相连接的抗体轻链的可变(v)结构域和抗体重链的v结构域。类似地,二硫键稳定的可变区片段(dsfv)可以通过重组dna技术制备。然而,本发明的抗体片段不限于这些示例性的抗体片段类型。
[0110]
另外,抗体或其抗原结合部分可修饰为包含可检测标记,例如放射性同位素、荧光团(例如异硫氰酸荧光素(fitc)、藻红蛋白(pe))、酶(例如碱性磷酸酶、辣根过氧化物酶)和元素颗粒(例如金颗粒)。
[0111]
本发明的tcr、多肽、蛋白、核酸、重组表达载体、宿主细胞(包括其群体)和抗体(包括其抗原结合部分)可以是分离的和/或纯化的。如本文所用,术语“分离的”意指已经脱离
其天然环境。如本文所用,术语“纯化的”意指纯度已经增加,其中“纯度”为相对术语,并且不一定解释为绝对纯度。例如,纯度可以为至少约50%,可以大于60%、70%、80%、90%、95%或可以为100%。
[0112]
本发明的tcr、多肽、蛋白、核酸、重组表达载体、宿主细胞(包括其群体)和抗体(包括其抗原结合部分),在下文中全部被统称为“本发明的tcr物质”,其可以被配制成组合物,如药物组合物。在这方面,本发明提供了药物组合物,其包含本文所述的tcr、多肽、蛋白、核酸、表达载体、宿主细胞(包括其群体)和抗体(包括其抗原结合部分)中的任一种以及药学上可接受的载体。含有任何本发明的tcr物质的本发明的药物组合物,可以包含多于一种本发明的tcr物质,例如多肽和核酸,或两种或更多种不同的tcr。可选地,所述药物组合物可以包含本发明的tcr物质并组合有另一药物活性剂或药物,如化学治疗剂,例如天冬酰胺酶、白消安、卡铂、顺铂、柔红霉素、阿霉素、氟尿嘧啶、吉西他滨、羟基脲、甲氨蝶呤、紫杉醇、利妥昔单抗(rituximab)、长春碱、长春新碱等。
[0113]
优选地,所述载体为药学上可接受的载体。关于药物组合物,所述载体可以为常规地用于考虑中的本发明的具体tcr物质的那些中的任何一种。此类药学上可接受的载体为本领域技术人员熟知的并且容易被公众获得。优选的是,所述药学上可接受的载体为在使用条件下无有害副作用或毒性的载体。
[0114]
载体的选择将部分由本发明的具体tcr物质以及用于施用本发明tcr物质的具体方法来确定。因此,存在本发明的药物组合物的多种合适的制剂。合适的制剂可以包括任何用于口服、肠胃外、皮下、静脉内、肌内、动脉内、鞘内或腹膜内施用的那些制剂。可以使用多于一种途径来施用本发明的tcr物质,并且在某些情况下,特定的途径可以提供比另一途径更直接且更有效的应答。
[0115]
优选地,本发明的tcr物质通过注射如静脉内注射施用。当本发明的tcr物质为表达本发明的tcr(或其功能变体)的宿主细胞时,用于注射的所述细胞的药学上可接受的载体可以包括任何等渗载体,例如生理盐水(约0.90%w/v的nacl水溶液、约300mosm/l的nacl水溶液、或约9.0g nacl/l水)、normosol r电解质溶液(abbott,chicago,il)、plasma-lyte a(baxter,deerfield,il)、约5%葡萄糖水溶液、或乳酸林格氏液。在实施方案中,药学上可接受的载体补充有人血清白蛋白。
[0116]
为了本发明的目的,施用的本发明tcr物质的量或剂量(例如,本发明的tcr物质为一种或多种细胞时的细胞数目),应足以在合理的时间范围内使受试者或动物产生例如治疗性或预防性应答。例如,本发明的tcr物质的剂量,应在从施用时起约2小时或更久,例如12-24小时或更久的时段内,足以结合癌症抗原(例如,突变的kras)或检测、治疗或预防癌症。在某些实施方案中,时间段甚至可以更久。所述剂量将由本发明的具体tcr物质的功效和动物(例如人)的状况以及待治疗的动物(例如人)的体重来确定。
[0117]
用于确定施用剂量的许多测定为本领域已知的。为了本发明的目的,测定可用于确定待施用于哺乳动物的起始剂量,所述测定包括,将给定剂量的表达本发明tcr、多肽或蛋白的t细胞施用于一组哺乳动物(各自被给予不同剂量的t细胞)中的哺乳动物后,比较靶细胞裂解或由此类t细胞分泌的ifn-γ的程度。在施用某剂量后,靶细胞裂解或ifn-γ分泌的程度可以通过本领域已知的方法测定。
[0118]
本发明tcr物质的剂量,也通过可能伴随本发明具体tcr物质施用的任何不利副作
用的存在、性质和程度来确定。通常,主治医师会考虑多种因素如年龄、体重、总体健康、饮食、性别、待施用的本发明tcr物质、施用途径以及被治疗的癌症的严重程度,来决定用于治疗每个个体患者的本发明tcr物质的剂量。在本发明的tcr物质为细胞群的实施方案中,每次输注施用的细胞数目可以例如从约1
×
106至约1
×
10
12
个细胞或更多进行变化。在某些实施方案中,可以施用少于1
×
106个细胞。
[0119]
本领域普通技术人员将容易理解,本发明的tcr物质可以以许多方式进行修饰,以使得本发明tcr物质的治疗性或预防性功效通过修饰增加。例如,本发明的tcr物质可以直接地或通过桥间接地缀合于靶向部分。将化合物,例如本发明的tcr物质缀合于靶向部分的实践为本领域已知的。如本文所用,术语“靶向部分”是指这样的任何分子或试剂:其特异性识别并结合细胞表面受体,以使得靶向部分引导本发明tcr物质至在其表面表达受体的细胞群的递送。靶向部分包括但不限于抗体或其片段、肽、激素、生长因子、细胞因子以及能结合于细胞表面受体(例如,上皮生长因子受体(egfr)、t细胞受体(tcr)、b-细胞受体(bcr)、cd28、血小板来源的生长因子受体(pdgf)、烟碱乙酰胆碱受体(nachr)等)的任何其它天然或非天然的配体。如本文所用,术语“桥”是指将本发明的tcr物质连接于靶向部分的任何试剂或分子。本领域普通技术人员意识到,本发明的tcr物质上对本发明tcr物质的功能并非必需的位点,是附接桥和/或靶向部分的理想位点,前提是一旦所述桥和/或靶向部分被附接到本发明的tcr物质上,不会干扰本发明tcr物质的功能,即结合突变的靶标如突变的kras或检测、治疗或预防癌症的能力。
[0120]
预期本发明的药物组合物、tcr、多肽、蛋白、核酸、重组表达载体、宿主细胞或细胞群可以用于治疗或预防癌症的方法中。不受特定理论的束缚,认为本发明的tcr能特异性结合突变的靶标如突变的kras,以使得当由细胞表达时,tcr(或相关的本发明多肽或蛋白)能够介导针对表达突变的靶标如突变的kras的靶细胞的免疫应答。在这方面,本发明提供了治疗或预防哺乳动物中癌症的方法,其包括以有效治疗或预防哺乳动物中癌症的量,向哺乳动物施用本文所述的药物组合物、tcr、多肽或蛋白中的任一种,包含编码本文所述的tcr、多肽、蛋白中的任一种的核苷酸序列的任何核酸或重组表达载体,或包含编码本文所述的tcr、多肽或蛋白中的任一种的重组载体的任何宿主细胞或细胞群。
[0121]
本发明的实施方案提供了本文所述的药物组合物、tcr、多肽或蛋白中的任一种,包含编码本文所述的tcr、多肽、蛋白中的任一种的核苷酸序列的任何核酸或重组表达载体,或包含编码本文所述的tcr、多肽或蛋白中的任一种的重组载体的任何宿主细胞或细胞群,用于治疗或预防哺乳动物中的癌症的用途。
[0122]
如本文所用,术语“治疗”和“预防”以及源自于此的词汇,不一定意味着100%或完全治疗或预防。相反,存在不同程度的治疗或预防,其被本领域普通技术人员认为具有潜在的益处或治疗效果。在这方面,本发明方法可以提供任何水平的任何量的对哺乳动物癌症的治疗或预防。此外,本发明方法提供的治疗或预防可以包括对正在治疗或预防的癌症的一种或多种病况或症状的治疗或预防。例如,治疗或预防可以包括促进肿瘤的消退。另外,为了本文的目的,“预防”可以涵盖延迟癌症或其症状或病况的发作。
[0123]
还提供了检测哺乳动物中癌症的存在的方法。所述方法包括(i)将包含来自哺乳动物的一种或多种细胞的样品与本文所述的本发明tcr、多肽、蛋白、核酸、重组表达载体、宿主细胞、细胞群、抗体或其抗原结合部分、或药物组合物中的任一种相接触,从而形成复
合物,以及检测所述复合物,其中检测到复合物指示哺乳动物中癌症的存在。
[0124]
关于本发明的检测哺乳动物中癌症的方法,细胞的样品可为包含全细胞、其裂解物、或全细胞裂解物的一部分,例如细胞核或细胞质部分、全蛋白部分、或核酸部分的样品。
[0125]
为了本发明检测方法的目的,接触可以在相对于哺乳动物的体外或体内发生。优选地,所述接触为体外的。
[0126]
另外,复合物的检测可以通过本领域已知的多种方法进行。例如,本文所述的本发明tcr、多肽、蛋白、核酸、重组表达载体、宿主细胞、细胞群、或抗体或其抗原结合部分可以用可检测标记,如放射性同位素、荧光团(例如异硫氰酸荧光素(fitc)、藻红蛋白(pe))、酶(例如碱性磷酸酶、辣根过氧化物酶)和元素颗粒(例如,金颗粒)进行标记。
[0127]
为了本发明方法的目的,其中当施用宿主细胞或细胞群时,所述细胞可为与哺乳动物同种异体或哺乳动物自体的细胞。优选地,所述细胞为哺乳动物自体的。
[0128]
关于本发明方法,所述癌症可为任何癌症,包括以下的任一种:急性淋巴细胞性癌症、急性骨髓性白血病、腺泡状横纹肌肉瘤、骨癌、脑癌、乳腺癌、肛门癌、肛管癌或直肠肛门癌、眼癌、肝内胆管癌、关节癌、颈癌、胆囊癌或胸膜癌、鼻癌、鼻腔癌或中耳癌、口腔癌、阴道癌、外阴癌、慢性淋巴细胞白血病、慢性骨髓性癌症、结肠癌、结直肠癌、子宫内膜癌、食管癌、宫颈癌、胃肠道类癌肿瘤、胶质瘤、霍奇金淋巴瘤、下咽癌、肾癌、喉癌、肝癌、肺癌、恶性间皮瘤、黑素瘤、多发性骨髓瘤、鼻咽癌、非霍奇金淋巴瘤、口咽癌、卵巢癌、阴茎癌、胰癌、腹膜癌、网膜癌和肠系膜癌、咽癌、前列腺癌、直肠癌、肾癌、皮肤癌、小肠癌、软组织癌、胃癌、睾丸癌、甲状腺癌、子宫癌、输尿管癌和膀胱癌。优选的癌症为胰癌、结直肠癌、肺癌、子宫内膜癌、卵巢癌或前列腺癌。优选地,所述肺癌是肺部腺癌,所述卵巢癌是上皮性卵巢癌,以及所述胰癌是胰腺癌。在另一优选实施方案中,所述癌症是表达vvvgadgvgk(seq id no:2)、vvgadgvgk(seq id no:34)、vvvgavgvgk(seq id no:33)、或vvgavgvgk(seq id no:35)的突变的氨基酸序列的癌症,这些序列存在于突变的人kras、突变的人nras和突变的人hras中。
[0129]
本发明方法提及的哺乳动物可为任何哺乳动物。如本文所用,术语“哺乳动物”是指任何哺乳动物,包括但不限于:啮齿目的哺乳动物如小鼠和仓鼠,以及兔形目的哺乳动物如兔。优选所述哺乳动物来自食肉目,包括猫科动物(猫)和犬科动物(犬)。更优选所述哺乳动物来自偶蹄目包括牛科动物(牛)和猪科动物(猪),或来自奇蹄目包括马科动物(马)。最优选所述哺乳动物来自灵长目、猿(ceboids)目或猴(simoids)目(猴),或来自类人猿亚目(人和类人猿)。特别优选是哺乳动物为人。
[0130]
以下实施例进一步阐述了本发明,但当然不应视为以任何方式限制本发明的范围。
[0131]
实施例1
[0132]
该实施例显示了鼠抗-kras
7-16 g12d 10-mer tcr的分离。
[0133]
采用计算机算法来产生候选的hla-a11*01kras肽。对于该算法,强结合剂的阈值为50nm,以及弱结合剂的阈值为500nm。候选肽如表1所示。
[0134]
表1
[0135][0136][0137]
用g12d 10-mer肽(seq id no:2)使hla-a11转基因小鼠免疫3次。第三次免疫后,移出脾脏和淋巴结,并在体外用不同浓度(1μm、0.1μm和0.01μm)的g12d 10-mer肽培养7天。测试分离自淋巴结(ln)和脾脏培养物的t细胞针对以下细胞的反应性:(i)经转导以表达hla-a11的cos7细胞(cos7/a11),其已经用以下肽进行脉冲:(a)无肽(cos/a11),(b)wt kras
7-16
肽(seq id no:30)(cos/a11+wt肽),(c)g12d 10-mer肽(seq id no:2)(cos/a11+g12d肽),或(d)g12v 10-mer肽(seq id no:33)(cos/a11+g12v肽);以及(ii)用载体转染的cos7/a11细胞,所述载体编码(a)wt kras小基因(编码23-mer seq id no:118)(cos/a11/wt)或(b)g12d小基因(编码23-mer seq id no:119)(cos/a11/g12d)。测量干扰素(ifn)-γ。结果显示于表2a(脉冲的靶细胞)和表2b(转染的靶细胞)中。如表2a和2b所示,hla-a11限制性鼠t细胞针对kras g12d肽seq id no:2具有反应性。
[0138]
表2a
[0139]
[0140][0141]
表2b
[0142][0143]
采用cdna末端的5’快速扩增(race),从每个阳性孔中的细胞分离tcr。鉴定了2条优势的α链和4条优势的β链(表3)。
[0144]
表3
[0145][0146]
实施例2
[0147]
该实施例显示,经转导以表达包含seq id no:11的tcrα链和包含seq id no:12的tcrβ链的pbl,对于hla-a11+/g12d 10-mer+靶标具有反应性。
[0148]
将表3的两条优势的α链和4条优势的β链单独地克隆到msgv1逆转录病毒载体。如表4所示,将pbl单独共转导以表达不同的α和β链对之一。筛选转导的pbl针对以下的细胞的反应性:(i)表达hla-a11的t2/a11+(表4a)或cos7/a11+(表4b)细胞,所述细胞用以下的肽
进行了脉冲:(a)g12d 10-mer肽(seq id no:2),(b)g12v 10-mer肽(seq id no:33),(c)wt kras 10-mer肽(seq id no:30),或(d)没有肽(无);或者(ii)用以下的小基因转导的cos7/a11细胞:(a)g12d小基因(编码23-mer seq id no:119)(cos/a11/g12d),(b)g12v小基因(编码23-mer seq id no:120)(cos/a11/g12v),(c)wt kras小基因(编码23-mer seq id no:118)(cos/a11/wt),或(d)无细胞(仅培养基)(表4c)。测量了ifn-γ分泌。结果显示于表4a-c。在表4a-c中,粗体的ifn-γ分泌值指示那些表现出反应性的tcrα和β链对,以及加下划线的粗体ifn-γ分泌值指示该表现出最佳反应性的tcrα和β链对。如表4a-c所示,共转导以表达鼠tcrα链trav12n-3*01(seq id no:11)和鼠tcrβ链trbv4*01(seq id no:12)的pbl,表现出对用g12d 10-mer脉冲的表达hla-a11的cos7细胞或g12d转染子靶细胞具有反应性。
[0149]
表4a
[0150][0151][0152]
表4b
[0153][0154]
表4c
[0155][0156]
实施例3
[0157]
该实施例显示,用包含seq id no:11的tcrα链和包含seq id no:12的tcrβ链共转导的pbl,针对hla-a11+/g12d+胰肿瘤细胞系fa6-2/a11具有反应性。
[0158]
用包含seq id no:11的tcrα链和包含seq id no:12的tcrβ链对人pbl进行共转导。将共转导的细胞与以下共培养:(i)用以下转染的cos7细胞:(a)单独的hla-a11(cos7/a11),或(b)用wt kras小基因(编码23-mer seq id no:118)转导的hla-a11(cos7/a11/kras wt),(c)用kras g12d小基因(编码23-mer seq id no:119)转导的hla-a11(cos7/a11/kras g12d),(d)用kras g12v小基因(编码23-mer seq id no:120)转导的hla-a11(cos7/a11/kras g12v);(ii)胰肿瘤细胞系mia-paca2/a11、t3m4/a11、aspc-1、fa6-2/a11、mda-panc-48/a11、panc-1、pk-45p/a11、sk.pc.3/a11、x135m1/a11,或(iii)仅培养基。测量了ifn-γ分泌。结果显示于表5。肿瘤细胞系的kras突变显示于括号内。如表5所示,用tcrα链trav12n-3*01(seq id no:11)和tcrβ链trbv4*01(seq id no:12)共转导的pbl,表现出针对hla-a11+/g12d+胰肿瘤细胞系fa6-2/a11的反应性。
[0159]
表5
[0160]
靶细胞ifn-γ(pg/ml)cos7/a11146cos7/a11/kras wt116cos7/a11/kras(g12d)18231cos7/a11/kras(g12v)111mia-paca2/a11(g12c)*53t3m4/a11(q61h)*178sk.pc.3/a11(g12v)**53x135m1/a11(g12v)**105aspc-1(g12d)**18fa6-2/a11(g12d)**3982mda-panc-48/a11(g12d)**56panc-1(a11+,g12d)**28pk.45p/a11(g12d)**231
培养基(无细胞)26
[0161]
*通过基因分型测定的突变。
[0162]
**通过基因分型和mrna表达测定的突变(参见表13和20)。
[0163]
实施例4
[0164]
该实施例显示,用编码tcrα链trav12n-3*01(seq id no:11)和tcrβ链trbv4*01(seq id no:12)的逆转录病毒载体转导的pbl,表现出针对用kras g12d 10-mer肽(seq id no:2)脉冲的cos7/a11细胞的反应性。
[0165]
用编码tcrα链trav12n-3*01(seq id no:11)和tcrβ链trbv4*01(seq id no:12)的逆转录病毒载体来转导人pbl。将转导的pbl与用以下的肽以表6所示的浓度脉冲的cos7/a11细胞共培养:kras g12d 10-mer肽(seq id no:2),kras g12d 9-mer肽(seq id no:34),kras g12d 9-mer肽seq id no:124,kras g12v 10-mer肽(seq id no:33),或wt kras 10-mer肽(seq id no:30)。测量了ifn-γ分泌。结果显示于表6。如表6所示,经转导以表达tcrα链trav12n-3*01(seq id no:11)和tcrβ链trbv4*01(seq id no:12)的人pbl,表现出针对用kras g12d 10-mer肽(seq id no:2)脉冲的cos7/a11细胞的反应性。
[0166]
表6
[0167][0168]
实施例5
[0169]
该实施例显示,用编码tcrα链trav12n-3*01(seq id no:11)和tcrβ链trbv4*01(seq id no:12)的逆转录病毒载体转导的pbl,表现出针对表达hla-a11的胰肿瘤系fa6-2/a11的反应性。
[0170]
用编码tcrα链trav12n-3*01(seq id no:11)和tcrβ链trbv4*01(seq id no:12)的逆转录病毒载体来转导人pbl。将未转导的对照pbl或转导的pbl与表7所列出的靶细胞一起共培养。测量了ifn-γ分泌。结果显示于表7。肿瘤细胞系的kras突变显示于括号内。如表7所示,经转导以表达tcrα链trav12n-3*01(seq id no:11)和tcrβ链trbv4*01(seq id no:12)的人pbl,表现出针对fa6-2/a11肿瘤细胞系的反应性。当与表7所列的每种靶细胞共培养时,未转导的pbl分泌小于100pg/ml的ifn-γ。
[0171]
表7
[0172]
[0173][0174]
*由基因分型测定的突变(或无突变,即“wt”)。
[0175]
**由基因分型和mrna表达测定的突变(参见表13和20)。
[0176]
实施例6
[0177]
该实施例显示了对鼠抗-kras
7-16 g12v 10-mer tcr的分离。
[0178]
用g12v 10-mer肽(seq id no:33)使hla-a11转基因小鼠免疫两次。第二次免疫后,移出脾脏和淋巴结并在体外用不同浓度(1μm、0.1μm和0.01μm)的g12v 10-mer肽培养7天。测试分离自淋巴结和脾脏培养物的t细胞针对以下的反应性:(i)经编码以下小基因的载体转染的cos7/a11细胞:(a)g12v小基因(编码23-mer seq id no:120)(cosa11/g12v);(b)wt kras小基因(编码23-mer seq id no:118)(cosa11/wt);(c)g12d小基因(编码23-mer seq id no:119)(cosa11/g12d);(ii)表达hla-a11的kras g12v+胰肿瘤细胞系paca44/a11、skpc3/a11或x135m1/a11;或(iii)无靶细胞(培养基)(表8)。结果显示于表8。在表8中,加下划线的ifn-γ分泌值指示对转染子和肿瘤表现出反应性的那些细胞。
[0179]
表8
[0180][0181][0182]
采用5’race,从表现出高度特异性g12v肽和转染子反应性的细胞分离寡克隆的tcr。鉴定了两条优势的α链和3条优势的β链(表9)。
[0183]
表9
[0184][0185]
实施例7
[0186]
该实施例显示,经转导以表达(i)包含seq id no:133的tcrα链和包含seq id no:134的tcrβ链或(ii)包含seq id no:145的tcrα链和包含seq id no:146的tcrβ链的pbl,对hla-a11+/g12v 10-mer+靶标具有反应性。
[0187]
将表9中两条优势的α链和3条优势的β链单独地克隆到msgv1逆转录病毒载体。将抗-cd3刺激的pbl单独地共转导以表达不同的α和β链对之一,如表10a-10b所示。筛选转导的pbl对以下的细胞的反应性:(i)用以下的肽脉冲的cos7/a11+细胞:(a)g12d 10-mer肽(seq id no:2),(b)g12v 10-mer肽(seq id no:33),或(c)wt kras 10-mer肽(seq id no:30)(表10a),或者(ii)用以下的小基因转导的cos7/a11细胞:(a)g12d小基因(编码23-mer seq id no:119)(cos/a11/g12d),(b)g12v小基因(编码23-mer seq id no:120)(cos/a11/g12v),或(c)wt kras小基因(编码23-mer seq id no:118)(cos/a11/wt)(表10b)。将没有用肽脉冲的未转染的cos7/a11细胞(cos7/a11)和无细胞的培养基(培养基)用作阴性对照。用gfp脉冲或转导的pbl用作阳性对照。测量了ifn-γ分泌。
[0188]
结果显示于表10a-10b。在表10a-10b中,粗体的ifn-γ分泌值指示那些表现出反应性的tcrα和β链对。如表10a-10b所示,经共转导以表达(i)鼠tcrα链trav19*01(seq id no:145)和鼠tcrβ链trbv13-1*02(seq id no:146)或(ii)鼠tcrα链trav3-3*01(seq id no:133)和鼠tcrβ链trbv4*01(seq id no:134)的pbl,表现出针对用g12v 10-mer脉冲的表达hla-a11的cos7细胞或g12v转染子靶细胞,而非对照肽或对照转染子的反应性。
[0189]
表10a
[0190][0191]
表10b
[0192][0193]
实施例8
[0194]
该实施例显示,相比trav19*01/trbv13-1*02鼠抗-kras g12vtcr(seq id no:145和146),trav3-3*01/trbv4*01鼠抗-kras g12vtcr(seq id no:133和134)对脉冲的靶肽具有更高的亲和力。
[0195]
用(i)trav3-3*01/trbv4*01鼠抗-kras g12v tcr(seq id no:133和134)或(ii)trav19*01/trbv13-1*02鼠抗-kras g12v tcr(seq id no:145和146)来转导pbl。将转导的细胞与用以下的肽以表11a和11b中所示的浓度脉冲的cos7/a11细胞共培养:(a)g12d 10-mer肽(seq id no:2),(b)g12v 10-mer肽(seq id no:33),(c)wt kras 10-mer肽(seq id no:30),(d)g12d 9-mer肽(seq id no:34),或(e)g12v 9-mer肽(seq id no:35)。测量了ifn-γ分泌。
[0196]
结果显示于表11a(trav3-3*01/trbv4*01(seq id no:133和134))和表11b(trav19*01/trbv13-1*02(seq id no:145和146))。在表11a-11b中,粗体的ifn-γ分泌值指示所述tcr表现出反应性时的那些靶肽浓度。如表11a-11b所示,用trav3-3*01/trbv4*01tcr(seq id no:133和134)转导的t细胞,识别了用9-mer和10-mer肽脉冲的cos7/a11,并识别了在以0.01nm浓度脉冲时的9-mer。因此,相比trav19*01/trbv13-1*02(seq id no:145和146)tcr,trav3-3*01/trbv4*01tcr(seq id no:133和134)以更高的亲和力识别了脉冲的靶肽。相比10-mer肽,trav3-3*01/trbv4*01(seq id no:145和146)tcr针对g12v 9-mer肽具有增加的反应性,这也表明了9-mer肽是最小的决定子。
[0197]
表11a
[0198]
[0199][0200]
表11b
[0201][0202]
实施例9
[0203]
该实施例显示,trav3-3*01/trbv4*01鼠抗-kras g12vtcr(seq id no:133和134)识别了hla-a11+kras g12v+胰肿瘤细胞系。
[0204]
用(i)trav3-3*01/trbv4*01鼠抗-kras g12v tcr(seq id no:133和134)或(ii)trav19*01/trbv13-1*02鼠抗-kras g12v tcr(seq id no:145和146)转导pbl。将转导的细胞与以下的细胞共培养:(i)用以下的小基因转导的cos7/a11细胞:(a)g12d小基因(编码23-mer seq id no:119)(cos/a11/g12d),(b)g12v小基因(编码23-mer seq id no:120)(cos/a11/g12v),或(c)wt kras小基因(编码23-mer seq id no:118)(cos/a11/wt);(ii)用hla-a11转导的kras g12v阴性胰肿瘤细胞系;(iii)用hla-a11转导kras g12v+胰肿瘤细胞系;或(iv)母体(未转导的)胰肿瘤细胞系,如表12所示。测量了ifn-γ分泌。
[0205]
结果显示于表12。在表12中,粗体的ifn-γ分泌值指示所述tcr对其表现出反应性的那些靶细胞。如表12所示,相比trav19*01/trbv13-1*02鼠抗-kras g12v tcr(seq id no:145和146),trav3-3*01/trbv4*01鼠抗-kras g12v tcr(seq id no:133和134)识别了更多的hla-a11+kras g12v+胰肿瘤细胞系。
[0206]
表12
[0207][0208][0209]
*由基因分型测定的突变(或无突变,即“wt”)。
[0210]
**由基因分型和mrna表达测定的突变(参见表13和20)。
[0211]
实施例10
[0212]
该实施例显示了,对于trav3-3*01/bv4*01鼠抗-kras g12vtcr(seq id no:133和134),ifn-γ产生和突变的kras表达之间的相关性。
[0213]
测量由表13所示的每种胰肿瘤细胞系所表达的kras g12v mrna的拷贝数,并与由指示的细胞系(表13)表达的β-肌动蛋白mrna的拷贝数进行比较。当与实施例9测量的每种
细胞系共培养时,用trav3-3*01/bv4*01鼠抗-kras g12v tcr(seq id no:133和134)转导的pbl分泌的ifn-γ的量,重现于表13。trav3-3*01/bv4*01鼠抗-kras g12v tcr(seq id no:133和134)的反应性(依据与靶细胞共培养时的ifn-γ分泌),与kras g12v mrna的拷贝数有相关性。
[0214]
表13
[0215][0216]
实施例11
[0217]
该实施例显示,在(i)存在cd4且不存在cd8,或(ii)存在cd8且不存在cd4的情况下,trav3-3*01/bv4*01鼠抗-kras g12v tcr(seq id no:133和134)识别了突变的kras。
[0218]
用编码trav3-3*01/bv4*01鼠抗-kras g12v tcr(seq id no:133和134)的核苷酸序列转导pbl。通过流式细胞术将转导的细胞分选为表14所示的群体。将分选的细胞群与以下的细胞共培养:(i)用以下的小基因转导的cos7/a11细胞:(a)g12d小基因(编码163-mer)(cos/a11/g12d),(b)g12v小基因(编码163-mer)(cos/a11/g12v),或(c)wt kras小基因(编码163-mer)(cos/a11/wt);或者(ii)未转导的或用hla-a11转导的sk.pc3胰肿瘤细胞系。无细胞的培养基用作阴性对照。测量了ifn-γ分泌。
[0219]
结果显示于表14。在表14中,粗体的ifn-γ分泌值指示所述tcr对其表现出反应性的那些靶细胞。如表14所示,在(i)存在cd4且不存在cd8,或(ii)存在cd8且不存在cd4的情况下,trav3-3*01/bv4*01鼠抗-kras g12v tcr(seq id no:133和134)识别了靶细胞。因此,trav3-3*01/bv4*01鼠抗-kras g12v tcr(seq id no:133和134)提供了对靶标具有高度亲合力的识别。
[0220]
表14
[0221][0222]
实施例12
[0223]
该实施例显示了对鼠抗-kras
7-16 g12d 10-mer tcr的分离。
[0224]
用g12d 10-mer肽(seq id no:2)使hla-a11转基因小鼠免疫3次。第三次免疫后,移出脾脏和淋巴结,并在体外用不同浓度(1μm、0.1μm和0.01μm)的g12d 10-mer肽培养7天。测试从ln和脾脏培养物分离的t细胞针对以下的细胞的反应性:(i)经转导以表达hla-a11的cos7细胞(cos7/a11),所述cos7细胞已经用以下进行了脉冲:(a)没有肽(无),(b)wt kras
7-16
肽(seq id no:30)(cos/a11+wt肽),(c)g12d 10-mer肽(seq id no:2)(cos/a11+g12d肽),(d)g12v 10-mer肽(seq id no:33)(cos/a11+g12v肽),(e)g12v 9-mer肽(seq id no:35),或(f)g12d9-mer肽(seq id no:34);和(ii)用编码以下的小基因的载体转染的cos7/a11细胞:(a)wt kras小基因(编码23-mer seq id no:118)(cos/a11/wt),(b)g12d小基因(编码23-mer seq id no:119)(cos/a11/g12d),或(c)(b)g12v小基因(编码23-mer seq id no:120)(cos/a11/g12d)。测量了干扰素(ifn)-γ。
[0225]
结果显示于表15a(肽脉冲)和表15b(转染子)。在表15a和15b中,粗体的ifn-γ分泌值指示所述tcr对其表现出反应性的那些靶肽和靶细胞。如表15a和15b所示,hla-a11限制性鼠t细胞对kras g12d肽seq id no:2具有反应性。
[0226]
表15a
[0227][0228]
表15b
[0229][0230]
将从ln和脾脏培养物分离的t细胞还用不同浓度的g12d肽在体外刺激6-7天,然后与表16所示的表达hla-a11的kras g12d+胰细胞系共培养。测量了ifn-γ。
[0231]
结果显示于表16,在表16中,粗体的ifn-γ分泌值指示所述tcr对其表现出反应性的那些靶细胞。如表16所示,从ln和脾脏培养物分离的t细胞对表达hla-a11的kras g12d+胰细胞系具有反应性。
[0232]
表16
[0233][0234]
采用5’race从反应性细胞分离tcr。鉴定了两条优势的α链和一条优势的β链(表17)。
[0235]
表17
[0236][0237]
实施例13
[0238]
该实施例显示,经转导以表达包含seq id no:157的tcrα链和包含seq id no:158的tcrβ链的pbl,对hla-a11+/g12d 10-mer+靶标具有反应性。
[0239]
将表17的两条优势的α链和所述β链单独地克隆至msgv1逆转录病毒载体。将pbl单独共转导以表达两对α和β链之一,如表18所示。筛选转导的pbl对以下的反应性:(i)用以下的小基因转导的cos7/a11细胞:(a)g12d小基因(编码23-mer seq id no:119)(cos/a11/g12d),(b)g12v小基因(编码23-mer seq id no:120)(cos/a11/g12v),(c)wt kras小基因(编码23-mer seq id no:118)(cos/a11/wt),或(d)无细胞(仅培养基)(表18)。测量了ifn-γ分泌。
[0240]
结果显示于表18。如表18所示,经共转导以表达鼠tcrα链trav4-4*01(1)(seq id no:157)和鼠tcrβ链trbv12-2*01(seq id no:158)的pbl,表现出针对表达hla-a11的g12d转染子靶细胞的反应性。
[0241]
表18
[0242][0243]
转导pbl以表达tcr trav4-4*01(1)/trbv12-2*01(seq id no:157和158),并筛选针对用(a)g12d小基因(编码23-mer seq id no:119)(cos/a11/g12d),(b)g12v小基因(编码23-mer seq id no:120)(cos/a11/g12v),(c)wt kras小基因(编码23-mer seq id no:
118)(cos/a11/wt)转导的cos7/a11细胞和(d)表19所示的胰肿瘤细胞系的反应性,所述胰肿瘤细胞系未经转导或经转导以表达hla-a11和指示的kras突变。在表19中,指示了每种胰肿瘤细胞系表达的kras突变。测量了ifn-γ分泌。
[0244]
结果显示于表19。如表19所示,用tcr trav4-4*01(1)/trbv12-2*01(seq id no:157和158)转导的pbl识别了hla-a11+g12d+胰肿瘤细胞系。
[0245]
表19
[0246][0247][0248]
*由基因分型测定的突变(或无突变,即“wt”)。
[0249]
**由基因分型和mrna表达测定的突变(参见表13和20)。
[0250]
实施例14
[0251]
该实施例显示了,对于trav4-4*01(1)/trbv12-2*01鼠抗-kras g12d tcr(seq id no:157和158),ifn-γ产生和突变的kras表达之间的相关性。
[0252]
测量由表20所示的每种胰肿瘤细胞系表达的kras g12d mrna的拷贝数,并与每种细胞系(表20)表达的β-肌动蛋白mrna的拷贝数进行比较。当与每种细胞系共培养时,用trav4-4*01(1)/trbv12-2*01鼠抗-kras g12d tcr(seq id no:157和158)转导的pbl分泌的ifn-γ的量显示于表13。trav4-4*01(1)/trbv12-2*01鼠抗-kras g12d tcr(seq id no:157和158)的反应性(依据与靶细胞共培养时的ifn-γ分泌),与kras g12d mrna的拷贝数
有相关性。
[0253]
表20
[0254][0255]
实施例15
[0256]
该实施例显示,相比trav12n-3*01/bv4*01鼠抗-kras g12dtcr(seq id no:11和12),trav4-4/dv10*01/bv12-2*01鼠抗-kras g12d tcr(seq id no:157和158)对脉冲的靶肽具有更高的亲和力。
[0257]
用(i)t trav4-4/dv10*01/bv12-2*01鼠抗-kras g12d tcr(seq id no:157和158)或(ii)trav12n-3*01/bv4*01鼠抗-kras g12dtcr(seq id no:11和12)来转导pbl。将转导的细胞与用以下的肽以表21a和21b所示的浓度脉冲的cos7/a11细胞共培养:(a)g12d 10-mer肽(seq id no:2),(b)wt kras 10-mer肽(seq id no:30),(c)g12d9-mer肽(seq id no:34),或(d)wt kras 9-mer肽(seq id no:31)。测量了ifn-γ分泌。
[0258]
结果显示于表21a(trav4-4/dv10*01/bv12-2*0(seq id no:157和158))和表21b(trav12n-3*01/bv4*01(seq id no:11和12))。如表21a-21b所示,用trav4-4/dv10*01/bv12-2*0(seq id no:157和158)转导的t细胞识别了在以1
×
10-9
m的浓度脉冲时的10-mer。因此,相比trav12n-3*01/bv4*01(seq id no:11和12)tcr,trav4-4/dv10*01/bv12-2*0(seq id no:157和158)以更高的亲合力识别了脉冲的靶肽。
[0259]
表21a
[0260]
[0261][0262]
表21b
[0263][0264]
实施例16
[0265]
该实施例显示,相比trav12n-3*01/bv4*01鼠抗-kras g12dtcr(seq id no:11和12),trav4-4/dv10*01/bv12-2*01鼠抗-kras g12d tcr(seq id no:157和158)对g12d+胰肿瘤细胞系具有更高的亲和力。
[0266]
用(i)trav4-4/dv10*01/bv12-2*01鼠抗-kras g12d tcr(seq id no:157和158)或(ii)trav12n-3*01/bv4*01鼠抗-kras g12dtcr(seq id no:11和12)转导pbl。将转导的细胞与胰细胞系共培养,所述胰细胞系未经转导或用hla-a11和突变的kras转导,如表22所示。测量了ifn-γ分泌。
[0267]
结果显示于表22。如表22所示,相比trav12n-3*01/bv4*01(seq id no:11和12)tcr,用trav4-4/dv10*01/bv12-2*0(seq id no:157和158)转导的t细胞以更高的亲合力识别了g12d+胰肿瘤细胞系。
[0268]
表22
[0269][0270]
*由基因分型测定的突变(或无突变,即“wt”)。
[0271]
**由基因分型和mrna表达测定的突变(参见表13和20)。
[0272]
实施例17
[0273]
该实施例显示了向表达突变的kras的癌症患者施用pbl的i/ii期研究,所述pbl转导了编码能识别突变的kras的鼠tcr的载体。
[0274]
为了取得纳入该研究的资格,患者符合关于过继性细胞治疗(act)/il-2的正常标准并且有以下特征:
[0275]
·
hla-a11+、表达突变的kras的肿瘤(通过免疫组织化学进行测量);
[0276]
·
放射性碘难治性癌症;和
[0277]
·
正电子发射断层成像(pet)亲合性肿瘤,或在最近的6个月内表现出肿瘤进展。
[0278]
用编码鼠抗-突变的kras tcr的α和β链(seq id no:11和12)的载体以逆转录病毒方式来转导自体pbl。用制备型、非清髓性的高剂量环磷酰胺(cy)和氟达拉滨(flu)治疗患者。用高剂量il-2每8小时对患者进行治疗直至耐受。在i期中,用1
×
108个逆转录病毒转导的细胞的起始剂量治疗患者。所述剂量以半对数的方式增加,每个群组中一名患者直到1
×
10
10
个细胞的剂量,然后是每个群组3名患者。ii期有两个阶段的设计,具有20%的靶向应答率。
[0279]
实施例18
[0280]
该实施例显示了在人癌症中kras突变的频率。
[0281]
不同的人癌症中kras突变的频率(%)列举于表23中。表23还显示了在所有kras突变中特定kras突变的频率(%)。
[0282]
表23
[0283][0284]
实施例19
[0285]
该实施例显示,相比野生型trav4-4/dv10*01/bv12-2*01tcr,trav4-4/dv10*01/bv12-2*01tcr的cdr3α区中甘氨酸残基的置换提供了增强的抗-kras反应性。
[0286]
trav4-4/dv10*01/bv12-2*01tcr的cdr3α区中的甘氨酸残基被换成丙氨酸残基,以提供置换的trav4-4/dv10*01/bv12-2*01tcr(cdr3αg112a)。用(i)野生型trav4-4/dv10*01/bv12-2*01tcr(seq id no:157和158)或(ii)置换的trav4-4/dv10*01/bv12-2*01tcr(seq id no:209和158)转导pbl。将转导的细胞与以下的细胞共培养:用hla-a11和wt kras转导的cos细胞(cos/a11/wt),用hla-a11和g12d kras转导的cos细胞(cos/a11/g12d),用hla-a11转导的胰肿瘤细胞系fa6-2(fa6-2/a11),或胰肿瘤细胞系panc-1。单独(培养基)培养的转导的细胞作为对照。测量了ifn-γ分泌(pg/ml)。结果显示于表24。
[0287]
表24
[0288][0289]
如表24所示,相比野生型trav4-4/dv10*01/bv12-2*01tcr,trav4-4/dv10*01/bv12-2*01tcr的cdr3α区中甘氨酸残基的置换提供了增强的抗-kras反应性。
[0290]
在此将本文引用的所有参考文献,包括出版物、专利申请和专利通过引用并入,其程度如同将各参考文献单独且明确指明通过引用并入,并且在本文整体示出一样。
[0291]
术语“一个/一种(a)”和“一个/一种(an)”和“所述(the)”以及类似的指代物在描述本发明的上下文中(特别是在下述权利要求的上下文中)的使用被解释为既涵盖单数又涵盖复数,除非本文另外指明或者上下文明显矛盾。术语一项或多项的列表的“至少一种/一个”(例如,“a和b中的至少一种/一个”)的使用,应被解释为意指选自列出的项中的一项(a或b)或两个或更多个列出的项的组合(a和b)。术语“包含(comprising)”、“具有(having)”、“包括(including)”以及“含有(containing)”被解释为开放式术语(即,意为“包括但不限于”)除非另外标注。本文数值范围的叙述仅意图作为单独指落入范围内的各独立数值的速记法,除非本文另外指明,并且各独立的数值并入说明书如同本文单独对其进行叙述一样。可以以任何合适的顺序实施本文所述的所有方法,除非本文另外指明或者在其它方面与上下文明显矛盾。本文提供的任何或所有实施例或者示例性语言(例如“如”)的使用仅意图更好地阐明本发明,并且不对本发明的范围构成限制,除非另外声明。说明书中的语言均不应被解释为指示任何未要求保护的元素对于本发明的实践是必要的。
[0292]
本文描述了本发明的优选实施方案,包括发明人已知的实施本发明的最佳方式。经阅读前述描述,那些优选实施方案的改变对于本领域普通技术人员而言可以变得显而易见。发明人期望本领域技术人员视情况应用此类改变,并且发明人意图以与本文具体所述的不同的方式实践本发明。因此,如适用的法律所允许的,本发明包括在此所附的权利要求中所述的主题的所有修饰和等同物。此外,本发明涵盖以上所述元素的所有可能的改变的任何组合,除非本文另外指明或者在其它方面与上下文明显矛盾。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1