一种融合蛋白及其制备方法与流程
本发明涉及基因工程,涉及一种融合蛋白及其制备方法;尤其涉及一种抗牛病毒性腹泻病毒和传染性牛鼻气管炎病毒的融合蛋白及其制备方法。
背景技术:
1、牛病毒腹泻病毒(bovine viral diarrhea virus,bvdv)属于黄病毒科猪瘟病毒属,是导致牛病毒性腹泻(bovine viral diarrhea,bvd)的病原体之一。目前,bvdv在世界范围内普遍存在,畜牧业发达地区动物感染率较高。bvdv感染范围广,可感染牛、绵羊、山羊、鹿和骆驼。在这些易感动物中,bvdv感染牛的临床症状最为严重,表现为腹泻、呼吸系统疾病、免疫抑制、生长迟缓、流产、繁殖功能下降,严重影响了牛群的生产和健康,给世界养殖业造成了巨大的经济损失。因此,世界动物卫生组织(oie)将bvd列为b类传染病。
2、bvdv为12.3~12.5kbp的正性、单链、包膜rna病毒。bvdv包含一个约编码4000个氨基酸的开放阅读框(open reading frame,orf),该orf可分为不同区域来编码多聚蛋白,其中编码的e2蛋白为病毒结构蛋白,由370个氨基酸残基组成,分子量为55~58kda,可单独形成同源二聚体,属于i型跨膜蛋白,具有n端的胞外区和c端的疏水锚定。e2蛋白含有17个半胱氨酸和4个糖基化位点,研究人员将其分为4个功能区(domain),即da、db、dc和dd功能区,其中dd功能区在瘟病毒的成员中最具保守性。同时e2蛋白的n末端含有主要的抗原决定簇,而e2蛋白的c末端则含有与细胞受体结合以及与细胞膜融合的重要功能区,可形成二聚体。
3、目前,控制bvdv的传播主要有两种方法:消灭持续感染动物和疫苗接种。改良活疫苗或灭活疫苗主要用于bvdv疫苗接种计划,但这些疫苗分别存在安全风险或免疫保护不足等问题。灭活疫苗对怀孕牛安全,但其免疫期短;而弱毒疫苗虽免疫期长,但对怀孕牛存在安全风险。
4、牛传染性鼻气管炎(infectious bovine rhinotracheitis,ibr)是由牛传染性鼻气管炎病毒(infectious bovine rhinotracheitis virus,ibrv)感染引起的严重危害养牛业的传染病,在国内外的养牛场广泛流行。牛感染ibrv后死亡率较低,在整体饲养条件良好的情况下,ibrv多呈一过性感染,症状不明显,只能通过血清学诊断确诊。ibrv通常寄居在三叉神经节内,因此常表现出持续性感染。一些地区的饲养条件和气候条件都比较好,牛群的整体健康情况良好,ibrv一过性感染后病毒会潜伏其体内,甚至造成牛终生带毒,给养殖业带来了较大的经济损失。
5、gd糖蛋白位于ibrv囊膜及感染细胞的表面,是ibrv表面的主要糖蛋白之一,在病毒吸附、侵入宿主细胞的过程中发挥着重要作用,不仅能诱导体液免疫,还能诱导细胞免疫,且抗gd单克隆抗体还具有中和活性,可中和病毒。
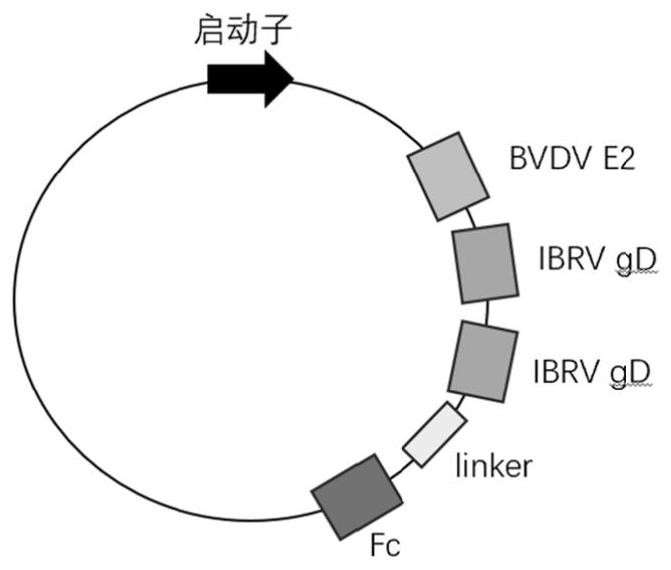
6、目前,市面上已有bvdv和ibrv灭活二联苗,但灭活的bvdv和ibrv可能含有没有灭活彻底的核酸分子,该核酸分子可能会与野生型的bvdv和ibrv重组,导致病毒进一步变异,造成疫苗效果变差的风险。并且灭活疫苗虽然能够诱导产生包括中和抗体在内的免疫反应,但不能诱导细胞毒t淋巴细胞反应。免疫灭活疫苗,无法区分是疫苗免疫产生的效价还是感染野生型病毒产生的效价,不能从根本上净化这两种疾病。亚单位疫苗是由病毒的抗原蛋白组成,不存在病毒重组和变异的风险,还能区分野毒感染和疫苗免疫产生的效价。但通常亚单位疫苗的免疫原性较低,免疫持续期较短,并且现有的二联疫苗是将两个抗原进行体外混合,导致疫苗生产步骤复杂化。因此基于以上科学问题,本研究将bvdv结构蛋白e2与ibrv结构蛋白gd进行串联融合,并添加突变的fc标签,成功利用哺乳动物细胞表达系统制备了融合蛋白,做到了一个蛋白两种作用,通过免疫动物评价其免疫原性,为bvdv和ibrv的基因工程亚单位疫苗的研发奠定良好的基础。
技术实现思路
1、为提高牛病毒性腹泻病和传染性牛鼻气管炎病疫苗的免疫原性和免疫持续期,减少生产步骤,本发明提出了一种融合蛋白及其制备方法;具体是提供了一种能稳定高效表达牛病毒性腹泻病毒e2抗原和传染性牛鼻气管炎病毒gd抗原和牛免疫球蛋白fc的亚单位融合蛋白re2-2gd-fc及其在cho或293t细胞系统中构建和表达方法。本发明针对牛igg中的fc片段进行分析和突变,筛选了可显著增加fc融合蛋白免疫持续期的突变体,其序列如seqid no.2所示。本发明获得的可以分泌表达亚单位融合蛋白re2-2gd-fc的单克隆细胞株,表达产量高,表达量1.3g/l的融合蛋白。相比现有cho细胞表达的融合蛋白e2-fc表达量0.5g/l,我们筛选的细胞株的蛋白表达量有显著的优势。
2、本发明的目的是通过以下技术方案来实现的:
3、<第一方面>
4、本发明提供以下重组融合蛋白,含有牛病毒性腹泻病毒e2抗原和传染性牛鼻气管炎病毒gd抗原和牛的抗体fc蛋白片段,所述抗体fc蛋白片段为牛的igg的重链恒定区片段,其氨基酸序列如seq id no.1所示(记为fc,编码基因序列如seq id no.16所示);
5、或,为牛的igg的重链恒定区片段的突变体1,其氨基酸序列如seq id no.2所示(记为fc-m1,编码基因序列如seq id no.17所示);
6、或,为牛的igg的重链恒定区片段的突变体2,其氨基酸序列如seq id no.3所示(记为fc-m2,编码基因序列如seq id no.18所示);
7、或,为牛的igg的重链恒定区片段的突变体3,其氨基酸序列如seq id no.4所示(记为fc-m1,编码基因序列如seq id no.19所示)。
8、作为一个实施方案,所述牛病毒性腹泻病毒e2抗原的氨基酸序列如seq id no.5所示(编码基因序列如seq id no.20所示);
9、或,为如seq id no.5所示的氨基酸序列包括经过取代、缺失或添加一个氨基酸或几个氨基酸且具有免疫原性的衍生的蛋白。
10、作为一个实施方案,所述传染性牛鼻气管炎病毒gd抗原的氨基酸序列如seq idno.6所示(编码基因序列如seq id no.21所示);
11、或,为如seq id no.6所示的氨基酸序列包括经过取代、缺失或添加一个氨基酸或几个氨基酸且具有免疫原性的衍生的蛋白。
12、作为一个实施方案,所述e2抗原与gd抗原单独分别与牛的抗体fc蛋白片段通过富含甘氨酸和丝氨酸的linker连接。
13、作为一个实施方案,所述e2抗原与gd抗原(以1:1、1:2或2:1)融合后与牛的抗体fc蛋白片段通过富含甘氨酸和丝氨酸的linker连接。
14、作为一个实施方案,所述linker序列为ggggsggggsggggs。
15、作为一个实施方案,所述目的蛋白位于linker的n端,所述fc蛋白片段位于linker的c端;或所述目的蛋白位于linker的c端,所述fc蛋白片段位于linker的n端。
16、作为一个实施方案,本发明提供以下重组亚单位融合蛋白:re2-fc、rgd-fc、re2-gd-fc、rgd-e2-fc、r2e2-gd-fc、re2-2gd-fc,优选re2-2gd-fc。
17、作为一个实施方案,所述融合蛋白re2-fc为氨基酸序列如seq id no.7所示的蛋白。
18、作为一个实施方案,所述融合蛋白rgd-fc为氨基酸序列如seq id no.8所示的蛋白。
19、作为一个实施方案,所述融合蛋白re2-gd-fc为氨基酸序列如seq id no.9所示的蛋白。
20、作为一个实施方案,所述融合蛋白rgd-e2-fc为氨基酸序列如seq id no.10所示的蛋白。
21、作为一个实施方案,所述融合蛋白r2e2-gd-fc为氨基酸序列如seq id no.11所示的蛋白。
22、作为一个实施方案,所述融合蛋白re2-2gd-fc为氨基酸序列如seq id no.12所示的蛋白。
23、作为一个实施方案,fc突变的融合蛋白re2-2gd-fc-m1为氨基酸序列如seq idno.13所示的蛋白。
24、作为一个实施方案,fc突变的融合蛋白re2-2gd-fc-m2为氨基酸序列如seq idno.14所示的蛋白。
25、作为一个实施方案,fc突变的融合蛋白re2-2gd-fc-m3为氨基酸序列如seq idno.15所示的蛋白。
26、作为一个实施方案,以上所述融合蛋白的氨基酸序列的氨基末端或羧基末端上连接有一种或多种标签。
27、作为一个实施方案,所述标签选自poly-arg、poly-his、flag、c-myc、ha。
28、作为一个实施方案,所述融合蛋白的表达系统包括但不限于哺乳动物细胞。
29、作为一个实施方案,所述哺乳动物细胞为cho细胞、293t细胞。更优选地,所述哺乳动物细胞为cho细胞。
30、<第二方面>
31、本发明提供了一种重组亚单位融合蛋白的制备方法,所述方法包括如下步骤:
32、s1、将所述重组融合蛋白的编码基因克隆到真核表达载体中得到含有融合蛋白编码基因的重组质粒;
33、如将re2-fc融合蛋白编码的基因克隆到真核表达载体中得到含有re2-fc融合蛋白编码基因的重组质粒;
34、或将rgd-fc融合蛋白编码的基因克隆到真核表达载体中得到含有rgd-fc融合蛋白编码基因的重组质粒;
35、或将re2-gd-fc融合蛋白编码的基因克隆到真核表达载体中得到含有re2-gd-fc融合蛋白编码基因的重组质粒;
36、或将rgd-e2-fc融合蛋白编码的基因克隆到真核表达载体中得到含有rgd-e2-fc融合蛋白编码基因的重组质粒;
37、或将r2e2-gd-fc融合蛋白编码的基因克隆到真核表达载体中得到含有r2e2-gd-fc融合蛋白编码基因的重组质粒;
38、或将re2-2gd-fc融合蛋白编码的基因克隆到真核表达载体中得到含有re2-2gd-fc融合蛋白编码基因的重组质粒;
39、或将re2-2gd-fc-m1融合蛋白编码的基因克隆到真核表达载体中得到含有re2-2gd-fc-m1融合蛋白编码基因的重组质粒;
40、或将re2-2gd-fc-m2融合蛋白编码的基因克隆到真核表达载体中得到含有re2-2gd-fc-m2融合蛋白编码基因的重组质粒;
41、或将re2-2gd-fc-m3融合蛋白编码的基因克隆到真核表达载体中得到含有re2-2gd-fc-m3融合蛋白编码基因的重组质粒;
42、s2、将所述重组质粒转染至细胞株中;
43、如再将含re2-fc融合蛋白编码基因的重组质粒转染至cho细胞株中;
44、或将含rgd-fc融合蛋白编码基因的重组质粒转染至cho细胞株中;
45、或将含re2-gd-fc融合蛋白编码基因的重组质粒转染至cho细胞株中;
46、或将含rgd-e2-fc融合蛋白编码基因的重组质粒转染至cho细胞株中;
47、或将含r2e2-gd-fc融合蛋白编码基因的重组质粒转染至cho细胞株中;
48、或将含re2-2gd-fc融合蛋白编码基因的重组质粒转染至cho细胞株中;
49、或将含re2-2gd-fc-m1融合蛋白编码基因的重组质粒转染至cho细胞株中;
50、或将含re2-2gd-fc-m2融合蛋白编码基因的重组质粒转染至cho细胞株中;
51、或将含re2-2gd-fc-m3融合蛋白编码基因的重组质粒转染至cho细胞株中;
52、s3、发酵培养、纯化,筛选出重组蛋白表达细胞株;具体可以为:发酵培养步骤s2所得瞬时表达的细胞,纯化后得到各重组融合蛋白;筛选出表达量高,免疫原性好的重组蛋白表达细胞株;
53、s4、通过培养、筛选、驯化步骤s3中筛选到的重组蛋白表达细胞株,得到高度表达的细胞株;
54、s5、发酵培养所述高度表达的细胞株,纯化后得到所述融合蛋白。
55、作为一个实施方案,步骤s1中,re2-fc融合蛋白的编码基因序列如seq id no.22所示;rgd-fc融合蛋白的编码基因如seq id no.23所示;re2-gd-fc融合蛋白的编码基因如seq id no.24所示;rgd-e2-fc融合蛋白的编码基因如seq id no.25所示;r2e2-gd-fc融合蛋白的编码基因如seq id no.26所示;re2-2gd-fc融合蛋白的编码基因如seq id no.27所示,re2-2gd-fc-m1融合蛋白的编码基因如seq id no.28所示,re2-2gd-fc-m2融合蛋白的编码基因如seq id no.29所示,re2-2gd-fc-m3融合蛋白的编码基因如seq id no.30所示。
56、作为一个实施方案,所述真核表达载体为哺乳动物细胞表达载体。优选地,所述真核表达载体为pee6.4、pee12.4、pgl4.13、pcdna3.1,更优选地,所述真核表达载体为pcdna3.1。
57、作为一个实施方案,用于表达重组亚单位融合蛋白(re2-2gd-fc)的细胞为cho细胞。优选地,所述cho细胞株为dg44、dxb11、cho-k1或cho-s细胞株。更优选地,所述cho细胞株为cho-k1。
58、<第三方面>
59、本发明提供了一种cho细胞株cho 3f7-re2-2gd-fc-m1),为中国仓鼠卵巢细胞slpcb03,保藏编号为cctcc no:c2022315。
60、本发明中,中国仓鼠卵巢细胞slpcb03已经递交中国典型培养物保藏中心保藏,保藏地址为中国武汉武汉大学,保藏编号为cctcc no:c2022315,保藏日期为2022年10月12日。
61、<第四方面>
62、本发明提供了前述重组融合蛋白或cho细胞株在制备预防牛病毒性腹泻和传染性牛鼻气管炎的疫苗中的应用。
63、<第五方面>
64、本发明提供了前述重组融合蛋白或cho细胞株在制备预防和/或治疗牛病毒性腹泻和传染性牛鼻气管炎的药物中的应用。
65、与现有技术相比,本发明具有如下有益效果:
66、1)本发明构建了re2-2gd-fc融合蛋白突变体,且本突变体相对于野生型的融合蛋白,免疫持续期显著提高。
67、2)本发明构建并筛选了悬浮稳定高效分泌表达牛病毒性腹泻病毒e2蛋白和传染性牛鼻气管炎病毒gd蛋白的亚单位融合蛋白re2-2gd-fc的cho细胞株,该细胞株表达重组亚单位融合蛋白re2-2gd-fc产量高达0.5-1.3g/l、易于纯化,细胞培养上清中的目的蛋白纯度都能达到85%以上,只需一步亲和层析就能使目的蛋白纯度达到90%以上,远远满足亚单位疫苗和诊断试剂的需求,易于大规模生产;
68、3)另外,由于生产用的cho细胞株在培养时可控制性高、质控容易、生产蛋白批次间稳定,生物安全高(没有病毒,不存在散毒的风险)。
- 还没有人留言评论。精彩留言会获得点赞!