基于碳量子点荧光猝灭法定量检测维生素B12的荧光探针及其制备方法和应用与流程
本发明属于荧光探针
技术领域:
,具体涉及一种基于碳量子点荧光猝灭法定量检测维生素b12的荧光探针及其制备方法和应用。
背景技术:
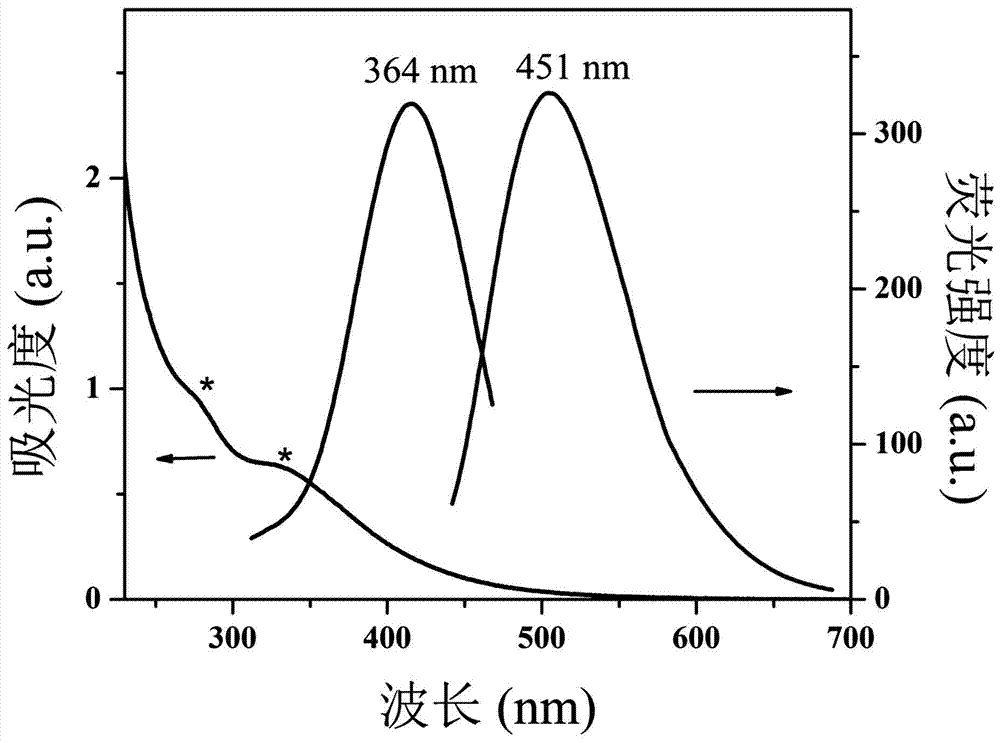
:维生素b12(vitaminb12,vb12)又称钴胺素或氰钴素,是一种由含钴的卟啉类化合物组成的b族维生素。vb12也是唯一含必需矿物质的维生素,因含钴而呈红色,又称红色维生素,是少数有色的维生素,也是维持人体正常机能以及新陈代谢必不可少的维生素。当成人缺乏vb12时会引起恶性贫血,舌、口腔、消化道的粘膜发炎,脊髓变性,神经和周围神经退化;小孩缺乏vb12的早期表现为精神情绪异常、表情呆滞、少哭少闹、反应迟钝、爱睡觉等症状,最后会引起贫血,另外,缺乏vb12可能引起精神忧郁。然而,当vb12过量时,人体会发生哮喘、荨麻疹、湿疹、面部浮肿、寒颤等过敏反应,也可能引发神经兴奋、心前区痛和心悸,还可导致叶酸缺乏。目前已报道的检测vb12的方法有:微生物法、原子吸收分光光度法、高效液相色谱法以及液相色谱质谱联用系统。这些方法有自身独特的优势,但都存在以下缺陷:步骤繁琐,耗时费力,仪器装置复杂昂贵,检测周期长,技术含量高,成本高,抗干扰能力弱以及准确度低等,导致这些检测方法无法得到广泛应用。因此,亟需发展一种快速、高效、定量检测vb12的方法。碳量子点又称为碳纳米点,是碳家族中新型成员,具有光致发光性能,良好的水溶性和稳定性,生物相容性以及低细胞毒性等优点。基于碳量子点已经构筑了多种荧光探针用于各种金属离子、氨基酸、药物和环境污染物等的检测。以其为基础,通过荧光猝灭法,发展一种快速、高效、定量检测vb12的方法具有重要的意义和广阔的应用前景。技术实现要素:本发明的目的在于提供一种基于碳量子点荧光猝灭法定量检测vb12的荧光探针及其制备方法和应用。本发明由如下技术方案实现的:一种基于碳量子点荧光猝灭法定量检测vb12的荧光探针,以蔗糖作为碳源,乙二胺作为氮源,浓磷酸作为磷源,通过酸碱中和放热碳化法制备pncqds,离心除去不溶物,透析去除未反应的前体物质和小分子,冷冻干燥得到荧光探针pncqds固体粉末;所述荧光探针的具体制备方法如下:(1)前体物质的获得:称量0.4g蔗糖,向其中加6ml乙二胺和4ml浓磷酸,通过酸碱中和放热碳化法得到深褐色黏稠物;(2)待反应体系温度冷却至室温后,将深褐色黏稠物溶解于二次水中,溶液8000转/分钟离心15分钟,上清液在500-1000da的透析袋中透析处理三天,透析袋中的溶液冷冻干燥,即得pncqds固体粉末。所述浓磷酸为市售的85%的浓磷酸,浓度14.6mol/l。利用所述的基于碳量子点荧光猝灭法定量检测vb12的荧光探针检测vb12的方法,具体步骤为:(1)pncqds储备液的制备:0.5gpncqds固体粉末中加入50ml二次水,搅拌使其充分溶解得到浓度为10mg/ml的pncqds储备液;(2)vb12储备液的制备:称取0.1402gvb12粉末,加入到20ml生理盐水中,搅拌溶解,配制浓度为5.17mmol/l的vb12储备液;(3)vb12含量与pncqds荧光强度的线性方程的获得:将若干体积的vb12储备液加入到浓度为2mg/ml的pncqds溶液中,在365nm激发波长下,记录pncqds在451nm下的荧光强度值;通过origin软件线性拟合vb12浓度与pncqds荧光强度,得到线性方程:f0/f=0.11956[vb12]+1.35303,r2=0.994。式中f0、f分别为vb12加入前后pncqds的荧光强度;可检测的线性范围为1.99-31.01µmol/l,最低检出限为0.785µmol/l;(4)待测样品的检测:将待测样品溶于生理盐水中,通过测量加入样品前后pncqds荧光强度的变化,代入线性方程即可得到样品中vb12的含量;(5)实际样品中vb12的加标回收率的测定:向待测样品中加入pncqds储备液,使体系中pncqds浓度为0.2mg/ml;vb12储备液用生理盐水稀释至vb12的浓度为2mmol/l的vb12标准溶液,然后将vb12标准溶液加入体系中,测试实际样品中vb12的加标回收率。本方法的优点在于:碳源蔗糖廉价易得,乙二胺和浓磷酸均为普通试剂,容易采购。探针制备方法简单,无需昂贵仪器,可快速、高效、定量实现vb12的检测。所制备的荧光探针性能稳定,抗干扰能力强。总而言之,与其他检测vb12的方法相比,该方法具有快速有效,性能稳定,抗干扰能力强,无需昂贵的仪器设备,操作简便,检测成本低等优点,为vb12检测提供了一种全新的方法。附图说明图1为实施例1中所制备的pncqds的紫外光谱图以及荧光光谱图。图2为实施例1中所制备的pncqds的激发波长依赖性光谱图。图3为实施例2中各种金属离子(fe3+,pb2+,k+,fe2+,mg2+,cu2+,al3+,ni2+,ag+,ca2+,cr3+,na+,mn2+,zn2+)对vb12检测的干扰实验结果图。图4为实施例2中各种氨基酸(半胱氨酸、色氨酸、天冬氨酸、赖氨酸、苏氨酸、丙氨酸、缬氨酸、酪氨酸、谷氨酸、苯丙氨酸、天冬酰胺、甘氨酸、组氨酸、异亮氨酸、甲硫氨酸、l-亮氨酸、丝氨酸)以及一些b族维生素(vb1、vb3、vb7)对vb12检测的干扰实验结果。图5为实施例3中利用vb12滴定pncqds溶液,pncqds荧光强度的变化曲线图。图6为实施例3中vb12浓度与pncqds荧光强度的线性图。具体实施方式实施例1:pncqds的制备及表征步骤一,称量0.4g蔗糖,向其中加入6ml乙二胺和4ml浓磷酸,得到深褐色黏稠物。步骤二,待烧杯冷却至室温后,向其中加入30ml二次水,搅拌,8000转/分钟离心15分钟,利用500-1000da的透析袋透析处理三天,得到澄清的pncqds溶液。步骤三,冷冻干燥制得pncqds固体粉末。步骤四,称量0.5gpncqds固体粉末于烧杯中,向其中加入50ml二次水,搅拌使其充分溶解,得到浓度为10mg/ml的pncqds储备液。性质表征见图1和图2。图1在pncqds的紫外吸收光谱图中,有两个明显的吸收峰位于276nm和323nm,分别由c=o的n→π*跃迁和n/p掺杂产生的表面缺陷引起;图1中pncqds的最佳激发和发射峰分别位于365nm和451nm。图2是pncqds在不同激发波长下的发射光谱图,当激发波长从300nm变化到500nm时,发射波长由439nm红移到561nm,说明pncqds具有激发波长依赖性。实施例2:维生素b12检测的抗干扰实验步骤一,称量不同质量金属离子(fe3+,pb2+,k+,fe2+,mg2+,cu2+,al3+,ni2+,ag+,ca2+,cr3+,na+,mn2+,zn2+)化合物,加入10ml二次水,配制成浓度为0.1mol/l的金属离子储备液。步骤二,分别称量一定质量半胱氨酸、色氨酸、天冬氨酸、赖氨酸、苏氨酸、丙氨酸、缬氨酸、酪氨酸、谷氨酸、苯丙氨酸、天冬酰胺、甘氨酸、组氨酸、异亮氨酸、甲硫氨酸、l-亮氨酸、丝氨酸,加入5ml二次水,配制成浓度为0.01mol/l的氨基酸储备液。步骤三,分别称量0.015gvb1,0.0062gvb3,0.0122gvb7,加入5ml生理盐水,搅拌使其溶解,配制0.01mol/l的b族维生素储备液。步骤四,向浓度为2mg/ml碳点溶液(2ml)中加入金属离子储备液9µl,此时金属离子浓度为0.3mmol/l,测量此时的荧光强度,记为f0;再向其中加入20µlvb12储备液,此时vb12浓度为34µmol/l,测量此时的荧光强度,记为f。实验结果见图3。步骤五,向浓度为2mg/ml碳点溶液(2ml)中加入氨基酸储备液90µl,此时氨基酸浓度为0.3mmol/l,测量此时的荧光强度,记为f0;再向其中加入20µlvb12储备液,此时vb12浓度为34µmol/l,测量此时的荧光强度,记为f。实验结果见图4。步骤六,向浓度为2mg/ml碳点溶液(2ml)中加入b族维生素储备液90µl,此时b族维生素浓度为0.3mmol/l,测量此时的荧光强度,记为f0;再向其中加入20µlvb12储备液,此时vb12浓度为34µmol/l,测量此时的荧光强度,记为f。实验结果见图4。图3是不同金属离子对vb12检测的干扰性研究,说明vb12检测不受金属离子的干扰;图4是不同氨基酸和其他b族维生素对vb12检测的干扰性研究,说明vb12检测不受氨基酸和其他b族维生素的干扰。结果说明pncqds对vb12检测时具有很好的抗干扰性。实施例3:维生素b12滴定pncqds的线性方程步骤一,测量2mg/ml碳点溶液的荧光强度,记为f0。步骤二,向其中逐滴滴加vb12储备液,分别记录荧光强度,记为f。荧光强度变化见图5。步骤三,利用origin软件,拟合荧光强度变化(f0/f)和vb12浓度之间的线性方程,结果见图6。图5表明随着vb12储备液的加入,pncqds的荧光逐渐被猝灭,说明vb12对pncqds的荧光有特异的猝灭效果。图6是pncqds荧光强度的变化值与vb12浓度之间的线性关系图,线性方程为f0/f=0.11956[vb12]+1.35303,线性范围为1.99-31.01µmol/l,最低检出限为0.785µmol/l,相关性系数r2=0.994。实施例4:实际样品中vb12含量检测步骤一,取四片利丰vb12片剂(山西利丰华瑞制药有限公司,国药准字h14023061),将其全部捣碎,加入10ml生理盐水,搅拌使其充分溶解,溶液在6000转/分钟的台式离心机下离心15分钟,取上清液,取该溶液5ml,稀释至10ml,备用。步骤二,取四片国润vb12片剂(山西国润制药有限公司,国药准字h14022782),将其全部捣碎,加入20ml生理盐水,搅拌使其完全溶解,溶液在6000转/分钟的台式离心机下离心15分钟,取上清液,备用。步骤三,取0.4ml方明vb12注射剂(山东方明药业集团股份有限公司h37021054),用生理盐水稀释至10ml,备用。步骤四,向1600µl二次水中加400µlpncqds储备液,此时碳点浓度为0.2mg/ml,测量荧光强度,记为f0。步骤五,将步骤四中的二次水分别替换为样品溶液,测量此时的荧光强度,记为f。步骤六,将f0/f代入线性方程,计算得到所对应样品中vb12的含量。结果见表1,表明利用pncqds检测vb12的方法可用于实际样品中vb12含量的检测,且相对标准偏差均小于6.8%,具有良好的重现性。表1:三种实际样品中vb12的含量样品vb12含量(µm)相对标准偏差(%)利丰vb12片剂10.5871.8国润vb12片剂4.6123.1方明vb12注射剂7.7796.8实施例5:实际样品中维生素b12的加标回收实验步骤一,取3.868mlvb12储备液稀释至10ml,此时vb12浓度为2mmol/l。步骤二,向1600µl样品溶液中加400µlpncqds储备液,测量荧光强度,记为f0。步骤三,向利丰vb12溶液中滴加12.62µl浓度为2mmol/l的vb12溶液,测量荧光强度,记为f。步骤四,向国润vb12溶液中滴加2.62µl浓度为2mmol/l的vb12溶液,测量荧光强度,记为f。步骤五,向2ml方明vb12注射剂溶液中滴加2.62µl浓度为2mmol/l的vb12溶液,测量荧光强度,记为f。步骤六,将f0/f代入线性方程,计算得到三种实际样品中vb12的加标回收率。结果见表2。表2说明三种实际样品中的vb12的加标回收率介于94.5%与103.9%之间,相对标准偏差小于7.8%,表明pncqds可用于实际样品中vb12的检测,该方法具有很好的重现性。表2:实施例5中三种实际样品中vb12的加标回收实验结果实际样品vb12加入量(µm)vb12检出量(µm)相对标准偏差(%)回收率(%)利丰vb12片2.6213.6552.7103.9国润vb12片2.626.8324.394.5方明vb12注射剂2.6210.1577.897.7当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1