一种复合催化材料、制备方法及其在双羟基/双甲基呋喃类化合物可控制备中的应用与流程
本发明属于生物质能源化工领域,具体涉及一种复合催化材料、制备方法及其在双羟基/双甲基呋喃类化合物可控制备中的应用。
背景技术:
随着全球化石资源供需矛盾的日益凸显以及环境污染现象的不断加剧,利用廉价可再生的生物质资源制备高附加值的化学品和高品质的液体燃料已经引起了国内外众多研究者的广泛关注。由生物质基5-羟甲基糠醛经过选择性加氢制备得到的2,5-二羟甲基呋喃和2,5-二甲基呋喃是一类新型对称的呋喃类化合物,用途极为广泛。其中,2,5二羟甲基呋喃可以作为单体合成聚酯类、聚醚类和冠醚类材料等,还可以作为原料合成药物中间体、核苷衍生物和表面活性剂等;2,5-二甲基呋喃不仅是一种能量密度高、辛烷值高、沸点高和汽柴油混溶性好的液体燃料,还可以用于合成大宗化学品对二甲苯等。众所周知,5-羟甲基糠醛分子中同时含有一个醛基、一个醇羟基和一个呋喃环,这使得它的化学性质非常活泼,发生加氢反应时的产物比较复杂,因此,如何保证醛基和醇羟基的优先加氢,同时尽量避免呋喃环的过度加氢是5-羟甲基糠醛选择性加氢制备2,5-二羟甲基呋喃和2,5-二甲基呋喃过程中需要首先解决的问题,而开发合适的催化反应体系对于解决这一问题则起着至关重要的作用。
cn105712854a公开了一种选择性制备2,5-二羟甲基呋喃的方法,该方法使用半三明治型ir络合物为催化剂,甲酸、甲酸盐、氢气为氢源,虽可高得率累积2,5-二羟甲基呋喃,但其需要贵金属催化剂且催化剂制备过程较为复杂,而且甲酸具有强腐蚀性,氢气存在极大的安全隐患。
中国专利cn106946820a公开了一种5-羟甲基糠醛制备2,5-二羟甲基呋喃及其醚化产物的方法,该方法使用的催化剂为zro2/beta1401、zro2/mcm-41、zro2/usy和zno-zro2/sba-15等负载型催化剂,其制备过程较为繁琐,制备时间较长。
中国专利cn108084119a公开了一种低相转移温度共混体系中制备2,5-二羟甲基呋喃的方法,该方法使用的低共熔溶剂和硼氢化钠作为催化反应体系,其组成非常复杂,操作步骤繁多。
中国专利cn104557802a公开了一种5-羟甲基糠醛选择性加氢脱氧制备2,5-二甲基呋喃的方法,该方法使用负载型贵金属作为催化剂,催化剂成本高,使用氢气为氢源,原子利用率和安全性差。
中国专利cn108586392a公开了一种种5-羟甲基糠醛原位加氢制备2,5-二甲基呋喃的方法,该方法虽然使用廉价的非贵金属催化剂和乙醇氢供体,但是催化剂制备过程和催化反应过程温度极高,能耗高。
另外,2,5-二羟甲基呋喃和2,5-二甲基呋喃的选择性合成过程一般情况下需要不同的催化反应体系,适合于2,5-二羟甲基呋喃合成的不一定适合2,5-二甲基呋喃的合成,反之亦然。
技术实现要素:
开发一种新型催化反应体系,既适合于2,5-二羟甲基呋喃的合成,又适合于2,5-二甲基呋喃的合成,那么对于生物质的高效利用来说意义重大。本发明的目的在于提供一种新型对称双羟基/双甲基呋喃类化合物的可控制备方法,通过控制催化剂载体的酸碱性、活性金属类型和负载量以及反应温度时间,可以让2,5-二羟甲基呋喃和2,5-二甲基呋喃能够在同一个反应体系中实现选择性可控合成。
本发明的第一个方面,提供了:
一种催化材料,所述的催化材料包括载体及负载于载体之上的活性金属;所述的活性金属为cu、ni、co、zn、fe、al或sn中的一种,更优选为cu或ni中的一种;所述的催化剂的载体为zr或hf的有机膦酸配位聚合物。
在一个实施方式中,所述的催化剂的载体为zr-medpa(锆-亚甲基二膦酸聚合物)、zr-bpdpa(锆-联苯-4,4-二膦酸聚合物)、hf-detpmpa(铪-2,5-二羟基-1,4-苯二膦酸聚合物)、hf-hedpa(铪-羟基乙叉二膦酸聚合物)、hf-tppa(铪-三聚膦酸聚合物)或hf-ihpa(铪-肌醇六膦酸聚合物)中的一种,更有选为zr-bpdpa、hf-hedpa或hf-ihpa中的一种。
在一个实施方式中,所述的活性金属在无定型介孔金属膦酸聚合物载体上的负载量为2-5wt%。
本发明的第二个方面,提供了:
上述的催化材料的制备方法,包括如下步骤:
载体的制备:将第一金属氯化物与有机溶剂混合,得到第一混合溶液;将有机膦酸配体与有机溶剂混合,得到第二混合溶液;将第一混合溶液加入至第二混合溶液中,再加入三乙胺,进行反应后,陈化,将生成的沉淀洗涤、干燥、粉碎后,得到无定型介孔金属膦酸聚合物载体;
活性中心的负载:将无定型介孔金属膦酸聚合物载体分散于含有第二金属氯化物的溶液当中,再加入nabh4的水溶液进行反应,将生成的沉淀洗涤、干燥、粉碎后,得到活性金属负载无定型介孔金属膦酸聚合物催化剂。
在一个实施方式中,有机溶剂是二甲基甲酰胺。
在一个实施方式中,第一金属氯化物、有机膦酸配体、三乙胺的摩尔比是1:0.8-1.2:5.5-6.5。
在一个实施方式中,载体的制备中,反应条件是室温下反应3-5h,陈化条件是80℃静置陈化4h。
在一个实施方式中,活性中心的负载中,无定型介孔金属膦酸聚合物载体和nabh4的配比是1g:40-80mg;反应条件是室温超声搅拌15-45min后继续搅拌1-3h。
在一个实施方式中,第一金属氯化物是四氯化锆或四氯化铪;第二金属氯化物是cu、ni、co、zn、fe、al或sn的氯化物盐。
在一个实施方式中,有机膦酸选自亚甲基二膦酸、联苯-4,4-二膦酸、2,5-二羟基-1,4-苯二膦酸、羟基乙叉二膦酸、三聚膦酸、肌醇六膦酸中的一种或几种的混合。
本发明的第三个方面,提供了:
上述的催化材料在对称双羟基/双甲基呋喃类化合物的可控制备中的应用。
在一个实施方式中,所述的应用包括如下步骤:
第1步,将5-羟甲基糠醛、活性金属负载无定型介孔金属膦酸聚合物催化剂、有机二元醇混合物作为原料液置于高压反应釜中;
第2步,先升温至第一温度,进行反应得到2,5-二羟甲基呋喃;
第3步,再升温至第二温度,进行反应得到2,5-二甲基呋喃。
在一个实施方式中,所述的有机二元醇为1,4-丁二醇或1,4-戊二醇中的一种。
在一个实施方式中,所述的5-羟甲基糠醛用量为有机二元醇用量的2-4wt%。
在一个实施方式中,所述的催化剂用量为5-羟甲基糠醛用量的50-80wt%。
在一个实施方式中,第2步,反应温度为120-150℃,反应时间为2-6h。
在一个实施方式中,第3步,反应温度为180-220℃,反应时间为1-5h。
有益效果
1)催化剂由廉价易得的非贵金属和具有无定型介孔结构且具有lewis酸碱性位点和brϕnsted酸性位点的金属膦酸配位聚合物组成,同时具备较强的羰基还原能力和羟基氢解能力,即可以将5-羟甲基糠醛选择性还原为2,5-二羟甲基呋喃,又可以将2,5-二羟甲基呋喃氢解为2,5-二甲基呋喃;2)1,4-丁二醇和1,4-戊二醇是一类可再生的有机二元醇,不仅可以同时作为高效的原位氢供体和反应介质,避免了外源氢供体和其他反应溶剂的使用,而且其脱氢产物g-丁内酯和δ-戊内酯也是一类高附加值的化学品,进一步提高了整个反应过程的经济性;3)采用分段控温法,可以选择性控制催化剂的羰基还原能力和羟基氢解能力,根据实际需要在同一个反应体系中实现2,5-二羟甲基呋喃和2,5-二甲基呋喃的可控制备,具备良好的工业化应用前景。
附图说明
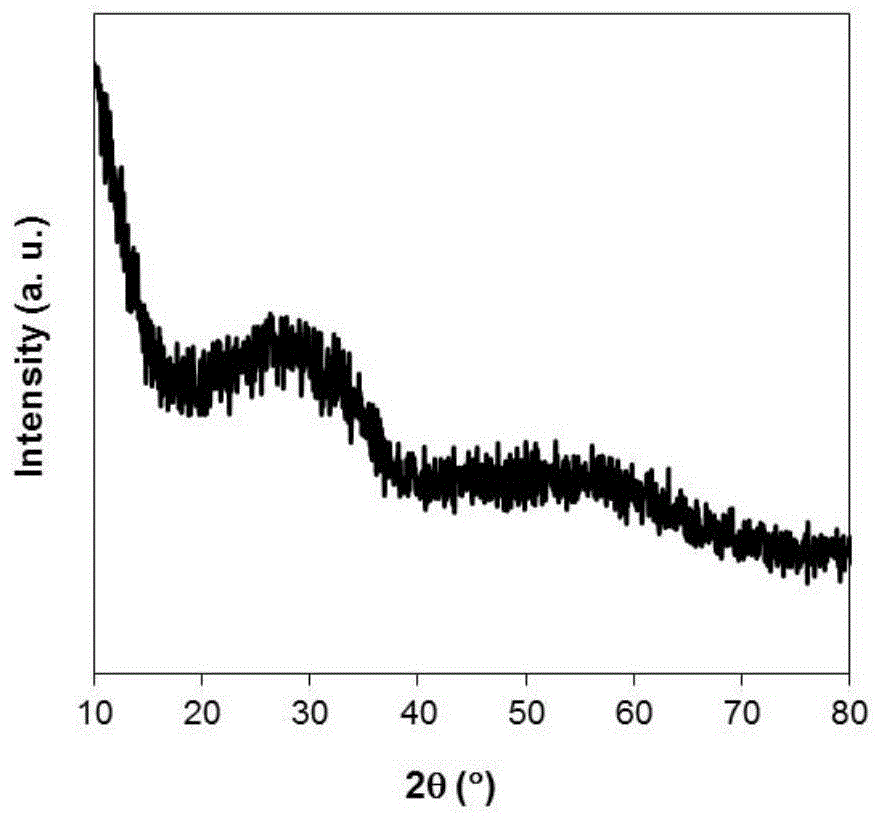
图1是本发明实施例1中所用催化剂的xrd图。
图2是本发明实施例1中所用催化剂的孔径分布图。
图3是本发明实施例1中所用催化剂的ft-ir图。
图4是本发明实施例2中制备得到的2,5-二羟甲基呋喃的气相色谱图;
图5是本发明实施例2中制备得到的2,5-二甲基呋喃的气相色谱图;
具体实施方式
本发明首先提出了一种催化材料,其应用于对称双羟基/双甲基呋喃类化合物的可控制备中,所述的催化材料包括载体及负载于载体之上的活性金属;所述的活性金属为cu、ni、co、zn、fe、al或sn中的一种,更优选为cu或ni中的一种。
在一个实施方式中,所述的催化剂的载体为zr或hf的有机膦酸配位聚合物。
在一个实施方式中,所述的催化剂的载体为zr-medpa(锆-亚甲基二膦酸聚合物)、zr-bpdpa(锆-联苯-4,4-二膦酸聚合物)、hf-detpmpa(铪-2,5-二羟基-1,4-苯二膦酸聚合物)、hf-hedpa(铪-羟基乙叉二膦酸聚合物)、hf-tppa(铪-三聚膦酸聚合物)或hf-ihpa(铪-肌醇六膦酸聚合物)中的一种,更有选为zr-bpdpa、hf-hedpa或hf-ihpa中的一种。
在一个实施方式中,所述的活性金属在无定型介孔金属膦酸聚合物载体上的负载量为2-5wt%。
上述的催化剂由廉价易得的非贵金属和具有无定型介孔结构且具有lewis酸碱性位点和brϕnsted酸性位点的金属膦酸配位聚合物组成,主要技术构思是:金属膦酸配位聚合物载体上形成的zr-o-p或hf-o-p结构中,zr4+/hf4+显示lewis酸性,o2-显示lewis碱性,而p元素的存在又可以增强o2-的lewis碱性,在三者相互作用下可以使5-羟甲基糠醛上的醛基选择性转化为2,5-二羟甲基呋喃;另外,金属膦酸配位聚合物载体上未参与配位的膦羟基显示brϕnsted酸性,它的存在可以增强活性金属的醇羟基氢解能力,有利于促进碳氧键的断裂,进而使2,5-二羟甲基呋喃选择性转化为2,5-二甲基呋喃。
上述的催化材料的制备方法,包括如下步骤:
载体的制备:将第一金属氯化物与有机溶剂混合,得到第一混合溶液;将有机膦酸配体与有机溶剂混合,得到第二混合溶液;将第一混合溶液加入至第二混合溶液中,再加入三乙胺,进行反应后,陈化,将生成的沉淀洗涤、干燥、粉碎后,得到无定型介孔金属膦酸聚合物载体;
活性中心的负载:将无定型介孔金属膦酸聚合物载体分散于含有第二金属氯化物的溶液当中,再加入nabh4的水溶液进行反应,将生成的沉淀洗涤、干燥、粉碎后,得到活性金属负载无定型介孔金属膦酸聚合物催化剂。
在一个实施方式中,第一金属氯化物、有机膦酸配体、三乙胺的摩尔比是1:0.8-1.2:5.5-6.5。
在一个实施方式中,载体的制备中,反应条件是室温下反应3-5h,陈化条件是80℃静置陈化4h。
在一个实施方式中,活性中心的负载中,无定型介孔金属膦酸聚合物载体和nabh4的配比是1g:40-80mg;反应条件是室温超声搅拌15-45min后继续搅拌1-3h。
在一个实施方式中,第一金属氯化物是四氯化锆或四氯化铪;第二金属氯化物是cu、ni、co、zn、fe、al或sn的氯化物盐。
在一个实施方式中,有机膦酸选自亚甲基二膦酸、联苯-4,4-二膦酸、2,5-二羟基-1,4-苯二膦酸、羟基乙叉二膦酸、三聚膦酸、肌醇六膦酸中的一种或几种的混合。
更具体地,一个典型的制备方法如下:
上述的催化剂的制备方法如下,将10mmol四氯化锆或四氯化铪和10mmol相应的有机膦酸配体分别加入到400ml二甲基甲酰胺溶剂中,充分搅拌至完全溶解;将四氯化锆或四氯化铪溶液缓慢加入到有机膦酸配体溶液中,再向上述混合溶液中逐滴加入60mmol的三乙胺,室温条件下继续搅拌4h,升温至80℃静置陈化4h;固体沉淀经过滤分离后,用二甲基甲酰胺和乙醇反复洗涤直至检测不到氯离子存在为止;将洗涤后的固体沉淀在80℃真空干燥12h,并将其研磨粉碎至约200目,即可得到无定型介孔金属膦酸聚合物载体;取1g无定型介孔金属膦酸聚合物载体分散于300ml含有活性金属氯化物的去离子水中,超声搅拌30min后继续室温搅拌2h;在冰浴条件下向上述混合液中缓慢逐滴加入100ml含有50mgnabh4的水溶液,继续室温搅拌2h;固体沉淀用去离子水和乙醇洗涤6次,最后在80℃下真空干燥12h,即可得活性金属负载无定型介孔金属膦酸聚合物催化剂。
上述的催化剂应用于新型对称双羟基/双甲基呋喃类化合物的可控制备方法,具体步骤为:将5-羟甲基糠醛和活性金属负载无定型介孔金属膦酸聚合物催化剂加入到有机二元醇中,反应釜经密封、置换空气和分段控温加热后,即可在同一反应体系中选择性得到2,5-二羟甲基呋喃和2,5-二甲基呋喃。本发明使用的催化剂由廉价易得的非贵金属和无定型介孔的金属膦酸聚合物载体组成,同时具备较强的羰基还原能力和羟基氢解能力;使用可再生的有机二元醇同时作为高效的原位氢供体和反应介质,可以避免外源氢供体和其他反应溶剂的使用,而且有机二元醇的脱氢产物也是一类高附加值的化学品,可以进一步提高整个反应过程的经济性;采用分段控温法,可以选择性控制催化剂的羰基还原能力和羟基氢解能力,根据实际需要实现2,5-二羟甲基呋喃和2,5-二甲基呋喃的可控制备,具备良好的工业化应用前景。
更具体的说,本发明的制备方法如下:
将5-羟甲基糠醛和活性金属负载无定型介孔金属膦酸聚合物催化剂按照一定比例加入到有机二元醇中,混合均匀后将所得混合物作为原料液置于高压反应釜中,高压反应釜经密封置换空气后,在400rpm的搅拌速度下先升温至指定温度1,经过一段反应时间1后可得2,5-二羟甲基呋喃,再继续升温至指定温度2,经过一段反应时间2后,即可得2,5-二甲基呋喃。
其中,所述的有机二元醇为1,4-丁二醇或1,4-戊二醇中的一种。
其中,所述的5-羟甲基糠醛用量为有机二元醇用量的2-4wt%。
其中,所述的催化剂用量为5-羟甲基糠醛用量的50-80wt%。
其中,所述的活性金属在无定型介孔金属膦酸聚合物载体上的负载量为2-5wt%。
其中,所述的指定温度1为120-150℃,反应时间1为2-6h,指定温度2为180-220℃,反应时间为1-5h。
实施例1
将10mmol四氯化锆和10mmol联苯-4,4-二膦酸配体分别加入到400ml二甲基甲酰胺溶剂中,充分搅拌至完全溶解;将四氯化锆溶液缓慢加入到有机膦酸配体溶液中,再向上述混合溶液中逐滴加入60mmol的三乙胺,室温条件下继续搅拌4h,升温至80℃静置陈化4h;固体沉淀经过滤分离后,用二甲基甲酰胺和乙醇反复洗涤直至检测不到氯离子存在为止;将洗涤后的固体沉淀在80℃真空干燥12h,并将其研磨粉碎至约200目,即可得到无定型介孔金属膦酸聚合物载体;取1g无定型介孔金属膦酸聚合物载体分散于300ml含有根据负载量计的cucl2的去离子水中,超声搅拌30min后继续室温搅拌2h;在冰浴条件下向上述混合液中缓慢逐滴加入100ml含有50mgnabh4的水溶液,继续室温搅拌2h;固体沉淀用去离子水和乙醇洗涤6次,最后在80℃下真空干燥12h,即可得活性金属负载无定型介孔金属膦酸聚合物催化剂(cu/zr-bpdpa)。
图1和图2分别为cu/zr-bpdpa的xrd图和孔径分布图,其结果显示,cu/zr-bpdpa仅在2q为20-40°和40-70°范围内有两个较宽的衍射峰,除此之外无其他明显的衍射峰,另外,cu/zr-bpdpa的平均孔径约为10nm,这说明zr-bpdpa载体具有无定型介孔结构,而且活性金属cu在zr-bpdpa载体上分散非常均匀,无团聚现象。图3为cu/zr-bpdpa的ft-ir图,其中,560/757、1121和1023cm-1分别归属于zr-bpdpa载体上zr-o、p-o和zr-o-p的伸缩振动峰,2413cm-1归属于zr-bpdpa载体上未配位的p-oh的伸缩振动峰,这说明zr-bpdpa载体具有lewis酸碱性位点和brϕnsted酸性位点。
将0.5g5-羟甲基糠醛和0.3gcu/zr-bpdpa(cu负载量为3wt%)加入到24.5g1,4-丁二醇中,混合均匀后将所得混合物作为原料液置于高压反应釜中,高压反应釜经密封置换空气后,在400rpm的搅拌速度下升温至140℃,保持3h后,可得2,5-二羟甲基呋喃,经气相色谱仪检测可知,5-羟甲基糠醛转化率为100%,2,5-二羟甲基呋喃得率为94.5%;随后,高压反应釜继续升温至200℃,保持2h后,可得2,5-二甲基呋喃,经气相色谱仪检测可知,2,5-二羟甲基呋喃的转化率为98.8%,2,5-二甲基呋喃最终得率为93.2%。
实施例2
将10mmol四氯化铪和10mmol羟基乙叉二膦酸配体分别加入到400ml二甲基甲酰胺溶剂中,充分搅拌至完全溶解;将四氯化铪溶液缓慢加入到有机膦酸配体溶液中,再向上述混合溶液中逐滴加入60mmol的三乙胺,室温条件下继续搅拌4h,升温至80℃静置陈化4h;固体沉淀经过滤分离后,用二甲基甲酰胺和乙醇反复洗涤直至检测不到氯离子存在为止;将洗涤后的固体沉淀在80℃真空干燥12h,并将其研磨粉碎至约200目,即可得到无定型介孔金属膦酸聚合物载体;取1g无定型介孔金属膦酸聚合物载体分散于300ml含有根据负载量计的cucl2的去离子水中,超声搅拌30min后继续室温搅拌2h;在冰浴条件下向上述混合液中缓慢逐滴加入100ml含有50mgnabh4的水溶液,继续室温搅拌2h;固体沉淀用去离子水和乙醇洗涤6次,最后在80℃下真空干燥12h,即可得活性金属负载无定型介孔金属膦酸聚合物催化剂(cu/hf-hedpa)。
将1g5-羟甲基糠醛和0.7gcu/hf-hedpa(cu负载量为4wt%)加入到24g1,4-丁二醇中,混合均匀后将所得混合物作为原料液置于高压反应釜中,高压反应釜经密封置换空气后,在400rpm的搅拌速度下升温至120℃,保持6h后,可得2,5-二羟甲基呋喃,经气相色谱仪检测可知,5-羟甲基糠醛转化率为98.1%,2,5-二羟甲基呋喃得率为93.1%(图4);随后,高压反应釜继续升温至220℃,保持1h后,可得2,5-二甲基呋喃,经气相色谱仪检测可知,2,5-二羟甲基呋喃的转化率为99.3%,2,5-二甲基呋喃最终得率为90.4%(图5)。
实施例3
将10mmol四氯化铪和10mmol肌醇六膦酸配体分别加入到400ml二甲基甲酰胺溶剂中,充分搅拌至完全溶解;将四氯化铪溶液缓慢加入到有机膦酸配体溶液中,再向上述混合溶液中逐滴加入60mmol的三乙胺,室温条件下继续搅拌4h,升温至80℃静置陈化4h;固体沉淀经过滤分离后,用二甲基甲酰胺和乙醇反复洗涤直至检测不到氯离子存在为止;将洗涤后的固体沉淀在80℃真空干燥12h,并将其研磨粉碎至约200目,即可得到无定型介孔金属膦酸聚合物载体;取1g无定型介孔金属膦酸聚合物载体分散于300ml含有根据负载量计的cucl2的去离子水中,超声搅拌30min后继续室温搅拌2h;在冰浴条件下向上述混合液中缓慢逐滴加入100ml含有50mgnabh4的水溶液,继续室温搅拌2h;固体沉淀用去离子水和乙醇洗涤6次,最后在80℃下真空干燥12h,即可得活性金属负载无定型介孔金属膦酸聚合物催化剂(cu/hf-ihpa)。
将0.6g5-羟甲基糠醛和0.3gcu/hf-ihpa(cu负载量为5wt%)加入到19.4g1,4-丁二醇中,混合均匀后将所得混合物作为原料液置于高压反应釜中,高压反应釜经密封置换空气后,在400rpm的搅拌速度下升温至150℃,保持2h后,可得2,5-二羟甲基呋喃,经气相色谱仪检测可知,5-羟甲基糠醛转化率为100%,2,5-二羟甲基呋喃得率为96.5%;随后,高压反应釜继续升温至190℃,保持3h后,可得2,5-二甲基呋喃,经气相色谱仪检测可知,2,5-二羟甲基呋喃的转化率为99.8%,2,5-二甲基呋喃最终得率为94.0%。
实施例4
将10mmol四氯化锆和10mmol联苯-4,4-二膦酸配体分别加入到400ml二甲基甲酰胺溶剂中,充分搅拌至完全溶解;将四氯化锆溶液缓慢加入到有机膦酸配体溶液中,再向上述混合溶液中逐滴加入60mmol的三乙胺,室温条件下继续搅拌4h,升温至80℃静置陈化4h;固体沉淀经过滤分离后,用二甲基甲酰胺和乙醇反复洗涤直至检测不到氯离子存在为止;将洗涤后的固体沉淀在80℃真空干燥12h,并将其研磨粉碎至约200目,即可得到无定型介孔金属膦酸聚合物载体;取1g无定型介孔金属膦酸聚合物载体分散于300ml含有根据负载量计的nicl2的去离子水中,超声搅拌30min后继续室温搅拌2h;在冰浴条件下向上述混合液中缓慢逐滴加入100ml含有50mgnabh4的水溶液,继续室温搅拌2h;固体沉淀用去离子水和乙醇洗涤6次,最后在80℃下真空干燥12h,即可得活性金属负载无定型介孔金属膦酸聚合物催化剂(ni/zr-bpdpa)。
将0.5g5-羟甲基糠醛和0.4gni/zr-bpdpa(ni负载量为2wt%)加入到24.5g1,4-戊二醇中,混合均匀后将所得混合物作为原料液置于高压反应釜中,高压反应釜经密封置换空气后,在400rpm的搅拌速度下升温至130℃,保持4h后,可得2,5-二羟甲基呋喃,经气相色谱仪检测可知,5-羟甲基糠醛转化率为100%,2,5-二羟甲基呋喃得率为95.7%;随后,高压反应釜继续升温至180℃,保持5h后,可得2,5-二甲基呋喃,经气相色谱仪检测可知,2,5-二羟甲基呋喃的转化率为99.4%,2,5-二甲基呋喃最终得率为92.9%。
实施例5
将10mmol四氯化铪和10mmol羟基乙叉二膦酸配体分别加入到400ml二甲基甲酰胺溶剂中,充分搅拌至完全溶解;将四氯化铪溶液缓慢加入到有机膦酸配体溶液中,再向上述混合溶液中逐滴加入60mmol的三乙胺,室温条件下继续搅拌4h,升温至80℃静置陈化4h;固体沉淀经过滤分离后,用二甲基甲酰胺和乙醇反复洗涤直至检测不到氯离子存在为止;将洗涤后的固体沉淀在80℃真空干燥12h,并将其研磨粉碎至约200目,即可得到无定型介孔金属膦酸聚合物载体;取1g无定型介孔金属膦酸聚合物载体分散于300ml含有根据负载量计的nicl2的去离子水中,超声搅拌30min后继续室温搅拌2h;在冰浴条件下向上述混合液中缓慢逐滴加入100ml含有50mgnabh4的水溶液,继续室温搅拌2h;固体沉淀用去离子水和乙醇洗涤6次,最后在80℃下真空干燥12h,即可得活性金属负载无定型介孔金属膦酸聚合物催化剂(ni/hf-hedpa)。
将0.6g5-羟甲基糠醛和0.36gni/hf-hedpa(ni负载量为3wt%)加入到19.4g1,4-戊二醇中,混合均匀后将所得混合物作为原料液置于高压反应釜中,高压反应釜经密封置换空气后,在400rpm的搅拌速度下升温至140℃,保持4h后,可得2,5-二羟甲基呋喃,经气相色谱仪检测可知,5-羟甲基糠醛转化率为100%,2,5-二羟甲基呋喃得率为94.8%;随后,高压反应釜继续升温至200℃,保持3h后,可得2,5-二甲基呋喃,经气相色谱仪检测可知,2,5-二羟甲基呋喃的转化率为99.2%,2,5-二甲基呋喃最终得率为91.8%。
实施例6
将10mmol四氯化铪和10mmol肌醇六膦酸配体分别加入到400ml二甲基甲酰胺溶剂中,充分搅拌至完全溶解;将四氯化铪溶液缓慢加入到有机膦酸配体溶液中,再向上述混合溶液中逐滴加入60mmol的三乙胺,室温条件下继续搅拌4h,升温至80℃静置陈化4h;固体沉淀经过滤分离后,用二甲基甲酰胺和乙醇反复洗涤直至检测不到氯离子存在为止;将洗涤后的固体沉淀在80℃真空干燥12h,并将其研磨粉碎至约200目,即可得到无定型介孔金属膦酸聚合物载体;取1g无定型介孔金属膦酸聚合物载体分散于300ml含有根据负载量计的性nicl2的去离子水中,超声搅拌30min后继续室温搅拌2h;在冰浴条件下向上述混合液中缓慢逐滴加入100ml含有50mgnabh4的水溶液,继续室温搅拌2h;固体沉淀用去离子水和乙醇洗涤6次,最后在80℃下真空干燥12h,即可得活性金属负载无定型介孔金属膦酸聚合物催化剂(ni/hf-ihpa)。
将0.5g5-羟甲基糠醛和0.35gni/hf-ihpa(ni负载量为4wt%)加入到24.5g1,4-戊二醇中,混合均匀后将所得混合物作为原料液置于高压反应釜中,高压反应釜经密封置换空气后,在400rpm的搅拌速度下升温至150℃,保持2h后,可得2,5-二羟甲基呋喃,经气相色谱仪检测可知,5-羟甲基糠醛转化率为100%,2,5-二羟甲基呋喃得率为93.3%;随后,高压反应釜继续升温至220℃,保持2h后,可得2,5-二甲基呋喃,经气相色谱仪检测可知,2,5-二羟甲基呋喃的转化率为98.9%,2,5-二甲基呋喃最终得率为93.1%。
- 还没有人留言评论。精彩留言会获得点赞!