一种基于氧化石墨烯的光电化学双功能传感器的制作方法
本发明涉及生物分析检测领域,尤其是将氧化石墨烯用于光电阴极的制作,并将此光电阴极用作光电化学双功能传感器,实现了碱性磷酸酶与酪氨酸酶活性的测定。
背景技术:
:
碱性磷酸酶(ALP)和酪氨酸酶(TR)是生物分析中广泛使用的酶。ALP与TR的含量与多种疾病密切相关,如ALP是诊断乳腺癌、骨疾病、糖尿病、肝炎等疾病的重要指标之一[Park K S,Lee C Y,Park H G.Analyst,2014,139(18):4691-4695;而TR的活性高低与帕金森病、黑色素瘤以及多种皮肤病等的发生有一定联系[Tessari I,Bisaglia M,Valle F,et al.J.Biol.Chem.,2008,283,16808-16817;Angeletti C,Khomitch V,Halaban R,et al.Diagn.Cytopathol.,2004,31,33-37;Oetting W,King R,J.Invest.Dermatol.,1994,103,131S.]。ALP因其催化活性高且特异性底物众多,从而被广泛使用为免疫分析标记物,用于酶联免疫测定[Khalid W,G,Hühn D,et al.J.Nanobiotechnol.,2011,9(1):46-55]。另外,最近的研究也指出用TR用作免疫分析标记物的良好应用前景[Park S,Singh A,Kim S,et al.Anal.Chem.,2014,86,1560-1566.]。因此,建立ALP与TR的测定方法具有重要意义。目前,已有荧光、电化学、比色等[Qian Z S,Chai L J,Huang Y Y,et al.Biosens.Bioelectron.,2015,68:675-680;Ding J W,Wang X W,Qin W.ACS Appl.Mater.Interfaces,2013,5(19):9488-9493;Yang J J,Zheng L,Wang Y,et al.Biosens.Bioelectron.,2016,77:549-556;Teng Y,Jia X,Li J,et al.Anal.Chem.,2015,87(9):4897-4902;Freeman R,Elbaz J,Gill R,et al.Chem.Eur.J.,2007,13(26):7288-7293;Baron R,Zayats M,Willner I.Anal.Chem.,2005,77(6):1566-1571]方法对ALP与TR进行检测,但这些方法大都存在耗时、灵敏度低等问题,所以寻找更为新颖、简便、灵敏的方法实现ALP以及TR的快速检测具有重要意义。
光电化学法是一种新型的分析技术[Liu S L,Li C,Cheng J,et al.Anal.Chem.2006,78(13):4722-4726],其检测过程与电致化学发光正好相反。由于采用不同形式的检测信号和激发,背景信号低,能达到与电致化学发光相当的高灵敏度。且光电化学具有设备简单、价格低廉、易微型化、响应快速等优点,现已成功用于各种目标物的分析,如DNA测定、免疫分析、环境有害物监测等[Zhang Z X,Zhao C Z.Chin.J.Anal.Chem.,2013,41(3):436-444;Zhao W W,Xu J J,Chen H Y.Chem.Soc.Rev.,2015,44(3):729-741]。但目前大多数的光电化学检测都依赖常规的半导体金属氧化物(TiO2、ZnO等)及量子点(CdS、CdSe等)[An Y R,Tang L L,Jiang X L,et al.Chem.Eur.J.,2010,16(48):14439-14446;Tu W W,Lei J P,Wang P,et al.Chem.Eur.J.,2011,17(34):9440-9447;Wang G L,Xu J J,Chen H Y,et al.Biosens.Bioelectron.,2009,25(4):791-796;Stoll C,Kudera S,Parak W J,et al.Small,2006,2(6):741-743;Zhang X,Guo Y,Liu M,et al.RSC Adv.,2013,3(9):2846-2857],这些材料往往含有金属离子,容易对环境产生危害;而且这些材料易与还原性物质发生光电化学作用,导致方法的选择性不够高,因而急切需要开发新的材料以用于光电化学检测。
氧化石墨烯(GO)是一种最近刚刚兴起的新型碳材料,表面富含多种含氧官能团(羟基、环氧基、羰基、羧基),其制备方法简单、水溶性好、生物相容性好[Lee C,Wei X D,Kysar J W,et al.Science,2008,321(5887):385-388;Kim S J,Lee J M,Kumer R A,et al.Chem.Asian J.,2015,10(5):1192-1197],已被广泛应用于药物传输、光催化、及荧光生物传感等领域[Dreyer D R,Jia H P,Bielawski C W.Angew.Chem.,2010,122(38):6965-6968;Pyun J.Angew.Chem.Int.Ed.,2011,50(1):46-48;Loh K P,Bao Q,Eda G,et al.Nat.Chem.,2010,2(12):1015-1024]。在电化学分析领域,由于GO的导电能力不佳,常将GO还原成还原石墨烯(rGO)或rGO与其它物质复合来构成电极材料[黄海平,朱俊杰.分析化学,2011,39(7):963-971;Akyüz D,Keskin B,U,et al.Appl.Catal.B-Environ.,2016,188:217-226]。在光电化学传感领域,GO主要作为导电材料提高其它的常规半导体纳米材料(作为光电化学传感材料)的光电化学性能从而制备光电化学传感器[Li R Z,Liu Y,Cheng L,et al.Anal.Chem.2014,86(19):9372-9375;Zeng X,Tu W,Li J,et al.ACS Appl.Mater.Interfaces,2014,6(18):16197-16203]。据我们所知,利用单纯的GO修饰电极作为光电化学传感材料构建光电化学传感器的应用还很少。本发明中,我们利用单纯的GO修饰电极作为光电阴极,GO与邻苯二酚(及其衍生物)可以发生氧化还原反应导致光电流的增大,成功实现了对两种天然酶(ALP与TR)的酶活性的高灵敏、高选择性光电化学检测。ALP催化邻苯二酚磷酸酯水解产生邻苯二酚,邻苯二酚与GO发生氧化还原反应,将GO还原为还原氧化石墨烯的同时自身氧化为聚邻苯二酚黏附到电极表面。光照下,聚邻苯二酚作为还原氧化石墨烯的电子受体,抑制了其电子-空穴的复合,使其阴极光电流增大,从而实现ALP的检测。同样,TR催化氧化酪氨酸酶形成的产物左旋多巴也会与GO发生氧化还原反应,导致其阴极光电流的明显增大,基于此,也可实现对TR的检测。本发明开拓了光电阴极在光电化学酶传感中的应用,为ALP以及TR的光电化学检测提供了新原理与新方法。与目前的光电化学酶传感器需要将天然酶固定到电极表面进行测定相比,该方法能成功实现溶液中的酶活性的检测。
技术实现要素:
:
本发明的目的是提供一种基于GO的双功能光电阴极,将GO应用于光电化学传感领域,实现了碱性磷酸酶与酪氨酸酶的活性的测定,为光电化学分析提供了新材料、新原理和新方法。
本发明的目的可通过如下技术措施来实现:
a、氧化石墨烯的制备:将17.5mL浓硫酸和5.4mL的发烟硝酸加入到反应瓶中,冷却至0℃,再加入1g石墨原料搅拌均匀避免结块,之后,在0.5h的时间内缓慢加入一定量的氯酸钾,在室温下搅拌一段时间至反应完全,加入大量的去离子水稀释,过滤直至滤液pH呈中性,真空干燥,将所得到的氧化石墨烯固体加入去离子水中超声,即得到分散后的氧化石墨烯水溶液;
b、氧化石墨烯修饰电极的制备:将预处理过的ITO玻璃浸在含有0.5mol/L NaCl的2%PDDA溶液中,10min后用去离子水洗涤,再在电极表面滴涂25μL 0.5mg/mL的氧化石墨烯溶液,自然干燥后备用;
c、天然酶活性的测定:将250μL一定pH的0.01mol/L的Tris-HCl缓冲溶液,30μL 1.0mmol/L的碱性磷酸酶或者酪氨酸酶的底物、20μL不同浓度的碱性磷酸酶或者酪氨酸酶加入到96微孔板中室温下混合反应20–40min;之后将氧化石墨烯修饰的ITO电极浸入到上述的酶反应溶液中反应5min,随后以pH为7.8的0.01mol/L的Tris-HCl缓冲溶液洗涤电极,将反应后的电极放于pH为7.8的Tris-HCl缓冲溶液中,在相对于Ag/AgCl参比电极为-0.2V的电位下,在自制的光电化学仪器上进行光电流的测定。
本发明的目的还可通过如下技术措施来实现:
制备氧化石墨烯时选用的石墨原料,选自微晶石墨、鳞片石墨;氧化石墨烯的制备过程中加入氯酸钾的量为6–12g,在室温下石墨原料、浓硫酸、发烟硝酸的反应时间为11–22h;酶活性测定时,碱性磷酸酶的反应溶液的pH为8.2,酪氨酸酶的反应溶液的pH为7.8;酶活性测定时选用的碱性磷酸酶的底物为邻苯二酚磷酸酯,酪氨酸酶的底物为苯酚,L-酪氨酸。
附图说明:
图1是实施实例1制备的GO修饰电极与不同浓度的邻苯二酚(从a到g依次为0,0.005,0.01,0.1,0.5,1.0,5.0μmol/L)反应之后的光电流
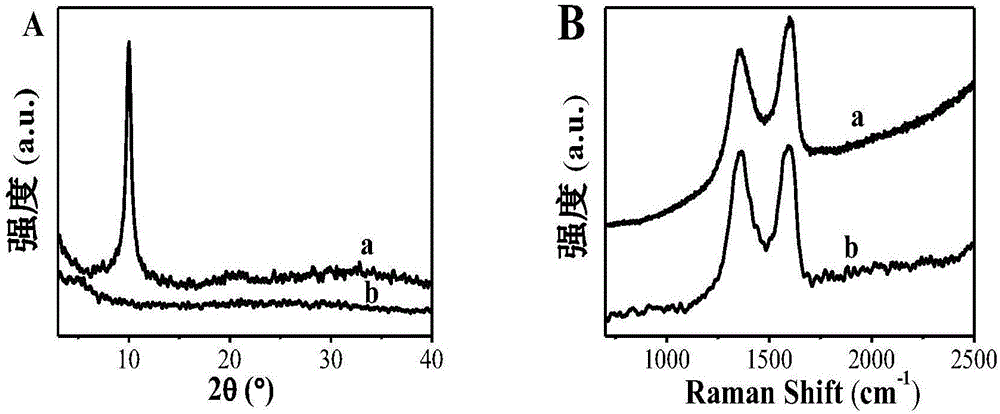
图2是(a)实施实例1制备的GO、(b)与邻苯二酚反应后的GO的(A)X射线衍射图和(B)拉曼光谱图。
图3是(A)不同浓度ALP(0,0.005,0.01,0.1,0.5,1,5,10,50,100U/L)对实施实例1制备的GO修饰电极的光电流影响;(B)光电流变化程度(I/I0)与ALP浓度对数的线性关系。
图4是(A)不同浓度TR(0,0.0005,0.001,0.005,0.01,0.05,0.1,0.5,5.0U/mL)对实施实例2制备的GO修饰电极的光电流影响;(B)光电流变化程度(I/I0)与酪氨酸酶浓度对数的线性关系。
实施实例1:
a、氧化石墨烯的制备:将17.5mL浓硫酸和5.4mL的发烟硝酸加入到反应瓶中,冷却至0℃,再加入1g天然鳞片石墨搅拌均匀避免结块,之后在0.5h的时间内缓慢加入11g氯酸钾,在室温下搅拌20h至反应完全,加入大量的去离子水稀释,过滤直至滤液pH呈中性,真空干燥,将所得到的氧化石墨烯固体加入去离子水中超声,即得到分散后的氧化石墨烯水溶液;
b、氧化石墨烯修饰电极的制备:将预处理过的ITO玻璃浸在含有0.5mol/L NaCl的2%PDDA溶液中,10min后用去离子水洗涤,再在电极表面滴涂25μL 0.5mg/mL的氧化石墨烯溶液,自然干燥后备用;
c、天然酶活性的测定:将250μL pH为8.2的0.01mol/L的Tris-HCl缓冲溶液,30μL 1.0mmol/L的邻苯二酚磷酸酯、20μL不同浓度的碱性磷酸酶加入到96微孔板中室温下混合反应40min;之后将氧化石墨烯修饰的ITO电极浸入到上述的酶反应溶液中反应5min,随后以pH为7.8的0.01mol/L的Tris-HCl缓冲溶液洗涤电极,将反应后的电极放于pH为7.8的Tris-HCl缓冲溶液中,在相对于Ag/AgCl参比电极为-0.2V的电位下,在自制的光电化学仪器上进行光电流的测定。
实施实例2:
a、氧化石墨烯的制备:将17.5mL浓硫酸和5.4mL的发烟硝酸加入到反应瓶中,冷却至0℃,在加入1g膨胀石墨搅拌均匀避免结块,之后在0.5h的时间内缓慢加入9g氯酸钾,在室温下搅拌12h至反应完全,加入大量的去离子水稀释,过滤直至滤液pH呈中性,真空干燥,将所得到的氧化石墨烯固体加入去离子水中超声,即得到分散后的氧化石墨烯水溶液;
b、氧化石墨烯修饰电极的制备:将预处理过的ITO玻璃浸在含有0.5mol/L NaCl的2%PDDA溶液中,10min后用去离子水洗涤,再在电极表面滴涂25μL 0.5mg/mL的氧化石墨烯溶液,自然干燥后备用;
c、天然酶活性的测定:将250μL pH为7.8的0.01mol/L的Tris-HCl缓冲溶液,30μL 1.0mmol/L的L-酪氨酸、20μL不同浓度的酪氨酸酶加入到96微孔板中室温下混合反应30min;之后将氧化石墨烯修饰的ITO电极浸入到上述的酶反应溶液中反应5min,随后以pH为7.8的0.01mol/L的Tris-HCl缓冲溶液洗涤电极,将反应后的电极放于pH为7.8的Tris-HCl缓冲溶液中,在自制的光电化学仪器上进行光电流的测定。
- 还没有人留言评论。精彩留言会获得点赞!