量子点荧光探针及其制备方法、免疫层析试纸与流程
本发明涉及食品安全检测领域,具体而言,涉及一种量子点荧光探针及其制备方法、免疫层析试纸。
背景技术:
“瘦肉精”是一类药物的统称,任何能够促进瘦肉生长、抑制肥肉生长的物质都可以叫做“瘦肉精”。但是,瘦肉精在人体内蓄积会使人出现恶心、呕吐、头晕、心律失常等症状,严重时甚至能导致死亡。瘦肉精残留的检测一直是食品安全的重点。目前,关于瘦肉精的检测方法很多,但是,这些方法需要专业实验人员、大型实验仪器和繁琐的样品预处理,难以满足高通量、现场快速检测的需要,很难适应许多场合快速检测的需要。
技术实现要素:
本发明的第一方面,提供了一种量子点荧光探针,其具有寿命长、不易降解、生物相容性好的优点。
本发明的第二方面,提供了一种量子点荧光探针的制备方法,可提高灵敏度。
本发明的第三方面,提供了一种免疫层析试纸,利用前述的量子点荧光探针可以实现高灵敏度、高稳定性以及高效地检测瘦肉精的效果,并且可以简化检测流程,降低检测难度和成本。
本发明是这样实现的:
一种制备量子点荧光探针的方法,包括:
利用含有1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐的活化剂对量子点进行活化处理,得到活化溶液;使抗瘦肉精抗体与活化溶液混合、反应,得到反应液;以及使反应液与封闭剂混合反应。
一种量子点荧光探针,由前述的制备量子点荧光探针的方法制备而成。
一种免疫层析试纸,包括底板和设置于底板的检测层,检测层包括依次布置的样品垫、结合垫、反应膜以及吸水垫,结合垫吸附有上述量子点荧光探针。
本发明实施例的有益效果:本发明实施例提供的免疫层析试纸条利用量子点与抗瘦肉精抗体偶联作为荧光探针,与免疫层析技术结合,可实现对多种瘦肉精类药物的同时快速筛查。而且,量子点的荧光强度高,稳定性好,荧光寿命长,经过多次激发都不会被光漂白和化学降解,相比胶体金、有机荧光材料等,可以大大提高灵敏度。另外,本发明操作方便,结果准确,较好的解决了现有的检测方法只能检测一种瘦肉精药物和稳定性差等问题。本发明能够实现对多种瘦肉精类药物的同时快速筛查,检测方法简便、快捷、结果准确、灵敏度高,可做定性、定量检测,价格低廉,适用范围广,具有很好的推广应用前景。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
图1为本发明实施例4提供的免疫层析试纸的结构示意图;
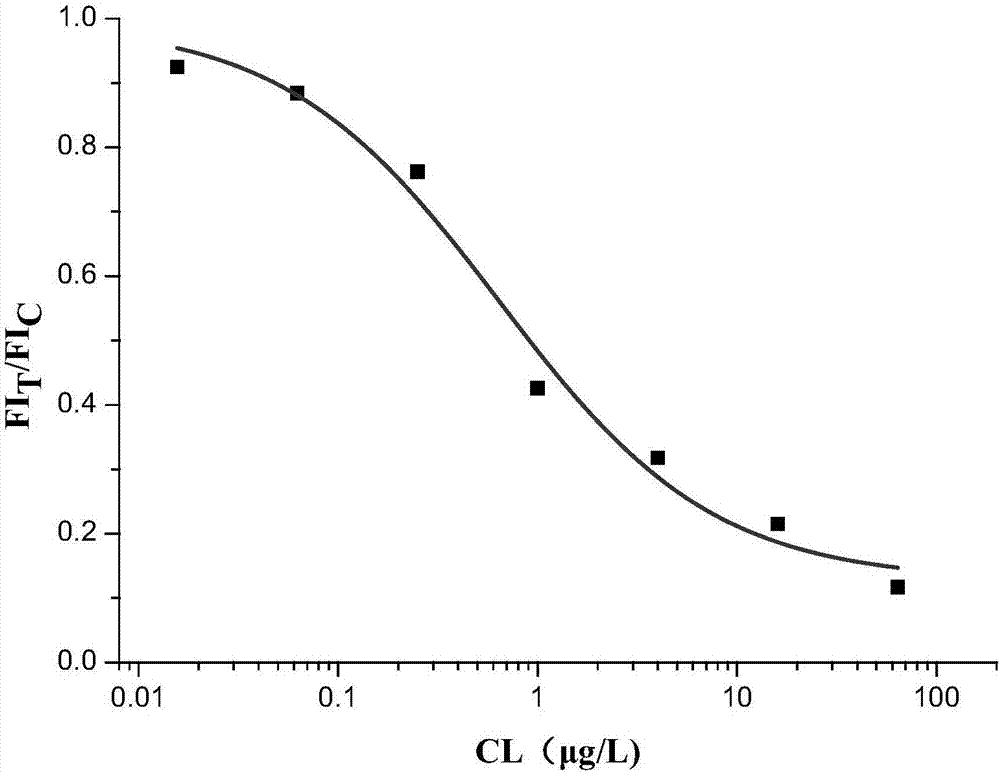
图2为盐酸克伦特罗的标准曲线;
图3为沙丁胺醇的标准曲线。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
以下针对本发明实施例的量子点荧光探针及其制备方法、免疫层析试纸进行具体说明:
一种制备量子点荧光探针的方法,包括:
(1)利用含有1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐的活化剂对量子点进行活化处理,得到活化溶液。
量子点特殊的表面效应和尺寸效应,使其具有独特光化学性质,如量子成率高、激发波长范围宽,发射波长窄且对称,斯托克斯位移大,因此可以采用同一激发光同时激发不同粒径的量子点进行多元检测。量子点的发射波长区间较大,可以跨域紫外到红外区间,且发射波长可以根据改变量子点的尺寸大小和化学组成来改变的。量子点的荧光强度高,稳定性好,荧光寿命长,经过多次激发都不会被光漂白和化学降解,且量子点有较好的生物相容性,适合作为荧光标记物。量子点主要选用ⅱ-ⅳ族、ⅲ-ⅴ族或ⅳ-ⅵ族等一系列元素组成的半导体荧光纳米材料。
基于实际测试的需求,如安全性、制备的简便性,量子点可以选用水溶性量子点。进一步地,量子点为水溶性的羧基化量子点。更进一步地,量子点是具有核壳结构的cdse/zns量子点。在本发明的一些示例中,量子点也可以是多种量子点的组合。
作为一种可选的方案,活化处理量子点的方法包括:将量子点溶解在缓冲液中,再加入1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐,室温搅拌10~30分钟,或15~25分钟。较佳地,室温搅拌时间为20分钟。
优选地,量子点与1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐的摩尔比为1:1000~10000。量子点与1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐的摩尔比还可以是1:2000~8000,或1:3000~6000,或1:5000:~7000。在本发明的较优示例中,量子点与1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐的摩尔比为1:2500。
其中,缓冲液可以是磷酸盐缓冲液。
其中,量子点可以是将2种或2种以上的半导体材料在纳米尺度复合而成的具有核壳结构的纳米半导体量子点。其尺度均一、荧光效率高、稳定性好。
例如,cdse/zns核亮结构量子点可以通过以下方式制备:在室温条件下,分别将醋酸锌、硫化钠溶于蒸馏水中,加热,磁力搅拌至完全溶解,得到无色澄清溶液,即为锌的前驱体水溶液和硫前驱体水溶液。向cdse量子点溶液中缓慢加入锌的前驱体水溶液和硫前驱体水溶液,磁力搅拌,且100℃水浴回流,充分反应后得到黄色至粉红色胶状cdse/zns核壳结构量子点粗品。然后,经过洗涤、离心沉降和冷冻干燥后,既得粉末状的目标量子点。
cdse量子点可以通过以下方式制备:
溶液a:在cdcl2·2.5h2o水溶液中,加入硫代乙醇钠,剧烈搅拌,浓氨水调节ph值至8.2~9.0之间。将溶液水浴加热接近至100℃,通入氮气脱氧10分钟备用。溶液b:将se粉加入na2so3水溶液中,通氮气保护下脱氧,加热回流,直至se粉全部溶解。溶液c:se粉添加到蒸馏水中,90℃水浴回流,氮气保护下脱氧10分钟,加入nabh4,磁力搅拌,剧烈反应发出气体,直至se粉完全溶解。氮气为保护气的环境中,将溶液b或溶液c缓慢加入溶液a中进行反应,水浴90℃,磁力搅拌、回流。充分反应后,取出cdse的水溶液样品,离心沉降,用蒸馏水洗涤、干燥。
(2)使抗瘦肉精抗体与活化溶液混合、反应,得到反应液。
抗瘦肉精抗体与活化溶液混合的方式可以是:将抗瘦肉精抗体加入到活化溶液中。抗瘦肉精抗体与活化溶液的反应时间优选为60~120分钟,例如,80~100分钟,或90~110分钟。
其中,抗瘦肉精抗体可以是单克隆抗体或多克隆抗体。优选地,单克隆抗体包括抗克伦特罗单克隆抗体、抗沙丁胺醇单克隆抗体、抗莱克多巴胺单克隆抗体中的任一种或多种。当抗瘦肉精抗体包含有多种抗体时,可以实现多检的目的,即可对多种目标检测物质进行检测。
活化溶液中的量子点与抗瘦肉精抗体的相对用量可以根据实际情况选择。在本发明的较佳实施例中,量子点与抗克伦特罗单克隆抗体的摩尔比为1:18;量子点与抗沙丁胺醇单克隆抗体的摩尔比为1:25;量子点与抗莱克多巴胺单克隆抗体的摩尔比为1:42。
(3)使反应液与封闭剂混合反应。
反应液与封闭剂混合的方式可以是室温(如25~28℃)下搅拌混合。例如,在搅拌的条件下,将封闭剂加入反应液。待封闭剂添加完成后,静置30~90分钟,或40~80分钟,或50~70分钟。
作为一种实现的方案,封闭剂选用为含乙醇胺的溶液。进一步地,溶液中的乙醇胺浓度可以为10wt%。
封闭剂中的氨基,能与量子点表面的羧基进行共价偶联反应。封闭剂的使用起到了在保持偶联在量子点表面的抗体分子的空间构象同时,提高了量子点/抗体复合物的免疫特性,克服了量子点偶联抗体后颗粒的团聚、沉淀的问题,从而达到减少了检测结构出现假阳性等问题。
(4)在使反应液与封闭剂混合反应之后,可选地对反应产物进行纯化。
纯化反应产物的方法有多种选择,例如,离心、凝胶色谱、超滤等。其中,离心的纯化方式包括:对反应产物进行离心,然后去除上清液。其中,离心的条件优选为:离心机在10000r/min的转速下离心30min。
进一步地,将由反应产物经纯化得到的纯化产物分散在复溶液中,避光保存。较佳地,避光保存的温度为4℃。复溶液复溶纯化产物后,通过避光保存可以避免防止量子点发生猝灭,荧光强度减弱,同时减少干扰以提高测试精度和灵敏度。
其中,复溶液可以为磷酸盐缓冲液。较佳地,复溶液中的磷酸盐浓度为0.05mol/l,ph为7.4。进一步地,复溶液中还可以含有吐温-20和牛血清白蛋白的。作为一种优选的方案,磷酸盐缓冲液中含有0.4wt%的吐温-20、0.5wt%的牛血清白蛋白。
本发明还提供了一种量子点荧光探针,其通过前述的制备量子点荧光探针的方法制备而成。
本发明还提供了基于前述的量子点荧光探针的免疫层析试纸。
免疫层析试纸条,包括底板、样品垫、结合垫、反应膜、吸水垫。其中,样品垫、结合垫、反应膜、吸水垫依次贴附在底板上。进一步地,结合垫的两端分别与样品垫、反应膜呈交叠布置。反应膜的另一端与吸水垫呈交叠布置。
其中,结合垫吸附有多种(如两种或三种)量子点荧光探针。即,结合垫吸附由多种探针组合的混合探针。量子点荧光探针为量子点与抗瘦肉精的抗体(单克隆抗体或多克隆抗体)的结合物。即,量子点荧光探针分别为盐酸克伦特罗-量子点荧光探针,沙丁胺醇-量子点荧光探针,莱克多巴胺-量子点荧光探针。
其中,反应膜上设置有检测线和质控线,且检测线位于样品垫一侧,质控线位于吸水垫一侧。检测线可以为多条(如二条或三条)与前述抗体(抗瘦肉精的抗体)相对应的抗原,即瘦肉精-载体蛋白结合抗原。质控线为羊抗鼠或羊抗兔igg抗体。即,瘦肉精-载体蛋白结合抗原分别为:盐酸克伦特罗-载体蛋白结合抗原,沙丁胺醇-载体蛋白结合抗原,莱克多巴胺-载体蛋白结合抗原。
通过选择相对应的量子点荧光探针和结合抗原,可以分别组成二联试纸条或三联试纸条。即,通过不同的量子点荧光探针和结合抗原的不同组合,可以实现对不同的物质进行检测。
本发明实施例提供的免疫层析试纸是一种基于量子点的瘦肉精多残留免疫层析试纸条。利用前述的免疫层析试纸可实现定性检测、半定量检测、定量检测。
例如,定性检测:对免疫层析试纸的样品垫滴加样品后,采用紫外灯观察反应膜的显色情况。当检测线出现荧光信号时判定该指标为阴性,不出现荧光信号时为判定该指标为阳性。无论何种情况,质控线不出现荧光信号则判定检测结果无效。
定量检测:配置一系列不同浓度的待测物质的混合标准品,然后利用荧光免疫层析定量仪进行检测,通过不同浓度的标准溶液对应的t/c值做标准曲线,在根据标准曲线求得未知样品中待测物质含量。
样品溶液中有待测药物(如瘦肉精)时,加入待测样品溶液后,待测溶液通过毛细管作用带动待测物及结合垫中的量子点荧光探针一起向反应膜层析。在层析过程中待测药物可与量子点荧光探针相结合,从而封闭了量子点荧光探针上的结合位点,阻止量子点荧光探针与反应膜上的瘦肉精-载体蛋白结合抗原,检测线无荧光,而羊抗或兔抗小鼠igg(或羊抗兔igg)抗体可拦截量子点荧光探针,质控线显示荧光。
样品溶液中无待测药物(如瘦肉精)时,则不能阻止量子点荧光探针与反应膜上的结合抗原结合,显示荧光。但羊抗或兔抗小鼠igg(或羊抗兔igg)抗体也拦截量子点荧光探针,质控线限制荧光。结果为:瘦肉精阴性。
如果反应膜上没有荧光显示,则表明试纸已失效。
以下结合实施例对本发明的量子点荧光探针及其制备方法、免疫层析试纸作进一步的详细描述。
实施例1
一种量子点荧光探针。其制备方法如下。
盐酸克伦特罗量子点荧光探针的制备:将50μl量子点溶解于350μl、0.01mol/l、ph7.4的磷酸盐缓冲液中,加入偶联剂1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐,室温搅拌20min,再加入108μg盐酸克伦特罗单克隆抗体,室温搅拌反应1.2h,继续加入0.1ml乙醇胺溶液封闭反应40min,将反应溶液以12000r/min离心30min,去除上清液,用复溶液复溶沉淀,得到量子点与β-兴奋剂单克隆抗体的标记复合物,4℃避光保存。
实施例2
一种量子点荧光探针。其制备方法如下。
沙丁胺醇量子点荧光探针的制备:将50μl量子点溶解于350μl0.01mol/lph7.4的磷酸盐缓冲液中,加入偶联剂1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐,室温搅拌20min,再加入150μg沙丁胺醇单克隆抗体,室温搅拌反应1.2h,继续加入0.1ml乙醇胺溶液封闭反应40min,将反应溶液以12000r/min离心30min,去除上清液,用复溶液复溶沉淀,得到量子点与β-兴奋剂单克隆抗体的标记复合物,4℃避光保存。
实施例3
一种量子点荧光探针。其制备方法如下。
取25μl量子点溶解于4ml、0.02mol/l、ph为7.2的磷酸盐缓冲液中。加入偶联剂,室温搅拌30min,再加入46μg的β-兴奋剂单克隆抗体(莱克多巴胺),室温搅拌反应1h,继续加入0.4ml的10%乙醇胺溶液封闭反应2h。将反应溶液以11000r/min离心60min,去除上清液,得到沉淀。用复溶液对沉淀进行复溶,得到量子点与β-兴奋剂单克隆抗体的标记复合物,4℃避光保存。其中,量子点、复溶液均如实施例1中所示进行配制。偶联剂为1-(3-二甲基丙基)-3-乙基碳二亚胺盐酸盐。
实施例4
一种免疫层析试纸,其结构如图1所示。其制备方法如下。
在底板上依次贴附样品垫、结合垫、反应膜、吸水垫,并且使形成于反应膜的质控线邻近吸水垫,形成于反应膜的检测线邻近样品垫。其中,底板为聚氯乙烯材质,结合垫和样品垫为玻璃纤维素膜,吸水垫为吸水纸,反应膜为硝酸纤维素膜。试纸(底板)的长度为4mm,样品垫、结合垫、硝酸纤维素膜、吸水垫的长度分别为1.8cm、0.4cm、2.7cm、1.5cm,彼此搭接贴附在底板上。其中,样品垫与结合垫的重合长度为2mm,结合垫与硝酸纤维素膜的重合长度为2mm,硝酸纤维素膜与样品垫的重合长度为2mm。
结合垫吸附有多种混合量子点荧光探针。其中,量子点荧光探针分别如实施例1和2提供的方法制作而成。反应膜通过包被形成有多条检测线和一条质控线,且相邻的检测线和质控线之间的距离为5mm。检测线分别通过0.01mol/l、ph7.4的磷酸盐缓冲液为包被溶液将盐酸克伦特罗-载体蛋白结合抗原、沙丁胺醇-载体蛋白结合抗原、莱克多巴胺-载体蛋白结合抗原包被于硝酸纤维素膜形成。质控线通过0.01mol/l、ph7.4的磷酸盐缓冲液为包被溶液将由羊抗鼠igg抗体包被于硝酸纤维素膜形成。在硝酸纤维素膜包被形成检测线和质控线之后,在37℃烘箱中干燥2h后备用。
实施例5
基于量子点的瘦肉精多残留免疫层析试纸条的定性或半定量结果的判断
1.本实验中所使用的盐酸克伦特罗、沙丁胺醇单克隆抗体及羊抗鼠igg二抗均为商业化试剂,购自广州优抗多生物技术有限公司。
2.将配置好的一系列混合标准品滴加在组装好的试纸条的样品垫上,静置反应5~10min,用紫外灯观察反应膜的显色情况。经多次重复实验,盐酸克伦特罗、沙丁胺醇检测限如表1所示。
表1量子点免疫层析试纸条检测限(n>3)
实施例6
基于量子点的瘦肉精多残留免疫层析试纸条的标准曲线的建立
1.本实验中所使用的盐酸克伦特罗、沙丁胺醇单克隆抗体及羊抗鼠igg二抗均为商业化试剂,购自广州优抗多生物技术有限公司。
2.分别配制浓度为0、0.0156、0.0625、0.250、1.00、4.00、16.00和64.0μg/l的系列混合标准溶液,用于试纸条检测。每个浓度重复检测3次,5~10min后用荧光免疫层析读数仪读取试纸条fit/fic比值。以fit/fic为纵坐标,以标准品浓度为横坐标,绘制试纸条竞争抑制曲线,计算试纸条50%竞争抑制率浓度以及确定试纸条检测线性范围。
结果如图2~3所示,盐酸克伦特罗的标准曲线的检测线性范围为(ic20-ic80)为0.12~3.56μg/l,50%竞争抑制率浓度(ic50)为0.64μg/l。沙丁胺醇的标准曲线的检测线性范围为(ic20-ic80)为0.16~4.06μg/l,50%竞争抑制率浓度(ic50)为0.82μg/l。
其中,图2为盐酸克伦特罗的标准曲线;图3沙丁胺醇的标准曲线。
实施例3
基于量子点的瘦肉精多残留免疫层析试纸条实际样品的检测
1.样品前处理
猪尿的前处理:取澄清透明的尿样备用,如有沉淀,离心取上清即可。
猪肉的前处理:将猪肉样本剪碎,称取1g猪肉装入离心管中,加入1ml蒸馏水盖紧管盖。放入95℃以上沸水浴加热10~15min,取出此离心管放至室温,用5000~10000r/min离心5~10min,移出上清液备用。
如表2所示,所构建的量子点的瘦肉精多残留免疫层析试纸条对猪尿的回收率在66.0~97.3%之间,猪肉的回收率在64.0~95.3%之间,各个样品的变异系数均小于15%,说明该方法有较好的准确性。
表2量子点试纸条样品添加回收实验结果(n=3)
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以作出许多其它的更改和修改。因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些变化和修改。
- 还没有人留言评论。精彩留言会获得点赞!
- 基于量子点的CA15‑3免疫层析试纸条的制备方法与制造工艺
- 肌红蛋白荧光免疫层析试纸条用活化荧光乳胶微球及应用的制造方法与工艺
- 铁蛋白荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 全程C‑反应蛋白荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 一种微流控芯片上基于荧光量子点磁性富集并分离结核分枝杆菌TB的方法及装置与制造工艺
- 25‑羟基维生素D荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 25‑羟基维生素D3荧光免疫层析用活化荧光乳胶微球的制造方法与工艺
- 降钙素原荧光免疫层析检测卡用活化荧光乳胶微球的制造方法与工艺
- 一种改变量子点荧光色的方法与制造工艺
- 一种基于荧光免疫层析技术的定量检测计算方法与制造工艺