基于芬顿反应构建的ELISA可视化检测试剂盒及其在检测ZEN中的应用的制作方法
本发明属于食品分析领域,具体涉及一种基于芬顿反应对aunrs的刻蚀作用构建的新型酶联免疫反应(elisa)可视化检测试剂盒及其在检测玉米赤霉烯酮(zen)中的应用。
背景技术:
玉米赤霉烯酮(zenralenone,zen)又称f-2毒素,主要是由粉红镰刀菌及禾谷镰刀菌产生的一种非甾体。zen不仅具有动物雌性激素作用,还是某些真菌的性激素。zen能引起动物流产、死胎、返情等生殖机能异常,还可以导致生长下降、免疫抑制、不育、畸形等。由于我国多数地区雨量充沛,相对湿度较高,谷物和动物饲料更易受到霉菌毒素污染,尤其玉米、小麦、燕麦和大麦等作物易受到zen污染。通过国内外对zen毒性机理的研究发现它主要通过影响机体的生殖性能,引起细胞凋亡、致畸、损伤dna、氧化损害、影响免疫机能等机制,来影响动物与人类的健康。通过对zen毒性的研究发现它对植物的毒性主要体现在它与植物的受精、授粉有关,而它对动物的毒性主要体现在它具有生殖发育毒性、免疫毒性、肝肾毒性及它对内分泌系统的影响。
调查发现zen在饲料厂抽取的样品中污染最大,而在粮食集散地、养殖场(户)中污染最轻。这与饲料厂中玉米类样品较多而玉米类样品受到zen污染最严重有关。当猪食用了被zen污染的饲料后,育肥猪除精神轻度兴奋、食欲轻度下降外,主要表现为泌尿生殖器官的发情样症状。动物一旦食用了被zen污染的饲料后没有特效药能够对它们进行治疗,所以zen的检测变得尤为重要。
检测zen的方法主要有色谱法和免疫学方法。色谱法如气相色谱-质谱联用法和高效液相色谱法等,具有检测灵敏、可靠的特点,但是需要昂贵仪器,并且检测所需时间长,对操作人员要求较高。免疫学方法具有简便、灵敏、快捷、成本低、适合大批量检测等特点,尤其适合我国很多生产企业单位的自检。目前国内外对利用酶联免疫吸附测定法(elisa)检测zen有较多研究,并取得了一定成果。但是与进口试剂盒相比,国内的检测试剂盒存在检测范围较窄、灵敏度不高的缺点。
技术实现要素:
鉴于上述现有技术中的不足,本发明的目的在于提供一种基于芬顿反应构建的新型酶联免疫反应(elisa)可视化检测试剂盒,其是在elisa反应的基础上,引入aunrs作为显色底物,以改变传统elisa单一显色的问题。本发明基于芬顿反应构建新型elisa可视化检测试剂盒对zen进行检测,是在zen和人工抗原zen-cat可与抗体结合特异性的基础上,利用芬顿反应对aunrs的刻蚀作用导致aunrs颜色改变达到显色的效果,以最终通过aunrs的颜色变化对zen浓度进行可视化检测及精确定量测定。
为实现上述目的,本发明采用如下技术方案:
一种基于芬顿反应构建的elisa可视化检测试剂盒,其包括zen单克隆抗体、人工抗原zen-cat、h2o2、fecl2和金纳米棒(aunrs),其利用fe2+的催化作用加速h2o2对aunrs的刻蚀,而通过aunrs的颜色变化进行测定。
所述人工抗原zen-cat的合成包括半抗原的合成及人工抗原的合成两个部分,其具体步骤为:
(1)半抗原的合成:精确称取1mgzen溶于0.4ml吡啶中,加入4mg羧甲基羟胺半盐酸盐(cmo),室温搅拌反应24h后,45℃真空干燥,残留物溶于0.4ml蒸馏水中,用1mol/l的naoh溶液调ph至8.0,然后用0.4ml苯反复萃取3次以从水相中除去未反应的zen,反应产物用hcl调节ph至3.0,生成沉淀,然后用0.5ml乙酸乙酯抽提4次,再于45℃真空干燥,得zen-cmo半抗原;
(2)人工抗原的合成:将n,n-二环己基碳二亚胺(dcc)、琥珀酰亚胺(nhs)和步骤(1)所得半抗原按质量比5:2:1溶于1mln,n-二甲基甲酰胺(dmf)中,室温搅拌反应2h后,4℃搅拌继续反应24h,再于3000r/min离心10min,然后取上清液缓慢滴加入预冷的1.5ml、2.3mg/ml的过氧化氢酶(cat)溶液中,4℃搅拌反应24h,反应液用2l、0.01mol/l、ph=7.4的磷酸盐缓冲溶液(pbs,其是将4gnacl,1.45gna2hpo4•12h2o,0.1gkcl,0.2gkh2po4溶于双蒸水ddh2o中并定容到1000ml制得)透析3天,得到所述人工抗原zen-cat。
所述aunrs的制备包括纳米金核的制备及金纳米棒的生长两个部分,其具体步骤为:
(1)将250μl、10mmol/l的氯金酸(haucl4)溶液加入到9.75ml、0.1mol/l的十六烷基三甲基溴化铵(ctab)溶液中,放置于30℃水浴中,以700r/min的转速磁力搅拌,混合均匀;然后调节磁力搅拌机转速为1200r/min,将0.9ml、10mmol/l冷冻新制的硼氢化钠(nabh4)溶液快速加入上述溶液中,剧烈搅拌2min后停止搅拌,并将磁力搅拌子取出,再将反应液于30℃水浴中静置30min,得纳米金核溶液(制备的金核溶液必须在2h内使用);
(2)称取3.425gctab置于250ml平底烧瓶中,加入100ml超纯水,随后加入960μl、10mmol/l的agno3溶液,30℃静置15min,随后加入5ml、10mmol/l的haucl4溶液,700r/min持续搅拌90min;
(3)在步骤(2)所得溶液中加入640μl、100mmol/l的抗坏血酸(aa)溶液,1200r/min剧烈搅拌30s后,再往溶液中加入450μl步骤(1)制得的纳米金核溶液,1200r/min持续剧烈搅拌30s后停止搅拌,并将磁力搅棒子取出,30℃水浴静置12h以上,待aunrs生长完全;
所得aunrs的长径比约为3.8。
所述elisa检测试剂盒可用于zen的检测,如对饲料中zen的检测。其应用方法具体为:将50μlzen单克隆抗体包被在酶标板上,同时向孔中加入50μl含zen的待测物以及50μl人工抗原zen-cat,于37℃下孵育30min,使zen和zen-cat竞争酶标板上的单克隆抗体,用含tween20的磷酸盐缓冲溶液(pbst,其是将5mltween20,4gnacl,1.45gna2hpo4•12h2o,0.1gkcl,0.2gkh2po4溶于双蒸水ddh2o中并定容到1000ml制得)洗板三次,甩干后加入50μl含h2o21mol/l的pbs溶液,于37℃下孵育10min,用pbst洗板三次,甩干后再加入50μl10mmol/l的fecl2溶液和100μlaunrs,于室温下反应10min后,加入终止液h2so4终止反应,通过观察aunrs的颜色变化判断zen的浓度,或通过测定450-900nm处的紫外吸收值来对zen的浓度进行准确定量测定。
在室温条件下高浓度的h2o2会与aunrs发生氧化还原反应,使得aunrs的长径比发生改变,并且在当存在有ctab为软模板时,aunrs与氧化剂之间的氧化还原反应优先从aunrs的两端进行,aunrs的长度逐渐缩短,而直径基本不发生变化。但在室温条件下,低浓度的h2o2(<100mmol/l)与aunrs之间的反应需要长达12h才能够将aunrs完全氧化。而在芬顿反应中,fe2+作为催化剂将h2o2分解为·oh和·ooh,由于·oh的氧化能力远远高于h2o2的氧化能力,因此采用芬顿反应后的产物与aunrs反应,能够大大缩短反应时间。即本发明通过芬顿反应产生的羟基自由基,提高了h2o2与aunrs之间的反应速率。
本发明基于芬顿反应对aunrs的刻蚀作用构建了一种新型elisa可视化检测试剂盒,其根据目标物zen与人工抗原和zen单克隆抗体的特异性结合作用,使目标物与人工抗原zen-cat竞争酶标板上的单克隆抗体,再通过洗板、甩干等操作,使结合上抗体的人工抗原zen-cat留在酶标板上,此时再加入h2o2,cat就会分解h2o2,再加入fecl2和aunrs,未被分解的h2o2就会在fe2+的催化下加速对aunrs的刻蚀,aunrs被刻蚀之后,纵向等离子共振吸收峰会发生蓝移,长径比也会发生改变,导致aunrs的颜色发生变化,所以可以直观用肉眼观察颜色变化来大致对zen的浓度进行半定量的分析,另外也可以利用aunrs纵向等离子共振吸收峰对应的吸光值的大小来进行精确的定量分析。
相比现有技术的不足,本发明的优点:
1.本发明利用芬顿反应对aunrs的刻蚀作用构建的新型elisa可视化检测试剂盒,其通过fe2+加速h2o2对aunrs的刻蚀作用,使aunrs的颜色发生变化,从而可实现对zen浓度的粗略半定量检测以及精确定量分析。
2.本发明所使用的aunrs被h2o2刻蚀之后会呈现蓝色、绿色、浅红色、黄色等多种颜色,即具有多重显色性,是一种优良的显色底物。
3.本发明所使用的aunrs通过种子生长法制备获得,其以十六烷基二甲基溴化铵作为生长溶液,制备出的aunrs长径比约为3.8,具备良好的多重显色性。
4.本发明在检测过程中不需要复杂的仪器和繁琐的操作,每次检测所需的aunrs的量极少(50μl),检测成本低。
5.本发明检测zen的线性范围为0.2-4000ng/ml,检测限为0.2ng/ml,检测的灵敏度高、选择性好,检测过程简便,经济成本低,稳定性好,易于推广使用。
附图说明
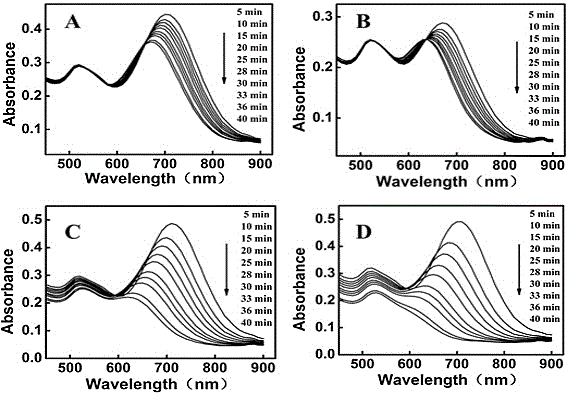
图1为在芬顿反应中不同浓度的h2o2刻蚀aunrs不同时间的紫外吸收光谱图,其中,(a)0.04mmol/lh2o2;(b)0.2mmol/lh2o2;(c)1mmol/lh2o2;(d)5mmol/lh2o2。
图2为在芬顿反应中不同浓度的h2o2对aunrs的紫外吸收光谱图(a)、显色图像(b)和tem图像(c),其中,1-13代表h2o2的浓度分别为0、1、2、3、4、5、10、40、50、60、600、800和1000mmol/l,tem标尺为50纳米。
图3为人工抗原zen-cat的鉴定结果;其中,(a)为紫外线吸收鉴定zen-cat,(b)为sds-page鉴定zen-cat,泳道1是260μg/mlcat,泳道2和3是zen-cat,(c)为wb鉴定zen-cat,泳道1是260μg/mlcat,泳道2,3和4是zen-cat。
图4为反应过程中反应时间的优化情况图。
图5为反应过程中fecl2浓度的优化情况图。其中,(a)、(b)、(c)分别为反应时间为5min、10min、20min时加入不同浓度fecl2的紫外吸收光谱图,(d)为显色照片。
图6为与不同浓度的zen反应后的aunrs的紫外吸收光谱图(a)、吸光度与zen浓度之间的线性关系(b)及显色图像(c),其中,1-18代表zen的浓度分别为0、0.2、0.3、0.6、0.8、2、5、8、20、30、50、70、300、400、700、900、3000和4000ng/ml。
具体实施方式
一种基于芬顿反应构建的elisa可视化检测试剂盒,其包括zen单克隆抗体(购买自abcam)、人工抗原zen-cat、h2o2、fecl2和金纳米棒(aunrs)。
所述人工抗原zen-cat的合成包括半抗原的合成及人工抗原的合成两个部分,其具体步骤为:
(1)半抗原的合成:精确称取1mgzen溶于0.4ml吡啶中,加入4mg羧甲基羟胺半盐酸盐(cmo),室温搅拌反应24h后,45℃真空干燥,残留物溶于0.4ml蒸馏水中,用1mol/l的naoh溶液调ph至8.0,然后用0.4ml苯反复萃取3次以从水相中除去未反应的zen,反应产物用hcl调节ph至3.0,生成沉淀,然后用0.5ml乙酸乙酯抽提4次,再于45℃真空干燥,得zen-cmo半抗原;
(2)人工抗原的合成:将n,n-二环己基碳二亚胺(dcc)、琥珀酰亚胺(nhs)和步骤(1)所得半抗原按质量比5:2:1溶于1mln,n-二甲基甲酰胺(dmf)中,室温搅拌反应2h后,4℃搅拌继续反应24h,再于3000r/min离心10min,然后取上清液缓慢滴加入预冷的1.5ml、2.3mg/ml的过氧化氢酶(cat)溶液中,4℃搅拌反应24h,反应液用2l、0.01mol/l、ph=7.4的磷酸盐缓冲溶液(pbs,其是将4gnacl,1.45gna2hpo4•12h2o,0.1gkcl,0.2gkh2po4溶于双蒸水ddh2o中并定容到1000ml制得)透析3天,得到所述人工抗原zen-cat。
所述aunrs的制备包括纳米金核的制备及金纳米棒的生长两个部分,其具体步骤为:
(1)将250μl、10mmol/l的haucl4溶液加入到9.75ml、0.1mol/l的ctab溶液中,放置于30℃水浴中,以700r/min的转速磁力搅拌,混合均匀;然后调节磁力搅拌机转速为1200r/min,将0.9ml、10mmol/l冷冻新制的nabh4溶液快速加入上述溶液中,剧烈搅拌2min后停止搅拌,并将磁力搅拌子取出,再将反应液于30℃水浴中静置30min,得纳米金核溶液(制备的金核溶液必须在2h内使用);
(2)称取3.425gctab置于250ml平底烧瓶中,加入100ml超纯水,随后加入960μl、10mmol/l的agno3溶液,30℃静置15min,随后加入5ml、10mmol/l的haucl4溶液,700r/min持续搅拌90min;
(3)在步骤(2)所得溶液中加入640μl、100mmol/l的aa溶液,1200r/min剧烈搅拌30s后,再往溶液中加入450μl步骤(1)制得的纳米金核溶液,1200r/min持续剧烈搅拌30s后停止搅拌,并将磁力搅棒子取出,30℃水浴静置12h以上,待aunrs生长完全;所得aunrs的长径比约为3.8。
基于芬顿反应对aunrs的刻蚀作用构建的新型elisa可视化检测试剂盒,通过fe2+加速h2o2对aunrs的刻蚀作用,导致aunrs的颜色发生变化,根据aunrs的颜色变化程度可判断出zen的大致浓度,或由aunrs纵向等离子共振吸收峰蓝移的紫外吸收曲线可以实现对zen浓度的精确定量。
图1为在芬顿反应中不同浓度的h2o2刻蚀aunrs不同时间的紫外吸收曲线图。如图1所示,在h2o2浓度为5mmol/l的条件下,以fe2+作为催化剂的芬顿反应,产物在10min内就能够将aunrs完全氧化,同时,高浓度的h2o2对aunrs的刻蚀程度相比低浓度的h2o2来说更加严重,即高浓度的h2o2使得aunrs的吸收峰蓝移更加明显,颜色变化也更快。
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
实施例1aunrs的合成与表征
(1)将250μl、10mmol/l的haucl4溶液加入到9.75ml、0.1mol/l的ctab溶液中,放置于30℃水浴中,以700r/min的转速磁力搅拌,混合均匀;然后调节磁力搅拌机转速为1200r/min,将0.9ml、10mmol/l冷冻新制的nabh4溶液快速加入上述溶液中(此时溶液应变为棕黄色;如果溶液变为红色,说明制备错误,应该重新制备),剧烈搅拌2min后停止搅拌,并将磁力搅拌子取出,再将反应液于30℃水浴中静置30min,得纳米金核溶液(制备的金核溶液必须在2h内使用);
(2)称取3.425gctab置于250ml平底烧瓶中,加入100ml超纯水,随后加入960μl、10mmol/l的agno3溶液,30℃静置15min,随后加入5ml、10mmol/l的haucl4溶液,700r/min持续搅拌90min;
(3)在步骤(2)所得溶液中加入640μl、100mmol/l的aa溶液,1200r/min剧烈搅拌30s后,再往溶液中加入450μl步骤(1)制得的纳米金核溶液,1200r/min持续剧烈搅拌30s后停止搅拌,并将磁力搅棒子取出,30℃水浴静置12h以上,待aunrs生长完全。
在fe2+催化下,h2o2氧化aunrs的紫外吸收光谱图见图2。如图2所示,不存在h2o2时,aunrs的紫外吸收光谱图中有两个吸收峰,长轴等离子共振吸收峰(~765nm)和短轴等离子共振吸收峰(~510nm)。当加入h2o2之后,aunrs的长轴等离子共振吸收峰开始蓝移,同时吸收峰的强度也逐渐下降,并且随着h2o2浓度的增大,aunrs的长轴等离子共振吸收峰的峰位置的蓝移程度也随之增大。因此,aunrs与不同浓度的h2o2发生反应之后,溶液的颜色由最初的淡紫色,开始转变为淡红色、蓝色、绿色、无色、淡黄色、姜黄色等多种颜色。由此可见,不同颜色的溶液与h2o2的浓度之间呈现一定的相关性,因此可以通过溶液的颜色变化对h2o2的浓度进行可视化半定量分析。
进一步地,为了证明溶液的颜色发生改变是因为aunrs与h2o2反应之后长径比发生了变化,采用tem对反应前后aunrs的几何形貌进行表征。如图2中(c)所示,原始的aunrs溶液的颜色为红棕色,长径比为~3.8。当aunrs与h2o2反应之后,aunrs的长径比减少,溶液的颜色也从原来的淡紫色变为黄色。当h2o2的浓度较大时,aunrs由原始的棒状纳米颗粒开始转变为球形,溶液的颜色也相应的变为黄色。
实施例2人工抗原zen-cat的合成及鉴定
(1)半抗原的合成:精确称取1mgzen溶于0.4ml吡啶中,加入4mg羧甲基羟胺半盐酸盐(cmo),室温搅拌反应24h后,45℃真空干燥,残留物溶于0.4ml蒸馏水中,用1mol/l的naoh溶液调ph至8.0,然后用0.4ml苯反复萃取3次以从水相中除去未反应的zen,反应产物用hcl调节ph至3.0,生成沉淀,然后用0.5ml乙酸乙酯抽提4次,再于45℃真空干燥,得zen-cmo半抗原;
(2)人工抗原的合成:将n,n-二环己基碳二亚胺(dcc)、琥珀酰亚胺(nhs)和步骤(1)所得半抗原按质量比5:2:1溶于1mln,n-二甲基甲酰胺(dmf)中,室温搅拌反应2h后,4℃搅拌继续反应24h,再于3000r/min离心10min,然后取上清液缓慢滴加入预冷的1.5ml、2.3mg/ml的过氧化氢酶(cat)溶液中,4℃搅拌反应24h,反应液用2l、0.01mol/l、ph=7.4的磷酸盐缓冲溶液(pbs)透析3天,得到人工抗原zen-cat。
为了对人工抗原zen-cat的合成结果进行鉴定,首先用考马斯亮蓝试剂盒检测人工抗原zen-cat的浓度,最后检测出zen-cat的浓度为260μg/ml。
①、紫外吸收初步鉴定人工抗原zen-cat
分别配制260μg/ml的cat溶液和zen溶液,与合成的zen-cat样品各取200μl于酶标孔中,测量230-400nm的吸收曲线。从图3中(a)可以看到,zen有2个紫外吸收特征峰,分别在274nm和316nm处;载体蛋白的紫外吸收特征峰主要在278nm处,然而人工抗原zen-cat的紫外吸收特征峰及吸收峰高度与zen及载体蛋白均不一样,在二者的基础上发生了叠加及平移,分别在276nm及316nm处出现了吸收,由于人工抗原zen-cat偶联后通过萃取除去了未偶联上的zen,而此处偶联后的人工抗原zen-cat在316nm出现了载体蛋白没有而zen特有的吸收峰,初步证明了zen人工抗原偶联成功。
②、sds-page鉴定人工抗原
紫外吸收光谱只能初步鉴定人工抗原的合成成功,为了进一步证明zen-cat的成功偶联,还需要通过sds-page进行鉴定,结果如图3中(b)所示,其中,泳道1是260μg/ml的cat标品,泳道2和3是合成的zen-cat。结果显示,cat在60kda左右有带,合成的zen-cat的条带弱于cat标品,可能是合成过程中cat的偶联量较少。但是sds-page的结果也能进一步说明zen-cat的偶联是成功的。
③、westernblot鉴定人工抗原
前两种鉴定方法都只是对zen-cat时候偶联成功做了初步的验证,要真正鉴定zen-cat是否偶联成功还需要利用western-blot看zen和cat是否真正完成了偶联。结果如图3中(c)所示,泳道2为cat的标品,泳道3、4、5均为合成的zen-cat,在60kd左右有带,说明zen-cat偶联成功。
实施例3:zen标准曲线的测定
图4、图5为对该可视化检测系统的反应时间及fecl2浓度的优化情况图。采用控制变量法,确定了最佳反应时间为10min,最佳的fecl2浓度为10mmol/l。
将稀释至一定浓度的zen标准品50μl加入到已包被有50μlzen单克隆抗体的反应孔中,随后加入50μl人工抗原zen-cat,混合均匀,盖膜,37℃下反应30min,然后用洗涤液pbst(将5mltween20,4gnacl,1.45gna2hpo4•12h2o,0.1gkcl,0.2gkh2po4溶于双蒸水ddh2o中并定容到1000ml制得)反复洗涤3~4次,拍干,加入溶解于pbs(0.1mol/lph=7.8)的h2o2(45μl,1mol/l),混合均匀,盖膜,37℃下反应10min。随后,加入aunrs(100μl)、fecl2(50μl,10mmol/l)溶液于上述酶标孔中,盖膜,室温下反应10min,加入终止液h2so4(10μl,2m),最后,扫描紫外吸收光谱,并拍照。
图6为与不同浓度的zen反应后的aunrs的紫外吸收光谱图(a)、吸光度与zen浓度之间的线性关系(b)及显色图像(c)。由图中可见,该可视化检测试剂盒在检测zen的线性范围为0.2-4000ng/ml,并且由图6中(c)所示,不同浓度的zen会呈现出浅红色、浅绿色、绿色、浅黄色、黄色等多种颜色,证明其具备很好的显色性。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
- 还没有人留言评论。精彩留言会获得点赞!