一种基于数学模型同时测定氨氧化速率和亚硝酸盐氧化速率的方法与流程
本发明属于环境科学领域,具体涉及一种基于数学模型同时测定氨氧化速率和亚硝酸盐氧化速率的方法。
背景技术:
硝化作用是氧化铵盐(nh4+)到亚硝酸盐(no2-)再到硝酸盐(no3-)的过程,氨氧化过程是由氨氧化细菌(aob)和氨氧化古菌(aoa)完成的,亚硝酸盐氧化通过亚硝酸盐氧化细菌(nob)完成的。硝化过程是氮素循环的重要环节,在全球氮循环中发挥重要作用。通常硝化速率的测定通过向样品中添加抑制剂的方法实现。当氨氧化过程被阻断时,可以通过亚硝酸盐的下降表示亚硝酸盐氧化速率。同样地,当亚硝酸盐氧化过程被抑制时,氨氧化速率可以通过亚硝酸盐的增加求出。目前,常用的几种氨氧化抑制剂有几种,包括乙炔(c2h2),三氯甲基吡啶(nitrapyrin),烯丙基硫脲(atu)等。使用抑制剂方法存在很多的不足:首先,在实际的硝化率测定过程中,atu和ptio并不能完全抑制氨氧化过程。在样品中aoa和aob丰度与活性不确定的条件下,不能确定加入atu或ptio抑制氨氧化过程。其次,用于一种途径的抑制剂可能会扰乱另一种途径的发生。第三,氨氧化和亚硝酸盐氧化均为连续过程,加入抑制剂可能会导致这两个过程解偶联。最后,抑制剂具有一定的时效性,在实验过程中,存在反应没有结束而抑制失效的情况。总的来说,用抑制剂测定的硝化速率与实际的硝化速率存在很大的偏差。
技术实现要素:
本发明的目的为了避免传统的抑制剂方法在硝化速率测定过程中存在的不足,在不添加抑制剂的条件下建立了一种基于数学模型计算同时测定水体及沉积物硝化速率的方法,这种方法避免了添加抑制剂带了的一些问题,同时准确地测出了氨氧化速率和亚硝酸氧化速率,并模拟出了瞬时速率的变化趋势,为环境中硝化过程的准确分析测定提供了一种简便快速准确的方法。
本发明的基于数学模型同时测定氨氧化速率和亚硝酸盐氧化速率的方法,包括以下步骤:
a、培养体系的建立
用250毫升无菌宽口瓶(hdpe,themo)建立培养体系。对于水样,在每个瓶子中注入125毫升原位水(用尼龙网过滤)。对沉积物样品,加入10g(湿重)沉积物和125毫升原位过滤水(用0.22μm滤膜过滤),在每个瓶子中混匀。培养瓶内的顶空部分可以保证足够的氧气用于硝化作用。然后,用水或沉积物物样品制备的培养瓶在原位温度下温和地摇动(75转/分钟),以保持它们处于充气有氧状态。样品在黑暗中培养以防止浮游植物对可溶性无机氮(din)的同化。每12小时取培养瓶中的上覆水溶液,并测量铵盐、亚硝酸盐和硝酸盐(din)的浓度。培养持续直到铵盐和亚硝酸盐完全消耗,并且硝酸盐浓度达到稳定。通过标准方法测定铵盐、亚硝酸盐和硝酸盐浓度,建立铵盐、硝酸盐和硝酸盐(din)的时间序列动力学变化曲线,用于进一步建立氨氧化和亚硝酸盐氧化速率的数学计算模型。
b、建立数学模型,计算氨氧化和亚硝酸盐氧化速率
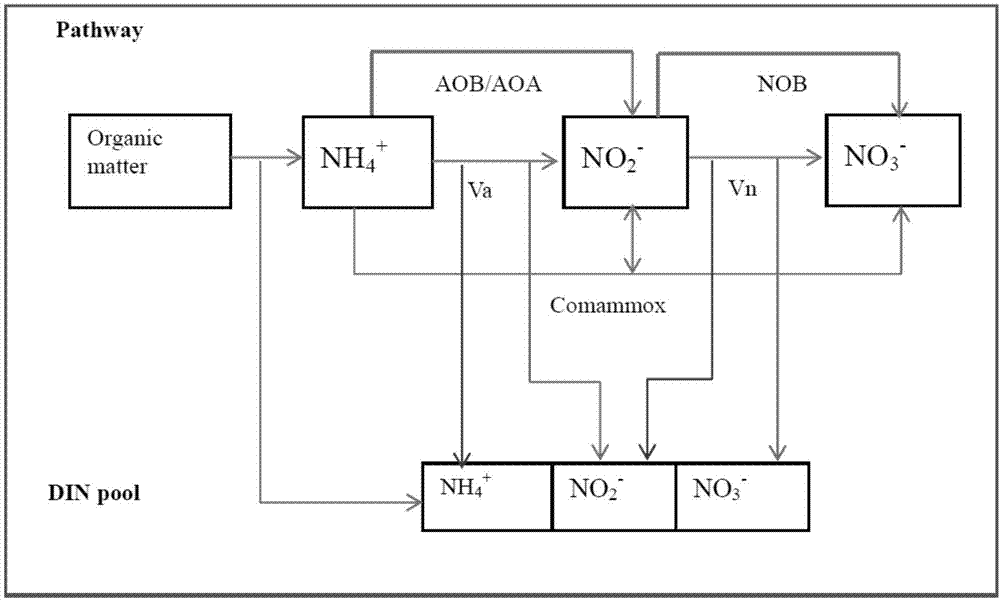
简单的盒模型(图1)被用来同时计算氨氧化速率(va)和亚硝酸盐氧化速率(vn)。该模型是基于两个假设条件建立的。首先,铵盐在培养系统中是不受限制的,允许它通过有机物矿化产生;第二,整个培养期内保持在有氧状态。因此,反硝化和厌氧氨氧化过程将保持抑制状态,因此不会从培养系统中有din的输出。在这些条件下,硝酸盐应是培养系统中的终产物。va可以用单位时间内亚硝酸盐和硝酸盐总浓度((va=δ[nox-]/δt))的增量来表示,vn可以通过单位时间内硝酸盐浓度的增量(vn=δ[no3-]/δt)来表示。
用二阶局部平滑过滤法对每种din的点的数据进行经验平滑,以减少由于采样引起的高频率噪声。然后,利用玻耳兹曼分布模式拟合din时间序列数据,并使用等式(1)获得。
其中,y为din的浓度,y0为初始浓度,ymax是反应浓度最大值,x为反应时间,x0为t1/2(1/2反应时间),1/dx为反应常数。
对等式(1)进行一阶微分,得到氨氧化或者亚硝酸盐氧化的瞬时速率,可以用等式(2)计算。
其中y′为瞬时速率,其他参数同等式(1)
va和vn的平均值可以通过拟合的玻尔兹曼分布模式(eqs)来计算,见等式(3)和(4)。
起始时间(ts)是培养开始的时间,结束时间(te)是no2-和no3-达到最大值的时间(δt=te-ts)。din物种的初始和最终浓度分别对应于ts和te。
在本发明中,建立了一种用于同时测定氨氧化和亚硝酸盐氧化速率的方法,不需要根据样品微生物群落的不同添加不同的抑制剂,避免了繁琐的抑制过程。该方法的反应时间长于传统的抑制剂方法,可以检测到整个反应过程。基于din时间序列和boltzmann拟合,形成了一个完整的计算系统。在传统的只能测量平均硝化速率的基础上,本研究模拟出了瞬时反应率的变化趋势。平均硝化速率可以指示一个地区的硝化能力的大小,瞬时速率是硝化能力的另一个重要标尺,它反映了氨氧化和亚硝酸盐氧化的速率的动态变化过程而并非一个线性增加的关系。
附图说明:
图1是硝化速率计算boltzmann分布盒式模型概念图。va与vn分别代表氨氧化与亚硝酸盐氧化过程。
图2是培养体系中nh4+,no2-,no3-的时间序列变化。
图3是boltzmann曲线拟合din的曲线。a-no2-+no3-的拟合曲线,用于分析氨氧化速率;b-no3-的拟合曲线,用于分析亚硝氧化速率。
图4是瞬时氨氧化速率以及亚硝酸盐氧化瞬时速率。a-氨氧化速率;b-亚硝氧化速率
具体实施方式:
以下实施例是对本发明的进一步说明,而不是对本发明的限制。
实施例1:
1、实验仪器与试剂
infinitem200pro多功能酶标仪(瑞士/tecan);vortex-genie2涡旋混合器(美国scientificindustry)。
氯化铵标准溶液(0.1μmol/l);亚硝酸钠标准溶液(0.1μmol/l);硝酸钾标准溶液(0.1μmol/l);对氨基苯磺酰胺溶液(10g/l);1-奈替乙二胺二盐酸溶液(1g/l)。
2、培养体系的建立
用250毫升无菌宽口瓶(hdpe,themo)建立培养体系。对于水样,在每个瓶子中注入125毫升原位水(用尼龙网过滤)。对沉积物样品,加入10g(湿重)沉积物和125毫升原位过滤水(用0.22μm滤膜过滤),在每个瓶子中混匀。培养瓶内的顶空部分可以保证足够的氧气用于硝化作用。然后,用水或沉积物物样品制备的培养瓶在原位温度下温和地摇动(75转/分钟),以保持它们处于充气有氧状态。样品在黑暗中培养以防止浮游植物对可溶性无机氮(din)的同化。每12小时取培养瓶中的上覆水溶液,并测量铵盐、亚硝酸盐和硝酸盐(din)的浓度。培养持续直到铵盐和亚硝酸盐完全消耗,并且硝酸盐浓度达到稳定。通过标准方法测定铵盐、亚硝酸盐和硝酸盐浓度,建立铵盐、亚硝酸盐和硝酸盐(din)的时间序列动力学变化曲线,用于进一步建立氨氧化和亚硝酸盐氧化速率的数学计算模型。
3、建立数学模型,计算氨氧化和亚硝酸盐氧化速率
简单的盒模型(图1)被用来同时计算氨氧化速率(va)和亚硝酸盐氧化速率(vn)。该模型是基于两个假设条件建立的。首先,铵盐在培养系统中是不受限制的,允许它通过有机物矿化产生;第二,整个培养期内保持在有氧状态。因此,反硝化和厌氧氨氧化过程将保持抑制状态,因此不会从培养系统中有din的输出。在这些条件下,硝酸盐应是培养系统中的终产物。va可以用单位时间内亚硝酸盐和硝酸盐总浓度((va=δ[nox-]/δt))的增量来表示,vn可以通过单位时间内硝酸盐浓度的增量(vn=δ[no3-]/δt)来表示。
用二阶局部平滑过滤法对每种din的点的数据进行经验平滑,以减少由于采样引起的高频率噪声。然后,利用玻耳兹曼分布模式拟合din时间序列数据,并使用等式1获得。
其中,y为din的浓度,y0为初始浓度,ymax是反应浓度最大值,x为反应时间,x0为t1/2(1/2反应时间),1/dx为反应常数。
对等式1进行一阶微分,得到氨氧化或者亚硝酸盐氧化的瞬时速率,可以用等式2计算。
其中y′为瞬时速率,其他参数同等式(1)
va和vn的平均值可以通过拟合的玻尔兹曼分布模式(eqs)来计算,见等式3和4。
起始时间(ts)是培养开始的时间,结束时间(te)是no2-和no3-达到最大值的时间(δt=te-ts)。din物种的初始和最终浓度分别对应于ts和te。
4、水体样品测定
本实验所用的水样于2016年5月取自珠江口(23°6'22.80n113°17'39.50e)表层水体(盐度为0psu)。样品采集之后,于4℃条件下保存,在4小时之内运回实验室,按照上述方法(步骤1、2、3)进行测定,计算氨氧化和亚硝酸盐氧化速率。
4.1boltzmann分布模型以及平均氨氧化与亚硝酸盐氧化速率
根据硝化过程构建一个简单的盒式模型(图1),通过测定不加入任何抑制剂条件下din时间序列的变化同时计算平均氨氧化(va)与亚硝酸盐氧化速率(vn)。该模型需在两个假定条件下运行:首先,nh4+的量不受到限制,可以从有机矿化过程产生;其次,保证培养在有氧条件下进行,体系中不存在反硝化或厌氧氨氧化导致的氮去除。因此,在不添加抑制剂情况下,硝酸盐是该模型的最终产物,反应速率仅需通过测量三个参数(no2-,nh4+和no3-)之间量的变化可以得出。va可以通过亚硝酸盐与硝酸盐总量的增加率表示,而vn可以通过系统内硝酸盐的增加率来表示。
水样中din时间序列的变化(图2)随着nh4+浓度的降低,no2-迅速生成并且积累,在75h时达到最大值。在75h左右,nh4+浓度下降为0,而亚硝酸盐氧化则开始,迅速转化no2-为no3-,在达到最大值之后,浓度基本稳定不再发生改变。
boltzmann拟合过程如图3所示。反应初始,水体中无论氨氧化还是亚硝酸盐氧化过程都相对较为缓慢,这个过程称之为缓冲期。而这种缓冲期的存在是由于实验所用的样品经混匀分装之后,水体或沉积物的微环境发生变化,在构建新的实验体系之后,样品中的平衡体系需重新建立。在水体培养过程中,亚硝酸盐氧化似乎有所抑制,导致这种现象的原因可能是,氨氧化过程积累了过高的亚硝酸盐,而亚硝酸盐对于微生物而言有一定的毒性,使得初始亚硝酸盐氧化过程受到抑制。亚硝酸盐氧化随后开始,硝酸盐开始积累,随着消耗完毕,硝酸盐的量最终稳定在一定的水平。
用二阶局部平滑对din数据进行平滑处理,之后使用originpro9.32对din时间序列进行boltzmann分布模式拟合(图4),得出如下方程(方程(6)):
其中,y为din的浓度,y0为初始浓度,ymax是反应浓度最大值,x为反应时间,x0为t1/2(1/2反应时间),1/dx为反应常数。
本文中的亚硝酸盐氧化平均速率通过如下方程(方程(7))求得:
水样的平均亚硝酸盐氧化速率为0.8μmolkg-1h-1。然后通过相同方程式计算沉积物样品的平均亚硝酸盐氧化率为8.75μmolkg-1h-1。
本文中的氨氧化平均速率通过以下方程(方程(8))求得:
水样的平均氨氧化速率为1.94μmolkg-1h-1。然后通过相同方程式计算沉积物样品的平均氨氧化率为10μmolkg-1h-1。
在本发明中,建立了一种用于同时测定氨氧化和亚硝酸盐氧化速率的方法,不需要根据样品微生物群落的不同添加不同的抑制剂,避免了繁琐的抑制过程。该方法的反应时间长于传统的抑制剂方法,可以检测到整个反应过程。基于din时间序列和boltzmann拟合,形成了一个完整的计算系统。在传统的只能测量平均硝化速率的基础上,本研究模拟出了瞬时反应率的变化趋势。平均硝化速率可以指示一个地区的硝化能力的大小,瞬时速率是硝化能力的另一个重要标尺,它反映了氨氧化和亚硝酸盐氧化的速率的动态变化过程而并非一个线性增加的关系。
- 还没有人留言评论。精彩留言会获得点赞!