一种可调控细胞响应的无机纳米涂层及制备方法与流程
本发明属于医疗器械领域,尤其涉及一种在可以调控细胞响应行为的无机纳米涂层及制备方法。
背景技术:
通过表面改性提高心血管生物材料的生物相容性,这一手段已得到国内外学者的认同并在临床上广泛应用。与血液接触材料表面,不仅要求材料具有良好的血液相容性,不会产生血栓源性,同时期望材料表面能够快速内皮化,完成血管组织的血运重构。目前的心血管植入器械有心脏血管支架、人工心脏瓣膜、腔静脉滤器、栓塞器械等,这类医疗器械大多数用生物医用金属材料设计加工而成,作为血管组织异物长期存留在血管内,在植入中、晚期时易出现再狭窄或晚期血栓形成等并发症,严重影响到器械的治疗效果和安全性。
在血管支架植入过程中,支架的径向支撑力会损伤血管壁,在血管组织修复过程中,平滑肌细胞便会过度的增殖或迁移到支架杆表面,造成新生内膜增生,导致支架内再狭窄。同时,支架植入局部产生炎症反应,金属材料在血液环境中,由于生物相容性的差异会在材料表面激活血小板或纤维蛋白原变形,造成急性血栓的形成。因此在心血管材料表面改性材料就上述发生再狭窄和血栓形成的机理进行设计,使得改性材料具有良好的生物相容性,可以抑制平滑肌细胞的增殖,同时加快内皮细胞的生长,促进植入物表面尽快内皮化,完成血管组织血运重构,从根本上减少再狭窄和血栓的形成。
药物洗脱支架(DES)是一种临床用得较多的表面改性方法,通过聚合物涂层装载药物附着在支架表面,通过释放的药物可以抑制内膜增生或炎症反应,降低支架的再狭窄率。目前国内有98%的血管支架应用均为DES,有报道称使用DES能将支架的再狭窄率从30%降低到10%,甚至更低。然而,也有研究者发现DES存在一些为足:由于大部分药物均为抗肿瘤药物,在抑制平滑肌细胞及内膜增生的同时,也阻止了内皮细胞的生长,延迟的内皮化或内皮化不完整可能导致晚期血栓形成;药物载体聚合物若不可降解,将是诱导血栓形成的重要因素,若载体聚合物可降解,在降解过程中易出现炎症反应导致血栓形成,病人须长期服用抗凝和抗血小板药物进行治疗,增加了患者经济负担,同时在双抗治疗期间无法进行其它手术。
在器械表面制备生物相容性好的无机薄膜或涂层是另一类对血管支架类材料的表面改性手段,由于该薄膜厚度不大于1um,远小于聚合物涂层,具有良好的结合力且对支架的安装、输送无影响。这些薄膜具有良好的血液相容性,可以减少血小板激活和纤维蛋白原的沉积,降低了血栓形成的风险;同时由于具有良好的组织相容性,能促进内皮细胞的增殖,加快材料表面的内皮化进程,常见的涂层有类金刚石薄膜(DLC)、钛或钛的化合物(TiN、Ti-O、Ti-C等)、Si-N薄膜等。Allen M.通过研究发现,DLC具有良好的生物相容性,并具有耐磨特性,已用于人工机械心脏瓣膜。而TiN、Ti-O膜涂层由于其良好的生物相容性和血液相容性,已用于了心血管植入器械。
事实上,上述两类表面改性方式均通过单一靶向来改变血栓形成、内膜增生或内皮化过程,然而这三者之间在生物学行为方面本存在着联系。对于不同的细胞,其应答机制不同,根据一种可调控细胞响应的方式来实现选择性功能,即在相同条件下有些细胞得到抑制,而部分细胞却被促进,以符合血管组织的生理功能。
目前采用载药聚合物涂层表面改性在一定程度上抑制了内膜增生防止了再狭窄的发生,但由于涂层较厚(约10-20um),影响了支架的安装性能和通过性能,同时支架内腔聚合物的粘性增加支架与球囊间的阻力,影响支架植入操作的安全性。
采用DES方式设计,载药聚合物本身会产生血栓源性:当聚合物不可降解时,作为异物附着在支架材料表面,会诱导晚期血栓形成;当聚合物可降解时,在降解过程中易引起周围组织的炎症反应,形成血栓。
无机薄膜在血管支架上的应用减少了血栓源性,并提高了血液相容性,但这些薄膜大多是金属化合物,为脆性薄膜,其支架变形过程中对薄膜物理性能要求很高。
无机薄膜具有良好的组织相容性,能促进内皮细胞的生长,加快内皮化进程,但同时由于支架植入过程中血管组织的损伤,该类薄膜却无法对造成内膜增生的平滑肌细胞进行控制。
技术实现要素:
本发明要解决的一个技术问题在于提供一种无机纳米涂层,该涂层通过调节涂层中的铜含量,实现涂层降解过程中铜离子释放来调控不同细胞的响应程度和增殖凋亡行为,实现无机涂层在生物材料细胞调控作用。
解决本发明的这个技术问题所采用的一种技术方案是:提供一种无机纳米涂层,其沉积在金属器械表面,通过涂层降解来释放出铜离子和铜离子含量的控制。
作为本发明无机纳米涂层的进一步改进,所述无机纳米涂层的含铜量为0.2-0.8mg/cm2。
作为本发明无机纳米涂层的进一步改进,所述无机纳米涂层的厚度为150-450nm。
作为本发明无机纳米涂层的进一步改进,在人体模拟液或人体内,所涂层的铜元素都能够以铜离子的形式缓慢释放。
本发明要解决的另一个技术问题在于提供一种在金属医疗器械的表面制备含铜涂层的方法,该方法使得该涂层具有较好的生物学性能且是一种金属涂层,具有好的延展性和力学行为,通过该方法保证医疗器械的力学性能和涂层的力学性能。
解决本发明的另一个技术问题所采用的技术方案是:提供一种在金属医疗器械的表面制备涂层的方法,所述方法包括以下步骤:
步骤一,对金属医疗器械表面进行清洗、干燥;
步骤二,在真空室内产生铜离子,在偏压的作用下,使铜离子和其它离化的金属离子向医疗器械表面移动并沉积;
步骤三,金属器械表面的沉积温度不低于200℃,所述铜离子和其它金属离子在金属器械表面处形成含铜涂层。
在本发明涂层的制备方法中,步骤二所述的铜离子和其它金属离子运动速率通过脉冲溅射方法调节。
在本发明涂层的制备方法中,步骤二中的所述偏压为150V~200V。
在本发明涂层的制备方法中,步骤二中的所述溅射过程调节靶工艺,实现涂层中铜离子释放速度为0.5-7.5ug/ml。
在本发明涂层的制备方法中,步骤三中的所述涂层沉积过程中真空室内的气压为0.5Pa~0.8Pa。
本发明又提供了一种含有以上所述的涂层的医疗器械。
与现有技术相比,本发明具备以下优点:
(1)通过无机涂层的降解产物来进行细胞调控行为,改变了传统采用药物进行细胞调节所产生的副作用,而且该涂层成分比例易控。
(2)将金属涂层应用于心血管医疗器械中,满足器械在使用过程中的力学要求和临床中金属变形的力学匹配性。
(3)该涂层以人体所需微量元素铜为基元,可掺杂不同的元素实现涂层的生物相容性和功能性。
附图说明
图1 平滑肌细胞和内皮细胞对不同铜离子的响应行为。
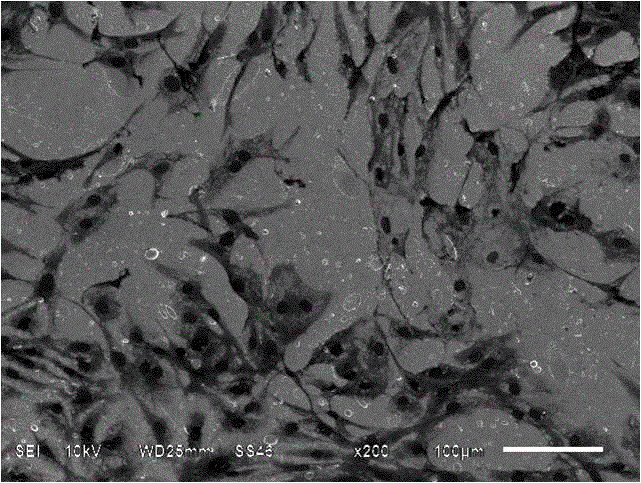
图2 不锈钢表面内皮细胞2天生长情况。
图3含铜涂层(铜含量为0.2mg/cm2)内皮细胞天生长情况。
图4含铜涂层(铜含量为0.5mg/cm2)内皮细胞天生长情况。
实施例一
铜钛复合薄膜的制备。
采用磁控溅射在L605合金表面沉积铜钛复合薄膜。
阴极靶材分别为高纯钛靶和高纯铜靶,通过调节靶电流来实现铜钛原子比例,铜钛结合形式可通过沉积工艺如沉积温度、偏压、时间来实现。
L605合金采用丙酮超声波进行清洗。先用清洗:在烧杯中到入少许丙酮,液面超过样品少许即可,然后用超声波清洗5分钟。接着用无水乙醇清洗。在烧杯中到入少许无水乙醇,液面超过样品少许即可,然后用超声波清洗5分钟。最后用蒸馏水清洗。在烧杯中到入蒸馏水,液面超过样品,然后用超声波清洗10分钟,为充分清洗干净可反复清洗2-3次。
将L605样品磁控溅射设备样品台上,开始建立真空系统,当真空室气压小于1.0×10-3Pa, 通入氩气流量为80-120sccm,使得真空室气压达到0.6-1.0Pa,调节偏压电源到400-500V,使氩离子进行溅射清洗样品表面,清洗时间为3-5分钟。
建立真空系统,真空室的基底真空为8.0×10-4~1.0×10-3Pa时,启动样品旋转,旋转速率为30-40rp/m,开启样品台加热系统,保证基底温度为200℃。通入氩气,气体流量为60-100sccm,保证真空室气压在0.5-0.8Pa。将溅射电流设定为2A,脉冲占空比40%,基底施加负偏压150V。同时开启钛靶和铜靶,其中钛靶电流为60A,铜靶电流为20A,离子流为120-140mA,靶间距为100mm,沉积时间为15min。经分析,有少量的铜钛合金化合物存在,该薄膜约为150nm,铜的含量为0.2mg/cm2。
同样通入氩气,气体流量为60-100sccm,保证真空室气压在0.5-0.8Pa。将溅射电流设定为4A,脉冲占空比60%,基底负偏压180V。开启钛靶和铜靶,其中钛靶电流为60A,铜靶电流为30A,离子流为140-160mA,靶间距为100mm,沉积时间为15min。经分析,该铜钛薄膜主要铜钛相化合物为主,该薄膜约为450nm,铜的含量为0.5mg/cm2。
上述薄膜厚度150-450nm、含铜量为0.2-0.5mg/cm2的铜钛复合涂层在体液中可经缓慢释放出铜离子,而铜离子的量随时间变化,从而影响铜离子对不同细胞的调控,实现细胞的不同响应行为。图1是铜离子对平滑肌细胞和内皮细胞的不同响应程度,可以看到铜离子释放量在0.5-7.5ug/ml时,对内皮细胞有促进作用,而平滑肌细胞却有抑制作用。
实施例二
铜铁复合薄膜的制备。
样品前处理及溅射清洗同实施例一。
本发明实验用阴极为纯铁,在脉冲触发电压下引燃电弧,产生铁的等离子体。采用磁过滤弯管过滤宏观颗粒和中性粒子,在溅射偏压的作用下,钛离子和铁离子向基体材料表面移动,从而在材料表面形成铜铁可降解薄膜。
建立真空系统,真空室的基底真空为1.0×10-3Pa时,启动样品旋转,旋转速率为30-40rp/m,开启样品台加热系统,保证基底温度为200℃。通入氩气,气体流量为60-100sccm,保证真空室气压在0.5-0.8Pa。将溅射功率设定为500W,脉冲占空比20%,基底施加负偏压200V。开启铁靶和铜靶,其中铁靶电流为80A,铜靶电流为30A,离子流为80-140mA,靶间距为100mm,沉积时间为15min。经分析,有少量的铁、铜合金化合物存在,该薄膜约为100nm,铜的含量为0.3mg/cm2。
同样通入氩气,气体流量为60-100sccm,保证真空室气压在0.5-0.8Pa。将溅射电流设定为4A,脉冲占空比60%,基底负偏压150V。开启铁靶和铜靶,其中铁靶电流为60A,铜靶电流为60A,离子流为140-200mA,靶间距为100mm,沉积时间为15min。经分析,该铁钛薄膜主要铜铁相化合物为主,该薄膜约为350nm,铜的含量为0.8mg/cm2。
铜是人体所需的微量元素之一,成年人体中铜的正常含量为100-150mg,只有摄入铜量超过正常值的10倍以上,才会出现明显的中毒现象。本发明中血管支架表面的复合薄膜,铜的含量低于1.0ug/cm,在植入短时间内完全释放,对血管局部组织和人体无不良反应。本发明中形成的铜铁合金容易腐蚀降解,产生铜、铁离子,对于短期铜离子浓度较高的需求的涂层,可以采用该无机涂层来调控细胞的响应行为。
实施例三
铜锌复合薄膜的制备。
样品前处理及溅射清洗同实施例一。
本发明实验用阴极为纯锌,在脉冲触发电压下引燃电弧,产生铁的锌离子体。在溅射偏压的作用下,锌离子和铜离子向基体材料表面移动,从而在材料表面形成铜锌可降解薄膜。
建立真空系统,真空室的基底真空为1.0×10-3Pa时,启动样品旋转,旋转速率为30-40rp/m,开启样品台加热系统,保证基底温度为200℃。通入氩气,气体流量为60-100sccm,保证真空室气压在0.5-0.8Pa。将溅射功率设定为500W,脉冲占空比20%,基底施加负偏压200V。开启锌靶和铜靶,其中锌靶电流为80A,铜靶电流为20A,离子流为80-120mA,靶间距为100mm,沉积时间为15min。经分析,该薄膜约为100nm,铜的含量为0.2mg/cm2。
同样通入氩气,气体流量为60-100sccm,保证真空室气压在0.5-0.8Pa。将溅射电流设定为5A,脉冲占空比60%,基底负偏压150V。开启铁靶和铜靶,其中锌靶电流为60A,铜靶电流为40A,离子流为150-200mA,靶间距为100mm,沉积时间为15min。经分析,该薄膜约为350nm,铜的含量为0.5mg/cm2。
图2是内皮细胞体外培养情况,随着铜离子浓度变化细胞响应程度的情况。当浓度较低时,可以促进内皮细胞的生长,当浓度较高时,内皮细胞出现凋亡现象。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!